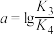室温时,通过实验探究 溶液的性质,操作及现象如下表所示:
溶液的性质,操作及现象如下表所示:
下列说法正确的是
 溶液的性质,操作及现象如下表所示:
溶液的性质,操作及现象如下表所示:| 实验 | 实验操作及现象 |
| 1 | 测定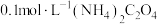 溶液的pH,测得溶液pH<7 溶液的pH,测得溶液pH<7 |
| 2 | 向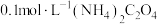 溶液中加入等体积 溶液中加入等体积 的 的 溶液,产生白色沉淀(草酸钙的 溶液,产生白色沉淀(草酸钙的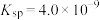 ) ) |
| 3 | 向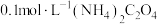 溶液中滴加少量NaOH溶液,加热产生刺激性气味气体,后冷却至室温 溶液中滴加少量NaOH溶液,加热产生刺激性气味气体,后冷却至室温 |
A.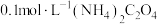 溶液中存在: 溶液中存在: |
B.由实验1可得: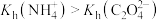 |
C.由实验2所得溶液: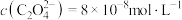 |
D.实验3所得溶液中水的电离程度大于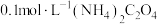 溶液 溶液 |
22-23高三下·重庆渝中·阶段练习 查看更多[3]
重庆市巴蜀中学2023届高三下学期适应性月考卷(九)化学试题(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)四川省仁寿第一中学校南校区2023-2024学年高三上学期开学考试化学试题
更新时间:2023-05-07 15:54:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】化学上常用AG表示溶液中的lg 。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的一元酸HA溶液,AG与所加NaOH溶液的体积(V)关系如图所示,下列说法正确的是
。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的一元酸HA溶液,AG与所加NaOH溶液的体积(V)关系如图所示,下列说法正确的是

 。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的一元酸HA溶液,AG与所加NaOH溶液的体积(V)关系如图所示,下列说法正确的是
。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的一元酸HA溶液,AG与所加NaOH溶液的体积(V)关系如图所示,下列说法正确的是
A.随着NaOH溶液的加入, 减小 减小 |
| B.25℃时,HA的电离常数Ka≈1.0×10-4.5 |
| C.b点溶液中存在c(H+)+c(HA)=c(OH-)+c(A-) |
| D.a、b、c、d、e五点的溶液中,水的电离程度最大的点是e |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下:某NaHSO3溶液的pH=5,则在NaHSO3溶液中微粒的物质的量浓度关系一定正确的是( )
| A.c(Na+)>c(HSO3﹣)>c(OH﹣)>c(H+)>(SO32﹣) |
| B.c(Na+)+c(H+)=c(OH﹣)+c(SO32﹣)+c(HSO3﹣) |
| C.c(Na+)=c(SO32﹣)+c(HSO3﹣)+c(H2SO3) |
| D.c(OH﹣)=c(H+)+c(HSO3﹣)+c(H2SO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列有关叙述不正确的是
A.若 溶液的 溶液的 ,则 ,则 |
B.0.2mol/L的亚硫酸氢钠溶液中: |
C. 和 和 混合溶液中: 混合溶液中: |
D.已知 的 的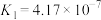 , , ,则NaHA溶液呈碱性 ,则NaHA溶液呈碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温时,向10mL0.1mol/LHX溶液中逐滴加入0.1mol/L的氨水,其导电能力、pH与V(NH3·H2O)的关系变化如图所示(假设反应过程中温度不变)。下列分析错误的是


| A.水的电离程度:b>d,a>c |
| B.a点对应的溶液中存在c(HX)+2c(H+)=c(X-)+2c(NH3·H2O)+2c(OH-) |
| C.d点所得溶液的pH<7 |
| D.Kb(NH3·H2O)=Ka(HX)=10-4.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列叙述中不正确的是
| A.0.1mol·L-1NH4HS溶液中有:c(NH4+)<c(HS-)+c(S2-)+c(H2S) |
B.25℃时,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合后,c(NH4+)=c(Cl-),则NH3·H2O的电离常数为 |
| C.等浓度的HCN和NaCN混合溶液中有:2c(Na+)=c(CN-)+c(HCN) |
| D.等pH的HA和HB溶液,分别与一定浓度的氢氧化钠溶液完全中和,HA消耗的氢氧化钠溶液体积多,则可证明酸性HA>HB |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】室温下,用0.100mol/L NaOH溶液滴定20.00 mL  溶液。滴定过程中含A微粒的分布分数(
溶液。滴定过程中含A微粒的分布分数( )和pH随NaOH溶液体积变化如图所示。下列说法正确的是
)和pH随NaOH溶液体积变化如图所示。下列说法正确的是

 溶液。滴定过程中含A微粒的分布分数(
溶液。滴定过程中含A微粒的分布分数( )和pH随NaOH溶液体积变化如图所示。下列说法正确的是
)和pH随NaOH溶液体积变化如图所示。下列说法正确的是
A.原 溶液的物质的量浓度为0.125mol/L 溶液的物质的量浓度为0.125mol/L |
B.pH=7时,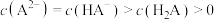 |
C.加入NaOH溶液越多, 越高,水的电离程度越大 越高,水的电离程度越大 |
D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验操作及现象、结论都正确的是
| 选项 | 实验操作及现象 | 结论 |
| A | 分别测浓度均为0.1mol·L-1的CH3COONH4和NaHCO3溶液的pH,后者大于前者 | Kh(CH3COO-)<Kh(HCO ) ) |
| B | 将铁锈溶于浓盐酸,滴入KMnO4溶液,紫色褪去 | 铁锈中含有二价铁 |
| C | FeCl3+3KSCN Fe(SCN)3+3KCl在平衡体系中加入KCl晶体,溶液颜色不变 Fe(SCN)3+3KCl在平衡体系中加入KCl晶体,溶液颜色不变 | 加入少量KCl晶体,不会影响该化学平衡 |
| D | 向溶液中滴加少量NaOH稀溶液,将湿润的红色石蕊试纸靠近试管口,观察石蕊试纸变蓝 | 原溶液中含有NH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】298K时,在20mL0.1mol•L-1H2R稀溶液中滴入相同浓度的NaOH溶液,用pH传感器测得混合溶液的pH变化曲线如图所示(已知的H2R的Ka2为1.0×10-10),下列有关叙述正确的是


| A.H2R的Ka1约为1.0×10-3 |
| B.a点存在:c(HR-)>c(R2-) |
| C.b点时:c(Na+)>c(HR-)>c(R2-)>c(H2R) |
| D.c点时:2c(H+)+3c(H2R)+c(HR-)=2c(OH-)+c(R2-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知:Ka1(H2SO3)=1.0×10-1.85、Ka2(H2SO3)=1.0×10-7。通过0.1mol·L−1NaOH溶液滴定20 mL0.1mol·L−1H2SO3溶液实验探究H2SO3、Na2SO3、NaHSO3溶液的性质。
实验1:滴入10 mL 0.1mol·L−1NaOH溶液时测得溶液的pH=1.85。
实验2:向实验1所得溶液中继续滴入10 mL 0.1mol·L−1NaOH溶液时无明显现象。
实验3:向实验2所得溶液中通入NH3至溶液pH=7(通入气体对溶液体积的影响可忽略)。
实验4:向实验2所得溶液中滴加HNO3酸化的Ba(NO3)2溶液,产生白色沉淀。
下列说法正确的是
实验1:滴入10 mL 0.1mol·L−1NaOH溶液时测得溶液的pH=1.85。
实验2:向实验1所得溶液中继续滴入10 mL 0.1mol·L−1NaOH溶液时无明显现象。
实验3:向实验2所得溶液中通入NH3至溶液pH=7(通入气体对溶液体积的影响可忽略)。
实验4:向实验2所得溶液中滴加HNO3酸化的Ba(NO3)2溶液,产生白色沉淀。
下列说法正确的是
A.实验1溶液中存在:2c(H2SO3)+ c(SO )=0.1 mol·L−1 )=0.1 mol·L−1 |
B.实验2溶液中存在:c(Na+)>c(HSO )>c(SO )>c(SO )>c(H2SO3) )>c(H2SO3) |
C.实验3溶液中存在:c(Na+)>c(NH )>c(SO )>c(SO ) ) |
D.实验4反应后静置所得上层清液中一定有:c(Ba2+)×c(SO )=Ksp(BaSO3) )=Ksp(BaSO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列“实际应用”对应“化学知识原理”说法错误的是( )
| 选项 | 实际应用 | 化学知识原理 |
| A | 泡沫灭火器中装有碳酸氢钠溶液 和硫酸铝溶液 | 碳酸氢钠溶液和硫酸铝溶液水解且相互促进 |
| B | 工业上采用高压(20-50MPa)合成NH3 | 应用勒夏特列原理 |
| C | 施加石膏降低盐碱地(含Na2CO3)的碱性 | CaCO3溶度积小于CaSO4 |
| D | 选用金属锂做电池电极材料 | 锂轻且在空气中稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】常温下,有关物质的溶度积如下,下列有关说法不正确的是
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.60×10-12 | 2.80×10-39 |
| A.常温下,除去NaCl溶液中的MgCl2杂质,选用NaOH溶液比Na2CO3溶液效果好 |
| B.常温下,除去NaCl溶液中的CaCl2杂质,选用NaOH溶液比Na2CO3溶液效果好 |
| C.向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=2.0×10-21 |
| D.将适量的Ca(OH)2固体溶于100mL水中,刚好达到饱和[c(Ca2+)=1.0×10-2mol/L],若保持温度不变,向其中加入100mL0.012mol/L的NaOH,则该溶液变为不饱和溶液 |
您最近一年使用:0次

 的溶液中,随着
的溶液中,随着 的变化存在平衡关系:
的变化存在平衡关系: ,
, ,
, ,
, ,
, ,
,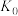 、
、 、
、 、
、 、
、 。
。 、
、 、
、 、
、 随
随 的变化关系如图所示,下列说法错误的是
的变化关系如图所示,下列说法错误的是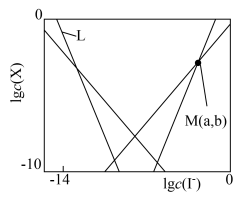
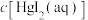 不变。
不变。