Ⅰ.在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2混合气体,2 min后,反应达到平衡,生成SO3气体0.5 mol,同时放出热量Q kJ。回答下列问题
(1)写出该反应的热化学方程式为___________ 。
(2)在该条件下,反应前后容器的体积之比为___________ 。
(3)①若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)___________ 0.5mol(填 “大于”、“小于”或“等于”);
②若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量___________ Q kJ(填 “大于”、“小于”或“等于”)。
Ⅱ. 用焦炭还原NO2的反应为:2NO2(g)+2C(s ) N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
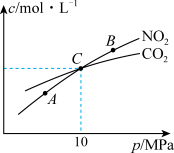
(4)A、B两点的浓度平衡常数关系:Kc(A)___________ Kc(B) (填 “﹥”、“<”或“﹦”)。
(5)A、B、C三点中NO2的转化率最高的是___________ (填“A”或“B”或“C”)点。
(6)计算C点时该反应的压强平衡常数Kp(C)=___________ (Kp是用平衡分压代替平衡浓度计算,分压=总压物质的量分数)。
Ⅲ.25℃时,向10mL0.1mol•L-1NH4HSO4溶液中逐滴滴入0.1mol•L-1NaOH溶液,溶液的pH与NaOH溶液体积关系如图所示:
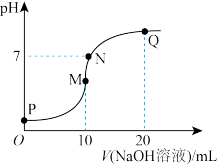
(7)M、Q两点中,水的电离程度较大的是___________ 点。
(8)下列关系中,正确的是___________ 。
a.M点c(Na+)>c(NH )
)
b.N点c(NH )+c(Na+)=2c(SO
)+c(Na+)=2c(SO )
)
c.Q点c(NH )+c(NH3•H2O)=c(Na+)
)+c(NH3•H2O)=c(Na+)
(1)写出该反应的热化学方程式为
(2)在该条件下,反应前后容器的体积之比为
(3)①若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)
②若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量
Ⅱ. 用焦炭还原NO2的反应为:2NO2(g)+2C(s )
 N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
(4)A、B两点的浓度平衡常数关系:Kc(A)
(5)A、B、C三点中NO2的转化率最高的是
(6)计算C点时该反应的压强平衡常数Kp(C)=
Ⅲ.25℃时,向10mL0.1mol•L-1NH4HSO4溶液中逐滴滴入0.1mol•L-1NaOH溶液,溶液的pH与NaOH溶液体积关系如图所示:

(7)M、Q两点中,水的电离程度较大的是
(8)下列关系中,正确的是
a.M点c(Na+)>c(NH
 )
)b.N点c(NH
 )+c(Na+)=2c(SO
)+c(Na+)=2c(SO )
)c.Q点c(NH
 )+c(NH3•H2O)=c(Na+)
)+c(NH3•H2O)=c(Na+)
更新时间:2023-10-10 18:36:40
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】Ⅰ.由四种常见元素组成的化合物X,按如下流程进行实验。气体C能使带火星木条复燃,溶液B和溶液E的焰色反应为黄色,固体A和D组成元素相同,X可由蓝色溶液F与过量的浓的强碱性溶液B反应获得。
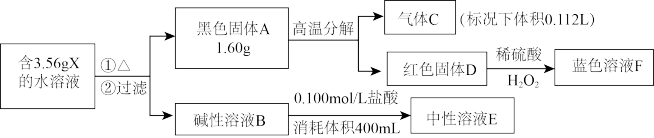
请回答:
(1)X的化学式________________ 。
(2)写出F+B→X反应的离子方程式:________________ 。
(3)黑色固体A可在高温下与氨气作用生成红色固体D,同时生成一种单质,写出该反应的方程式:________________ 。
Ⅱ.已知CuCl晶体呈白色,熔点为430℃,沸点为1490℃,见光分解,露置于潮湿空气中易被氧化,溶于水、稀盐酸、乙醇,易溶于浓盐酸生成H3CuCl4,反应的化学方程式为:CuCl(白色,s)+3HCl(aq) H3CuCl4(黄色,aq)。实验室用下图所示装置制取CuCl,反应原理为:2Cu2++SO2+8Cl−+2H2O=2
H3CuCl4(黄色,aq)。实验室用下图所示装置制取CuCl,反应原理为:2Cu2++SO2+8Cl−+2H2O=2 +
+ +4H+;
+4H+; (aq)
(aq) CuCl(s)+3Cl-(aq)
CuCl(s)+3Cl-(aq)
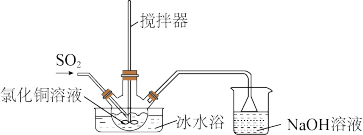
反应结束后,取出三颈烧瓶中的混合物进行一系列操作可得到CuCl晶体。
(4)反应过程中要通入过量SO2的原因是:________________ 。
(5)欲提纯某混有铜粉的CuCl晶体,请简述实验方案:_____________ 。

请回答:
(1)X的化学式
(2)写出F+B→X反应的离子方程式:
(3)黑色固体A可在高温下与氨气作用生成红色固体D,同时生成一种单质,写出该反应的方程式:
Ⅱ.已知CuCl晶体呈白色,熔点为430℃,沸点为1490℃,见光分解,露置于潮湿空气中易被氧化,溶于水、稀盐酸、乙醇,易溶于浓盐酸生成H3CuCl4,反应的化学方程式为:CuCl(白色,s)+3HCl(aq)
 H3CuCl4(黄色,aq)。实验室用下图所示装置制取CuCl,反应原理为:2Cu2++SO2+8Cl−+2H2O=2
H3CuCl4(黄色,aq)。实验室用下图所示装置制取CuCl,反应原理为:2Cu2++SO2+8Cl−+2H2O=2 +
+ +4H+;
+4H+; (aq)
(aq) CuCl(s)+3Cl-(aq)
CuCl(s)+3Cl-(aq)
反应结束后,取出三颈烧瓶中的混合物进行一系列操作可得到CuCl晶体。
(4)反应过程中要通入过量SO2的原因是:
(5)欲提纯某混有铜粉的CuCl晶体,请简述实验方案:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】弱电解质的电离平衡、盐类的水解平衡和难溶电解质的溶解平衡均属于化学学习中的动态平衡。
(1)已知室温时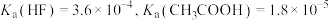
① 的
的 溶液与
溶液与 的
的 溶液相比,一定有
溶液相比,一定有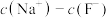
___________ 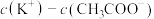 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
②向 溶液中滴加
溶液中滴加 溶液至
溶液至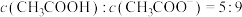 ,此时溶液
,此时溶液
___________ 。
(2)化学上常用 表示溶液中的酸碱度,
表示溶液中的酸碱度,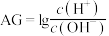 。
。 时,用
时,用 的
的 溶液滴定
溶液滴定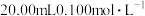 某酸(HA)溶液,
某酸(HA)溶液, 与所加
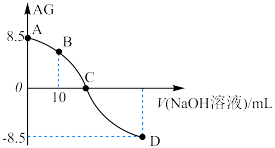
与所加 溶液的体积(V)关系如图所示,B点溶液中:
溶液的体积(V)关系如图所示,B点溶液中:
___________  (填“>”、“=”或“<”,下同)。
(填“>”、“=”或“<”,下同)。
(3) 时,将
时,将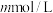 的醋酸钠溶液与
的醋酸钠溶液与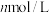 盐酸溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数
盐酸溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数
___________ (用含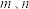 的代数式表示)。
的代数式表示)。
(4) 溶液中存在多个平衡
溶液中存在多个平衡
(i)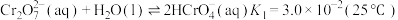
(ii)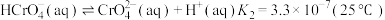
①下列有关 溶液的说法正确的有
溶液的说法正确的有___________ 。
A.加入少量水稀释,溶液中离子总数增加
B.加入少量硫酸,溶液的 不变
不变
C.加入少量 固体,平衡时
固体,平衡时 与
与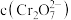 的比值保持不变
的比值保持不变
D.加入少量 溶液,反应(ⅰ)的平衡逆向移动
溶液,反应(ⅰ)的平衡逆向移动
② 时,
时,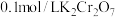 溶液中
溶液中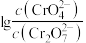 随
随 的变化关系如图。
的变化关系如图。
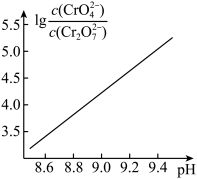
当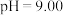 时,设
时,设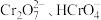 与
与 的平衡浓度分别为
的平衡浓度分别为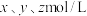 ,则
,则 之间的关系式为
之间的关系式为________  ;计算溶液中
;计算溶液中 的平衡浓度
的平衡浓度_______ (结果保留两位有效数字)。
(1)已知室温时
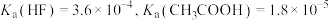
①
 的
的 溶液与
溶液与 的
的 溶液相比,一定有
溶液相比,一定有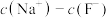
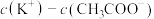 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。②向
 溶液中滴加
溶液中滴加 溶液至
溶液至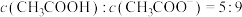 ,此时溶液
,此时溶液
(2)化学上常用
 表示溶液中的酸碱度,
表示溶液中的酸碱度,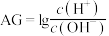 。
。 时,用
时,用 的
的 溶液滴定
溶液滴定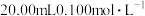 某酸(HA)溶液,
某酸(HA)溶液, 与所加
与所加 溶液的体积(V)关系如图所示,B点溶液中:
溶液的体积(V)关系如图所示,B点溶液中:
 (填“>”、“=”或“<”,下同)。
(填“>”、“=”或“<”,下同)。
(3)
 时,将
时,将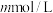 的醋酸钠溶液与
的醋酸钠溶液与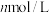 盐酸溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数
盐酸溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数
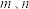 的代数式表示)。
的代数式表示)。(4)
 溶液中存在多个平衡
溶液中存在多个平衡(i)
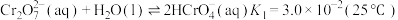
(ii)
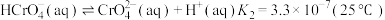
①下列有关
 溶液的说法正确的有
溶液的说法正确的有A.加入少量水稀释,溶液中离子总数增加
B.加入少量硫酸,溶液的
 不变
不变C.加入少量
 固体,平衡时
固体,平衡时 与
与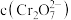 的比值保持不变
的比值保持不变D.加入少量
 溶液,反应(ⅰ)的平衡逆向移动
溶液,反应(ⅰ)的平衡逆向移动②
 时,
时,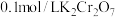 溶液中
溶液中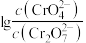 随
随 的变化关系如图。
的变化关系如图。
当
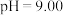 时,设
时,设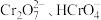 与
与 的平衡浓度分别为
的平衡浓度分别为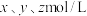 ,则
,则 之间的关系式为
之间的关系式为 ;计算溶液中
;计算溶液中 的平衡浓度
的平衡浓度
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】苯乙腈主要用于有机合成及生产医药,农药的中间体,对环境有危害。常温常压下,苯乙腈水解一般需加入酸碱催化剂。但研究人员发现,在近临界水(指温度在523~623K之间的压缩液态水)中,不加任何催化剂的情况下,苯乙腈就能发生水解反应生成苯乙酞胺:
C6H5CH2CN(l)+H2O(l) C6H5CH2CONH2(l) △H
C6H5CH2CONH2(l) △H
(苯乙腈) (苯乙酰胺)
请回答下列问题:
(1)已知近临界水中,水的离子积常数为10-10,则此条件下,pH=7的NaAc溶液中由水电离的c(H+)=________ mol·L-1。该反应不加任何催化剂就能发生的主要原因是___________ 。
(2)研究反应的平衡常数(记作lgK)与温度(T)的关系,得到如图1所示的关系,判断该反应的△H__________ 0(填“>”“<”或“=”)。
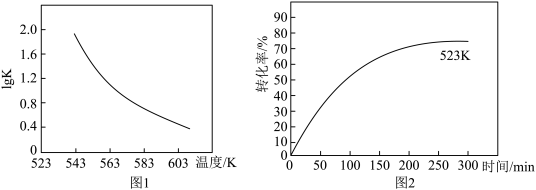
(3)图2表示其他条件不变时,温度和时间对苯乙腈转化率的影响曲线图(不完整)。若图中曲线对应的温度为523K,请你在原图中作出温度为583K的影响曲线。___________ 。
(4)下列哪种仪器可用于分析水解反应过程中苯乙腈浓度的变化_________ (填编号)。
A.元素分析仪B.核磁共振仪C.原子吸收光谱仪D.分光光度计
(5)科学家还在近临界水中分别添加CO2、NH3,研究后得到了如下的图示:
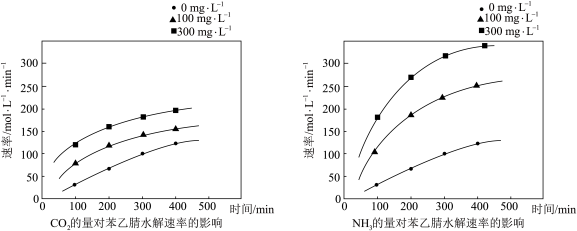
从中你可以得出什么结论(至少写出2点___________ 。
(6)水的用途很广,可利用太阳能光伏电池电解水制高纯氢,工作示意图如图。通过控制开关连接K1或K2,可交替得到H2和O2。
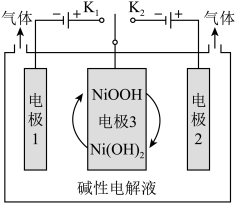
①制H2时,连接______________ ,可得H2。
②改变开关连接方式,产生O2的电极反应式__________________________ 。
③选用NiOOH、Ni(OH)2作为电极3材料的优点(请结合电极反应式进行阐述)___________ 。
C6H5CH2CN(l)+H2O(l)
 C6H5CH2CONH2(l) △H
C6H5CH2CONH2(l) △H(苯乙腈) (苯乙酰胺)
请回答下列问题:
(1)已知近临界水中,水的离子积常数为10-10,则此条件下,pH=7的NaAc溶液中由水电离的c(H+)=
(2)研究反应的平衡常数(记作lgK)与温度(T)的关系,得到如图1所示的关系,判断该反应的△H

(3)图2表示其他条件不变时,温度和时间对苯乙腈转化率的影响曲线图(不完整)。若图中曲线对应的温度为523K,请你在原图中作出温度为583K的影响曲线。
(4)下列哪种仪器可用于分析水解反应过程中苯乙腈浓度的变化
A.元素分析仪B.核磁共振仪C.原子吸收光谱仪D.分光光度计
(5)科学家还在近临界水中分别添加CO2、NH3,研究后得到了如下的图示:

从中你可以得出什么结论(至少写出2点
(6)水的用途很广,可利用太阳能光伏电池电解水制高纯氢,工作示意图如图。通过控制开关连接K1或K2,可交替得到H2和O2。

①制H2时,连接
②改变开关连接方式,产生O2的电极反应式
③选用NiOOH、Ni(OH)2作为电极3材料的优点(请结合电极反应式进行阐述)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】工业上,利用水煤气(主要成分为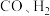 )合成
)合成 ,向
,向 的恒容密闭容器中加入
的恒容密闭容器中加入 和
和 ,在一定温度下只发生反应
,在一定温度下只发生反应
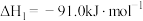 ,
, 后反应达到平衡状态,测得放出的热量为
后反应达到平衡状态,测得放出的热量为 。
。
(1)从反应开始至恰好达到平衡状态时, 的平均反应速率
的平均反应速率
_______ 。
(2)在温度不变条件下,上述反应达到平衡后,再向容器中充入 和
和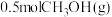 ,此时
,此时
______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)对于上述反应, 的平衡转化率与温度、压强的关系如图所示:
的平衡转化率与温度、压强的关系如图所示:

①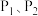 的大小关系是
的大小关系是
______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②A、B、C三点对应的平衡常数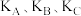 的大小关系是
的大小关系是______ 。
③在不考虑催化剂影响的情况下,A、B、C三点中活化分子百分数最大的是______ 点。
(4)上述反应的反应速率(v)随时间(t)的变化关系如图所示,若 、
、 时刻只改变一个条件,下列说法错误的是
时刻只改变一个条件,下列说法错误的是_______ (填字母)。

A.在 时,采取的措施可以是升高温度
时,采取的措施可以是升高温度
B.在 时,采取的措施可以是增大
时,采取的措施可以是增大 的浓度
的浓度
C.在 时,容器内
时,容器内 的转化率是整个过程中的最大值
的转化率是整个过程中的最大值
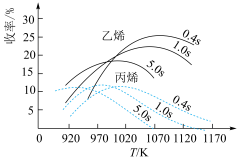
(5)实验测得柴油裂解得到乙烯和丙烯的收率与温度、柴油在裂解设备内的停留时间的关系如图所示。工业上为获得较多的乙烯应选择较为适宜的温度和停留时间分别为_______ K和______ s。
(6)下列叙述中能说明反应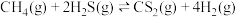 达到平衡状态的是_______(填字母)。
达到平衡状态的是_______(填字母)。
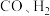 )合成
)合成 ,向
,向 的恒容密闭容器中加入
的恒容密闭容器中加入 和
和 ,在一定温度下只发生反应
,在一定温度下只发生反应
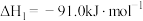 ,
, 后反应达到平衡状态,测得放出的热量为
后反应达到平衡状态,测得放出的热量为 。
。(1)从反应开始至恰好达到平衡状态时,
 的平均反应速率
的平均反应速率
(2)在温度不变条件下,上述反应达到平衡后,再向容器中充入
 和
和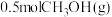 ,此时
,此时
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)对于上述反应,
 的平衡转化率与温度、压强的关系如图所示:
的平衡转化率与温度、压强的关系如图所示:
①
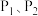 的大小关系是
的大小关系是
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②A、B、C三点对应的平衡常数
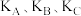 的大小关系是
的大小关系是③在不考虑催化剂影响的情况下,A、B、C三点中活化分子百分数最大的是
(4)上述反应的反应速率(v)随时间(t)的变化关系如图所示,若
 、
、 时刻只改变一个条件,下列说法错误的是
时刻只改变一个条件,下列说法错误的是
A.在
 时,采取的措施可以是升高温度
时,采取的措施可以是升高温度B.在
 时,采取的措施可以是增大
时,采取的措施可以是增大 的浓度
的浓度C.在
 时,容器内
时,容器内 的转化率是整个过程中的最大值
的转化率是整个过程中的最大值(5)实验测得柴油裂解得到乙烯和丙烯的收率与温度、柴油在裂解设备内的停留时间的关系如图所示。工业上为获得较多的乙烯应选择较为适宜的温度和停留时间分别为

(6)下列叙述中能说明反应
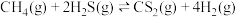 达到平衡状态的是_______(填字母)。
达到平衡状态的是_______(填字母)。A.断裂 的同时生成 的同时生成 | B.恒容条件下,体系压强不再变化 |
| C.恒容条件下,气体的密度不再变化 | D.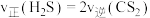 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】从古至今,铁及其化合物在人类生产生活中的作用发生了巨大变化。
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是______ (填字母序号)。
a. Fe b. FeO c. Fe3O4 d. Fe2O3
(2)现代利用铁的氧化物循环裂解水制氢气的过程如下图所示。 整个过程与温度密切相关, 当温度低于 570℃时,反应Fe3O4(s)+4 CO(g) 3Fe(s)+4CO2(g),阻碍循环反应的进行。
3Fe(s)+4CO2(g),阻碍循环反应的进行。
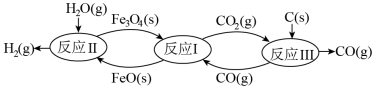
①已知:Fe3O4(s) + CO(g) 3FeO(s) +CO2(g) ΔH1 = +19.3 kJ·mol-1
3FeO(s) +CO2(g) ΔH1 = +19.3 kJ·mol-1
3FeO(s) + H2O(g) Fe3O4(s) + H2(g) ΔH2 =-57.2 kJ·mol-1
Fe3O4(s) + H2(g) ΔH2 =-57.2 kJ·mol-1
C(s)+CO2 2CO(g) ΔH3 =+172.4 kJ·mol-1 。
2CO(g) ΔH3 =+172.4 kJ·mol-1 。
铁氧化物循环裂解水制氢气总反应的热化学方程式是_________ 。
②下图表示其他条件一定时,Fe3O4(s)和CO(g)反应达平衡时 CO(g)的体积百分含量随温度的变化关系。
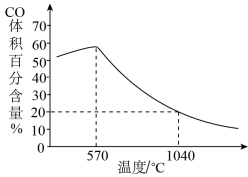
i. 当温度低于570℃时,温度降低CO的转化率____ (填“增大”、“减小”或“不变”),理由是______ 。
ii. 当温度高于570℃时,随温度升高,反应 Fe3O4(s) + CO(g) 3FeO(s) + CO2(g)平衡常数的变化趋势是
3FeO(s) + CO2(g)平衡常数的变化趋势是________ ;(填“增大”、“减小”或“不变”)1040℃时,该反应的化学平衡常数的数值是________ 。
(3)①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应 ii 的离子方程式是_______________ 。
②如今基于普鲁士蓝合成原理可检测食品中 CN-,方案如下:
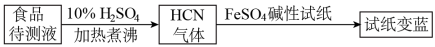
若试纸变蓝则证明食品中含有 CN-,请解释检测时试纸变蓝的原因_________ 。
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配置100mL 5mol/LFeCl3溶液,为使配置过程中不出现浑浊现象,则至少需要加入2mol/L的盐酸_________ mL(忽略加入盐酸体积)。
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是
a. Fe b. FeO c. Fe3O4 d. Fe2O3
(2)现代利用铁的氧化物循环裂解水制氢气的过程如下图所示。 整个过程与温度密切相关, 当温度低于 570℃时,反应Fe3O4(s)+4 CO(g)
 3Fe(s)+4CO2(g),阻碍循环反应的进行。
3Fe(s)+4CO2(g),阻碍循环反应的进行。
①已知:Fe3O4(s) + CO(g)
 3FeO(s) +CO2(g) ΔH1 = +19.3 kJ·mol-1
3FeO(s) +CO2(g) ΔH1 = +19.3 kJ·mol-13FeO(s) + H2O(g)
 Fe3O4(s) + H2(g) ΔH2 =-57.2 kJ·mol-1
Fe3O4(s) + H2(g) ΔH2 =-57.2 kJ·mol-1C(s)+CO2
 2CO(g) ΔH3 =+172.4 kJ·mol-1 。
2CO(g) ΔH3 =+172.4 kJ·mol-1 。铁氧化物循环裂解水制氢气总反应的热化学方程式是
②下图表示其他条件一定时,Fe3O4(s)和CO(g)反应达平衡时 CO(g)的体积百分含量随温度的变化关系。

i. 当温度低于570℃时,温度降低CO的转化率
ii. 当温度高于570℃时,随温度升高,反应 Fe3O4(s) + CO(g)
 3FeO(s) + CO2(g)平衡常数的变化趋势是
3FeO(s) + CO2(g)平衡常数的变化趋势是(3)①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应 ii 的离子方程式是
②如今基于普鲁士蓝合成原理可检测食品中 CN-,方案如下:

若试纸变蓝则证明食品中含有 CN-,请解释检测时试纸变蓝的原因
(4)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,此温度下若在实验室中配置100mL 5mol/LFeCl3溶液,为使配置过程中不出现浑浊现象,则至少需要加入2mol/L的盐酸
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】源开发和利用是科学研究的热点课题。
(1)几个有关CO的热化学方程式如下:
I.CO(g)+2H2(g)⇌CH3OH(g) ∆H1
II.2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ∆H2
III.CO(g)+H2O(g)⇌CO2(g)+H2(g) ∆H3
则3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g) ∆H=_______ (用含∆H1、∆H2、∆H3的代数表示)。
(2)在1L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ∆H,测得CH3OH的浓度与温度的关系如图所示:
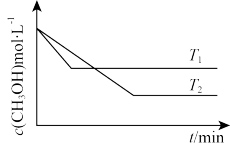
则T1_______ T2;∆H_______ 0(填“>”“<”或“=”)。
(3)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g)⇌CH3OH(g) ∆H=-91.0kJ·mol-1,向1L的恒容密容器中加入0.1molH2和0.05molCO在一定温度下发生上述反应,10min后反应达到平衡状态,测得放出的热量为3.64kJ。
①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为_______ 。
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01molH2和0.05molCH3OH(g)时,平衡_______ (填“向左移动”、“向右移动”或“不移动”)。
(4)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H=-49.5kJ·mol-1
II.CO(g)+2H2(g)⇌CH3OH(g) ∆H2=-90.4kJ·mol-1
III.CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H3
一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的浓度为_______ mol·L-1(用含a、b、V的代数式表示,下同),反应III的平衡常数为_______ 。
(1)几个有关CO的热化学方程式如下:
I.CO(g)+2H2(g)⇌CH3OH(g) ∆H1
II.2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ∆H2
III.CO(g)+H2O(g)⇌CO2(g)+H2(g) ∆H3
则3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g) ∆H=
(2)在1L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ∆H,测得CH3OH的浓度与温度的关系如图所示:

则T1
(3)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g)⇌CH3OH(g) ∆H=-91.0kJ·mol-1,向1L的恒容密容器中加入0.1molH2和0.05molCO在一定温度下发生上述反应,10min后反应达到平衡状态,测得放出的热量为3.64kJ。
①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01molH2和0.05molCH3OH(g)时,平衡
(4)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H=-49.5kJ·mol-1
II.CO(g)+2H2(g)⇌CH3OH(g) ∆H2=-90.4kJ·mol-1
III.CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H3
一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的浓度为
您最近一年使用:0次
【推荐1】中国在氢能研究方面已取得显著进展。绿氢的生产及储存作为氢能利用的关键技术,是当前关注的热点之一、
I.制氢
(1)化学制氢。工业上制取氢气时涉及的一个重要反应是: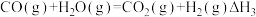
已知:①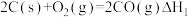
②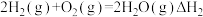
利用 和
和 计算
计算 时,还需要利用
时,还需要利用_______ 反应的 。
。
(2)电化学制氢。光、电催化——化学环反应耦合分解 制
制 的原理示意图如下图所示。
的原理示意图如下图所示。_______ 。
②除了 外,
外,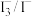 也能实现如图所示循环过程。结合化学用语,说明
也能实现如图所示循环过程。结合化学用语,说明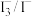 能够使S源源不断产生的原因:
能够使S源源不断产生的原因:_______ 。
Ⅱ.储氢与释氢
(3) 是一种重要的储氢载体,能与水反应生成
是一种重要的储氢载体,能与水反应生成 ,且反应前后B的化合价不变,反应消耗
,且反应前后B的化合价不变,反应消耗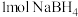 时转移的电子数目为
时转移的电子数目为_______ 。
(4)有机物释氢与储氢。其中一种方法为利用环己烷和苯之间的可逆反应来实现释氢和储氢。
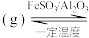
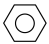
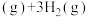
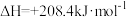 。
。
①在某温度下,向恒容容器中加入环己烷,其起始浓度为 ,平衡时苯的浓度为
,平衡时苯的浓度为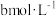 ,该反应的平衡常数
,该反应的平衡常数
_______ 。
②有利于释氢的措施为:_______ (从反应限度的角度回答)。
(5)一定条件下,下图所示装置可实现有机物的电化学储氢(忽略其它有机物)。_______ 。
②该储氢装置的电流效率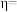
_______ 。( )(计算结果保留小数点后一位)
)(计算结果保留小数点后一位)
I.制氢
(1)化学制氢。工业上制取氢气时涉及的一个重要反应是:
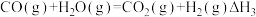
已知:①
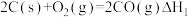
②
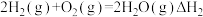
利用
 和
和 计算
计算 时,还需要利用
时,还需要利用 。
。(2)电化学制氢。光、电催化——化学环反应耦合分解
 制
制 的原理示意图如下图所示。
的原理示意图如下图所示。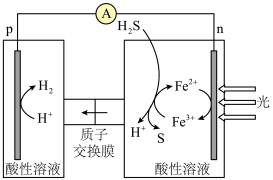
②除了
 外,
外,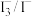 也能实现如图所示循环过程。结合化学用语,说明
也能实现如图所示循环过程。结合化学用语,说明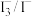 能够使S源源不断产生的原因:
能够使S源源不断产生的原因:Ⅱ.储氢与释氢
(3)
 是一种重要的储氢载体,能与水反应生成
是一种重要的储氢载体,能与水反应生成 ,且反应前后B的化合价不变,反应消耗
,且反应前后B的化合价不变,反应消耗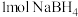 时转移的电子数目为
时转移的电子数目为(4)有机物释氢与储氢。其中一种方法为利用环己烷和苯之间的可逆反应来实现释氢和储氢。

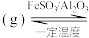

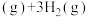
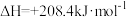 。
。①在某温度下,向恒容容器中加入环己烷,其起始浓度为
 ,平衡时苯的浓度为
,平衡时苯的浓度为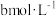 ,该反应的平衡常数
,该反应的平衡常数
②有利于释氢的措施为:
(5)一定条件下,下图所示装置可实现有机物的电化学储氢(忽略其它有机物)。
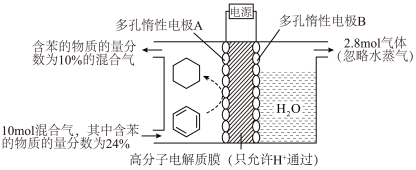
②该储氢装置的电流效率
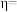
 )(计算结果保留小数点后一位)
)(计算结果保留小数点后一位)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】研究减少CO2排放是一项重要课题。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应Ⅰ:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.6 kJ/mol
CH3OH(g)+H2O(g) △H1=-49.6 kJ/mol
反应Ⅱ:CH3OCH3(g)+H2O(g) 2CH3OH(g) △H2=+23.4 kJ/mol
2CH3OH(g) △H2=+23.4 kJ/mol
反应Ⅲ:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H3
CH3OCH3(g)+3H2O(g) △H3
(1)△H3=________ kJ/mol。
(2)恒温恒容条件下,在密闭容器中通入等物质的量的CO2和H2,发生反应I。下列描述能说明反应I达到平衡状态的是_______ (填序号)。
A.反应体系总压强保持不变
B.容器内的混合气体的密度保持不变
C.水分子中断裂2NA个H-O键,同时氢分子中断裂3NA个H-H键
D.CH3OH和H2O的浓度之比保持不变
(3)反应II在某温度下的平衡常数为0.25,此温度下,在密闭容器中加入等物质的量的CH3OCH3(g)和H2O(g),反应到某时刻测得各组分浓度如下:
此时v正___ v逆(填“>”、“<”或“=”),当反应达到平衡状态时,混合气体中CH3OH体积分数(CH3OH)% =___ %。
(4)在某压强下,反应III在不同温度、不同投料比时,CO2的平衡转化率如图所示。T1温度下,将6mol CO2和12mol H2充入2 L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率v(CH3OCH3)=____ ;KA、KB、KC三者之间的大小关系为____ 。

(5)恒压下将CO2和H2按体积比1:3混合,在不同催化剂作用下发生反应I和反应III,在相同的时间段内CH3OH的选择性和产率随温度的变化如图。其中:CH3OH的选择性=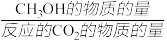 ×100%
×100%
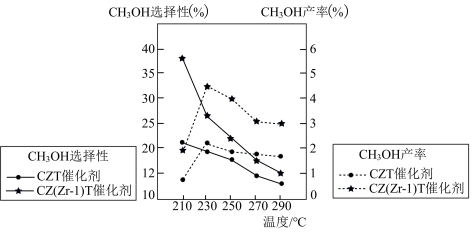
在上述条件下合成甲醇的工业条件是____ 。
A.210℃ B.230℃ C.催化剂CZT D.催化剂CZ(Zr-1)T
反应Ⅰ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.6 kJ/mol
CH3OH(g)+H2O(g) △H1=-49.6 kJ/mol反应Ⅱ:CH3OCH3(g)+H2O(g)
 2CH3OH(g) △H2=+23.4 kJ/mol
2CH3OH(g) △H2=+23.4 kJ/mol反应Ⅲ:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g) △H3
CH3OCH3(g)+3H2O(g) △H3(1)△H3=
(2)恒温恒容条件下,在密闭容器中通入等物质的量的CO2和H2,发生反应I。下列描述能说明反应I达到平衡状态的是
A.反应体系总压强保持不变
B.容器内的混合气体的密度保持不变
C.水分子中断裂2NA个H-O键,同时氢分子中断裂3NA个H-H键
D.CH3OH和H2O的浓度之比保持不变
(3)反应II在某温度下的平衡常数为0.25,此温度下,在密闭容器中加入等物质的量的CH3OCH3(g)和H2O(g),反应到某时刻测得各组分浓度如下:
| 物质 | CH3OCH3(g) | H2O(g) | CH3OH(g) |
| 浓度/mol·L-1 | 1.8 | 1.8 | 0.4 |
(4)在某压强下,反应III在不同温度、不同投料比时,CO2的平衡转化率如图所示。T1温度下,将6mol CO2和12mol H2充入2 L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率v(CH3OCH3)=

(5)恒压下将CO2和H2按体积比1:3混合,在不同催化剂作用下发生反应I和反应III,在相同的时间段内CH3OH的选择性和产率随温度的变化如图。其中:CH3OH的选择性=
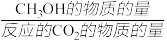 ×100%
×100%
在上述条件下合成甲醇的工业条件是
A.210℃ B.230℃ C.催化剂CZT D.催化剂CZ(Zr-1)T
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】二甲醚又称甲醚(CH3OCH3),简称DME,是清洁、高效的新型燃料。
Ⅰ.由合成气(CO、H2)制备二甲醚的反应原理如下:
①
②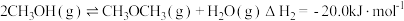
③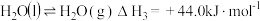
回答下列问题:
(1)由合成气(CO、H2)制备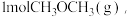 且生成
且生成  其热化学方程式为
其热化学方程式为_______ 。
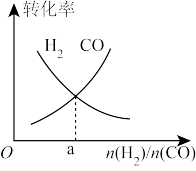
(2)一定条件下在恒温恒容的密闭容器中,按不同投料比充入CO(g)和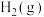 进行反应①,平衡时CO(g)和
进行反应①,平衡时CO(g)和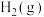 的转化率如图所示,则a=
的转化率如图所示,则a= _______ (填数值)。
(3)在体积一定的密闭容器中发生反应②,如果该反应的平衡常数 值变小,下列说法正确的是_______(填序号)。
值变小,下列说法正确的是_______(填序号)。
Ⅱ.由合成气(CO2、H2)制备二甲醚的反应原理如下:
④
⑤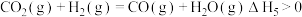
(4)若在体积为2L的密闭容器中,控制 流速为
流速为 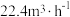 (已换算为标准状况),
(已换算为标准状况),  的转化率为80.0%,则
的转化率为80.0%,则  的反应速率为
的反应速率为_______ 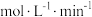 (保留三位有效数字)。
(保留三位有效数字)。
(5)在恒压条件下,按 与
与  的物质的量之比为1:3投料,测得
的物质的量之比为1:3投料,测得  平衡转化率和平衡时CO的选择性转化的
平衡转化率和平衡时CO的选择性转化的 中生成CO的物质的量分数)随温度的变化如图所示:
中生成CO的物质的量分数)随温度的变化如图所示:
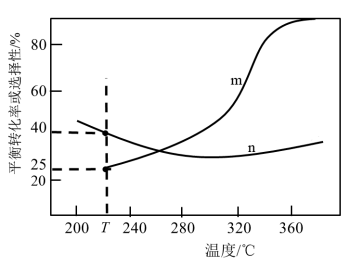
①曲线n随温度升高显示如图所示变化的原因是_______ 。
②T℃时反应⑤的平衡常数K=_______ (保留两位有效数字)。
③合成甲醚的适宜温度为260℃, 理由是_______ 。
④其他条件不变,改为恒容条件,CO平衡选择性比恒压条件下的平衡选择性_______ (填“高”“低”或“不变”)。
Ⅰ.由合成气(CO、H2)制备二甲醚的反应原理如下:
①

②
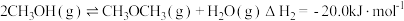
③
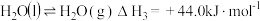
回答下列问题:
(1)由合成气(CO、H2)制备
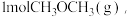 且生成
且生成  其热化学方程式为
其热化学方程式为(2)一定条件下在恒温恒容的密闭容器中,按不同投料比充入CO(g)和
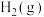 进行反应①,平衡时CO(g)和
进行反应①,平衡时CO(g)和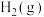 的转化率如图所示,则a=
的转化率如图所示,则a= 
(3)在体积一定的密闭容器中发生反应②,如果该反应的平衡常数
 值变小,下列说法正确的是_______(填序号)。
值变小,下列说法正确的是_______(填序号)。| A.平衡向正反应方向移动 | B.平衡移动的原因是升高了温度 |
| C.达到新平衡后体系的压强不变 | D.容器中 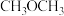 的体积分数减小 的体积分数减小 |
Ⅱ.由合成气(CO2、H2)制备二甲醚的反应原理如下:
④

⑤
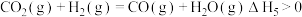
(4)若在体积为2L的密闭容器中,控制
 流速为
流速为 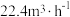 (已换算为标准状况),
(已换算为标准状况),  的转化率为80.0%,则
的转化率为80.0%,则  的反应速率为
的反应速率为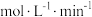 (保留三位有效数字)。
(保留三位有效数字)。(5)在恒压条件下,按
 与
与  的物质的量之比为1:3投料,测得
的物质的量之比为1:3投料,测得  平衡转化率和平衡时CO的选择性转化的
平衡转化率和平衡时CO的选择性转化的 中生成CO的物质的量分数)随温度的变化如图所示:
中生成CO的物质的量分数)随温度的变化如图所示:
①曲线n随温度升高显示如图所示变化的原因是
②T℃时反应⑤的平衡常数K=
③合成甲醚的适宜温度为260℃, 理由是
④其他条件不变,改为恒容条件,CO平衡选择性比恒压条件下的平衡选择性
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】(1)①常温下,.某溶液中由水电离出的c(OH-)=1.0×10-10mol/L,该溶液可以是_________ 。(填选项)
A. pH=4的CH3COOH B.pH=10的NaOH C. pH=9的 Na2CO3
D. pH=2的 H2SO4 E. pH=4的 NH4C1
(2)常温下,aml/0.lmol/L盐酸与bmL0.lmol/L氨水混合,充分反应,若混合后溶液呈中性,则a____ b (填“<”、“>”或“=”)。
(3)常温下,amLpH=3的盐酸与bmLpH=11的氨水混合,充分反应,若a=b,,则反应后溶液中离子浓度从大到小的顺序是___________ 。
(4)氯化铝水溶液呈酸性,原因是(用离子方程式表示〉:___________ 。把A1Cl3溶液蒸干,灼烧,最后得到的主要固体产物是___________ 。
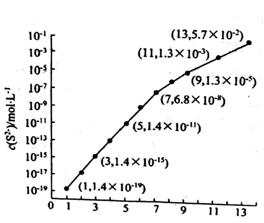
(5)25℃,在0.10 mol/LH2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如下图(忽略溶液体积的变化、H2S的挥发)。
① pH=13时,溶液中的 c(H2S)+c(HS-)=_________ mol/L。
② 某溶液含 0.020 mol /LMn2+、0.10 mol/LH2S,当溶液pH=_____ 时,Mn2+开始沉淀。(Ksp(MnS) =2.8×10−13)
A. pH=4的CH3COOH B.pH=10的NaOH C. pH=9的 Na2CO3
D. pH=2的 H2SO4 E. pH=4的 NH4C1
(2)常温下,aml/0.lmol/L盐酸与bmL0.lmol/L氨水混合,充分反应,若混合后溶液呈中性,则a
(3)常温下,amLpH=3的盐酸与bmLpH=11的氨水混合,充分反应,若a=b,,则反应后溶液中离子浓度从大到小的顺序是
(4)氯化铝水溶液呈酸性,原因是(用离子方程式表示〉:
(5)25℃,在0.10 mol/LH2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如下图(忽略溶液体积的变化、H2S的挥发)。
① pH=13时,溶液中的 c(H2S)+c(HS-)=
② 某溶液含 0.020 mol /LMn2+、0.10 mol/LH2S,当溶液pH=

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】I.高铁酸钾(K2FeO4)具有很强的氧化性,在生产,生活中有广泛应用。
(1)K2FeO4常用做高效水处理剂,其两种作用分别是_____ 。
(2)制备K2FeO4可以采用湿式氧化法,流程如图:

已知:①温度较低时,Cl2通入KOH溶液生成次氯酸盐;温度较高时,Cl2通入KOH溶液生成氯酸盐;②Fe(NO3)3溶液与KClO溶液在强碱性环境中生成K2FeO4。请回答下列问题:
①该生产工艺应在_____ (填“温度较高”或“温度较低”)的情况下进行。
②写出产生K2FeO4的离子方程式_________ 。
(3)实验室模拟工业电解法制取K2FeO4,装置如图.
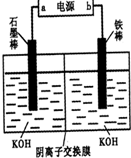
①此装置中电源的负极是______ (填“a”或“b”).
②阳极的电极反应式为______ .
II.常温下,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8。试回答以下问题:
(1)混合溶液的pH=8的原因_____________ (用离子方程式表示)。
(2)混合溶液中由水电离出的c(H+)_____ (填“>”、“<”或“=”)0.1mol/LNaOH溶液中由水电离出的c(H+)。
(1)K2FeO4常用做高效水处理剂,其两种作用分别是
(2)制备K2FeO4可以采用湿式氧化法,流程如图:

已知:①温度较低时,Cl2通入KOH溶液生成次氯酸盐;温度较高时,Cl2通入KOH溶液生成氯酸盐;②Fe(NO3)3溶液与KClO溶液在强碱性环境中生成K2FeO4。请回答下列问题:
①该生产工艺应在
②写出产生K2FeO4的离子方程式
(3)实验室模拟工业电解法制取K2FeO4,装置如图.

①此装置中电源的负极是
②阳极的电极反应式为
II.常温下,如果取0.1mol/LHA溶液与0.1mol/LNaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8。试回答以下问题:
(1)混合溶液的pH=8的原因
(2)混合溶液中由水电离出的c(H+)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】雪碧、可乐是深受人们青睐的碳酸型饮料.
Ⅰ.雪琩是一款柠檬味汽水饮料,其中所含酸性物质包括碳酸、柠檬酸、苯甲酸. 时,上述三种酸的电离常数如表所示:
时,上述三种酸的电离常数如表所示:
(1)上述三种酸的酸性由强到弱的顺序为____________ (填字母并用“>”符号连接)。
a.苯甲酸 b.碳酸 c.柠檬酸
(2)水中存在平衡 ,欲使平衡向右移动且溶液显碱性,下列方法可行的是
,欲使平衡向右移动且溶液显碱性,下列方法可行的是____________ (填字母)。
a.通入氨气 b.加入 c.加热至
c.加热至 d.加入
d.加入 固体
固体
(3)室温下,向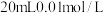 苯甲酸
苯甲酸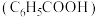 溶液中滴加等物质的量浓度的
溶液中滴加等物质的量浓度的 溶液,溶液的
溶液,溶液的 与加入
与加入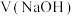 之间的关系如图所示,已知
之间的关系如图所示,已知 。
。

① 点溶液的
点溶液的
____________ (保留小数点后一位)。
②下列说法正确的有____________ 。
a.为准确判断滴定终点,可使用甲基橙做指示剂
b. 点溶液
点溶液 ,且有
,且有
c. 点溶液中一定存在
点溶液中一定存在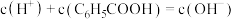
d.D点溶液中有
e.从 点到
点到 点,溶液中水的电离程度最小的是
点,溶液中水的电离程度最小的是 点
点
Ⅱ.可乐中的食品添加剂有白砂糖、二氧化碳、焦糖、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为 )有一定关系,已知磷酸电离常数为:
)有一定关系,已知磷酸电离常数为: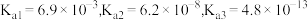
(4)室温下,测得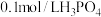 溶液的
溶液的 ,原因是
,原因是____________ (用电离方程式表示)。
(5)向含磷酸的溶液中滴加 溶液,此过程中各含磷微粒在溶液中的物质的量分数与
溶液,此过程中各含磷微粒在溶液中的物质的量分数与 的关系如图所示:
的关系如图所示:
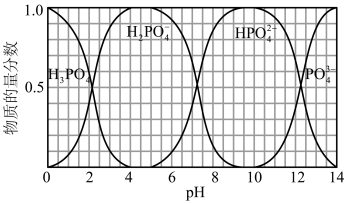
①溶液 由11增大到14的过程中,发生反应的离子方程式为
由11增大到14的过程中,发生反应的离子方程式为____________ 。
②若已知碳酸的电离常数,将磷酸滴入碳酸钠溶液中,发生反应的离子方程式错误的为____________ 。
A.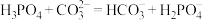 B.
B.
C.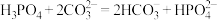 D.
D.
Ⅰ.雪琩是一款柠檬味汽水饮料,其中所含酸性物质包括碳酸、柠檬酸、苯甲酸.
 时,上述三种酸的电离常数如表所示:
时,上述三种酸的电离常数如表所示:| 物质 | 苯甲酸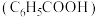 | 碳酸 | 柠檬酸 |
| 电离常数 |  |  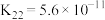 | 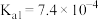 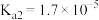  |
(1)上述三种酸的酸性由强到弱的顺序为
a.苯甲酸 b.碳酸 c.柠檬酸
(2)水中存在平衡
 ,欲使平衡向右移动且溶液显碱性,下列方法可行的是
,欲使平衡向右移动且溶液显碱性,下列方法可行的是a.通入氨气 b.加入
 c.加热至
c.加热至 d.加入
d.加入 固体
固体(3)室温下,向
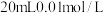 苯甲酸
苯甲酸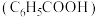 溶液中滴加等物质的量浓度的
溶液中滴加等物质的量浓度的 溶液,溶液的
溶液,溶液的 与加入
与加入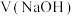 之间的关系如图所示,已知
之间的关系如图所示,已知 。
。
①
 点溶液的
点溶液的
②下列说法正确的有
a.为准确判断滴定终点,可使用甲基橙做指示剂
b.
 点溶液
点溶液 ,且有
,且有
c.
 点溶液中一定存在
点溶液中一定存在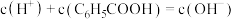
d.D点溶液中有

e.从
 点到
点到 点,溶液中水的电离程度最小的是
点,溶液中水的电离程度最小的是 点
点Ⅱ.可乐中的食品添加剂有白砂糖、二氧化碳、焦糖、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为
 )有一定关系,已知磷酸电离常数为:
)有一定关系,已知磷酸电离常数为: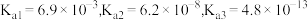
(4)室温下,测得
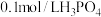 溶液的
溶液的 ,原因是
,原因是(5)向含磷酸的溶液中滴加
 溶液,此过程中各含磷微粒在溶液中的物质的量分数与
溶液,此过程中各含磷微粒在溶液中的物质的量分数与 的关系如图所示:
的关系如图所示:
①溶液
 由11增大到14的过程中,发生反应的离子方程式为
由11增大到14的过程中,发生反应的离子方程式为②若已知碳酸的电离常数,将磷酸滴入碳酸钠溶液中,发生反应的离子方程式错误的为
A.
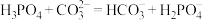 B.
B.
C.
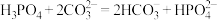 D.
D.
您最近一年使用:0次



