恒温恒容的密闭容器中,某催化剂表面发生氨的分解反应: ,测得不同起始浓度和催化剂表面积下氨的浓度随时间的变化
,测得不同起始浓度和催化剂表面积下氨的浓度随时间的变化
下列说法不正确的是
 ,测得不同起始浓度和催化剂表面积下氨的浓度随时间的变化
,测得不同起始浓度和催化剂表面积下氨的浓度随时间的变化| 编号 | 时间/min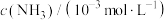 表面积/cm  | 0 | 20 | 40 | 60 | 80 |
| ① | a | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| ② | a | 1.20 | 0.80 | 0.40 | x | |
| ③ | 2a | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
A.实验①,0∼40min,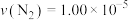 mol⋅L mol⋅L ∙min ∙min |
| B.相同条件下,增加氨气的浓度,反应速率增大 |
| C.相同条件下,增加催化剂的表面积,反应速率增大 |
D.实验②,60min时处于平衡状态, |
2022高三·全国·专题练习 查看更多[31]
安徽省淮北市树人高级中学2023-2024学年高二下学期开学考试化学试题上海市建平世纪中学2023-2024学年高二上学期阶段练习二 化学(等级)试题(已下线)题型10 反应微观机理分析 速率方程及其应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)吉林省长春市第二实验中学2023-2024学年高二上学期10月月考化学试题北京师范大学附属中学2022-2023学年高二上学期10月月考化学试题河南省周口恒大中学2023-2024学年高二上学期11月期中考试化学试题(已下线)考点2 化学平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)第二章 章末训练(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)考点21 化学反应速率(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第13练 化学反应速率与化学平衡的综合考查 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)上海市奉贤区2022-2023学年高三上学期一模练习卷化学试题安徽省六安第一中学2022-2023学年高二上学期期末考试化学试题辽宁省营口市2022-2023学年高三上学期期末考试化学试题安徽省合肥一六八中学2022-2023学年高二上学期化学学科学情调研试题(已下线)专题09 化学反应速率与化学平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)化学预测卷(五)-预测卷(浙江专版)(已下线)2023年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷A黑龙江省佳木斯市第一中学2022-2023学年高三上学期第三次调研化学试题天津市五校(杨村宝坻蓟州芦台静海一中)2022-2023学年高二上学期期中考试化学试题(已下线)易错点22 化学反应平衡和移动-备战2023年高考化学考试易错题(已下线)易错点21 化学反应速率-备战2023年高考化学考试易错题(已下线)第19讲 化学平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)辽宁省朝阳市建平县实验中学2022-2023学年高二上学期第一次月考化学试题江西省新余市第一中学2022-2023学年高二上学期开学考试化学试题浙江省浙里卷天下2022-2023学年高三8月开学测试化学试题(已下线)第20讲 化学反应速率(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第16练 化学反应的速率与限度-2023年高考化学一轮复习小题多维练(全国通用)黑龙江省鹤岗市第一中学2021-2022学年高一下学期期末考试化学试题黑龙江省双鸭山市第一中学2021-2022学年高一下学期期末考试化学试题(已下线)考点21 化学反应速率-备战2023年高考化学一轮复习考点帮(全国通用)
更新时间:2023-11-23 22:53:49
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】已知:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H= -49.0kJ·mol-1。一定条件下,向体积为1L的密闭容器中充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示,下列叙述中正确的是
CH3OH(g)+H2O(g) △H= -49.0kJ·mol-1。一定条件下,向体积为1L的密闭容器中充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示,下列叙述中正确的是
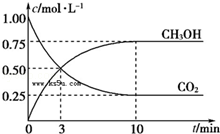
 CH3OH(g)+H2O(g) △H= -49.0kJ·mol-1。一定条件下,向体积为1L的密闭容器中充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示,下列叙述中正确的是
CH3OH(g)+H2O(g) △H= -49.0kJ·mol-1。一定条件下,向体积为1L的密闭容器中充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示,下列叙述中正确的是
| A.欲增大平衡状态时c(CH3OH)/c(CO2)的比值, 可采用 升高温度的方法 |
| B.3min时,CO2的消耗速率等于CH3OH的生成速率,且二者浓度相同 |
| C.欲提高H2的平衡转化率只能减小反应容器的体积 |
| D.从反应开始到平衡,CO2的平均反应速率v(CO2)=0.025mol·L﹣1·min﹣1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】向体积为4L的固定密闭容器中通入5molX气体,在一定温度下发生如下反应: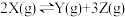 ,经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则下列说法正确的
,经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则下列说法正确的
①用Y表示的速率为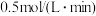
②若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:甲: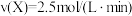 ;乙:
;乙: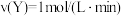 ;丙:
;丙: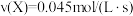 。若其它条件相同,温度不同,则温度由高到低的顺序是丙>甲>乙
。若其它条件相同,温度不同,则温度由高到低的顺序是丙>甲>乙
③若向达到平衡的体系中充入不参加反应的氮气,则平衡向左移动
④若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为1.5<c≤7.5
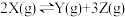 ,经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则下列说法正确的
,经5min后反应达到平衡,此时测得容器内的压强为起始时的1.2倍,则下列说法正确的①用Y表示的速率为
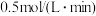
②若上述反应在甲、乙、丙、丁四个同样的密闭容器中进行,在同一段时间内测得容器内的反应速率分别为:甲:
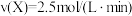 ;乙:
;乙: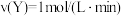 ;丙:
;丙: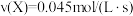 。若其它条件相同,温度不同,则温度由高到低的顺序是丙>甲>乙
。若其它条件相同,温度不同,则温度由高到低的顺序是丙>甲>乙③若向达到平衡的体系中充入不参加反应的氮气,则平衡向左移动
④若保持温度和体积不变,起始时加入X、Y、Z物质的量分别为amol、bmol、cmol,达到平衡时仍与(1)的平衡等效,且起始时维持化学反应向逆反应方向进行,则c的取值范围应该为1.5<c≤7.5
| A.①④ | B.①② | C.②③ | D.②④ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】在容积不变的密闭容器中通入一定量的A发生反应:2A(g) B(g)+C(g) ΔH>0,T1温度下的部分实验数据为:
B(g)+C(g) ΔH>0,T1温度下的部分实验数据为:
下列说法正确的是
 B(g)+C(g) ΔH>0,T1温度下的部分实验数据为:
B(g)+C(g) ΔH>0,T1温度下的部分实验数据为:| t/s | 0 | 500 | 1 000 | 1 500 |
| c(A)/(mol·L-1) | 6.00 | 3.50 | 3.00 | 3.00 |
下列说法正确的是
| A.500 s内A的分解速率为3.0×10-3mol·L-1·s-1 |
| B.1 000 s时A的转化率为50%,T1温度下的平衡常数为K1=0.75 |
| C.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若K1>K2,则T1>T2 |
| D.平衡时,其他条件不变,再加入一定量的A,达新平衡后K值增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】某同学设计实验探究镁与铵盐溶液的反应,仔细分析以下记录后,所得结论正确的是
| 实验编号 | ① | ② | ③ | ④ |
| 溶液种类 |   |   |   |  |
m( )/g )/g | 0.48 | 0.48 | 0.48 | 0.48 |
| V(溶液)/mL | 100 | 100 | 100 | 100 |
| 实验现象 | 有气体产生,并产生白色沉淀 | 有气体产生,并产生白色沉淀 | 有气体产生,并产生白色沉淀 | 几乎看不到现象 |
6h时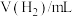 | 433 | 255 | 347 | 12 |
A.实验中产生的气体仅为 ,沉淀为 ,沉淀为 |
B.由实验①②可得,溶液中阴离子的浓度或种类对产生 的速率有影响 的速率有影响 |
C.由实验①③可得,溶液中 越大,反应速率越快 越大,反应速率越快 |
D.由实验①~④可得,溶液的 越小,产生 越小,产生 的速率越快 的速率越快 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】 下列图示与对应的叙述一致的是


| A.图1表示在新型催化剂作用下利用太阳能使水分解的能量变化曲线 |
| B.图2表示KNO3溶解度曲线,α点所示溶液为50℃时的不饱和溶液 |
| C.图3表示常温下pH=2的HCl溶液加水稀释倍数与pH的变化关系 |
| D.图4表示10ml 0.01ml/L KMnO4酸性溶液与过量的0.1mol/L H2C2O4溶液混合时,n(Mn2+)随时间的变化(Mn2+对该反应有催化作用) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】对Pd单原子催化剂(Pd/SVG)上H2还原NO的反应进行研究,发现Pd/SVG上NO被还原生成N2和NH3的路径机理如图所示:
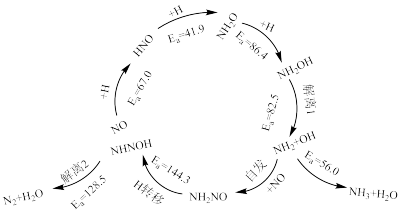
下列说法正确的是

下列说法正确的是
| A.Pd/SVG可以改变NO的平衡转化率 |
| B.NO被还原为N2的总反应为2NO+2H2=N2+2H2O |
| C.NO被还原为NH3的反应决速步为解离1反应 |
| D.Pd/SVG上H2还原NO过程中产物N2的形成更容易 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】在催化剂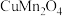 表面的
表面的 选择性催化还原NO的反应机理如下图所示(如)
选择性催化还原NO的反应机理如下图所示(如) 吸附在催化剂表面可表示为
吸附在催化剂表面可表示为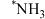 ,Ea表示活化能)。
,Ea表示活化能)。
 表面的
表面的 选择性催化还原NO的反应机理如下图所示(如)
选择性催化还原NO的反应机理如下图所示(如) 吸附在催化剂表面可表示为
吸附在催化剂表面可表示为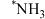 ,Ea表示活化能)。
,Ea表示活化能)。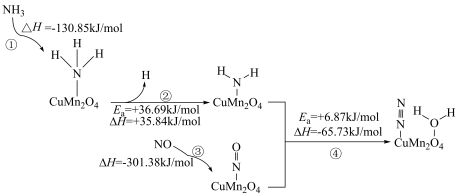
| A.该反应温度越高,反应速率越快 |
B. 比NO更易被催化剂 比NO更易被催化剂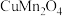 吸附 吸附 |
| C.反应过程中有非极性键的断裂与极性键的形成 |
D.决定总反应速率的基元反应可表示为: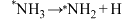 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】向体积为 的某恒容密闭容器中充入
的某恒容密闭容器中充入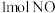 和
和 ,发生反应:
,发生反应:
 。已知反应体系的平衡温度与起始温度相同,体系总压强
。已知反应体系的平衡温度与起始温度相同,体系总压强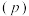 与时间
与时间 的关系如图中曲线I所示,曲线II为只改变某一条件体系总压强随时间的变化曲线。下列说法正确的是。
的关系如图中曲线I所示,曲线II为只改变某一条件体系总压强随时间的变化曲线。下列说法正确的是。
 的某恒容密闭容器中充入
的某恒容密闭容器中充入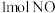 和
和 ,发生反应:
,发生反应:
 。已知反应体系的平衡温度与起始温度相同,体系总压强
。已知反应体系的平衡温度与起始温度相同,体系总压强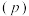 与时间
与时间 的关系如图中曲线I所示,曲线II为只改变某一条件体系总压强随时间的变化曲线。下列说法正确的是。
的关系如图中曲线I所示,曲线II为只改变某一条件体系总压强随时间的变化曲线。下列说法正确的是。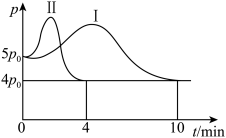
A. ,曲线II改变的条件可能是加入了催化剂 ,曲线II改变的条件可能是加入了催化剂 |
B. 内,曲线I对应的 内,曲线I对应的 |
C.4 时曲线I、II对应的 时曲线I、II对应的 的转化率均为80% 的转化率均为80% |
D.曲线I条件下,反应达平衡时,向平衡体系中同时充入 和 和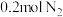 ,此时v(正)>v(逆) ,此时v(正)>v(逆) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】MTP是一类重要的药物中间体,可以由TOME经环化后合成。其反应式为:
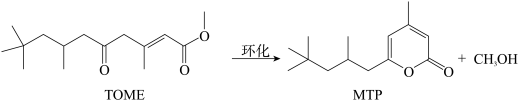
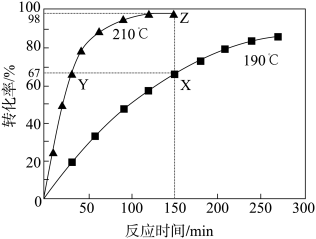
为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化率随反应时间的变化如图所示。设TOME的初始浓度为a mol/L,反应过程中的液体体积变化忽略不计。下列说法错误的是


为了提高TOME的转化率,反应进行时需及时从溶液体系中移出部分甲醇。TOME的转化率随反应时间的变化如图所示。设TOME的初始浓度为a mol/L,反应过程中的液体体积变化忽略不计。下列说法错误的是
| A.X、Y两点的MTP的物质的量浓度相等 |
| B.X、Z两点的瞬时速率大小为v(X)>v(Z) |
C.若Z点处于化学平衡,则210℃时反应的平衡常数K=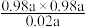 mol/L mol/L |
D.190℃时,0~150 min之间的MTP的平均反应速率为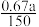 mol/(L·min) mol/(L·min) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】一定温度下,在甲、乙、丙三个体积均为10L的恒容密闭容器中分别发生反应 ,实验过程中测得的相关数据如下表所示。下列说法错误的是
,实验过程中测得的相关数据如下表所示。下列说法错误的是
 ,实验过程中测得的相关数据如下表所示。下列说法错误的是
,实验过程中测得的相关数据如下表所示。下列说法错误的是| 容器 | 温度/℃ | 物质的起始加入量 | 平衡时Z的物质的量 |
| 甲 | 1000 | 1molX、1molY、0molZ | 0.6mol |
| 乙 | 1000 | 2molX、2molY、0molZ | |
| 丙 | 1200 | 0molX、0molY、1molZ | 0.5mol |
| A.该反应的正反应放热 |
| B.平衡时逆反应速率:v(丙)>v(甲) |
| C.平衡时Z的物质的量:n(乙)>2n(甲) |
D.1200℃时,该反应的平衡常数 |
您最近一年使用:0次


 表示被吸附在催化剂表面的物种)。下列说法错误的是
表示被吸附在催化剂表面的物种)。下列说法错误的是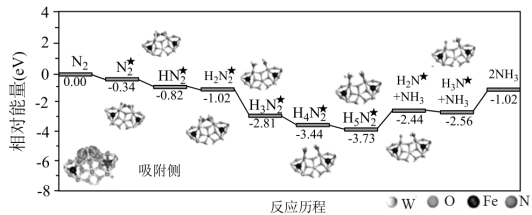
 ]越大,单位时间内合成氨的产量越高
]越大,单位时间内合成氨的产量越高

