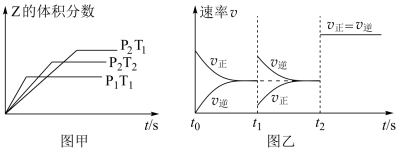
在一密闭容器中发生反应:2X(g)+Y(g) aZ(g) △H=QkJ/mol,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应,下列有关说法正确的是
aZ(g) △H=QkJ/mol,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应,下列有关说法正确的是
 aZ(g) △H=QkJ/mol,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应,下列有关说法正确的是
aZ(g) △H=QkJ/mol,开始按体积比2:1将X、Y充入反应器中,一定条件下发生反应,下列有关说法正确的是
| A.图甲,p1>p2 |
| B.图甲,T1<T2,Q>0 |
| C.图乙,t1时表示恒温、恒压条件下,向平衡体系中充入一定量的Z气体 |
| D.图乙,t2时表示压缩反应容器 |
更新时间:2023-11-29 19:39:11
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列实验操作、现象及结论均正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向盐酸溶液中滴入NaClO溶液,产生黄绿色气体 | 盐酸发生了分解反应 |
| B | 将淀粉水解液分成两份,向第一份中加入NaOH溶液至溶液呈碱性,加入银氨溶液并水浴加热,出现银镜;向第二份中滴加少量碘水,溶液变蓝 | 淀粉部分水解 |
| C | 铬酸钾溶液中存在平衡:2 (黄色)+2H+ (黄色)+2H+ H2O+ H2O+ (橙色),向黄色的铬酸钾溶液中加水稀释,溶液黄色加深 (橙色),向黄色的铬酸钾溶液中加水稀释,溶液黄色加深 | 平衡逆移 |
| D | 取A、B两支试管,各加入4mL0.01mol/L的H2C2O4溶液,然后向A试管中加入2mL0.01mol/酸性高锰酸钾溶液,同时向B试管中加入2mL0.02mo/L酸性高锰酸钾溶液,B试管褪色时间短 | 其他条件不变时,增大反应物的浓度,反应速率加快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】已知分解1 mol H2O2 放出热量98kJ,在含少量I-的溶液中,H2O2的分解机理为:第一步:H2O2+I-→ H2O +IO-(慢);第二步:H2O2+IO-→ H2O +O2+ I-(快)
下列有关反应的说法正确的是
下列有关反应的说法正确的是
| A.I-和IO-都是该反应的催化剂 |
| B.H2O2分解的速率取决于第二步反应的快慢 |
| C.反应物的总能量比生成物总能量低98kJ |
| D.第一步H2O2被还原,第二步H2O2被氧化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在不同浓度(c)、温度(T)条件下,蔗糖水解的瞬时速率(v)如下表,v 的单位为(mmol·L-1·min-1)。下列判断错误的是
| c(mol·L-1) T / K | 0.600 | 0.500 | 0.400 | 0.300 |
| 318.2 | 3.60 | 3.00 | a | 1.80 |
| 328.2 | 9.00 | 7.50 | 6.00 | 4.50 |
| b | 2.16 | 1.80 | 1.44 | 1.08 |
| A.318.2K,蔗糖起始浓度为0.400 mol·L-1,10min后蔗糖浓度略大于0.376 mol·L-1 |
| B.b K时,若蔗糖的浓度为0.35 mol·L-1,则v = 1.26 mmol·L-1·min-1 |
| C.b < 318.2 |
| D.若同时改变反应温度和蔗糖的浓度,则v肯定变化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】CO2催化加氢合成甲醇是重要的碳捕获利用与封存技术,该过程主要发生下列反应:
反应①:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-49.5kJ•mol-1
反应②:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=41.2kJ•mol-1
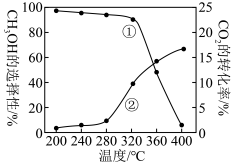
在0.5MPa条件下,将n(CO2)∶n(H2)为1∶3的混合气体以一定流速通过装有催化剂的反应器,实验测得CO2的转化率、CH3OH的选择性[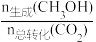 ×100%]与温度的关系如图所示。下列有关说法不正确的是
×100%]与温度的关系如图所示。下列有关说法不正确的是
反应①:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-49.5kJ•mol-1
反应②:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=41.2kJ•mol-1
在0.5MPa条件下,将n(CO2)∶n(H2)为1∶3的混合气体以一定流速通过装有催化剂的反应器,实验测得CO2的转化率、CH3OH的选择性[
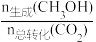 ×100%]与温度的关系如图所示。下列有关说法不正确的是
×100%]与温度的关系如图所示。下列有关说法不正确的是
| A.图中曲线①表示CH3OH的选择性随温度的变化 |
| B.一定温度下,增大起始n(CO2)∶n(H2)的比值,可提高H2的平衡转化率 |
| C.升高温度时,CO的选择性升高 |
| D.一定温度下,选用高效催化剂可提高CH3OH的平衡产率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】使用合适的催化剂进行乙酸直接加氢可制备乙醇,反应原理如下:
主反应:
副反应: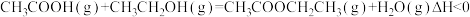 (热效应小可忽略)
(热效应小可忽略)
在密闭容器中控制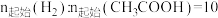 。2MPa下平衡时S(乙醇)和S(乙酸乙酯)随温度
。2MPa下平衡时S(乙醇)和S(乙酸乙酯)随温度
的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为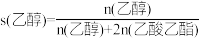 。下列说法正确的是
。下列说法正确的是
主反应:

副反应:
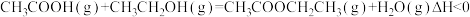 (热效应小可忽略)
(热效应小可忽略)在密闭容器中控制
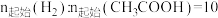 。2MPa下平衡时S(乙醇)和S(乙酸乙酯)随温度
。2MPa下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为
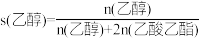 。下列说法正确的是
。下列说法正确的是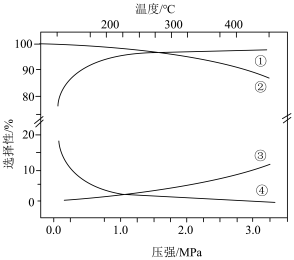
A.反应 |
| B.300℃、0.5MPa下,反应足够长时间,S(乙醇)<90% |
| C.图中曲线③表示250℃,乙醇选择性随压强变化的曲线 |
| D.曲线②变化的原因是随温度升高,副反应正向进行的程度减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】一定温度下可逆反应:A(s)+2B(g) 2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是

 2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
2C(g)+D(g) △H<0。现将1 mol A和2 mol B加入甲容器中,将4 mol C和2 mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动)。下列说法正确的是
| A.保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均减小 |
| B.保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
| C.保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
| D.保持温度不变,活塞P可自由移动,达到新的平衡后,乙中C的浓度和甲中C的浓度相等 |
您最近一年使用:0次
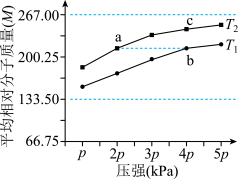
【推荐2】已知恒容密闭容器中发生反应:
 ,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示(已知:
,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示(已知: ,假设A的相对分子质量为267)。下列说法正确的是
,假设A的相对分子质量为267)。下列说法正确的是

 ,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示(已知:
,平衡体系中气体的平均相对分子质量(M)在不同温度下随压强的变化曲线如图所示(已知: ,假设A的相对分子质量为267)。下列说法正确的是
,假设A的相对分子质量为267)。下列说法正确的是
A. |
B.反应平衡常数: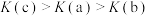 |
| C.当气体平均相对分子质量为200.25时,A的转化率约为50%(反应起始时B的浓度为0) |
D.若容器内发生反应: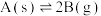 ,平衡后恒温压缩容器体积, ,平衡后恒温压缩容器体积, 的浓度不变 的浓度不变 |
您最近一年使用:0次
【推荐3】甲、乙两个密闭容器中均发生反应:C(s)+2H2O(g)  CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:
CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:
下列说法正确的是( )
 CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:
CO2(g)+2H2(g) ΔH>0,有关实验数据如下表所示:| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | 平衡常数 | |
| C(s) | H2O(g) | H2(g) | |||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 3.5 | K1 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 | K2 |
下列说法正确的是( )
| A.T1<T2 | B.乙容器中,当反应进行到1.5 min时,n(H2O)=1.4 mol |
| C.混合气体的密度始终保持不变 | D.K2=1.35 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】一定温度下,某密闭容器里发生如下反应:CO(g)+H2O(g) CO2(g)+H2(g) △H<0,当反应达到平衡式,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变的时,下列措施中可以采用的是( )
CO2(g)+H2(g) △H<0,当反应达到平衡式,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变的时,下列措施中可以采用的是( )
①升高温度②将容器容积压缩到原来的一半③再通入nmolCO2和nmolH2④再通入2nmolCO2和2nmolH2
 CO2(g)+H2(g) △H<0,当反应达到平衡式,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变的时,下列措施中可以采用的是( )
CO2(g)+H2(g) △H<0,当反应达到平衡式,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变的时,下列措施中可以采用的是( )①升高温度②将容器容积压缩到原来的一半③再通入nmolCO2和nmolH2④再通入2nmolCO2和2nmolH2
| A.①②④ | B.②④ | C.③④ | D.①②③ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在一密闭容器中,可逆反应:aA(g) + bB(g)  cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是
cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是
 cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是
cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是| A.a + b > c | B.平衡向正反应方向移动 |
| C.物质A的转化率降低 | D.物质C的质量分数增加 |
您最近一年使用:0次

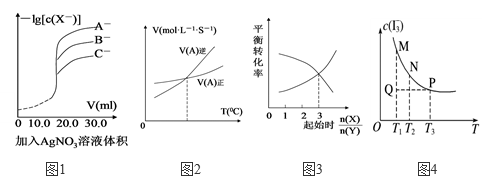

 CaO(s)+CO2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法不正确的是
CaO(s)+CO2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法不正确的是

