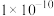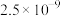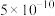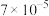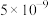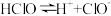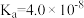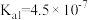描述弱电解质电离情况可以用电离度和电离平衡常数表示,常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),几种难(微)溶物的溶度积常数(Ksp)。
请回答下列问题
(1)下列能使醋酸溶液中CH3COOH的电离程度增大,电离常数不变__________(填字母序号)。
(2)CH3COONH4的水溶液呈__________ (填“酸性”、“中性”或“碱性”),该溶液中存在的各离子 浓度大小关系排序是__________ 。
(3)物质的量之比为 的
的 和
和 的混合溶液,该溶液中各
的混合溶液,该溶液中各离子 浓度从大到小的列排列为__________ 。
(4)工业中常将 转化为
转化为 ,具体做法是用饱和的纯碱溶液浸泡
,具体做法是用饱和的纯碱溶液浸泡 粉末,并不断补充纯碱,最后
粉末,并不断补充纯碱,最后 转化为
转化为 。
。
①写出该过程的离子方程式:__________ ;
②该反应的平衡常数为
__________ 。
酸或碱 | 电离平衡常数(Ka或Kb) | 难(微)溶物 | 溶度积常数(Ksp) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)下列能使醋酸溶液中CH3COOH的电离程度增大,电离常数不变__________(填字母序号)。
| A.升高温度 | B.加水稀释 |
| C.加少量的CH3COONa固体 | D.加少量冰醋酸 |
(3)物质的量之比为
 的
的 和
和 的混合溶液,该溶液中各
的混合溶液,该溶液中各(4)工业中常将
 转化为
转化为 ,具体做法是用饱和的纯碱溶液浸泡
,具体做法是用饱和的纯碱溶液浸泡 粉末,并不断补充纯碱,最后
粉末,并不断补充纯碱,最后 转化为
转化为 。
。①写出该过程的离子方程式:
②该反应的平衡常数为

更新时间:2023-12-14 21:35:21
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】氨氮废水可通过沉淀或氧化处理,使水中氨氮达到国家规定的排放标准后才可以排放。已知水溶液中氨氮的存在形式主要由pH决定。当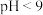 时,
时, 是主要存在形式;当
是主要存在形式;当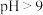 时,
时, 是主要存在形式。
是主要存在形式。
Ⅰ.沉淀法
向酸性废水中加入一定比例的 和
和 ,将氨氮转化为
,将氨氮转化为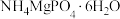 沉淀除去。已知25℃时磷酸电离平衡常数:
沉淀除去。已知25℃时磷酸电离平衡常数: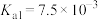 、
、 、
、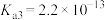 。
。
(1)写出生成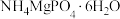 沉淀的离子方程式
沉淀的离子方程式_______ 。
(2) 溶液中:
溶液中: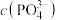
_______ 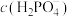 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
Ⅱ.氧化法
臭氧是一种相对安全的氧化剂,已被广泛应用于水处理中。已知臭氧很不稳定,在常温常压下即可分解为 ,在水中比在空气中更易分解。利用臭氧处理氨氮废水,实验跟踪监测
,在水中比在空气中更易分解。利用臭氧处理氨氮废水,实验跟踪监测 氧化氨氮情况如图所示,反应条件:温度10℃,初始pH不同的
氧化氨氮情况如图所示,反应条件:温度10℃,初始pH不同的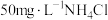 溶液(模拟氨氮废水)各250mL,
溶液(模拟氨氮废水)各250mL,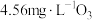 ,接触时间60min。
,接触时间60min。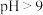 ,相同时间内氨氮去除率显著增大的可能原因是
,相同时间内氨氮去除率显著增大的可能原因是_______ 。
(4)若温度升高,相同时间内氨氮去除率降低,可能原因是_______ 。
(5)在弱酸性环境下,当废水中含有大量 时,
时, 氧化氨氮废水的过程如图所示,该过程可描述为
氧化氨氮废水的过程如图所示,该过程可描述为_______ 。
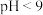 时,
时, 是主要存在形式;当
是主要存在形式;当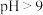 时,
时, 是主要存在形式。
是主要存在形式。Ⅰ.沉淀法
向酸性废水中加入一定比例的
 和
和 ,将氨氮转化为
,将氨氮转化为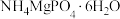 沉淀除去。已知25℃时磷酸电离平衡常数:
沉淀除去。已知25℃时磷酸电离平衡常数: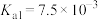 、
、 、
、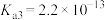 。
。(1)写出生成
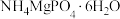 沉淀的离子方程式
沉淀的离子方程式(2)
 溶液中:
溶液中: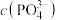
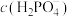 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。Ⅱ.氧化法
臭氧是一种相对安全的氧化剂,已被广泛应用于水处理中。已知臭氧很不稳定,在常温常压下即可分解为
 ,在水中比在空气中更易分解。利用臭氧处理氨氮废水,实验跟踪监测
,在水中比在空气中更易分解。利用臭氧处理氨氮废水,实验跟踪监测 氧化氨氮情况如图所示,反应条件:温度10℃,初始pH不同的
氧化氨氮情况如图所示,反应条件:温度10℃,初始pH不同的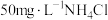 溶液(模拟氨氮废水)各250mL,
溶液(模拟氨氮废水)各250mL,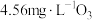 ,接触时间60min。
,接触时间60min。
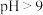 ,相同时间内氨氮去除率显著增大的可能原因是
,相同时间内氨氮去除率显著增大的可能原因是(4)若温度升高,相同时间内氨氮去除率降低,可能原因是
(5)在弱酸性环境下,当废水中含有大量
 时,
时, 氧化氨氮废水的过程如图所示,该过程可描述为
氧化氨氮废水的过程如图所示,该过程可描述为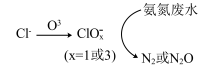
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.食醋(主要成分CH3COOH)、纯碱(Na2CO3)和小苏打(NaHCO3)均为家庭厨房中常用的物质。已知:
请回答下列问题:
(1)25℃时,0.10mol·L-1Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-)_______ ;
(2)常温下,将20mL0.10mol·L-1CH3COOH溶液和 20mL0.10mol·L-1HNO2溶液分别与 20mL 0.10mol·L-1NaHCO3溶液混合(混合后溶液体积变化忽略不计)。
①反应开始时,v (CH3COOH )_______ v (HNO2)(填“>”、“<”或“=”)。
②充分反应后。两溶液中c(CH3COO-)_______ c(NO2-)(填“>”、“<”或“=”)。
(3)25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的PH=6,则混合
液中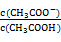 =
=_________ ;
(4)常温下,下列方法可以使0.1mol • L-1CH3COOH的电离程度增大的是_____________ 。
Ⅱ.常温时向一定体积pH= 12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液的ph=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积之比是____________________ 。
| 弱酸 | CH3COOH | H2CO3 | HNO2 |
| 电离常数 | K=1.8×10-5 | K=4.3×10-7 K=5.6×10-11 | K=5.0×10-4 |
请回答下列问题:
(1)25℃时,0.10mol·L-1Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-)
(2)常温下,将20mL0.10mol·L-1CH3COOH溶液和 20mL0.10mol·L-1HNO2溶液分别与 20mL 0.10mol·L-1NaHCO3溶液混合(混合后溶液体积变化忽略不计)。
①反应开始时,v (CH3COOH )
②充分反应后。两溶液中c(CH3COO-)
(3)25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的PH=6,则混合
液中
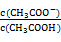 =
=(4)常温下,下列方法可以使0.1mol • L-1CH3COOH的电离程度增大的是
a.加入少量的稀盐酸 b.加热溶液 c.加水稀释 d.加入少量冰醋酸
Ⅱ.常温时向一定体积pH= 12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液的ph=11。若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积之比是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】常温下,几种酸的电离常数如表所示:
回答下列问题:
(1)物质的量浓度均为0.1mol/L的①NaClO溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液,pH由大到小的顺序是
溶液,pH由大到小的顺序是______________ (填标号)。
(2)用离子方程式表示NaClO溶液呈碱性的原因:_____________________ 。
(3)0.1mol/L 溶液中各离子的物质的量浓度由大到小的顺序是
溶液中各离子的物质的量浓度由大到小的顺序是________ ,只改变下列一个条件,能使 与
与 的比值变大的是
的比值变大的是_______ (填标号)。
A.加入 固体 B.通入少量HCl
固体 B.通入少量HCl
C.降低溶液温度 D.加入少量NaOH固体
(4)假设25℃时,0.1mol/L 溶液中由水电离出的
溶液中由水电离出的 浓度为
浓度为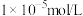 ,则在该温度下此溶液中氨水的电离常数
,则在该温度下此溶液中氨水的电离常数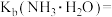
__________ 。
酸 | 电离方程式 | 电离常数 |
HClO |
|
|
|
|
|
|
|
|
回答下列问题:
(1)物质的量浓度均为0.1mol/L的①NaClO溶液 ②
 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液,pH由大到小的顺序是
溶液,pH由大到小的顺序是(2)用离子方程式表示NaClO溶液呈碱性的原因:
(3)0.1mol/L
 溶液中各离子的物质的量浓度由大到小的顺序是
溶液中各离子的物质的量浓度由大到小的顺序是 与
与 的比值变大的是
的比值变大的是A.加入
 固体 B.通入少量HCl
固体 B.通入少量HClC.降低溶液温度 D.加入少量NaOH固体
(4)假设25℃时,0.1mol/L
 溶液中由水电离出的
溶液中由水电离出的 浓度为
浓度为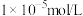 ,则在该温度下此溶液中氨水的电离常数
,则在该温度下此溶液中氨水的电离常数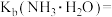
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知常温下部分弱电解质的电离平衡常数如表:
(1)常温下,物质的量浓度相同的三种溶液①NaF溶液②NaClO溶液③Na2CO3溶液,其pH由大到小的顺序是_______ 。(填序号)
(2)25℃时,pH=4的NH4Cl溶液中各离子浓度的大小关系为_______ ,水电离出的氢离子的浓度为_______ 。
(3)NaClO溶液中的质子守恒关系为_______ 。
(4)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式_______ 。
(5)25℃下,将pH=12的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=_______ 。
| 化学式 | HF | HClO | H2CO3 | NH3·H2O |
| 电离常数 | 6.8×10-4 | 4.7×10-8 | K1=4.3×10-7 K2=5.6×10-11 | Kb=1.7×10-5 |
(2)25℃时,pH=4的NH4Cl溶液中各离子浓度的大小关系为
(3)NaClO溶液中的质子守恒关系为
(4)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式
(5)25℃下,将pH=12的苛性钠溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)在25℃条件下将pH=11的氨水稀释100倍后溶液的pH为_______ (填序号)。
A.9 B.13 C. 11~13之间 D. 9~11之间
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,混合溶液中c(Na+)_______ C(CH3COO-)(填“>”、“=”或“<”)。
(3)常温下,已知某NH4Cl溶液中的c(NH4+)=c(Cl-),则该溶液的pH___ 7(填“>”、“=”或“<”)。
(4)如果将HCl和CH3COONa溶液等浓度、等体积混合,则混合溶液中各离子浓度的大小关系为_______________ 。
A.9 B.13 C. 11~13之间 D. 9~11之间
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,混合溶液中c(Na+)
(3)常温下,已知某NH4Cl溶液中的c(NH4+)=c(Cl-),则该溶液的pH
(4)如果将HCl和CH3COONa溶液等浓度、等体积混合,则混合溶液中各离子浓度的大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】
(1)25℃时,在等体积的 ① pH=0的H2SO4溶液、② 0.05 mol/L的Ba (OH)2溶液、③ pH=10的Na2S溶液、④ pH=5的NH4NO3溶液中,发生电离的水的物质的量之比______________________________ 。
(2)常温下,0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合后:
c(CH3COO−) + c(CH3COOH)=_______ mol/L
c(H+)_______ c(CH3COO−) - c(CH3COOH) +2c(OH−) (填“>”、“<”或“=”)
(3)常温下,把pH=11的氢氧化钠溶液与pH=3的醋酸溶液等体积混合,在所得溶液中离子浓度大小关系是__________________________________________ 。
(4)常温下,把pH=2的H2SO4和pH=11的NaOH溶液混和,混和液pH=7。则两溶液的体积比是_________ 。
(1)25℃时,在等体积的 ① pH=0的H2SO4溶液、② 0.05 mol/L的Ba (OH)2溶液、③ pH=10的Na2S溶液、④ pH=5的NH4NO3溶液中,发生电离的水的物质的量之比
(2)常温下,0.2mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合后:
c(CH3COO−) + c(CH3COOH)=
c(H+)
(3)常温下,把pH=11的氢氧化钠溶液与pH=3的醋酸溶液等体积混合,在所得溶液中离子浓度大小关系是
(4)常温下,把pH=2的H2SO4和pH=11的NaOH溶液混和,混和液pH=7。则两溶液的体积比是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)25℃时,浓度为0.1 mol·L-1的6种溶液:①HCl,②CH3COOH ③Ba(OH)2④Na2CO3⑤KCl ⑥NH4Cl溶液pH由小到大的顺序为_______________ (填写编号)
(2)25℃时,醋酸的电离常数Ka=1.7×10-5mol/L,则该温度下CH3COONa的水解平衡常数Kh=_______ mol·L-1(保留到小数点后一位)。
(3)25℃时,pH=3 的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈________ (填“酸性”,“中性”或“碱性”),请写出溶液中离子浓度间的一个等式:________________________________ 。
(4)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH= 7,则溶液中c (CH3COO-)+c(CH3COOH)=_____________ ,m与n的大小关系是m_____ n (填“>”“=”或“<”)。
(5)当300mL 1 mol·L-1的NaOH 溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为_________________________________________ 。
(2)25℃时,醋酸的电离常数Ka=1.7×10-5mol/L,则该温度下CH3COONa的水解平衡常数Kh=
(3)25℃时,pH=3 的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈
(4)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH= 7,则溶液中c (CH3COO-)+c(CH3COOH)=
(5)当300mL 1 mol·L-1的NaOH 溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)写出铝与氢氧化钾溶液反应的离子方程式___________ 。
(2)液氨中存在自耦电离,类似水的电离,写出液氨自耦电离方程式___________ 。
(3)比较给出 能力的相对强弱:
能力的相对强弱:
___________  ,(填“>”“<”或“=”);用一个化学方程式说明
,(填“>”“<”或“=”);用一个化学方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱___________ 。
(4)如下表数据(25℃):
①25℃时,等物质的量浓度的三种溶液:A. 溶液、B.
溶液、B. 溶液、C.
溶液、C. 溶液,
溶液, 由大到小的顺序为
由大到小的顺序为___________ (填字母编号)。
②25℃时,向 溶液中通入少量
溶液中通入少量 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
(2)液氨中存在自耦电离,类似水的电离,写出液氨自耦电离方程式
(3)比较给出
 能力的相对强弱:
能力的相对强弱:
 ,(填“>”“<”或“=”);用一个化学方程式说明
,(填“>”“<”或“=”);用一个化学方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱(4)如下表数据(25℃):
| 化学式 | 电离平衡常数 |
 | 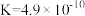 |
 | 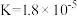 |
 |  , ,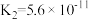 |
①25℃时,等物质的量浓度的三种溶液:A.
 溶液、B.
溶液、B. 溶液、C.
溶液、C. 溶液,
溶液, 由大到小的顺序为
由大到小的顺序为②25℃时,向
 溶液中通入少量
溶液中通入少量 ,发生反应的离子方程式为
,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题
(1)反应I2O5(s)+5CO(g) 5CO2(g)+I2(s)的平衡常数表达式为
5CO2(g)+I2(s)的平衡常数表达式为___________ 。
(2)碳酸钠溶液呈碱性的原因是___________ (用离子方程式表示)
(3)已知常温下H2A的Ka1=2.7×10-6,Ka2=6.3×10-10,则NaHA溶液中水的电离程度___________ 纯水中水的电离程度(填“>”“<”或“=”)。
(4)反应3ClO-(aq)
 (aq)+2Cl-(aq)在室温下能自发进行。
(aq)+2Cl-(aq)在室温下能自发进行。
①T°C时,该反应的平衡常数K=3.2×103.若某混合溶液中(Cl-)=0.5mol·L-1,c(ClO-)=0.24mol·L-1,c( )=0.32mol·L-1,则v(正)
)=0.32mol·L-1,则v(正)___________ v(逆)(填“>”“<”或“=”)。
②已知基元反应mA+nB→pC+qD的速率方程为v=kcm(A)cn(B)(k为只与温度有关的速率常数),一般反应的速率由基元反应中的慢反应决定,反应3ClO-(aq)
 (aq)+2Cl-(aq)可能的机理有如下几种:
(aq)+2Cl-(aq)可能的机理有如下几种:
I、3C1O-→ +2Cl-
+2Cl-
II、ClO-→Cl-+O(慢)、O+ClO-→Cl-+O2(快)、C1O-+O2→ (快)
(快)
III、ClO-+ClO-→ +Cl-(慢)、ClO-+
+Cl-(慢)、ClO-+ →
→ +Cl-(快)
+Cl-(快)
则机理II的中间体是___________ 。若反应3ClO-(aq)
 (aq)+2Cl-(aq)的速率方程为v=kc2(ClO-),则该反应的历程可能是
(aq)+2Cl-(aq)的速率方程为v=kc2(ClO-),则该反应的历程可能是___________ (填标号)。
(1)反应I2O5(s)+5CO(g)
 5CO2(g)+I2(s)的平衡常数表达式为
5CO2(g)+I2(s)的平衡常数表达式为(2)碳酸钠溶液呈碱性的原因是
(3)已知常温下H2A的Ka1=2.7×10-6,Ka2=6.3×10-10,则NaHA溶液中水的电离程度
(4)反应3ClO-(aq)

 (aq)+2Cl-(aq)在室温下能自发进行。
(aq)+2Cl-(aq)在室温下能自发进行。①T°C时,该反应的平衡常数K=3.2×103.若某混合溶液中(Cl-)=0.5mol·L-1,c(ClO-)=0.24mol·L-1,c(
 )=0.32mol·L-1,则v(正)
)=0.32mol·L-1,则v(正)②已知基元反应mA+nB→pC+qD的速率方程为v=kcm(A)cn(B)(k为只与温度有关的速率常数),一般反应的速率由基元反应中的慢反应决定,反应3ClO-(aq)

 (aq)+2Cl-(aq)可能的机理有如下几种:
(aq)+2Cl-(aq)可能的机理有如下几种:I、3C1O-→
 +2Cl-
+2Cl-II、ClO-→Cl-+O(慢)、O+ClO-→Cl-+O2(快)、C1O-+O2→
 (快)
(快)III、ClO-+ClO-→
 +Cl-(慢)、ClO-+
+Cl-(慢)、ClO-+ →
→ +Cl-(快)
+Cl-(快)则机理II的中间体是

 (aq)+2Cl-(aq)的速率方程为v=kc2(ClO-),则该反应的历程可能是
(aq)+2Cl-(aq)的速率方程为v=kc2(ClO-),则该反应的历程可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】Na2S又称臭碱、硫化碱,是应用广泛的化工原料,也常用于吸收工业废气中的SO2。完成下列填空:
(1)用离子方程式说明Na2S又称臭碱、硫化碱的原因___ 。
(2)向AgCl悬浊液中滴加Na2S溶液,生成黑色沉淀,写出反应的离子方程式___ 。结合你所学习过的其它离子反应分析,离子互换反应进行的方向是___ 。
向Na2S溶液中不断通入SO2,直至不再能吸收。其间看到溶液变浑浊,停止反应后溶液中含硫微粒为:S2O32-、HSO3-、H2SO3、HS-。
(3)反应过程中,溶液的pH逐渐___ (填“变大”、“变小”),生成的沉淀是___ ;
(4)关于反应后得到的溶液,下列离子浓度关系正确的是___ 。
a.c(Na+)=c(S2O32-) +2c(HSO3-)+2c(H2SO3) + 2c(HS-)
b.c(Na+)+c(H+)=2c(S2O32-)+c(HSO3-) +c(HS-) +c(OH-)
c.c(Na+)=2c(HS-)
d.c(Na+)=2c(HS-)+2c(S2O32-)+c(HSO3-)
(1)用离子方程式说明Na2S又称臭碱、硫化碱的原因
(2)向AgCl悬浊液中滴加Na2S溶液,生成黑色沉淀,写出反应的离子方程式
向Na2S溶液中不断通入SO2,直至不再能吸收。其间看到溶液变浑浊,停止反应后溶液中含硫微粒为:S2O32-、HSO3-、H2SO3、HS-。
(3)反应过程中,溶液的pH逐渐
(4)关于反应后得到的溶液,下列离子浓度关系正确的是
a.c(Na+)=c(S2O32-) +2c(HSO3-)+2c(H2SO3) + 2c(HS-)
b.c(Na+)+c(H+)=2c(S2O32-)+c(HSO3-) +c(HS-) +c(OH-)
c.c(Na+)=2c(HS-)
d.c(Na+)=2c(HS-)+2c(S2O32-)+c(HSO3-)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)下列物质:①Cu;②SO2;③冰醋酸;④NaHCO3;⑤Cu(OH)2;⑥H2SO4溶液;⑦NaCl,属于非电解质的是____ (填序号),属于强电解质的是___ (填序号)。
(2)写出NaHCO3水解的离子方程式:____ 。
(3)已知Ksp[Cu(OH)2]=2×10-20,常温下某CuSO4溶液里,c(Cu2+)=2.0mol/L,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于____ 。
(4)现有25℃、pH=1的H2SO4溶液,该溶液的物质的量浓度为____ ,溶液中由水电离出的c(OH-)=____ 。
(5)方铅矿(PbS)遇CuSO4溶液生成铜蓝(CuS)的离子方程式:____ 。
(1)下列物质:①Cu;②SO2;③冰醋酸;④NaHCO3;⑤Cu(OH)2;⑥H2SO4溶液;⑦NaCl,属于非电解质的是
(2)写出NaHCO3水解的离子方程式:
(3)已知Ksp[Cu(OH)2]=2×10-20,常温下某CuSO4溶液里,c(Cu2+)=2.0mol/L,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于
(4)现有25℃、pH=1的H2SO4溶液,该溶液的物质的量浓度为
(5)方铅矿(PbS)遇CuSO4溶液生成铜蓝(CuS)的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列溶解平衡:Ca5(PO4)3OH(s)⇌5Ca2+(aq)+3 PO43—(aq)+OH−(aq)。试回答问题:
(1)小孩吃糖后,如果不及时刷牙或漱口,细菌和酶就会作用于糖,在口腔内产生有机羧酸,久而久之,牙齿就会受到腐蚀,其原因是___________ 。
(2)已知Ca5 (PO4)3F(s)的溶解度比上述矿化产物Ca5(PO4)3OH的溶解度更小,质地更坚硬。当牙膏中配有氟化物添加剂后能防止龋齿,其原因是(用离子方程式和简要文字说明)___________ 。
(3)根据以上原理,请你提出一种其他促进矿化的方法:_________________________________ 。
(1)小孩吃糖后,如果不及时刷牙或漱口,细菌和酶就会作用于糖,在口腔内产生有机羧酸,久而久之,牙齿就会受到腐蚀,其原因是
(2)已知Ca5 (PO4)3F(s)的溶解度比上述矿化产物Ca5(PO4)3OH的溶解度更小,质地更坚硬。当牙膏中配有氟化物添加剂后能防止龋齿,其原因是(用离子方程式和简要文字说明)
(3)根据以上原理,请你提出一种其他促进矿化的方法:
您最近一年使用:0次