工业合成氨的反应为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是| A.使用铁触媒不能提高合成氨的日产量 |
| B.适当降温或加压,反应的平衡常数都增大 |
C.及时将体系中的 液化分离有利于平衡正向移动 液化分离有利于平衡正向移动 |
D.用E表示键能,则: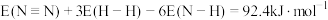 |
更新时间:2023-12-23 20:58:11
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】反应2C(s)+O2(g)=2CO(g)的能量变化如下图所示。下列说法正确的是


| A.C(s)与一定量O2(g)反应生成14g CO(g)放出的热量为110.5kJ |
| B.该反应的热化学方程式:2C(s)+O2(g)=2CO(g) ΔH=-221kJ |
| C.该反应的反应热等于CO分子中化学键形成时所释放的总能量与O2分子中化学键断裂时所吸收的总能量的差 |
| D.2mol C(s)与足量O2(g)充分反应,生成CO2(g),放出的热量大于221kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是( )
| A.H2的热值(单位质量的燃料完全燃烧时所放出的热量,叫做燃料的热值)为142.9kJ⋅g-1,则氢气燃烧的热化学方程式可表示为:2H2(g)+O2(g)=2H2O(l) △H=-285.8kJ⋅mol-1 |
| B.反应A(g)=2B(g),若正反应的活化能为EakJ⋅mol-1,逆反应的活化能为EbkJ⋅mol-1,则△H=(Ea-Eb)kJ⋅mol-1 |
| C.能自发进行的化学反应,一定是△H<0、△S>0 |
| D.增大反应物浓度,可增大单位体积内活化分子百分数,从而增加有效碰撞的次数 |
您最近一年使用:0次
【推荐3】甲烷与氯气发生取代反应分别生成1mol相关有机物的能量变化如图所示:

下列说法不正确的是

下列说法不正确的是
| A.CH4与Cl2的取代反应是放热反应 |
| B.1molCH4的能量比1molCH3Cl的能量多99kJ |
C. △H4≈ △H4≈ △H3≈ △H3≈ △H2≈△H1,说明CH4与Cl2的四步取代反应难易程度相当 △H2≈△H1,说明CH4与Cl2的四步取代反应难易程度相当 |
| D.已知Cl—Cl的键能为243kJ·mol-1,C—Cl的键能为327kJ·mol-1,则CH4(g)+Cl•(g)→CH3•(g)+HCl(g)的△H<0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度时,发生反应2HI(g)  H2(g)+I2(g),向三个体积相等的恒容密闭容器A、B、C中,分别加入①2molHI;②3molHI;③1molH2与1molI2,分别达到平衡时,以下关系正确的是
H2(g)+I2(g),向三个体积相等的恒容密闭容器A、B、C中,分别加入①2molHI;②3molHI;③1molH2与1molI2,分别达到平衡时,以下关系正确的是
 H2(g)+I2(g),向三个体积相等的恒容密闭容器A、B、C中,分别加入①2molHI;②3molHI;③1molH2与1molI2,分别达到平衡时,以下关系正确的是
H2(g)+I2(g),向三个体积相等的恒容密闭容器A、B、C中,分别加入①2molHI;②3molHI;③1molH2与1molI2,分别达到平衡时,以下关系正确的是| A.平衡时,各容器的压强:②=①=③ |
| B.平衡时,I2的浓度:②>①>③ |
| C.平衡时,I2的体积分数:②=①=③ |
| D.从反应开始到达平衡的时间:①>②=③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】如图所示为工业合成氨的流程图。下列说法错误的是
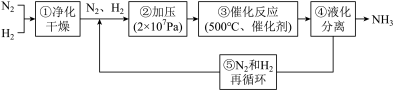

| A.步骤①中“净化”可以防止催化剂“中毒” |
| B.步骤③、④、⑤均有利于提高原料的平衡转化率 |
| C.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率 |
D.工业合成氨反应 ,该反应能在低温自发进行 ,该反应能在低温自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】向甲、乙、丙三个恒容密闭容器中分别充入一定量的A和B,发生反应:A(g)+xB(g)⇌2C(g) △H=akJ·mol-1。相关数据如表所示,反应过程中C的浓度随时间的变化关系如图所示。下列说法正确的是

| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5L | 0.5L | 1.0L |
| 温度 | T1 | T2 | T2 |
| 反应物起始量 | 1.5molA0.5molB | 1.5molA0.5molB | 6molA2molB |

| A.10min内甲容器中反应的平均速率v(A)=0.10mol·L-1·min-1 |
| B.a>0,x=1 |
| C.T2时,该反应的平衡常数为0.8 |
| D.平衡时,C的体积分数:丙>乙 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】由 羟基丁酸生成
羟基丁酸生成 丁内酯的反应为HOCH2CH2CH2COOH
丁内酯的反应为HOCH2CH2CH2COOH
 +H2O。在298 K下,
+H2O。在298 K下, 羟丁酸水溶液的初始浓度为0.180
羟丁酸水溶液的初始浓度为0.180 ,测得
,测得 丁内酯的浓度随时间变化的数据如图所示:
丁内酯的浓度随时间变化的数据如图所示:

则下列说法不正确的是
 羟基丁酸生成
羟基丁酸生成 丁内酯的反应为HOCH2CH2CH2COOH
丁内酯的反应为HOCH2CH2CH2COOH
 +H2O。在298 K下,
+H2O。在298 K下, 羟丁酸水溶液的初始浓度为0.180
羟丁酸水溶液的初始浓度为0.180 ,测得
,测得 丁内酯的浓度随时间变化的数据如图所示:
丁内酯的浓度随时间变化的数据如图所示:
则下列说法不正确的是
A.该反应在50~80 min内的平均反应速率为 |
B.120 min时 羟基丁酸的转化率为50% 羟基丁酸的转化率为50% |
C.298 K时该反应的平衡常数 |
D.为提高 羟基丁酸的转化率,除适当控制反应温度外,还可采用的措施是及时分离出产物 羟基丁酸的转化率,除适当控制反应温度外,还可采用的措施是及时分离出产物 丁内酯 丁内酯 |
您最近一年使用:0次

 资源化利用是解决资源和能源短缺、减少碳排放的一种途径。以
资源化利用是解决资源和能源短缺、减少碳排放的一种途径。以 作催化剂,可使
作催化剂,可使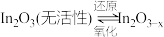 (有活性)
(有活性) 在活化后的催化剂表面合成甲醇,其反应历程如图:
在活化后的催化剂表面合成甲醇,其反应历程如图:
 和一定量的
和一定量的 ,发生反应:
,发生反应: 。
。 ]随温度的变化曲线如图所示。下列说法错误的是
]随温度的变化曲线如图所示。下列说法错误的是



 ,当容器内压强不变时,反应达到平衡状态
,当容器内压强不变时,反应达到平衡状态

