碳和氮的化合物是广泛的化工原料,回答下列问题:
I.在一定体积的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度t的关系如下表:
,其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应为反应___________ (填“吸热”、“放热”)。
(2)某温度下,平衡浓度符合下式: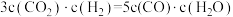 ,试判断此时的温度为
,试判断此时的温度为___________ ℃。
(3)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为 ,
,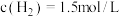 ,
, ,
, ,则下一时刻,
,则下一时刻,
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)反应达平衡后,向容器中通入与平衡混合气组成、比例相同的气体,达到新平衡时与原平衡相比,有关说法正确的是___________。
Ⅱ.NO2的二聚体 是火箭中常用氧化剂。完成下列问题。
是火箭中常用氧化剂。完成下列问题。
(5)在1000K下,在某恒容容器中发生下列反应: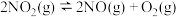 ,将一定量的
,将一定量的 放入恒容密闭容器中,测得其平衡转化率
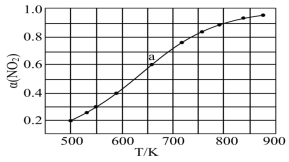
放入恒容密闭容器中,测得其平衡转化率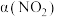 随温度变化如图所示。图中a点对应温度下,已知
随温度变化如图所示。图中a点对应温度下,已知 的起始压强
的起始压强 为120KPa,列式计算该温度下反应的平衡常数
为120KPa,列式计算该温度下反应的平衡常数
___________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅲ.
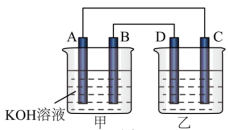
(6)下图是利用甲烷燃料电池给C电极上镀金属铜,A电极的电极反应式为___________ ,若C电极增重0.96g,则B电极上消耗O2的物质的质量为___________ 。
I.在一定体积的密闭容器中,进行如下化学反应:
 ,其化学平衡常数K和温度t的关系如下表:
,其化学平衡常数K和温度t的关系如下表:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应为反应
(2)某温度下,平衡浓度符合下式:
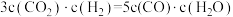 ,试判断此时的温度为
,试判断此时的温度为(3)在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为
 ,
,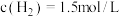 ,
, ,
, ,则下一时刻,
,则下一时刻,
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)反应达平衡后,向容器中通入与平衡混合气组成、比例相同的气体,达到新平衡时与原平衡相比,有关说法正确的是___________。
| A.反应物转化率增大 | B.逆反应速率增大 |
| C.各物质的比例不变 | D. 增大、 增大、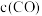 减小 减小 |
Ⅱ.NO2的二聚体
 是火箭中常用氧化剂。完成下列问题。
是火箭中常用氧化剂。完成下列问题。(5)在1000K下,在某恒容容器中发生下列反应:
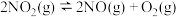 ,将一定量的
,将一定量的 放入恒容密闭容器中,测得其平衡转化率
放入恒容密闭容器中,测得其平衡转化率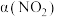 随温度变化如图所示。图中a点对应温度下,已知
随温度变化如图所示。图中a点对应温度下,已知 的起始压强
的起始压强 为120KPa,列式计算该温度下反应的平衡常数
为120KPa,列式计算该温度下反应的平衡常数

Ⅲ.
(6)下图是利用甲烷燃料电池给C电极上镀金属铜,A电极的电极反应式为

更新时间:2024-01-14 22:09:34
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】二硫化碳用于制造人造丝、杀虫剂、促进剂等,也用作溶剂。回答下列问题:
(1)下列反应的焓变及平衡常数如下:
(Ⅰ)


(Ⅱ)
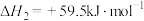
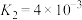
(Ⅲ)
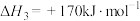
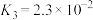
(Ⅳ)
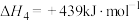

①反应(Ⅳ)自发进行的条件是_______ (填字母)。
A.高温 B.低温 C.任意温度
②
_______  ;
;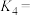
_______ 。
(2)硫化氢替代硫黄生产二硫化碳的原理为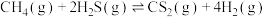 ,起始时,
,起始时,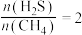 。在100 kPa压强下测得不同温度时的平衡组成如图1所示,在不同压强下测得的平衡组成如图2所示:
。在100 kPa压强下测得不同温度时的平衡组成如图1所示,在不同压强下测得的平衡组成如图2所示:

①该反应的
_______ 0(填“>”或“<”);图2中a、d代表的物质分别是_______ 、_______ 。
②图1中,X点H2S的转化率为_______ %。
③为提高该反应中H2S的平衡转化率,除改变温度和压强外,还可采取的措施是_______ 。
(1)下列反应的焓变及平衡常数如下:
(Ⅰ)



(Ⅱ)

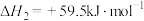
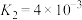
(Ⅲ)

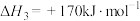
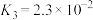
(Ⅳ)

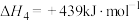

①反应(Ⅳ)自发进行的条件是
A.高温 B.低温 C.任意温度
②

 ;
;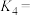
(2)硫化氢替代硫黄生产二硫化碳的原理为
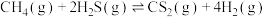 ,起始时,
,起始时,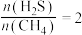 。在100 kPa压强下测得不同温度时的平衡组成如图1所示,在不同压强下测得的平衡组成如图2所示:
。在100 kPa压强下测得不同温度时的平衡组成如图1所示,在不同压强下测得的平衡组成如图2所示:
①该反应的

②图1中,X点H2S的转化率为
③为提高该反应中H2S的平衡转化率,除改变温度和压强外,还可采取的措施是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氮、磷及其化合物在生产、生活中有重要的用途。回答下列问题:
I (1)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。
①写出磷酸主要的电离方程式________________________ 。
②直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x=_____ (用n表示)。
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
H2PO2-+___ Ag++____ =PO43-+___ Ag+______
(3) 工业上生产硝酸铜晶体的流程图如下:
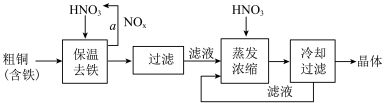
①在步骤a中,需要通入氧气和水,其目的是______ .
②进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明)______ .
③下图是某小组同学查阅资料所绘出的硝酸铜晶体[Cu(NO3)2•nH2O]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是______ (填字母).
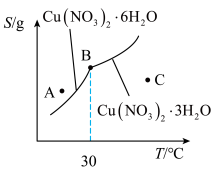
a.A点时的溶液为不饱和溶液
b.B点时两种晶体可以共存
c.按上述流程最终得到的晶体是Cu(NO3)2•3H2O
d.若将C点时的溶液降温至30℃以下,可以析出Cu(NO3)2•6H2O晶体
II (4)查阅资料可知:银氨溶液中存在平衡:Ag+(aq)+2NH3(aq) Ag(NH3)2+(aq),该反应平衡常数的表达式K稳[Ag(NH3)2+]=
Ag(NH3)2+(aq),该反应平衡常数的表达式K稳[Ag(NH3)2+]= _________ ,已知某温度下,K稳[Ag(NH3)2+]=1.10×107,Ksp[AgCl]=1.45×10﹣10。计算得到可逆反应AgCl(s)+2NH3(aq)  Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=
Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=_________ (保留2位有效数字),1L 1mol/L氨水中最多可以溶解AgCl_________ mol(保留1位有效数字)。
I (1)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。
①写出磷酸主要的电离方程式
②直链低聚磷酸铵的化学式可表示为(NH4)(n+2)PnOx,x=
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。
H2PO2-+
(3) 工业上生产硝酸铜晶体的流程图如下:

①在步骤a中,需要通入氧气和水,其目的是
②进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明)
③下图是某小组同学查阅资料所绘出的硝酸铜晶体[Cu(NO3)2•nH2O]的溶解度曲线(温度在30℃前后对应不同的晶体),下列说法正确的是

a.A点时的溶液为不饱和溶液
b.B点时两种晶体可以共存
c.按上述流程最终得到的晶体是Cu(NO3)2•3H2O
d.若将C点时的溶液降温至30℃以下,可以析出Cu(NO3)2•6H2O晶体
II (4)查阅资料可知:银氨溶液中存在平衡:Ag+(aq)+2NH3(aq)
 Ag(NH3)2+(aq),该反应平衡常数的表达式K稳[Ag(NH3)2+]=
Ag(NH3)2+(aq),该反应平衡常数的表达式K稳[Ag(NH3)2+]=  Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=
Ag(NH3)2+(aq)+Cl-(aq)的化学平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】低碳经济成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。请你结合下列有关图示和所学知识回答:
I.用CO2催化加氢可以制取乙烯:CO2(g)+3H2(g) 1/2C2H4(g)+2H2O(g)。
1/2C2H4(g)+2H2O(g)。
(l)若该反应体系的能量随反应过程变化关系如图所示,则该反应△H =___________ (用含a、b的式子表示);又知:相关化学键的键能如下表所示,实验测得上述反应的△H =-152 kJ/mol,则表中的x= ___ 。
II.用CO2催化加氢还可以制取二甲醚:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)△H =-122.5kJ/mol,某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的平衡转化率如图所示。
CH3OCH3(g)+3H2O(g)△H =-122.5kJ/mol,某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的平衡转化率如图所示。
(3)图中T1、T2分别表示反应温度,判断T1、T2大小关系的依据是____ ;图中A、B、C三点对应的平衡常数分别为KA、KB、Kc,其三者大小的关系是____ 。
(4)T1温度下,将6molCO2和12molH2充入2L的密闭容器中,经过5min反应达到平衡,则0~5min内的平均反应速率υ(H2)=_______ ,平衡常数K=__ (列出计算式即可)。
I.用CO2催化加氢可以制取乙烯:CO2(g)+3H2(g)
 1/2C2H4(g)+2H2O(g)。
1/2C2H4(g)+2H2O(g)。(l)若该反应体系的能量随反应过程变化关系如图所示,则该反应△H =

(2)以稀硫酸为电解质溶液,利用太阳能电池将CO2转化为乙烯的工作原理如图所示。则M极上的电极反应式为

II.用CO2催化加氢还可以制取二甲醚:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g)△H =-122.5kJ/mol,某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的平衡转化率如图所示。
CH3OCH3(g)+3H2O(g)△H =-122.5kJ/mol,某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的平衡转化率如图所示。
(3)图中T1、T2分别表示反应温度,判断T1、T2大小关系的依据是
(4)T1温度下,将6molCO2和12molH2充入2L的密闭容器中,经过5min反应达到平衡,则0~5min内的平均反应速率υ(H2)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g) 2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表,完成下列问题。
2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表,完成下列问题。
(1)该反应的化学平衡常数表达式为K=________ ;K1______ K2(填“>”“<”或“=”);若增大压强使平衡向正反应方向移动,则平衡常数_________ (填“变”或“不变”)。
(2)判断该反应达到化学平衡状态的依据是____________ (填序号):
A.2υH2(正)= 3υNH3(逆) B.混合气体的密度保持不变
C.容器内压强保持不变 D.N2的消耗速率等于H2的消耗速率
E.容器中气体的平均相对分子质量不随时间而变化 F.混合气体的颜色保持不变
(3)将不同量的N2和H2分别通入到体积为2L的恒容密闭容器中,进行上述反应得到如下两组数据:
实验1中以υ(NH3)表示的反应速率为______ ,实验2的速率比实验1快的原因是____________ ;
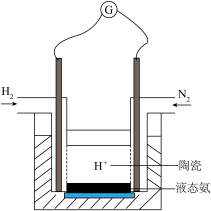
(4)有人设计采用高性能质子导电材料SCY陶瓷(能传递H+),实现了常压下既能合成氨又能发电的实验装置(如图)。则其正极的电极反应为_____________ 。
 2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表,完成下列问题。
2NH3(g) △H<0,其化学平衡常数K与温度t的关系如下表,完成下列问题。| t/℃ | 25 | 125 | 225 | … |
| K | 4.1×105 | K1 | K2 | … |
(2)判断该反应达到化学平衡状态的依据是
A.2υH2(正)= 3υNH3(逆) B.混合气体的密度保持不变
C.容器内压强保持不变 D.N2的消耗速率等于H2的消耗速率
E.容器中气体的平均相对分子质量不随时间而变化 F.混合气体的颜色保持不变
(3)将不同量的N2和H2分别通入到体积为2L的恒容密闭容器中,进行上述反应得到如下两组数据:
| 实验组 | 温度(℃) | 起始量(mol) | 平衡量(mol) | 达到平衡所需时间(min) | |
| N2 | H2 | NH3 | |||
| 1 | 650 | 2 | 4 | 0.9 | 9 |
| 2 | 900 | 1 | 2 | 0.3 | 0.01 |
(4)有人设计采用高性能质子导电材料SCY陶瓷(能传递H+),实现了常压下既能合成氨又能发电的实验装置(如图)。则其正极的电极反应为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】在2 L密闭容器中,800 ℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表所示:
2NO2(g)体系中,n(NO)随时间的变化如下表所示:
(1)写出该反应的平衡常数表达式:K=_____________ 。已知:K300℃>K350℃,则该反应是_____________ 反应。(填“吸热”或“放热”)
(2)下图中表示NO2的变化的曲线是_____________ 。用NO表示从0~2 s内该反应的平均速率v= _____________ 。

(3)能说明该反应已达到平衡状态的是_____________ 。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是_____________ 。
a.及时分离出NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
 2NO2(g)体系中,n(NO)随时间的变化如下表所示:
2NO2(g)体系中,n(NO)随时间的变化如下表所示:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)下图中表示NO2的变化的曲线是

(3)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内的密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是
a.及时分离出NO2气体 b.适当升高温度 c.增大O2的浓度 d.选择高效催化剂
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】I.氨气被广泛用于化工、轻工、化肥、合成纤维、制药等领域,已知工业合成氨的反应为 气态分子中
气态分子中 化学键解离成气态原子所吸收的能量称为键能
化学键解离成气态原子所吸收的能量称为键能 ,一些共价键的键能如下表所示。
,一些共价键的键能如下表所示。
(1)请根据上表数据计算,一定条件下,氮气与氢气生成 氨气时
氨气时___________ (填“放出”或“吸收”)的热量为 ,则
,则 为
为___________  。
。
(2)在与(1)相同条件下,将 氮气和
氮气和 氢气放入一密闭容器中发生上述反应,放出或吸收的热量为
氢气放入一密闭容器中发生上述反应,放出或吸收的热量为 ,则
,则 与
与 比较,正确的是
比较,正确的是___________ (填字母)。
A.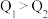 B.
B.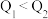 C.
C.
II.一定条件下铁可以和 发生反应:
发生反应: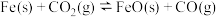 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和
气体和 气体的浓度与时间的关系如下图所示。
气体的浓度与时间的关系如下图所示。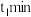 时,正、逆反应速率的大小关系为
时,正、逆反应速率的大小关系为
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(4) 内,
内, 的平均反应速率
的平均反应速率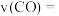
___________ 。
(5)下列条件的改变能减慢其反应速率的是___________ 。
①降低温度
②减小铁粉的质量
③保持压强不变,充入 使容器的容积增大
使容器的容积增大
④保持容积不变,充入 便体系压强增大
便体系压强增大
(6)下列描述能说明上述反应已达到平衡状态的是___________ 。
①
② 为定值
为定值
③容器中气体压强不随时间变化而变化
④容器中气体的平均相对分子质量不随时间变化而变化
III.已知: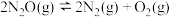 ,不同温度
,不同温度 下,
下,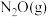 分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗一半时所需的相应时间)。
消耗一半时所需的相应时间)。
___________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
②当温度为 、起始压强为
、起始压强为 ,反应至
,反应至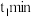 时,此时体系压强
时,此时体系压强
___________ (用含 代数式表示)。
代数式表示)。
 气态分子中
气态分子中 化学键解离成气态原子所吸收的能量称为键能
化学键解离成气态原子所吸收的能量称为键能 ,一些共价键的键能如下表所示。
,一些共价键的键能如下表所示。| 共价键 |  |  |  |
键能 | 436 | 946 | 391 |
(1)请根据上表数据计算,一定条件下,氮气与氢气生成
 氨气时
氨气时 ,则
,则 为
为 。
。(2)在与(1)相同条件下,将
 氮气和
氮气和 氢气放入一密闭容器中发生上述反应,放出或吸收的热量为
氢气放入一密闭容器中发生上述反应,放出或吸收的热量为 ,则
,则 与
与 比较,正确的是
比较,正确的是A.
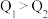 B.
B.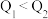 C.
C.
II.一定条件下铁可以和
 发生反应:
发生反应: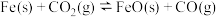 。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的
。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的 气体,反应过程中
气体,反应过程中 气体和
气体和 气体的浓度与时间的关系如下图所示。
气体的浓度与时间的关系如下图所示。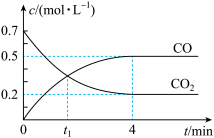
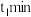 时,正、逆反应速率的大小关系为
时,正、逆反应速率的大小关系为
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(4)
 内,
内, 的平均反应速率
的平均反应速率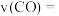
(5)下列条件的改变能减慢其反应速率的是
①降低温度
②减小铁粉的质量
③保持压强不变,充入
 使容器的容积增大
使容器的容积增大 ④保持容积不变,充入
 便体系压强增大
便体系压强增大(6)下列描述能说明上述反应已达到平衡状态的是
①

②
 为定值
为定值③容器中气体压强不随时间变化而变化
④容器中气体的平均相对分子质量不随时间变化而变化
III.已知:
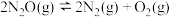 ,不同温度
,不同温度 下,
下,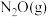 分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗一半时所需的相应时间)。
消耗一半时所需的相应时间)。

 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。②当温度为
 、起始压强为
、起始压强为 ,反应至
,反应至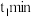 时,此时体系压强
时,此时体系压强
 代数式表示)。
代数式表示)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】研究氨氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:


 (I)
(I)
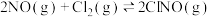

 (II)
(II)
(1)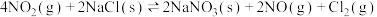 的平衡常数
的平衡常数
___________ (用 、
、 表示)。
表示)。
(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1mol ,10min时反应(II)达到平衡。测得10min内
,10min时反应(II)达到平衡。测得10min内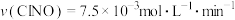 ,则平衡后
,则平衡后
___________ mol,NO的转化率α1___________ 其他条件保持不变,反应(I)在恒压条件下进行,平衡时NO的转化率α2___________ α1(填“>”“<”或“=”)。
(3)实验室可用NaOH溶液吸收 ,反应为
,反应为 。含0.2molNaOH的水溶液与0.2mol
。含0.2molNaOH的水溶液与0.2mol 恰好完全反应得1L溶液A,溶液B为0.1
恰好完全反应得1L溶液A,溶液B为0.1 的
的 溶液,则两溶液中
溶液,则两溶液中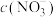 、
、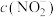 和
和 由大到小的顺序为
由大到小的顺序为___________ 。(已知 电离常数
电离常数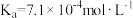 ,
, 的电离常数
的电离常数 )
)
可使溶液A和溶液B的pH相等的方法是___________
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH


 (I)
(I)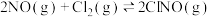

 (II)
(II)(1)
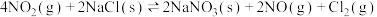 的平衡常数
的平衡常数
 、
、 表示)。
表示)。(2)为研究不同条件对反应(II)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1mol
 ,10min时反应(II)达到平衡。测得10min内
,10min时反应(II)达到平衡。测得10min内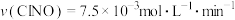 ,则平衡后
,则平衡后
(3)实验室可用NaOH溶液吸收
 ,反应为
,反应为 。含0.2molNaOH的水溶液与0.2mol
。含0.2molNaOH的水溶液与0.2mol 恰好完全反应得1L溶液A,溶液B为0.1
恰好完全反应得1L溶液A,溶液B为0.1 的
的 溶液,则两溶液中
溶液,则两溶液中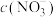 、
、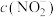 和
和 由大到小的顺序为
由大到小的顺序为 电离常数
电离常数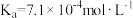 ,
, 的电离常数
的电离常数 )
)可使溶液A和溶液B的pH相等的方法是
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】工业上常用CO和H2合成甲醇,反应方程式为:CO(g)+2H2(g)  CH3OH (g) ΔH。
CH3OH (g) ΔH。
在T1时,体积为2 L的恒容容器中充入物质的量之和为3 mol的H2和CO,达到平衡时CH3OH的体积分数(V%)与 的关系如图1所示。
的关系如图1所示。

(1) 当起始 =2,经过5 min达到平衡,此时容器的压强是初始压强的0.7倍,则0~5min内平均反应速率v(H2)=
=2,经过5 min达到平衡,此时容器的压强是初始压强的0.7倍,则0~5min内平均反应速率v(H2)=___________________________________ 。
(2)B点的平衡常数为______________ (计算结果保留两位小数)。
(3)当起始 =3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的
=3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的______ 点(填“D”“E”或“F”)。
(4)由图2可知:

①该反应的ΔH______ 0(填“>”“<”或“=”,下同)。
②相同起始量达到x、y时,容器内气体密度ρx______ ρy 。
。
③当压强为p2时,在z点:v正______ v逆。
(5)有一种甲醇燃料电池,其电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。则该燃料电池通入甲醇的一极的电极反应方程式为:__________________ 。
 CH3OH (g) ΔH。
CH3OH (g) ΔH。在T1时,体积为2 L的恒容容器中充入物质的量之和为3 mol的H2和CO,达到平衡时CH3OH的体积分数(V%)与
 的关系如图1所示。
的关系如图1所示。
(1) 当起始
 =2,经过5 min达到平衡,此时容器的压强是初始压强的0.7倍,则0~5min内平均反应速率v(H2)=
=2,经过5 min达到平衡,此时容器的压强是初始压强的0.7倍,则0~5min内平均反应速率v(H2)=(2)B点的平衡常数为
(3)当起始
 =3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的
=3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的(4)由图2可知:

①该反应的ΔH
②相同起始量达到x、y时,容器内气体密度ρx
 。
。③当压强为p2时,在z点:v正
(5)有一种甲醇燃料电池,其电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。则该燃料电池通入甲醇的一极的电极反应方程式为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】Ⅰ.高炉炼铁过程中发生的主要反应为 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下,请回答下列问题:
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下,请回答下列问题:
(1)该反应的平衡常数表达式K=______ 。
(2)在一个容积为10 L的密闭容器中,1000 ℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10 min后达到平衡。CO的平衡转化率=_______ 。
(3)欲提高(2)中CO的平衡转化率,可采取的措施是____ (填字母序号)。
A.减少Fe的量 B.移出部分CO2 C.增加Fe2O3的量
D.减小容器的容积 E.提高反应温度 F.加入合适的催化剂
Ⅱ.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2 L的密闭容器中发生反应:N2O4(g) 2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。
2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。

(4)该温度下,该反应的平衡常数为________ ,若温度升高,K值将______ (填“增大”、“减小”或“不变”)。
(5)a、b、c、d四个点中,表示化学反应处于平衡状态的是_______ 点。从起点开始首次达到平衡时,以NO2表示的反应速率υ(NO2)=_______ mol·L−1·min−1。
(6)25 min时,加入了______ (填加入物质的化学式及加入的物质的量),使平衡发生了移动。
(7)25℃时,1.00 g N2H4(l) (联氨)与足量N2O4 (l)完全反应生成N2(g)和H2O (l)放出19.14 kJ的热量。则该反应的热化学方程式为:__________ 。
 Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)
 Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下,请回答下列问题:
Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下,请回答下列问题:| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(2)在一个容积为10 L的密闭容器中,1000 ℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10 min后达到平衡。CO的平衡转化率=
(3)欲提高(2)中CO的平衡转化率,可采取的措施是
A.减少Fe的量 B.移出部分CO2 C.增加Fe2O3的量
D.减小容器的容积 E.提高反应温度 F.加入合适的催化剂
Ⅱ.在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2 L的密闭容器中发生反应:N2O4(g)
 2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。
2NO2(g) ΔH>0,反应过程中各物质的物质的量浓度(c)随时间(t)的变化曲线如图所示。
(4)该温度下,该反应的平衡常数为
(5)a、b、c、d四个点中,表示化学反应处于平衡状态的是
(6)25 min时,加入了
(7)25℃时,1.00 g N2H4(l) (联氨)与足量N2O4 (l)完全反应生成N2(g)和H2O (l)放出19.14 kJ的热量。则该反应的热化学方程式为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】燃煤烟气中含有大量的二氧化硫,进行脱硫处理可以减少环境污染,变废为宝。
(1)H2还原法是处理燃煤烟气中SO2的方法之一。已知:2H2S(g)+SO2(g)=3S(s)+2H2O(l) ΔH=a kJ·mol-1;H2S(g)=H2(g)+S(s) ΔH=b kJ·mol-1;H2O(l)=H2O(g) ΔH=c kJ·mol-1;写出SO2(g)和H2(g)反应生成S(s)和H2O(g)的热化学方程式:_______ 。
(2)新型纳米材料氧缺位铁酸盐(ZnFe2Ox)能使工业废气中酸性氧化物分解除去,若2 mol ZnFe2Ox与足量SO2可生成2 mol ZnFe2O4和1.0 mol S,则x=_______ 。
(3)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:2SO2+2n Cu+(n+1)O2+(2-2 n)H2O=2n CuSO4+(2-2n) H2SO4,吸收标准状况下11.2L SO2,被SO2还原的O2的质量为______ g。
②利用如所示电化学装置吸收另一部分SO2,并完成Cu的再生。写出装置内所发生反应的离子方程式______ ;若用甲烷燃料电池作电源(电解质溶液呈碱性),负极的反应式为_______ 。

(1)H2还原法是处理燃煤烟气中SO2的方法之一。已知:2H2S(g)+SO2(g)=3S(s)+2H2O(l) ΔH=a kJ·mol-1;H2S(g)=H2(g)+S(s) ΔH=b kJ·mol-1;H2O(l)=H2O(g) ΔH=c kJ·mol-1;写出SO2(g)和H2(g)反应生成S(s)和H2O(g)的热化学方程式:
(2)新型纳米材料氧缺位铁酸盐(ZnFe2Ox)能使工业废气中酸性氧化物分解除去,若2 mol ZnFe2Ox与足量SO2可生成2 mol ZnFe2O4和1.0 mol S,则x=
(3)一种以铜作催化剂脱硫有如下两个过程:
①在铜的作用下完成工业尾气中SO2的部分催化氧化,所发生反应为:2SO2+2n Cu+(n+1)O2+(2-2 n)H2O=2n CuSO4+(2-2n) H2SO4,吸收标准状况下11.2L SO2,被SO2还原的O2的质量为
②利用如所示电化学装置吸收另一部分SO2,并完成Cu的再生。写出装置内所发生反应的离子方程式

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
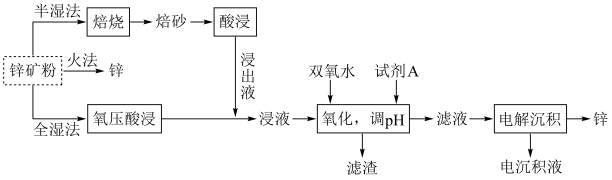
【推荐2】锌及锌合金(如黄铜)广泛应用于生产、生活。某小组拟以锌矿(主要成分是ZnS,含少量FeS等杂质)为原料采用多种方法冶炼锌,流程如图。回答下列问题:
已知:① 是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
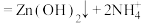 ,
,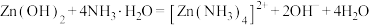 。
。
②常温下,几种金属离子转化成氢氧化物沉淀的pH如表:
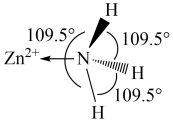
(1)已知 的部分结构如图所示,
的部分结构如图所示, 中
中 采用
采用 杂化,则
杂化,则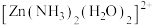 有
有_____ 种结构。 分子中的
分子中的 键角比
键角比 中的小的原因是
中的小的原因是_______ 。
(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内,封裹泥固,∙∙∙∙∙∙然后,逐层用煤炭饼垫盛,其底铺薪,发火煅红∙∙∙∙∙∙冷定,毁罐取出。∙∙∙∙∙∙即倭铅也。”(炉甘石主要成分是 ,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的
,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的_______ (填标号,下同)。从环保的角度来看,这三种方法中,最佳方法是_______ 。
a.半湿法 b.火法 c.全湿法
(3)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入 ,除生成
,除生成 外,还能回收非金属单质。ZnS参与反应的离子方程式为
外,还能回收非金属单质。ZnS参与反应的离子方程式为_________ 。
(4)“氧化,调pH”时试剂A不宜选择NaOH溶液,也不宜选择氨水,原因是________ 。
(5)“电解沉积”(以惰性材料为电极)时阳极的电极反应式为________ 。航母外壳常镶嵌一些锌块,这种保护航母的方法叫_______ 。
(6)通常认为离子浓度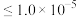 mol⋅L
mol⋅L 时表示该离子已完全除尽。根据表格数据计算
时表示该离子已完全除尽。根据表格数据计算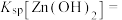
_____ 。

已知:①
 是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
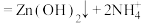 ,
,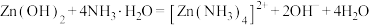 。
。②常温下,几种金属离子转化成氢氧化物沉淀的pH如表:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
 | 6.5 | 9.7 |
 | 5.4 | 8.0 |
 | 2.3 | 4.1 |
(1)已知
 的部分结构如图所示,
的部分结构如图所示, 中
中 采用
采用 杂化,则
杂化,则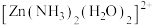 有
有 分子中的
分子中的 键角比
键角比 中的小的原因是
中的小的原因是
(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内,封裹泥固,∙∙∙∙∙∙然后,逐层用煤炭饼垫盛,其底铺薪,发火煅红∙∙∙∙∙∙冷定,毁罐取出。∙∙∙∙∙∙即倭铅也。”(炉甘石主要成分是
 ,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的
,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的a.半湿法 b.火法 c.全湿法
(3)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入
 ,除生成
,除生成 外,还能回收非金属单质。ZnS参与反应的离子方程式为
外,还能回收非金属单质。ZnS参与反应的离子方程式为(4)“氧化,调pH”时试剂A不宜选择NaOH溶液,也不宜选择氨水,原因是
(5)“电解沉积”(以惰性材料为电极)时阳极的电极反应式为
(6)通常认为离子浓度
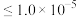 mol⋅L
mol⋅L 时表示该离子已完全除尽。根据表格数据计算
时表示该离子已完全除尽。根据表格数据计算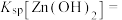
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】烟气的主要污染物为SO2和NO,是造成大气污染的重要因素,其治理方法主要有液体吸收法,固体吸收法,氧化反应法,电解法等。
(1)烟气中的SO2可以用“亚硫酸铵吸收法”处理,发生的反应为(NH4)2SO3+SO2+H2O=2NH4HSO3,测得25℃时溶液pH与各组分物质的量分数的变化关系如图,b点时溶液pH=7,n( ):n(
):n( )=
)=_______ 。

(2)一种基于吸收剂区分的同时脱硫脱硝反应的装置如图所示。反应器I吸收SO2,反应器II吸收NO,隔绝空气反应一段时间。
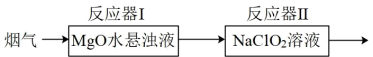
①当观察到反应器I中悬浊液变澄清时,反应的离子方程式_______ 。
②反应器II中所发生的反应为4NO+3 +2H2O=4
+2H2O=4 +3Cl-+4H+,盛有100mL0.15mol·L-1NaClO2溶液最多能吸收NO(标准状况下)的体积为
+3Cl-+4H+,盛有100mL0.15mol·L-1NaClO2溶液最多能吸收NO(标准状况下)的体积为_______ 。
③已知:NaClO2溶液中含氯组分的百分含量(δ)随pH变化如图甲所示,其他条件相同,NaClO2溶液中脱硝效率随溶液初始pH的变化如图乙所示。脱硝过程中,起脱硝作用的有效成分为_______ (填化学式)。将NaClO2溶液的pH从4调节至3的过程中,脱硝效率几乎不变的原因是_______ 。

(3)隔膜电解同时脱硫脱硝的装置如图所示,其中电极A、B均为惰性电极,电解液为稀硫酸。为了提高脱除效率,将阴极室的溶液pH调至4~7,则阴极上的电极反应为_______ 。

(1)烟气中的SO2可以用“亚硫酸铵吸收法”处理,发生的反应为(NH4)2SO3+SO2+H2O=2NH4HSO3,测得25℃时溶液pH与各组分物质的量分数的变化关系如图,b点时溶液pH=7,n(
 ):n(
):n( )=
)=
(2)一种基于吸收剂区分的同时脱硫脱硝反应的装置如图所示。反应器I吸收SO2,反应器II吸收NO,隔绝空气反应一段时间。

①当观察到反应器I中悬浊液变澄清时,反应的离子方程式
②反应器II中所发生的反应为4NO+3
 +2H2O=4
+2H2O=4 +3Cl-+4H+,盛有100mL0.15mol·L-1NaClO2溶液最多能吸收NO(标准状况下)的体积为
+3Cl-+4H+,盛有100mL0.15mol·L-1NaClO2溶液最多能吸收NO(标准状况下)的体积为③已知:NaClO2溶液中含氯组分的百分含量(δ)随pH变化如图甲所示,其他条件相同,NaClO2溶液中脱硝效率随溶液初始pH的变化如图乙所示。脱硝过程中,起脱硝作用的有效成分为

(3)隔膜电解同时脱硫脱硝的装置如图所示,其中电极A、B均为惰性电极,电解液为稀硫酸。为了提高脱除效率,将阴极室的溶液pH调至4~7,则阴极上的电极反应为

您最近一年使用:0次



