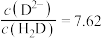柠檬酸三钠(Na3A)是一种常用食品添加剂。用0.01mol/L盐酸滴定10mL0.01mol/L的柠檬酸三钠溶液,测得溶液电导率与滴加盐酸体积V的关系如图所示,已知:柠檬酸H3A属于三元弱酸,25℃其电离平衡常数的pKa=﹣1gKa,pKa1=3.14,pKa2=4.77,pKa3=6.39。下列说法正确的是
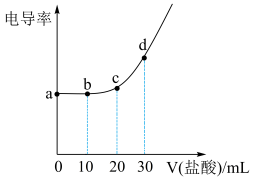

| A.a点代表正盐溶液,c(H+)的数量级为10-9 |
| B.b点溶液显碱性 |
| C.相同浓度的H+与Na+电导率相差不大 |
| D.曲线上任意一点满足:c(Cl–)+ c(H3A)+ c(H2A–)+ c(HA2–)+ c(A3–)= 0.01mol/L |
更新时间:2024-01-29 14:25:35
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知某二元酸H2X在水中的电离分两步进行H2X=H++HX﹣,HX﹣⇌H++X2﹣。常温下,在20mL0.1mol•L﹣1 NaHX溶液中滴加c mol•L﹣1NaOH溶液,溶液温度与滴加的NaOH溶液体积的关系如图所示。下列说法错误的是


| A.滴加的NaOH溶液pH=13 |
| B.F点溶液中c(OH﹣)>c(HX﹣) |
| C.G点溶液c(Na+)=3c(H2X)+3c(HX﹣)+3c(X2﹣) |
| D.滴加NaOH溶液过程中,水的电离程度先变大,后变小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,通过下列实验探究 、
、 溶液的性质
溶液的性质
实验1:向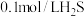 溶液中通入一定体积
溶液中通入一定体积 ,测得溶液pH为7
,测得溶液pH为7
实验2:向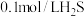 溶液中滴加等体积0.1mol/LNaOH溶液,充分反应后再滴入2滴酚酞,溶液呈红色
溶液中滴加等体积0.1mol/LNaOH溶液,充分反应后再滴入2滴酚酞,溶液呈红色
实验3:向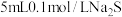 溶液中滴入
溶液中滴入 溶液,产生白色沉淀;再滴入几滴
溶液,产生白色沉淀;再滴入几滴 溶液,立即出现黑色沉淀
溶液,立即出现黑色沉淀
实验4:向 液中逐滴滴加等体积同浓度的盐酸,无明显现象
液中逐滴滴加等体积同浓度的盐酸,无明显现象
下列说法正确的是
 、
、 溶液的性质
溶液的性质实验1:向
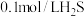 溶液中通入一定体积
溶液中通入一定体积 ,测得溶液pH为7
,测得溶液pH为7实验2:向
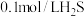 溶液中滴加等体积0.1mol/LNaOH溶液,充分反应后再滴入2滴酚酞,溶液呈红色
溶液中滴加等体积0.1mol/LNaOH溶液,充分反应后再滴入2滴酚酞,溶液呈红色实验3:向
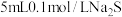 溶液中滴入
溶液中滴入 溶液,产生白色沉淀;再滴入几滴
溶液,产生白色沉淀;再滴入几滴 溶液,立即出现黑色沉淀
溶液,立即出现黑色沉淀实验4:向
 液中逐滴滴加等体积同浓度的盐酸,无明显现象
液中逐滴滴加等体积同浓度的盐酸,无明显现象下列说法正确的是
A.实验1得到的溶液中存在 |
B.由实验2可得出: |
C.由实验3可得出: |
D.实验4得到的溶液中存在: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关电解质溶液的说法不正确的是
| A.常温下向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中c(CH3COO-)·c(OH-)减小 |
B.将CH3COONa溶液从20℃升温至30℃,溶液中 减小 减小 |
C.向盐酸中加入氨水至中性,溶液中 =1 =1 |
D.向AgCl、AgBr的饱和溶液中加入少量AgNO3固体,溶液中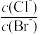 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某化学研究性学习小组对电解质溶液作如下归纳总结(均在常温下),正确的是
①常温下,pH=1的强酸溶液,加水稀释后,溶液中离子浓度均降低
②pH=2的盐酸和pH=1的盐酸, 之比为1:10
之比为1:10
③液态HCl、固体NaCl均不导电,所以HCl、NaCl均不是电解质
④已知醋酸电离平衡常数为 ;醋酸根水解常数为
;醋酸根水解常数为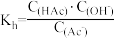 ;水的离子积为
;水的离子积为 ;则三者关系为
;则三者关系为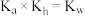
⑤pH值相同的醋酸和盐酸,分别用蒸馏水稀释到原来体积的m倍和n倍,稀释后两溶液的pH值仍相同,则m>n
①常温下,pH=1的强酸溶液,加水稀释后,溶液中离子浓度均降低
②pH=2的盐酸和pH=1的盐酸,
 之比为1:10
之比为1:10③液态HCl、固体NaCl均不导电,所以HCl、NaCl均不是电解质
④已知醋酸电离平衡常数为
 ;醋酸根水解常数为
;醋酸根水解常数为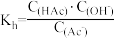 ;水的离子积为
;水的离子积为 ;则三者关系为
;则三者关系为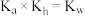
⑤pH值相同的醋酸和盐酸,分别用蒸馏水稀释到原来体积的m倍和n倍,稀释后两溶液的pH值仍相同,则m>n
| A.①②④ | B.③④⑤ | C.①②⑤ | D.②④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知室温时,0.1 mol·L-1 某一元酸HA在水中有0. 2%发生电离,下列叙述错误的是
| A.升高温度,溶液的酸性增强 |
| B.该溶液的c(H+)是2 ×10-4 mol·L-1 |
| C.此一元酸的电离平衡常数约为1×10-7 |
| D.向一元酸HA的溶液中,加水稀释,HA的电离平衡向正反应方向移动,但c(H+)减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,将浓度均为0.01mol/L的盐酸和醋酸分别加水稀释,溶液的pH随溶液体积变化的曲线如图所示(已知:电离度 ,
, ),下列说法正确的是
),下列说法正确的是

 ,
, ),下列说法正确的是
),下列说法正确的是
A. |
| B.Ⅰ为稀释醋酸时的pH变化曲线 |
| C.0.01mol/L的醋酸中,醋酸的电离度约为4% |
| D.在0.01mol/L的盐酸中,所含阴离子的总物质的量等于0.01mol |
您最近一年使用:0次

 溶液加水稀释,溶液中
溶液加水稀释,溶液中 和
和 的物质的量分数[
的物质的量分数[ 或
或 ]随溶液
]随溶液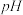 变化的关系如图所示。下列说法不正确的是
变化的关系如图所示。下列说法不正确的是
 时,
时,
 溶液加水稀释,
溶液加水稀释, 增大
增大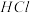 ,
, 增大,
增大, 减小
减小

 为阿伏加 德罗常数的值。关于常温下
为阿伏加 德罗常数的值。关于常温下 的
的 溶液,下列说法正确的是
溶液,下列说法正确的是 溶液中
溶液中 的数目为
的数目为
 增大,
增大, 减小
减小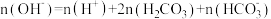
 ,则水解平衡向左移动,
,则水解平衡向左移动, 增大
增大 表示)、苹果酸(用
表示)、苹果酸(用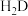 表示)、碳酸氢钠和碳酸钠等。已知:
表示)、碳酸氢钠和碳酸钠等。已知: ,常温下,柠檬酸的
,常温下,柠檬酸的 ,
,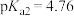 ,
, ;苹果酸的
;苹果酸的 ,
,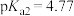 ;碳酸的
;碳酸的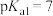 ,
,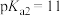 。下列说法正确的是
。下列说法正确的是