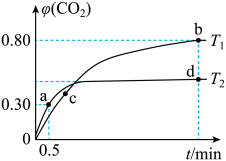
环境问题作为全球性问题,利用反应 I2O5(s)+5CO(g) I2(s)+5CO2(g)可消除CO 污染。不同温度下,向装有足量I2O5的2L恒容密闭容器中通入2molCO,测得CO2的体积分数 φ(CO2)随时间 t 变化曲线如图所示。下列说法正确的是
I2(s)+5CO2(g)可消除CO 污染。不同温度下,向装有足量I2O5的2L恒容密闭容器中通入2molCO,测得CO2的体积分数 φ(CO2)随时间 t 变化曲线如图所示。下列说法正确的是
 I2(s)+5CO2(g)可消除CO 污染。不同温度下,向装有足量I2O5的2L恒容密闭容器中通入2molCO,测得CO2的体积分数 φ(CO2)随时间 t 变化曲线如图所示。下列说法正确的是
I2(s)+5CO2(g)可消除CO 污染。不同温度下,向装有足量I2O5的2L恒容密闭容器中通入2molCO,测得CO2的体积分数 φ(CO2)随时间 t 变化曲线如图所示。下列说法正确的是
| A.T1<T2 ,K1 <K2 |
| B.0~a 段,v(CO)=0.12 mol / (L·min) |
| C.c 点时,正反应速率大于逆反应速率 |
| D.增大压强可以缩短反应时间和提高CO的平衡转化率 |
更新时间:2024-02-03 22:41:51
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在2L的密闭容器中,发生反应:3A(g)+B(g) 2C(g),若最初加入A和B都是4mol,10s时,反应达到平衡状态,已知0~10s内,v(A)=0.12mol·L-1·s-1。下列说法错误的是
2C(g),若最初加入A和B都是4mol,10s时,反应达到平衡状态,已知0~10s内,v(A)=0.12mol·L-1·s-1。下列说法错误的是
 2C(g),若最初加入A和B都是4mol,10s时,反应达到平衡状态,已知0~10s内,v(A)=0.12mol·L-1·s-1。下列说法错误的是
2C(g),若最初加入A和B都是4mol,10s时,反应达到平衡状态,已知0~10s内,v(A)=0.12mol·L-1·s-1。下列说法错误的是| A.达平衡时B的转化率为20% |
| B.0~10s内,v(C)=0.08mol·L-1·s-1 |
| C.反应过程中,A、B速率关系有v(A)=3v(B) |
| D.其他条件不变,延长反应时间,C的体积分数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温常压下向2L的恒温密闭容器中投入2mol A和1mol B,发生可逆反应 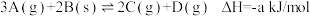 。5min后达平衡,测得容器中n(C)=0.8mol。则下列说法正确的是
。5min后达平衡,测得容器中n(C)=0.8mol。则下列说法正确的是
| A.3v(A)=2v(C)=0.16 mol/(L•min) |
| B.该可逆反应达平衡后,放出0.8a kJ的热能(假设化学能全转化为热能) |
| C.升高温度,该平衡正向速率减小,故平衡逆向移动 |
| D.使用催化剂或缩小容器体积,该平衡均不会移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某温度下,向2L密闭容器中通入1molNO和0.5molBr2,发生如下反应:2NO(g)+Br2(g) 2NOBr(g),Br2的物质的量随时间变化的实验数据如下表:
2NOBr(g),Br2的物质的量随时间变化的实验数据如下表:
下列说法正确的是
 2NOBr(g),Br2的物质的量随时间变化的实验数据如下表:
2NOBr(g),Br2的物质的量随时间变化的实验数据如下表:| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 | 35 |
| n(Br2)/mol | 0.38 | 0.30 | 0.25 | 0.23 | 0.20 | 0.20 | 0.20 |
| A.第18min的瞬时速率小于第25min的瞬时速率 |
| B.0~10min,消耗Br2的平均速率是0.02mol·L-1·min-1 |
| C.30~35min,NO的物质的量浓度逐渐降低 |
| D.任意时刻,容器中NO和Br2的转化率相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实中不能使用勒夏特列原理解释的是
| A.实验室中常使用饱和食盐水来收集氯气 |
| B.实验室制取乙酸乙酯时,将乙酸乙酯不断蒸出 |
| C.由H2(g)、I2(g)、HI(g)组成的平衡体系通过缩小体积加压后颜色变深 |
| D.将一氧化碳中毒者放入高压氧舱,缓解病人中毒症状 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】由下列实验及现象推出的相应结论正确的是
实验 | 现象 | 结论 | |
A | 向 溶液中滴加过量氯水,再加入淀粉 溶液中滴加过量氯水,再加入淀粉 溶液 溶液 | 先变橙色,后变蓝色 | 氧化性: |
B | 探究氢离子浓度对 、 、 相互转化的影响 相互转化的影响 | 向 | 增大氢离子浓度,转化平衡向生成 |
C | 向含有 和 和 的悬浊液中滴加 的悬浊液中滴加 溶液 溶液 | 生成黑色沉淀 |
|
D | ①某溶液中加入 溶液 溶液②再加足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】工业上用C6H5Cl和H2S高温气相反应制备苯硫酚(C6H5SH),同时有副产物C6H6生成:
I.C6H5Cl(g)+H2S(g)⇌C6H5SH(g)+HCl(g) ∆H1
II.C6H5Cl(g)+H2S(g) ⇌C6H6(g)+HCl(g)+ S8(g) ∆H2=-45.8kJ/mol
S8(g) ∆H2=-45.8kJ/mol
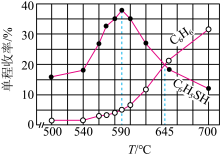
使C6H5Cl和H2S按物质的量1:1进入反应器,定时测定反应器尾端出来的混合气体中各产物的量,得到单程收率 与温度的关系如图所示,下列说法不正确的是
与温度的关系如图所示,下列说法不正确的是
I.C6H5Cl(g)+H2S(g)⇌C6H5SH(g)+HCl(g) ∆H1
II.C6H5Cl(g)+H2S(g) ⇌C6H6(g)+HCl(g)+
 S8(g) ∆H2=-45.8kJ/mol
S8(g) ∆H2=-45.8kJ/mol使C6H5Cl和H2S按物质的量1:1进入反应器,定时测定反应器尾端出来的混合气体中各产物的量,得到单程收率
 与温度的关系如图所示,下列说法不正确的是
与温度的关系如图所示,下列说法不正确的是
| A.ΔH1<0 |
| B.其他条件不变,增加H2S的量能提高C6H5Cl的平衡转化率 |
| C.645℃,延长反应时间,可以提高C6H6的单程收率 |
D.645℃时,反应I的化学平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某温度下反应:ClF(g)+F2(g) ClF3(g)
ClF3(g)  <0,在密闭容器中达到平衡,下列说法中正确的是
<0,在密闭容器中达到平衡,下列说法中正确的是
 ClF3(g)
ClF3(g)  <0,在密闭容器中达到平衡,下列说法中正确的是
<0,在密闭容器中达到平衡,下列说法中正确的是| A.温度不变,缩小体积,ClF的转化率增大 |
| B.温度不变,增大体积,ClF3的产率提高 |
| C.升高温度,增大体积,有利于平衡向正向移动 |
| D.降低温度,体积不变,F2的转化率减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法中正确的是
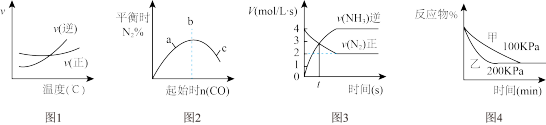

A. ,如图1说明此反应的正反应是放热反应 ,如图1说明此反应的正反应是放热反应 |
B.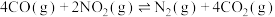 ,如图2说明 ,如图2说明 的转化率 的转化率 |
C.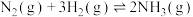 ,如图③说明t秒时合成氨反应达到平衡 ,如图③说明t秒时合成氨反应达到平衡 |
D. ,如图④说明生成物D一定不是气体 ,如图④说明生成物D一定不是气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在一密闭容器中,反应aA(g) bB(g)达平衡后,测得B的浓度为0.5 mol·L-1,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度变为0.3 mol·L-1,则下列说法正确的是
bB(g)达平衡后,测得B的浓度为0.5 mol·L-1,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度变为0.3 mol·L-1,则下列说法正确的是
 bB(g)达平衡后,测得B的浓度为0.5 mol·L-1,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度变为0.3 mol·L-1,则下列说法正确的是
bB(g)达平衡后,测得B的浓度为0.5 mol·L-1,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度变为0.3 mol·L-1,则下列说法正确的是| A.平衡向逆反应方向移动了 | B.物质A的转化率减少了 |
| C.物质B的质量分数增大了 | D.a>b |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)⇌2CO(g),平衡时,体系中气体体积分数与温度的关系如图所示,已知气体分压(P分)=气体总压(P总)×体积分数,下列说法不正确的是
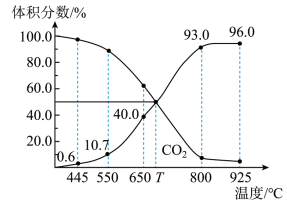
| A.550℃时,若充入惰性气体,v正,v逆均减小 |
| B.650℃时,反应达平衡后CO2的转化率为25.0% |
| C.T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动 |
| D.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp=23.04P总 |
您最近一年使用:0次


 溶液中缓慢滴加硫酸,黄色变为橙色
溶液中缓慢滴加硫酸,黄色变为橙色 的溶解度小于
的溶解度小于
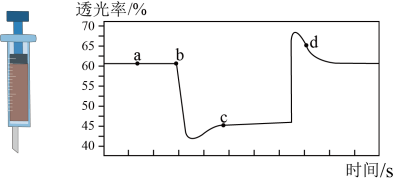
 装入带活塞的密闭容器中,当反应
装入带活塞的密闭容器中,当反应 达到平衡后,改变下列一个条件其中叙述正确的是
达到平衡后,改变下列一个条件其中叙述正确的是

