室温下,通过下列实验探究某些碳酸盐溶液及碳酸氢盐溶液的性质,
已知: ,
, ,
,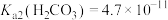 。
。
下列有关说法正确的是
已知:
 ,
, ,
,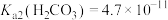 。
。| 实验 | 实验操作和现象 |
| 1 | 测量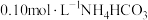 溶液的pH,测得pH为a 溶液的pH,测得pH为a |
| 2 | 测量某浓度的 溶液的pH,测得pH约为9.4 溶液的pH,测得pH约为9.4 |
| 3 | 向 通入足量二氧化碳充分反应后,测得pH约为6.6 通入足量二氧化碳充分反应后,测得pH约为6.6 |
| 4 | 向 溶液中加入 溶液中加入 粉末,过滤,向滤渣中加入HCl溶液产生气泡 粉末,过滤,向滤渣中加入HCl溶液产生气泡 |
| A.实验1测得的pH值a<7 |
B.实验2溶液中: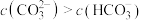 |
C.实验3所得溶液中: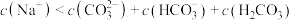 |
D.实验4第一步反应的离子方程式为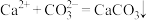 |
更新时间:2024-03-07 11:12:17
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】已知三种酸的电离平衡常数,下列说法不正确的是
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 |
| 电离平衡常数 | 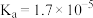 | 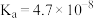 | 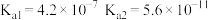 |
A.三种酸的酸性由强到弱的顺序是: |
B. 与NaClO溶液反应生成HClO与 与NaClO溶液反应生成HClO与 |
C.常温下,浓度均为0.1mol/L的溶液的碱性: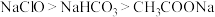 |
| D.向NaClO溶液中滴加醋酸,可生成HClO,使杀菌、消毒能力增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下进行下列实验,根据实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向X溶液中滴加几滴新制氯水,振荡,再加入少KSCN溶液,溶液变为红色 | X溶液中一定含有Fe2+ |
| B | 某澄清溶液中加入盐酸酸化的氯化钡溶液,产生白色沉淀 | 则原溶液中一定含有SO |
| C | 向3mLKI溶液中滴加几滴溴水,振荡,再滴加几滴淀粉溶液,溶液显蓝色 | Br2的氧化性比I2的强 |
| D | 用pH试纸测得:Na2CO3溶液的pH约为10,Na2SO3溶液的pH约为9 | H2SO3电离出H+的能力比H2CO3的强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温下,用相同浓度的NaOH溶液,分别滴定浓度均为0.1mol·L-1的三种酸(HA、HB和HD)溶液,滴定的曲线如图所示,下列判断正确的是( )


| A.同浓度的三种盐溶液的pH:pH(NaA)>pH(NaB)>pH(NaD) |
| B.pH=7时,三种溶液中:c(A-)<c(B-)<c(D-) |
| C.滴定至P点时,溶液中:c(Na+)>c(B-)>c(HB)>c(H+)>c(OH-) |
| D.当中和百分数达100%时将三种溶液混合后:c(HA)+c(HB)+c(HD)=c(OH-)-c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】若定义pC是溶液中微粒物质的量浓度的负对数,则常温下一定浓度的某酸(H2A)水溶液中pC(H2A)、pC(HA-)、pC(A2-)随着溶液pH的变化曲线如图所示。下列说法一定正确的是
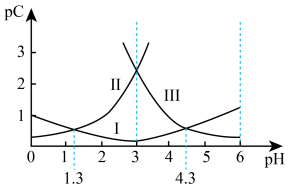

| A.0.1 mol/L的NaHA溶液显碱性 |
| B.常温下,该酸的电离常数Ka2=10-4.3 |
| C.常温下,c(H2A)+c(HA-)+c(A2-)是定值 |
| D.常温下,pH=3时,c(HA-)=c(A2-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列关于溶液中离子的说法正确的是
| A.0.1 mol·L-1的Na2CO3溶液中离子浓度关系:c (Na+)=2c (CO32-)+c (HCO3-)+c (H2CO3) |
| B.0.1 mol·L-1的NH4Cl和0.1 mol·L-1的NH3·H2O等体积混合后溶液中的离子浓度关系:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C.常温下,醋酸钠溶液中滴加少量醋酸使溶液的pH<7,则混合溶液中,离子浓度关系:c (Na+)=c (CH3COO-) |
| D.0.1 mol·L-1的NaHS溶液中离子浓度关系:c (OH-)=c (H+)-c (S2-)+c (H2S) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
| A.中和等体积等物质的量浓度的盐酸和氢硫酸,盐酸消耗的氢氧化钠更多 |
B.将等物质的量的Na2CO3和NaHCO3混合溶于水中: >1 >1 |
| C.pH=9的Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| D.pH相等的①NH4NO3 ②(NH4)2SO4 ③NH4HSO4溶液中,c(NH4+)大小顺序为:①>②>③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,下列实验方案以及得出的结论均正确的是
A.用广泛 试纸测 试纸测 溶液的 溶液的 ,证明 ,证明 为弱酸 为弱酸 |
B.分别测 溶液和 溶液和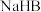 溶液的 溶液的 ,若 ,若 溶液的 溶液的 大,则 大,则 的酸性比 的酸性比 弱 弱 |
C.取等体积、等浓度的 溶液和盐酸,均稀释相同倍数,若稀释后 溶液和盐酸,均稀释相同倍数,若稀释后 溶液的 溶液的 较小,则 较小,则 为弱酸 为弱酸 |
D. 为二元弱酸,其电离平衡常数为 为二元弱酸,其电离平衡常数为 、 、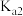 ,用广泛 ,用广泛 试纸测 试纸测 溶液的 溶液的 ,若 ,若 ,则 ,则 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关说法正确的是
| A.H3PO2与足量的NaOH反应生成NaH2PO2,则NaH2PO2属于酸式盐 |
B.已知电离平衡常数(25℃)HClO Ka=2.95×l0–8;H2CO3Ka1=4.3×l0–7、Ka2=5.6×l0–11,将少量的CO2通入NaClO溶液中反应离子方程式为2ClO-+CO2+H2O=2HClO+ |
| C.在测定中和热时,用铜质搅拌棒代替环形玻璃搅拌棒,对测定结果无影响 |
| D.探究温度对硫代硫酸钠与硫酸反应速率的影响时,若先将两种溶液混合并计时,再用水浴加热至设定温度,则测得的反应速率偏低 |
您最近一年使用:0次

 溶液可作金属焊接的除锈剂
溶液可作金属焊接的除锈剂 溶液时,为抑制
溶液时,为抑制 水解,先将
水解,先将 溶液和
溶液和 溶液蒸干所得产物相同
溶液蒸干所得产物相同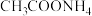 和
和 溶液中,
溶液中, 前者大于后者
前者大于后者 、
、 ,下列说法正确的是
,下列说法正确的是 溶液和
溶液和 溶液,溶质的物质的量浓度:
溶液,溶质的物质的量浓度: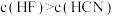
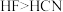
 溶液中滴加
溶液中滴加
 溶液和
溶液和


