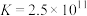常温下, 在Na2CO3溶液中发生反应,可能生成
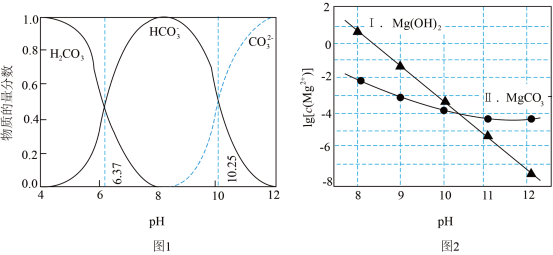
在Na2CO3溶液中发生反应,可能生成 或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合
或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合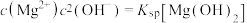 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合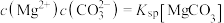 。利用平衡原理分析,下列说法正确的是
。利用平衡原理分析,下列说法正确的是
 在Na2CO3溶液中发生反应,可能生成
在Na2CO3溶液中发生反应,可能生成 或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合
或MgCO3。图1表示Na2CO3溶液中各含碳物种的物质的量分数与溶液pH的关系;图2中曲线Ⅰ的离子浓度关系符合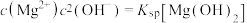 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合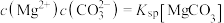 。利用平衡原理分析,下列说法正确的是
。利用平衡原理分析,下列说法正确的是
A.常温时, 的水解常数 的水解常数 |
B.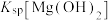 的数量级为 的数量级为 |
C.由图2,当pH=11, 时,有沉淀生成 时,有沉淀生成 |
D.由图1和图2,在pH=8,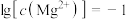 时,溶液中发生反应: 时,溶液中发生反应: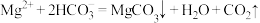 |
更新时间:2024-03-13 14:49:50
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】已知: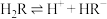 ,
, ,CuR难溶于水。常温下,
,CuR难溶于水。常温下,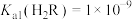 ,
, ,当10mL0.1mol/LH2R溶液中缓慢加入少量CuSO4粉末,溶液中
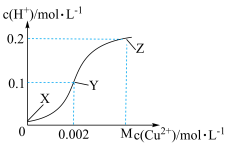
,当10mL0.1mol/LH2R溶液中缓慢加入少量CuSO4粉末,溶液中 与
与 的变化如图所示(忽略溶液的体积变化)。下列有关说法不正确的是
的变化如图所示(忽略溶液的体积变化)。下列有关说法不正确的是
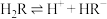 ,
, ,CuR难溶于水。常温下,
,CuR难溶于水。常温下,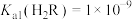 ,
, ,当10mL0.1mol/LH2R溶液中缓慢加入少量CuSO4粉末,溶液中
,当10mL0.1mol/LH2R溶液中缓慢加入少量CuSO4粉末,溶液中 与
与 的变化如图所示(忽略溶液的体积变化)。下列有关说法不正确的是
的变化如图所示(忽略溶液的体积变化)。下列有关说法不正确的是
A.根据Y点数据可求得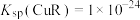 |
B.Y点对应的溶液中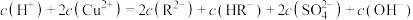 |
| C.常温下,NaHR溶液显碱性 |
| D.X点溶液的pH≈5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】已知常温下, 。用
。用 的氨水滴定
的氨水滴定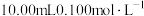 的一元酸HA的溶液,滴定过程中加入氨水的体积(V)与溶液中的
的一元酸HA的溶液,滴定过程中加入氨水的体积(V)与溶液中的 关系如图所示。下列说法不正确的是
关系如图所示。下列说法不正确的是
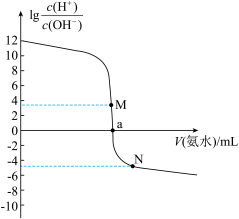
 。用
。用 的氨水滴定
的氨水滴定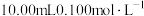 的一元酸HA的溶液,滴定过程中加入氨水的体积(V)与溶液中的
的一元酸HA的溶液,滴定过程中加入氨水的体积(V)与溶液中的 关系如图所示。下列说法不正确的是
关系如图所示。下列说法不正确的是
| A.HA为强酸,a=10 |
| B.水的电离程度:M点>N点 |
C.常温下,反应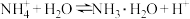 的平衡常数 的平衡常数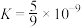 |
D.当滴入 氨水时,溶液中存在: 氨水时,溶液中存在: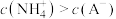 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】室温下,将cmol/L的CH3COOH溶液1.0L与0.1molNaOH固体混合,使之充分反应后得到b点对应的溶液。然后向该混合溶液中通入HCI 气体或加入NaOH固体(忽略体积和温度变化),溶液pH随通入(或加入)物质的量的变化如下图所示。下列叙述不正确的是
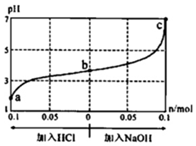

| A.a点对应的混合溶液中:c(CH3COOH)>c(Na+)=c(Cl-)>c(OH-) |
B.向b点对应的溶液中通入HCl气体,充分反应后,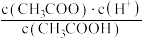 的值保持不变 的值保持不变 |
| C.c点对应的混合溶液中c(CH3COO-)=c(Na+) |
| D.起始醋酸溶液物质的量浓度c(CH3COOH)=0.2mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列有关说法正确的是
| A.向20mL0.5mol/LFeBr2(aq)中通入224mLCl2(标准状况):2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
| B.25℃时,向2mL0.1mol﹒L-1Na2S 溶液中滴入几滴 0.1mol﹒L-1ZnSO4 溶液,有白色沉淀生成;再滴加几滴 0.1mol﹒L-1CuSO4 溶液,则又有黑色沉淀生成,可以得出结论:Ksp(ZnS)>Ksp(CuS) |
| C.向30mL0.5mol/LNaOH(aq)中通入224mLCO2(标准状况):3OH-+2CO2=CO32-+HCO3-+H2O |
D.Cu(OH)2在水中存在着如下沉淀溶解平衡:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO4溶液中,c(Cu2+)=0.02 mol·L-1,在常温下如果要生成 Cu(OH)2 沉淀,需要向 CuSO4 溶液加入碱溶液来调整pH,使溶液的pH 大于3 Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO4溶液中,c(Cu2+)=0.02 mol·L-1,在常温下如果要生成 Cu(OH)2 沉淀,需要向 CuSO4 溶液加入碱溶液来调整pH,使溶液的pH 大于3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】已知常温下AgCl和AgBr的溶解度分别为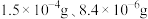 ,将AgCl与AgBr的饱和溶液等体积混合,再加入足量
,将AgCl与AgBr的饱和溶液等体积混合,再加入足量 溶液,发生的反应为
溶液,发生的反应为
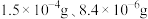 ,将AgCl与AgBr的饱和溶液等体积混合,再加入足量
,将AgCl与AgBr的饱和溶液等体积混合,再加入足量 溶液,发生的反应为
溶液,发生的反应为| A.只有AgBr沉淀生成 | B.AgCl和AgBr沉淀等量生成 |
| C.AgCl沉淀多于AgBr沉淀 | D.AgCl沉淀少于AgBr沉淀 |
您最近一年使用:0次
【推荐1】下图为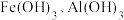 和
和 在水中达沉淀溶解平衡时的
在水中达沉淀溶解平衡时的 关系图(
关系图( ;
; 可认为
可认为 离子沉淀完全)。下列叙述正确的是
离子沉淀完全)。下列叙述正确的是
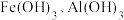 和
和 在水中达沉淀溶解平衡时的
在水中达沉淀溶解平衡时的 关系图(
关系图( ;
; 可认为
可认为 离子沉淀完全)。下列叙述正确的是
离子沉淀完全)。下列叙述正确的是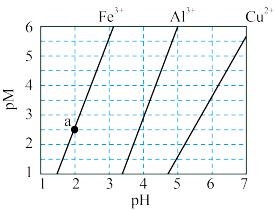
A.由 点可求得 点可求得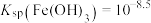 |
B. 时 时 的溶解度为 的溶解度为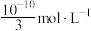 |
C.浓度均为 的 的 和 和 可通过分步沉淀进行分离 可通过分步沉淀进行分离 |
D.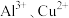 混合溶液中 混合溶液中 时二者不会同时沉淀 时二者不会同时沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
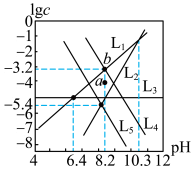
【推荐2】将CaCO3(s)或ZnCO3(s)悬浊液置于分压固定的CO2气相中,体系中pH与lgc关系如图所示,c为H2CO3、HCO 、CO
、CO 、Ca2+、Zn2+的浓度,单位为mol·L-1。已知:Ksp(CaCO3)>Ksp(ZnCO3),下列说法正确的是
、Ca2+、Zn2+的浓度,单位为mol·L-1。已知:Ksp(CaCO3)>Ksp(ZnCO3),下列说法正确的是
 、CO
、CO 、Ca2+、Zn2+的浓度,单位为mol·L-1。已知:Ksp(CaCO3)>Ksp(ZnCO3),下列说法正确的是
、Ca2+、Zn2+的浓度,单位为mol·L-1。已知:Ksp(CaCO3)>Ksp(ZnCO3),下列说法正确的是
| A.Kal(H2CO3)=10-6.4,Ksp(ZnCO3)=10-10.8 |
B.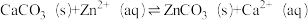 ,平衡常数: ,平衡常数: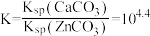 |
C.L1表示lgc(CO )-pH曲线 )-pH曲线 |
| D.向a点溶液中加入ZnCl2,可以达到b点溶液 |
您最近一年使用:0次

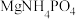 )沉淀法是一种新的处理高氨氮废水的方法,其基本原理是通过向高氨氮废水中投加含
)沉淀法是一种新的处理高氨氮废水的方法,其基本原理是通过向高氨氮废水中投加含 的化合物和磷酸盐,使之与
的化合物和磷酸盐,使之与 生成
生成 的关系如图。
的关系如图。

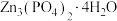 ,难溶于水]是一种性能优良的绿色环保防锈颜料。实验室以锌灰(含Zn、ZnO、PbO、CuO、FeO、
,难溶于水]是一种性能优良的绿色环保防锈颜料。实验室以锌灰(含Zn、ZnO、PbO、CuO、FeO、 、
、 等)为原料制备
等)为原料制备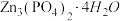 的流程如下:
的流程如下: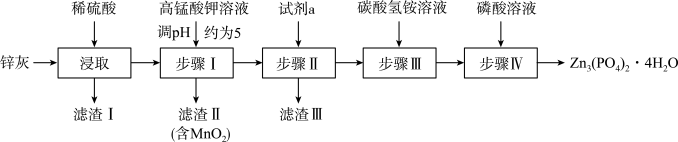
 ,
, 。
。 溶液反应的离子方程式为
溶液反应的离子方程式为
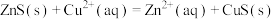 的
的