其他条件不变,升高温度,下列数据不一定增大的是
A. 的水解常数 的水解常数 | B. 电离常数 电离常数 |
C.可逆反应的化学平衡常数 | D.蒸馏水中的 电离度 电离度 |
更新时间:2024-03-18 09:25:13
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】室温下,分别向浓度均为 的
的 和盐酸各20mL,滴加
和盐酸各20mL,滴加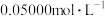 的
的 溶液,得到滴定曲线如下(忽略
溶液,得到滴定曲线如下(忽略 分解),下列叙述
分解),下列叙述不正确 的是

 的
的 和盐酸各20mL,滴加
和盐酸各20mL,滴加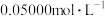 的
的 溶液,得到滴定曲线如下(忽略
溶液,得到滴定曲线如下(忽略 分解),下列叙述
分解),下列叙述
A. 的水解平衡常数约为 的水解平衡常数约为 |
B.b点与a点溶液混合后 |
C.加入 溶液时,两溶液中水的电离程度 溶液时,两溶液中水的电离程度 |
D.a点存在: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃时,将浓度均为0.1mol·L-1,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,且保持 Va+Vb=100mL,Va、Vb 与混合液的 pH 的关系如图所示.下列说法正确的是


| A.Ka(HA)≈1×10-6 |
B.c点时,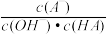 随温度升高而增大 随温度升高而增大 |
| C.a→c过程中水的电离程度始终增大 |
| D.b点时,c(B+)=c(A-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在298K下,“H2A-HA--A2-”的水溶液体系中,H2A、HA-、A2-三种微粒的物质的量分数随溶液pH变化(仅用H2A和NaOH调节pH)的关系如图所示。下列说法正确的是
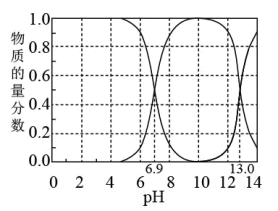

| A.Ka1(H2A)的数量级为10-6 |
| B.在pH=13.0的上述溶液中存在三个平衡 |
C.当体系呈中性时,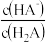 > >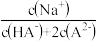 |
| D.NaHA溶液中,c(Na+)>c(HA-)>c(A2-)>c(H2A) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,向10mL0.2mol·L-1的MOH中逐滴加入 0.2mol·L-1的CH3COOH溶液,溶液的导电能力如图1所示,溶液的pH变化如图2所示(已知:常温时,相同浓度的氨水和醋酸溶液的电离常数均为1.8×10-5),下列说法不正确的是


| A.图1中N点时,加入CH3COOH溶液的体积为10mL |
| B.MOH是一种弱碱,相同条件下其碱性弱于NH3·H2O的碱性 |
| C.图2中bc 段,水的电离程度逐渐减弱 |
| D.若c点对应醋酸的体积是15ml,则此时溶液中c(CH3COOH)+c(CH3COO-)>0.1mol·L-1 |
您最近一年使用:0次

 ]是一元有机弱碱,简写为MOH。常温下,向20mL 0.5mol/L的MOH溶液中滴加浓度为0.25mol/L的HCl溶液,溶液中
]是一元有机弱碱,简写为MOH。常温下,向20mL 0.5mol/L的MOH溶液中滴加浓度为0.25mol/L的HCl溶液,溶液中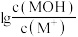 、
、 中和率(中和率=
中和率(中和率= )的变化如图所示。下列说法错误的是
)的变化如图所示。下列说法错误的是
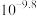

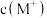 的浓度大小:d>c
的浓度大小:d>c
 ,25℃时,溶液中X+、
,25℃时,溶液中X+、 、X-的物质的量分数δ(X)随pH变化的曲线如图所示。已知δ(X)=
、X-的物质的量分数δ(X)随pH变化的曲线如图所示。已知δ(X)= ,下列叙述错误的是
,下列叙述错误的是


