二元有机酸( )的电离常数
)的电离常数 、
、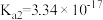 。BaX难溶于水,常温下,将BaX溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中
。BaX难溶于水,常温下,将BaX溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是 易溶于水。
易溶于水。
 )的电离常数
)的电离常数 、
、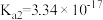 。BaX难溶于水,常温下,将BaX溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中
。BaX难溶于水,常温下,将BaX溶解在一定浓度的HY溶液中,直至不再溶解,测得混合液中 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是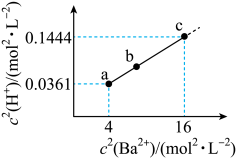
 易溶于水。
易溶于水。| A.NaHX溶液显碱性 |
B.溶度积 |
C.b点: |
D.若0.01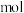 BaX溶于1L BaX溶于1L 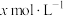 HY溶液中得到氢离子浓度与c点相等,则 HY溶液中得到氢离子浓度与c点相等,则 |
更新时间:2024-04-21 21:33:02
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】科学家发现某些生物酶能将海洋中的NO2转化为N2,该过程的总反应为 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是
 。设NA为阿伏加德罗常数的值,下列说法正确的是
。设NA为阿伏加德罗常数的值,下列说法正确的是A.1.5mol·L-1 NH4Cl溶液中含 的数目为1.5NA 的数目为1.5NA |
| B.标准状况下, 22.4 LN2中含π键的数目为2NA |
| C.18 g H2O 中含电子对的数目为2NA |
| D.生物酶将NO2转化为N2的过程叫作氮的固定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】证据推理是学习化学的重要方法,下列证据与推理的关系正确的是
| 选项 | 证据 | 推理 |
| A | 用pH试纸测得NaA溶液的pH约为10,NaB溶液的pH约为9 | Ka(HA)<Ka(HB) |
| B | 向KI稀溶液中滴加新制氯水,没有看到溶液颜色加深 | 过量的Cl2将I2氧化成IO |
| C | 向1mL2mol·L-1AgNO3溶液中依次加入2滴浓度均为0.1 mol·L-1的NaCl溶液和KI溶液,先出现白色沉淀,后出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 向淀粉溶液中加入稀硫酸,水浴加热后,再加入银氨溶液水浴加热,未出现银镜 | 淀粉未发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】侯氏制碱法中涉及反应: 。
。 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是
 。
。 是阿伏加德罗常数的值,下列说法正确的是
是阿伏加德罗常数的值,下列说法正确的是A.  溶液中所含配位键数目为 溶液中所含配位键数目为 |
B.常温常压下,44g 所含分子数目为 所含分子数目为 |
C.1mol 晶体中所含 晶体中所含 数目为 数目为 |
D.17g 溶于水所得溶液中 溶于水所得溶液中 和 和 数目之和为 数目之和为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
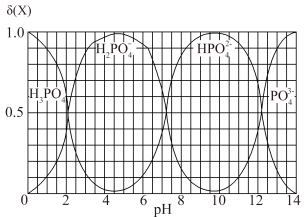
【推荐2】298K时,在H3PO4溶液中滴入NaOH溶液,溶液中H3PO4、H2PO 、HPO
、HPO 、PO
、PO 的物质的量分数δ(X),δ(X)随pH的变化如图所示。下列叙述错误的是
的物质的量分数δ(X),δ(X)随pH的变化如图所示。下列叙述错误的是
 、HPO
、HPO 、PO
、PO 的物质的量分数δ(X),δ(X)随pH的变化如图所示。下列叙述错误的是
的物质的量分数δ(X),δ(X)随pH的变化如图所示。下列叙述错误的是
| A.Ka2(H3PO4)的数量级为10-8 |
B.Kh(HPO )=1.0×10-6.8 )=1.0×10-6.8 |
C.pH=7时c(H2PO )>c(HPO )>c(HPO ) ) |
| D.NaH2PO4溶液显碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
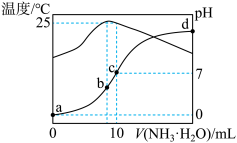
【推荐1】在某温度时,将n mol/L氨水滴入10 mL 1.0mol/L盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是

A.a点 |
| B.b点水的电离程度最大,c点水的电离程度最小 |
C.d点: |
D.25℃时, 水解平衡常数为 水解平衡常数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,常见的无机酸在水溶液中的电离子平衡常数如表,下列选项正确的是( )
| 氢氰酸(HCN) | 碳酸(H2CO3) | 氢氟酸(HF) |
| K=4.9×10﹣10 | K1=4.4×10﹣7 K2=4.7×10﹣11 | K=6.61×10﹣4 |
A.氰化钠溶液中通入少量CO2:2CN﹣+H2O+CO2═2HCN+CO |
| B.NaCN与HCN的混合溶液中一定有:c(Na+)>c(CN﹣)>c(HCN)>c(H+)>c(OH-) |
| C.25℃时CN-的水解平衡常数约为1.6×10-5 |
| D.NaCN与HCN的混合溶液中:2c(Na+)=c(CN-)+c(HCN) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
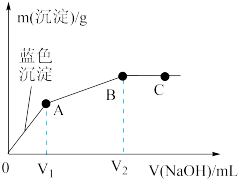
【推荐1】向含MgCl2和CuCl2的溶液中逐滴加入0.1mol/L的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是

| A.原溶液中MgCl2和CuCl2的物质的量浓度之比为3:1 |
| B.该实验不能证明Cu(OH)2的Ksp比Mg(OH)2的Ksp小 |
| C.若向Mg(OH)2悬浊液中滴入CuCl2溶液,一定会有Cu(OH)2生成 |
| D.水的电离程度:A>B>C |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】钌(Ru)广泛应用于电子、航空航天、化工等领域。自然界中钌的矿产资源很少,故从含钌废料中回收金属钌具有很强的现实意义。某科研小组设计了一种从含金属钌单质的废料中分离提纯金属钌的工艺,其流程图如下:
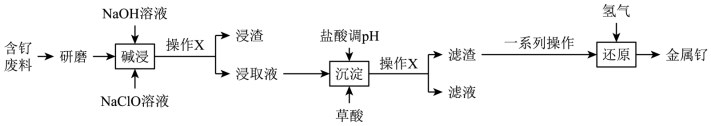
已知:“碱浸”工序中Ru单质生成了Na2RuO4;“沉淀”工序中滤渣的主要成分为RuO2。下列说法中错误的是

已知:“碱浸”工序中Ru单质生成了Na2RuO4;“沉淀”工序中滤渣的主要成分为RuO2。下列说法中错误的是
| A.为提高“碱浸”时钌的浸出率,可采取延长浸取时间、适当提高温度的措施 |
| B.“碱浸”时生成Na2RuO4的方程式中,氧化剂和还原剂的化学计量数之比为1:3 |
| C.在实验室进行操作X时,必须要用到的玻璃仪器为漏斗、烧杯、玻璃棒 |
| D.“沉淀”时加入草酸的目的是还原Na2RuO4 |
您最近一年使用:0次
【推荐3】常温下,用AgNO3溶液分别滴定浓度均为0.0lmol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如图所示(不考虑C2O42-的水解)。已知Ksp(AgC1)数量级为10-10。下列叙述不正确的是( )
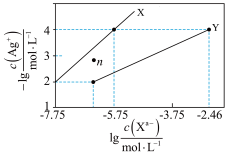

| A.图中Y线代表的Ag2C2O4 |
| B.n点表示AgCl的过饱和溶液 |
| C.向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成AgC1沉淀 |
| D.Ag2C2O4+2Cl-=2AgC1+C2O42-的平衡常数为1.0×10-0.7l |
您最近一年使用:0次

 溶液的pH比NaF溶液的小
溶液的pH比NaF溶液的小
 溶液中加入过量的稀
溶液中加入过量的稀 ,溶液变黄,再加入淀粉KI溶液,溶液变蓝
,溶液变黄,再加入淀粉KI溶液,溶液变蓝
 溶液,分别滴入相同浓度相同体积的NaCl和KI,只有后者有沉淀
溶液,分别滴入相同浓度相同体积的NaCl和KI,只有后者有沉淀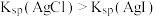
 :
: 固体
固体 、
、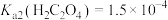 、
、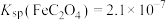 。下列说法正确的是
。下列说法正确的是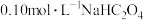 溶液中存在:
溶液中存在:



 溶液中存在平衡:
溶液中存在平衡: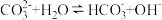 。下列有关说法正确的是
。下列有关说法正确的是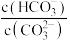 变大
变大

