25℃时,向二元弱酸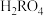 溶液中滴加NaOH溶液,混合溶液中
溶液中滴加NaOH溶液,混合溶液中 [X表示
[X表示 或
或 ]随pH的变化关系如图所示。下列说法正确的是
]随pH的变化关系如图所示。下列说法正确的是
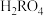 溶液中滴加NaOH溶液,混合溶液中
溶液中滴加NaOH溶液,混合溶液中 [X表示
[X表示 或
或 ]随pH的变化关系如图所示。下列说法正确的是
]随pH的变化关系如图所示。下列说法正确的是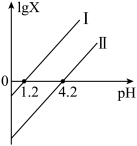
A.Ⅱ中X表示的是 |
B.当溶液pH=4.2时,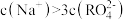 |
C.若溶液中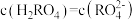 ,则pH=2.7 ,则pH=2.7 |
D.0.1 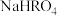 溶液中: 溶液中: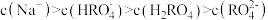 |
更新时间:2024-05-12 20:00:36
|
相似题推荐
单选题
|
较难
(0.4)
名校
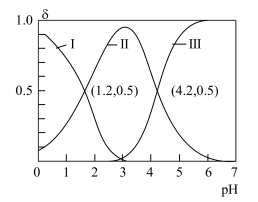
【推荐1】H2A为二元酸,其电离过程为:H2A⇌H++HA-、HA-⇌H++A2-。常温时,向10mL 0.1mol∙L-1H2A水溶液中逐滴滴加 0.1mol∙L-1NaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
A.H2A的 的数量级为 的数量级为 |
| B.当溶液中c(H2A)=c(A2-)时,pH=2.9 |
| C.当溶液中c(Na+)=2c(A2-)+c(HA-)时,加入V(NaOH溶液)>10mL |
D.向 的溶液中继续滴加NaOH溶液,水的电离程度减小 的溶液中继续滴加NaOH溶液,水的电离程度减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】25℃时,用 的NaOH溶液滴定100ml某二元弱酸
的NaOH溶液滴定100ml某二元弱酸 ,滴定过程中溶液的pH及
,滴定过程中溶液的pH及 、
、 及
及 的物质的量浓度变化如图所示,下列说法
的物质的量浓度变化如图所示,下列说法不正确 的是

 的NaOH溶液滴定100ml某二元弱酸
的NaOH溶液滴定100ml某二元弱酸 ,滴定过程中溶液的pH及
,滴定过程中溶液的pH及 、
、 及
及 的物质的量浓度变化如图所示,下列说法
的物质的量浓度变化如图所示,下列说法
A. 的 的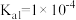 |
B.在Y点时,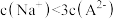 |
C.X点、Z点时水的电离程度: |
D. 溶液中: 溶液中: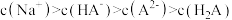 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】已知 为二元弱碱,
为二元弱碱, 。25℃时,
。25℃时, 的水溶液中有
的水溶液中有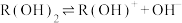
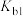 ,
,
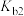 。25℃时,用
。25℃时,用 溶液滴定
溶液滴定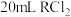 溶液,溶液中
溶液,溶液中 、
、 、
、 的分布分数
的分布分数 {如
{如 随pOH变化曲线及滴定曲线如图所示。下列说法错误的是
随pOH变化曲线及滴定曲线如图所示。下列说法错误的是
 为二元弱碱,
为二元弱碱, 。25℃时,
。25℃时, 的水溶液中有
的水溶液中有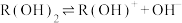
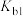 ,
,
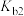 。25℃时,用
。25℃时,用 溶液滴定
溶液滴定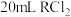 溶液,溶液中
溶液,溶液中 、
、 、
、 的分布分数
的分布分数 {如
{如 随pOH变化曲线及滴定曲线如图所示。下列说法错误的是
随pOH变化曲线及滴定曲线如图所示。下列说法错误的是
A.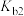 的数量级为 的数量级为 | B.水的电离度:w>z |
C.25℃时,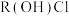 溶液呈酸性 溶液呈酸性 | D.z点可用甲基橙作指示剂指示滴定突变点 |
您最近一年使用:0次
【推荐1】利用平衡移动原理,分析一定温度下 在不同
在不同 的
的 体系中的可能产物。
体系中的可能产物。
已知:i.图1中曲线表示 体系中各含碳粒子的物质的量分数与
体系中各含碳粒子的物质的量分数与 的关系。
的关系。
ii.2中曲线Ⅰ的离子浓度关系符合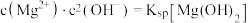 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合 [注:起始
[注:起始 ,不同
,不同 下
下 由图1得到]。
由图1得到]。
 在不同
在不同 的
的 体系中的可能产物。
体系中的可能产物。已知:i.图1中曲线表示
 体系中各含碳粒子的物质的量分数与
体系中各含碳粒子的物质的量分数与 的关系。
的关系。ii.2中曲线Ⅰ的离子浓度关系符合
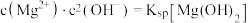 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合 [注:起始
[注:起始 ,不同
,不同 下
下 由图1得到]。
由图1得到]。
A.由图1, |
B.由图2,初始状态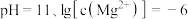 ,无沉淀生成 ,无沉淀生成 |
C.由图2,初始状态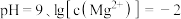 ,平衡后溶液中存在 ,平衡后溶液中存在 |
D.由图1和图2,初始状态 、 、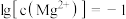 ,发生反应: ,发生反应: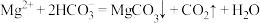 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】用NA表示阿伏伽德罗常数,N表示微粒数,下列说法正确的是
| A.7.8 g苯含有碳碳双键的数目为0.3NA |
| B.标准状况下,足量的Fe与2.24 L Cl2反应转移电子的数目为0.3NA |
| C.273K、101kPa下,28 g乙烯与丙烯混合物中含有C-H键的数目为5NA |
| D.100 mL1mol·L-1的的NaF中:N(F-)+N(HF)=0. 1 NA |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】甘氨酸盐酸盐(HOOCCH2NH3Cl)的水溶液呈酸性,溶液中存在以下平衡:
HOOCCH2NH
 -OOCCH2NH
-OOCCH2NH +H+ K1
+H+ K1
-OOCCH2NH
 -OOCCH2NH2+H+ K2
-OOCCH2NH2+H+ K2
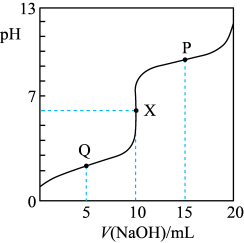
常温时,向10mL一定浓度的HOOCCH2NH3Cl的水溶液中滴入同浓度的NaOH溶液。混合溶液pH随加入NaOH溶液体积的变化如图所示。下列说法不正确的是
HOOCCH2NH

 -OOCCH2NH
-OOCCH2NH +H+ K1
+H+ K1-OOCCH2NH

 -OOCCH2NH2+H+ K2
-OOCCH2NH2+H+ K2常温时,向10mL一定浓度的HOOCCH2NH3Cl的水溶液中滴入同浓度的NaOH溶液。混合溶液pH随加入NaOH溶液体积的变化如图所示。下列说法不正确的是

A.Q→X过程中: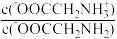 逐渐减小 逐渐减小 |
B.X点的溶液中:c(-OOCCH2NH2)>c(HOOCCH2NH ) ) |
C.P点的溶液中:c(HOOCCH2NH )+c(H+)=c(-OOCCH2NH2)+c(OH-) )+c(H+)=c(-OOCCH2NH2)+c(OH-) |
| D.当V(NaOH)=20mL时,混合溶液中的溶质主要为NaOOCCH2NH2和NaCl |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】已知甘氨酸在水中存在三种微粒,它们的转化关系如下:

pI 为该溶液中−COO−和H3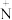 −数目相等时的pH,K1和 K2分别表示:−COOH 和H3
−数目相等时的pH,K1和 K2分别表示:−COOH 和H3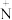 −的解离常数,K1=10−2.4,K2=10−9.4。其各微粒在水中的分布系数(各微粒数目占三种微粒总数的百分比)如图所示。下列判断错误的是:
−的解离常数,K1=10−2.4,K2=10−9.4。其各微粒在水中的分布系数(各微粒数目占三种微粒总数的百分比)如图所示。下列判断错误的是:


pI 为该溶液中−COO−和H3
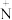 −数目相等时的pH,K1和 K2分别表示:−COOH 和H3
−数目相等时的pH,K1和 K2分别表示:−COOH 和H3 −的解离常数,K1=10−2.4,K2=10−9.4。其各微粒在水中的分布系数(各微粒数目占三种微粒总数的百分比)如图所示。下列判断错误的是:
−的解离常数,K1=10−2.4,K2=10−9.4。其各微粒在水中的分布系数(各微粒数目占三种微粒总数的百分比)如图所示。下列判断错误的是:
| A.a点对应的 pH=2.4 |
| B.pH=4 时,c(A±)>c(A-)>c(A+) |
| C.甘氨酸溶液的 pI=6 |
| D.甘氨酸溶于水后溶液显酸性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】298 K 时,0.1 mol/L H2R溶液中H2R、HR‾、R2‾ 三种微粒的分布系数δ随 pH 变化的关系如图所示。已知:298 K时,HF的Ka=1.0×10‾3.4。下列表述正确的是
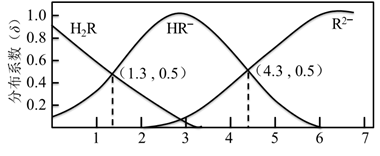

| A.H2R的Ka1 = 1.0×10‾1.3 |
| B.Na2R 溶液中离子存在关系:c(Na+) = c(HR‾ ) +2c(R2‾ ) |
| C.等物质的量的NaHR 和Na2R溶于水,所得溶液的pH 恰好为4.3 |
| D.在足量的NaF 溶液中加入少量 H2R 溶液:H2R + 2F‾ = 2HF + R2‾ |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,向含少量盐酸的0.1mol/L的CrCl3溶液中逐滴滴加NaOH溶液,所加NaOH溶液的体积与溶液pH变化如图所示。

已知:Cr(OH)3为灰绿色的沉淀,当Cr3+浓度为10-5mol/L时,可认为沉淀完全,碱过量时生成[Cr(OH)4]-离子。下列说法正确的是

已知:Cr(OH)3为灰绿色的沉淀,当Cr3+浓度为10-5mol/L时,可认为沉淀完全,碱过量时生成[Cr(OH)4]-离子。下列说法正确的是
| A.AB段发生反应的离子方程式为:Cr3++3OH-= Cr(OH)3↓ |
| B.A到D过程中,溶液中水的电离程度先减小后增大 |
| C.当溶液pH=5时,c(Cr3+)=10-3.8mol/L |
D.D点溶液中c(Na+)>c(Cl-)>c[Cr(OH) ]>c(OH-)>c(H+) ]>c(OH-)>c(H+) |
您最近一年使用:0次



