亚硝酸钠是一种工业盐,用途广泛;外观与食盐非常相似,但毒性较强。某化学兴趣小组对食盐与亚硝酸钠进行了如下探究:
㈠鉴别NaCl和NaNO2
(1)测定溶液pH
用pH试纸分别测定0.1mol•L-1两种盐溶液的pH,测得NaNO2溶液呈碱性.NaNO2溶液呈碱性的原因是__________ (用离子方程式解释),NaNO2溶液中c(HNO2)=__________ (用溶液中其它离子的浓度关系式表示)。
(2)沉淀法
取2mL0.1mol•L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液,两支试管均产生白色沉淀,分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。该温度下Ksp(AgNO2)=2×10-8 (mol•L-1)2; Ksp(AgCl)=1.8×10-10(mol•L-1)2,则反应AgNO2(s)+Cl-(aq)═AgCl(s)+NO2-(aq)的化学平衡常数K=__________ (计算结果写成分数)。
(二)实验室可用如下装置(略去部分夹持仪器)备亚硝酸钠。
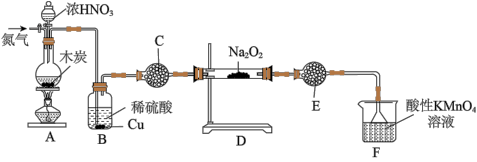
已知:①2NO+Na2O2=2NaNO2;②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(3)加热装置A前,先通一段时间N2,目的是__________ 。
(4)装置A中发生反应的化学方程式为__________ ,装置B的作用是__________ 。
(5)仪器C的名称为__________ ,其中盛放的药品为__________ (填名称)。
㈠鉴别NaCl和NaNO2
(1)测定溶液pH
用pH试纸分别测定0.1mol•L-1两种盐溶液的pH,测得NaNO2溶液呈碱性.NaNO2溶液呈碱性的原因是
(2)沉淀法
取2mL0.1mol•L-1两种盐溶液于试管中,分别滴加几滴稀硝酸银溶液,两支试管均产生白色沉淀,分别滴加几滴稀硝酸并振荡,盛NaNO2溶液的试管中沉淀溶解。该温度下Ksp(AgNO2)=2×10-8 (mol•L-1)2; Ksp(AgCl)=1.8×10-10(mol•L-1)2,则反应AgNO2(s)+Cl-(aq)═AgCl(s)+NO2-(aq)的化学平衡常数K=
(二)实验室可用如下装置(略去部分夹持仪器)备亚硝酸钠。

已知:①2NO+Na2O2=2NaNO2;②酸性条件下,NO和NO2都能与MnO4-反应生成NO3-和Mn2+;Na2O2能使酸性高锰酸钾溶液褪色.
(3)加热装置A前,先通一段时间N2,目的是
(4)装置A中发生反应的化学方程式为
(5)仪器C的名称为
更新时间:2016-12-09 14:32:45
|
相似题推荐
填空题
|
困难
(0.15)
解题方法
【推荐1】铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置为_________________ ,Fe3O4可写成FeO·Fe2O3的形式,如果将Pb3O4也写成相对应的形式应为:______________
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为___________________ 。PbO2可由PbO与次氯酸钠溶液反应制得,其反应的离子方程式为______________ 。
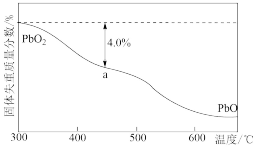
(3)PbO2在加热过程发生分解的失重曲线如右图所示,已知失重曲线上的a点为样品失重4.0%(即 ×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n
×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n_______________ ,____________ 。
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置为
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为

(3)PbO2在加热过程发生分解的失重曲线如右图所示,已知失重曲线上的a点为样品失重4.0%(即
 ×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n
×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐2】连二亚硫酸钠(Na2S2O4),又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验:
I.【查阅资料】
(1)连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇。
(2)2Na2S2O4+4HCl= 4NaCl+S↓+3SO2↑+2H2O;Na2S2O3+2HCl= 2NaCl+S↓+SO2↑+H2O。
II.【制备方法】
75℃时将甲酸钠和纯碱加入乙醇水溶液中,通入SO2进行反应,完成其反应方程式:

冷却至40~50℃,过滤,用___ 洗涤,干燥制得Na2S2O4。
III.【Na2S2O4的性质】
(1)Na2S2O4溶液在空气中易被氧化.课题小组测定0.050mol/L
Na2S2O4溶液在空气中pH变化如图所示:0~t1段主要先生成HSO3-,根据pH变化图,HSO3-的电离程度___ 水解程度(填“<”或“>”)。

课题小组推测Na2S2O4溶液在空气中易被氧化,0~t1段发生离子反应方程式为___ 。t3时溶液中主要阴离子符号是___ 。
(2)隔绝空气加热Na2S2O4固体完全分解,得到固体产物Na2SO3、Na2S2O3和气体为_______ (填化学式).
请你设计实验验证产物有Na2S2O3存在,完成下表中内容。
(供选择的试剂:稀盐酸、稀硝酸、BaCl2溶液、KMnO4溶液)
I.【查阅资料】
(1)连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇。
(2)2Na2S2O4+4HCl= 4NaCl+S↓+3SO2↑+2H2O;Na2S2O3+2HCl= 2NaCl+S↓+SO2↑+H2O。
II.【制备方法】
75℃时将甲酸钠和纯碱加入乙醇水溶液中,通入SO2进行反应,完成其反应方程式:

冷却至40~50℃,过滤,用
III.【Na2S2O4的性质】
(1)Na2S2O4溶液在空气中易被氧化.课题小组测定0.050mol/L
Na2S2O4溶液在空气中pH变化如图所示:0~t1段主要先生成HSO3-,根据pH变化图,HSO3-的电离程度

课题小组推测Na2S2O4溶液在空气中易被氧化,0~t1段发生离子反应方程式为
(2)隔绝空气加热Na2S2O4固体完全分解,得到固体产物Na2SO3、Na2S2O3和气体为
请你设计实验验证产物有Na2S2O3存在,完成下表中内容。
(供选择的试剂:稀盐酸、稀硝酸、BaCl2溶液、KMnO4溶液)
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐3】水合肼 常用于生产火箭燃料,其沸点是
常用于生产火箭燃料,其沸点是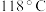 ,受热易分解。尿素法合成水合肼的基本流程如图所示。
,受热易分解。尿素法合成水合肼的基本流程如图所示。

回答下列问题:
(1) 是二元弱碱,在水中的电离方式与氨相似,写出
是二元弱碱,在水中的电离方式与氨相似,写出 第二步电离的方程式:
第二步电离的方程式:___________ 。
(2)已知次氯酸钠与盐酸混合能够生成 ,说明氧化性
,说明氧化性
___________  (填“>”或“<”)。实验发现,
(填“>”或“<”)。实验发现, 与烧碱溶液反应可以生成
与烧碱溶液反应可以生成 ,说明
,说明 与
与 的氧化性强弱关系与
的氧化性强弱关系与___________ 有关。
(3) 强碱性溶液与尿素
强碱性溶液与尿素 水溶液加热制备水合肼的离子方程式为
水溶液加热制备水合肼的离子方程式为___________ 。
(4)常通过减压蒸馏从反应后的混合溶液中获得水合肼,采用该操作的原因是___________ 。
(5)水合肼与硫酸反应生成的盐是农业上重要的杀虫剂、灭菌剂,写出水合肼与硫酸反应生成的碱式盐的化学式:___________ 。
(6)电化学方法制备 的装置如图所示。其中双极膜是阴、阳复合膜,层间的
的装置如图所示。其中双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。

①双极膜中产生的___________ (填“ ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。
②若电路中转移2mol电子,理论上负极区溶液增重___________ g。
 常用于生产火箭燃料,其沸点是
常用于生产火箭燃料,其沸点是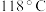 ,受热易分解。尿素法合成水合肼的基本流程如图所示。
,受热易分解。尿素法合成水合肼的基本流程如图所示。
回答下列问题:
(1)
 是二元弱碱,在水中的电离方式与氨相似,写出
是二元弱碱,在水中的电离方式与氨相似,写出 第二步电离的方程式:
第二步电离的方程式:(2)已知次氯酸钠与盐酸混合能够生成
 ,说明氧化性
,说明氧化性
 (填“>”或“<”)。实验发现,
(填“>”或“<”)。实验发现, 与烧碱溶液反应可以生成
与烧碱溶液反应可以生成 ,说明
,说明 与
与 的氧化性强弱关系与
的氧化性强弱关系与(3)
 强碱性溶液与尿素
强碱性溶液与尿素 水溶液加热制备水合肼的离子方程式为
水溶液加热制备水合肼的离子方程式为(4)常通过减压蒸馏从反应后的混合溶液中获得水合肼,采用该操作的原因是
(5)水合肼与硫酸反应生成的盐是农业上重要的杀虫剂、灭菌剂,写出水合肼与硫酸反应生成的碱式盐的化学式:
(6)电化学方法制备
 的装置如图所示。其中双极膜是阴、阳复合膜,层间的
的装置如图所示。其中双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
①双极膜中产生的
 ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。②若电路中转移2mol电子,理论上负极区溶液增重
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐1】现有0.175 mol·L-1醋酸钠溶液500 mL,(已知室温下,醋酸的电离平衡常数Ka=1.75×10-5)。
(1)写出醋酸钠水解反应的化学方程式 ______________________________ ;
(2)下列图象能说明醋酸钠的水解反应达到平衡的是____________ ;

A. 溶液中c(Na+)与反应时间t的关系
B.CH3COO-的水解速率与反应时间t的关系
C.溶液的pH与反应时间t的关系
D.KW与反应时间t的关系
(3)向醋酸钠溶液中加入少量下列物质,水解平衡向正向移动的有______;
(4)在醋酸钠溶液中加入冰醋酸,溶液中微粒浓度的关系式能成立的有__________;
(5)欲配制0.175 mol·L-1醋酸钠溶液500 mL,可采用以下两种方案:
方案一:用托盘天平称取___________ g无水醋酸钠,溶于适量水中,配成500 mL溶液。[已知:M(CH3COONa) = 82g/mol ]
方案二:用体积均为250 mL且浓度均为___________ mol·L-1的醋酸与氢氧化钠两溶液混合而成(设混合后的体积等于混合前两者体积之和)。
(6)在室温下,0.175 mol·L-1醋酸钠(CH3COONa)溶液的pH约为________ 。
(1)写出醋酸钠水解反应的
(2)下列图象能说明醋酸钠的水解反应达到平衡的是

A. 溶液中c(Na+)与反应时间t的关系
B.CH3COO-的水解速率与反应时间t的关系
C.溶液的pH与反应时间t的关系
D.KW与反应时间t的关系
(3)向醋酸钠溶液中加入少量下列物质,水解平衡向正向移动的有______;
| A.冰醋酸 | B.纯碱固体 | C.醋酸钠固体 | D.氯化铵固体 |
| A.c(CH3COO-) + c(CH3COOH)>c(Na+) |
| B.c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C.c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.c(CH3COO-)>c(H+)>c(OH-)>c(Na+) |
方案一:用托盘天平称取
方案二:用体积均为250 mL且浓度均为
(6)在室温下,0.175 mol·L-1醋酸钠(CH3COONa)溶液的pH约为
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐2】盐与碱的反应是水溶液中常见的反应,某学习小组展开相关探究。
Ⅰ.NH4Cl抗碱容量(σ)的测定
(1)某小组同学测定NH4Cl固体抗碱容量的实验步骤如下:
a.配置100mL0.2mol·L-1NaOH溶液;
b.称取xgNH4Cl固体,溶于20mL水中,用上述NaOH溶液滴定至pH=11.
已知:氯化铵的抗碱容量是指用NaOH溶液滴定NH4Cl溶液至pH=11时,单位质量的NH4Cl所消耗NaOH的物质的量,即σ=
①步骤a需要称量NaOH固体为______ g(保留一位小数)
②步骤b需要用到下图所示仪器中的______ (填名称)。______ mol·g-1
Ⅱ.NH4Cl-NH3混合溶液抗碱能力的探究
NH4Cl-NH3混合溶液具有抗碱能力。向该溶液中加入少量NaOH,溶液的pH变化不大。
已知:i.25℃时,NH3·H2O的Kb=1.75×10-5=10-4.8
ii.NH4Cl-NH3混合溶液的抗碱能力与 、[c(
、[c( )+c(NH3)]有关
)+c(NH3)]有关
(2)NH4Cl溶液显酸性,用离子方程式解释原因:______ 。
(3)小组同学设计实验探究[c )+c(NH3)]一定时,
)+c(NH3)]一定时, 对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
①实验结果显示,NaCl溶液不具备抗碱能力,即曲线______ (填曲线标号)表示溶液1.
②实验结果显示,当[c( )+c(NH3)]相同时,
)+c(NH3)]相同时, 越大,混合溶液的抗碱能力越强,则曲线b表示溶液
越大,混合溶液的抗碱能力越强,则曲线b表示溶液______ (填溶液组号)
③已知A点时,c(NH4+)=c(NH3·H2O),则此时溶液的pH=______ (精确至小数点后1位)。
Ⅰ.NH4Cl抗碱容量(σ)的测定
(1)某小组同学测定NH4Cl固体抗碱容量的实验步骤如下:
a.配置100mL0.2mol·L-1NaOH溶液;
b.称取xgNH4Cl固体,溶于20mL水中,用上述NaOH溶液滴定至pH=11.
已知:氯化铵的抗碱容量是指用NaOH溶液滴定NH4Cl溶液至pH=11时,单位质量的NH4Cl所消耗NaOH的物质的量,即σ=

①步骤a需要称量NaOH固体为
②步骤b需要用到下图所示仪器中的
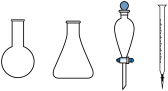
Ⅱ.NH4Cl-NH3混合溶液抗碱能力的探究
NH4Cl-NH3混合溶液具有抗碱能力。向该溶液中加入少量NaOH,溶液的pH变化不大。
已知:i.25℃时,NH3·H2O的Kb=1.75×10-5=10-4.8
ii.NH4Cl-NH3混合溶液的抗碱能力与
 、[c(
、[c( )+c(NH3)]有关
)+c(NH3)]有关(2)NH4Cl溶液显酸性,用离子方程式解释原因:
(3)小组同学设计实验探究[c
 )+c(NH3)]一定时,
)+c(NH3)]一定时, 对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示
对混合溶液抗碱能力的影响。分别向溶液1、溶液2、溶液3、溶液4中滴加0.1mol·L-1NaOH溶液,溶液的pH随加入NaOH的变化情况如下图所示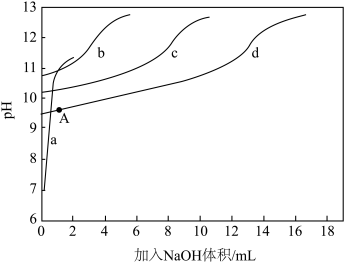
| 溶液组号 | 组成 | 体积/mL |
| 1 | 0.2mol·L-1NaCl溶液 | 15 |
| 2 | 0.1mol·L-1NH4Cl | 3 |
| 0.1mol·L-1氨水 | 12 | |
| 3 | 0.1mol·L-1NH4Cl | 7.5 |
| 0.1mol·L-1氨水 | 7.5 | |
| 4 | 0.1mol·L-1NH4Cl | 12 |
| 0.1mol·L-1氨水 | 3 |
②实验结果显示,当[c(
 )+c(NH3)]相同时,
)+c(NH3)]相同时, 越大,混合溶液的抗碱能力越强,则曲线b表示溶液
越大,混合溶液的抗碱能力越强,则曲线b表示溶液③已知A点时,c(NH4+)=c(NH3·H2O),则此时溶液的pH=
您最近一年使用:0次
填空题
|
困难
(0.15)
名校
解题方法
【推荐3】未来脑教学云平台*按要求回答下列问题∶
(1)常温下,向VL 0.1mol/L的醋酸溶液中加水稀释,下列说法中正确的是___________ (填字母)。
A.溶液中导电粒子的数目将减少
B.由水电离的c(H+)浓度将减小
C.溶液中 不变
不变
D. 溶液中 将减小
将减小
E.醋酸的电离程度将增大,c(H+)也增大
(2)①常温下,将0.1mol/L的硫酸V1mL与0.1mol/LNaOH溶液V2mL混合后,溶液的pH=1则V1∶V2=___________ (忽略溶液体积的变化)。
②常温下,若溶液由pH=3的盐酸V1mL与pH=11的某碱BOH溶液V2mL混合而得,则下列假设和结论都正确的是____________ (填字母)。
A.若混合后溶液呈中性,则c(H+)+c (OH-)=2×10-7h$mol/L
B.若V1=V2,则混合后溶液的pH一定等于7
C.若V1=V2,则混合后一定有∶c(Cl-)>c(B+)>c(H+)>c(OH-)
D.混合后的溶液中一定有c(B+)+c(H+)=c(Cl-)+c (OH-)
(3)常温下,浓度均为0.1mol/L的五种溶液的pH如下表所示∶
①写出向NaClO溶液中通入少量CO2的离子方程式___________________ 。
②将浓度均为0.01mol/L下列溶液分别加水稀释10倍,pH变化最小的是________ (填字母)。
A.HCN B.HClO C.H2CO3 D.CH3COOH
③常温下,等浓度的醋酸与醋酸钠组成的混合溶液pH=6,则c(CH3COO-)-c(CH3COOH)= ________________ (填准确数值)。
(4)已知常温下Ksp(AgCl)=1.0×10-10,Ksp (CH3COOAg)=9.0×10-4。常温下,CH3COOAg若要在NaCl溶液中开始转化为AgCl沉淀,则NaCl的浓度必须不低于_______________ 。
(1)常温下,向VL 0.1mol/L的醋酸溶液中加水稀释,下列说法中正确的是
A.溶液中导电粒子的数目将减少
B.由水电离的c(H+)浓度将减小
C.溶液中
 不变
不变D. 溶液中
 将减小
将减小E.醋酸的电离程度将增大,c(H+)也增大
(2)①常温下,将0.1mol/L的硫酸V1mL与0.1mol/LNaOH溶液V2mL混合后,溶液的pH=1则V1∶V2=
②常温下,若溶液由pH=3的盐酸V1mL与pH=11的某碱BOH溶液V2mL混合而得,则下列假设和结论都正确的是_
A.若混合后溶液呈中性,则c(H+)+c (OH-)=2×10-7h$mol/L
B.若V1=V2,则混合后溶液的pH一定等于7
C.若V1=V2,则混合后一定有∶c(Cl-)>c(B+)>c(H+)>c(OH-)
D.混合后的溶液中一定有c(B+)+c(H+)=c(Cl-)+c (OH-)
(3)常温下,浓度均为0.1mol/L的五种溶液的pH如下表所示∶
| 溶液 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
②将浓度均为0.01mol/L下列溶液分别加水稀释10倍,pH变化最小的是
A.HCN B.HClO C.H2CO3 D.CH3COOH
③常温下,等浓度的醋酸与醋酸钠组成的混合溶液pH=6,则c(CH3COO-)-c(CH3COOH)= _
(4)已知常温下Ksp(AgCl)=1.0×10-10,Ksp (CH3COOAg)=9.0×10-4。常温下,CH3COOAg若要在NaCl溶液中开始转化为AgCl沉淀,则NaCl的浓度必须不低于
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐1】天然水体中的 与空气中的
与空气中的 保持平衡。某温度下,溶洞水体中
保持平衡。某温度下,溶洞水体中 (X为
(X为 、
、 、
、 或
或 )与pH关系如图所示:
)与pH关系如图所示:
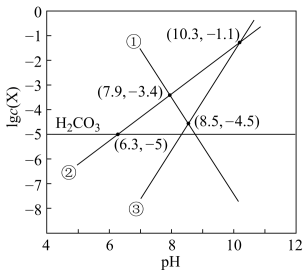
(1)①、②、③三条斜线中,能表示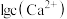 随pH变化关系的斜线是
随pH变化关系的斜线是___________ 。
(2)该温度下, 的电离平衡常数
的电离平衡常数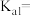
___________  ;
;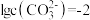 时溶液的pH=
时溶液的pH=___________ 。
(3)已知
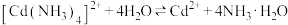
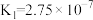
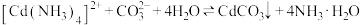
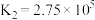 ;
;
室温下,取 溶液V mL,用0.1
溶液V mL,用0.1 氨水标准溶液进行滴定,先生成白色
氨水标准溶液进行滴定,先生成白色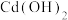 沉淀,继续滴加氨水,沉淀恰好溶解生成
沉淀,继续滴加氨水,沉淀恰好溶解生成 时,消耗标准液20mL。若向该
时,消耗标准液20mL。若向该 溶液加入
溶液加入 固体,当
固体,当 开始沉淀时,溶液中
开始沉淀时,溶液中 浓度为
浓度为___________  。[用含V的代数式表示,不考虑杂质反应]
。[用含V的代数式表示,不考虑杂质反应]
(4)测定纯碱产品中、 含量的方法:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,用c
含量的方法:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,用c 盐酸标准液采用“双指示剂法”滴定,先用酚酞作指示剂,到达终点a后,又滴加几滴甲基橙作指示剂,继续滴加到终点b。pH传感器测得混合溶液的pH变化曲线如图。
盐酸标准液采用“双指示剂法”滴定,先用酚酞作指示剂,到达终点a后,又滴加几滴甲基橙作指示剂,继续滴加到终点b。pH传感器测得混合溶液的pH变化曲线如图。
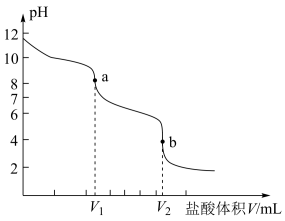
①酚酞作指示剂,判断到达滴定终点的方法是:___________ 。
②纯碱样品中 质量分数的计算式为:
质量分数的计算式为: ___________ 。
 与空气中的
与空气中的 保持平衡。某温度下,溶洞水体中
保持平衡。某温度下,溶洞水体中 (X为
(X为 、
、 、
、 或
或 )与pH关系如图所示:
)与pH关系如图所示:
(1)①、②、③三条斜线中,能表示
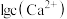 随pH变化关系的斜线是
随pH变化关系的斜线是(2)该温度下,
 的电离平衡常数
的电离平衡常数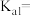
 ;
;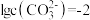 时溶液的pH=
时溶液的pH=(3)已知
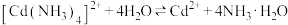
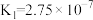
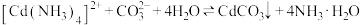
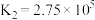 ;
;室温下,取
 溶液V mL,用0.1
溶液V mL,用0.1 氨水标准溶液进行滴定,先生成白色
氨水标准溶液进行滴定,先生成白色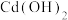 沉淀,继续滴加氨水,沉淀恰好溶解生成
沉淀,继续滴加氨水,沉淀恰好溶解生成 时,消耗标准液20mL。若向该
时,消耗标准液20mL。若向该 溶液加入
溶液加入 固体,当
固体,当 开始沉淀时,溶液中
开始沉淀时,溶液中 浓度为
浓度为 。[用含V的代数式表示,不考虑杂质反应]
。[用含V的代数式表示,不考虑杂质反应](4)测定纯碱产品中、
 含量的方法:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,用c
含量的方法:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,用c 盐酸标准液采用“双指示剂法”滴定,先用酚酞作指示剂,到达终点a后,又滴加几滴甲基橙作指示剂,继续滴加到终点b。pH传感器测得混合溶液的pH变化曲线如图。
盐酸标准液采用“双指示剂法”滴定,先用酚酞作指示剂,到达终点a后,又滴加几滴甲基橙作指示剂,继续滴加到终点b。pH传感器测得混合溶液的pH变化曲线如图。
①酚酞作指示剂,判断到达滴定终点的方法是:
②纯碱样品中
 质量分数的计算式为:
质量分数的计算式为:
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐2】CrO3主要用于电镀工业,做自行车、仪表等日用五金电镀铬的原料。CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率随温度的变化如图所示。
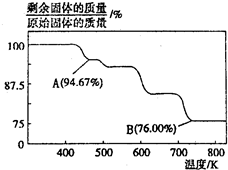
请回答下列问题:
(1)B点时剩余固体的化学式是____________ 。
(2)加热至A点时反应的化学方程式为______________________________ 。
(3)CrO3具有两性,写出CrO3溶解予KOH溶液的反应化学方程式____________________ 。
(4)三氧化铬还用于交警的酒精测试仪,以检查司机是否酒后驾车。若反应后红色的CrO3变为绿色的Cr2(SO4)3,酒精被完全氧化为CO2,则其离子方程式为_______________ 。
(5)由于CrO3和K2Cr2O7均易溶于水,所以电镀废水的排放是造成铬污染的主要原因。某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如图:
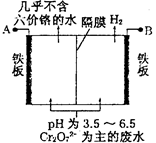
①A为电源___________ 极,阳极区溶液中发生的氧化还原反应为________________________ 。
②已知电解后阳极区溶液中c(Fe3+)为2.0×10-13 mol·L-1,则c(Cr3+)为__________ mol·L-1。{已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31}

请回答下列问题:
(1)B点时剩余固体的化学式是
(2)加热至A点时反应的化学方程式为
(3)CrO3具有两性,写出CrO3溶解予KOH溶液的反应化学方程式
(4)三氧化铬还用于交警的酒精测试仪,以检查司机是否酒后驾车。若反应后红色的CrO3变为绿色的Cr2(SO4)3,酒精被完全氧化为CO2,则其离子方程式为
(5)由于CrO3和K2Cr2O7均易溶于水,所以电镀废水的排放是造成铬污染的主要原因。某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,原理示意图如图:

①A为电源
②已知电解后阳极区溶液中c(Fe3+)为2.0×10-13 mol·L-1,则c(Cr3+)为
您最近一年使用:0次
【推荐3】高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性。
(1)已知:4 +10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有
+10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有___ 。
同浓度的高铁酸钾在pH为4.74、7.00、11.50的水溶液中最稳定的是pH=_______ 的溶液。
(2)高铁酸钾有以下几种常见制备方法:

①干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为___________ 。
②湿法制备中,若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:___________________________________ 。
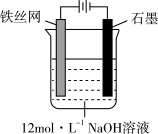
③制备中间产物Na2FeO4,可采用的装置如图所示,则阳极的电极反应式为_______________ 。
(3)比亚迪双模电动汽车使用高铁电池供电,其总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化
3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化_______________ ,正极反应为:____________________ 。
(4)25℃时,CaFeO4的Ksp=4.54×l0-9,若要使1000 L含有2.0×l0-4 mol·L-l K2FeO4的废水中的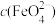 有沉淀产生,理论上至少加入Ca(OH)2的物质的量为
有沉淀产生,理论上至少加入Ca(OH)2的物质的量为________ mol。
(1)已知:4
 +10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有
+10H2O ⇌4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有同浓度的高铁酸钾在pH为4.74、7.00、11.50的水溶液中最稳定的是pH=
(2)高铁酸钾有以下几种常见制备方法:

①干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为
②湿法制备中,若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:
③制备中间产物Na2FeO4,可采用的装置如图所示,则阳极的电极反应式为

(3)比亚迪双模电动汽车使用高铁电池供电,其总反应为:3Zn+2K2FeO4+8H2O
 3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化
3Zn(OH)(OH)2+2Fe(OH)3+4KOH 放电时负极附近pH变化(4)25℃时,CaFeO4的Ksp=4.54×l0-9,若要使1000 L含有2.0×l0-4 mol·L-l K2FeO4的废水中的
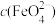 有沉淀产生,理论上至少加入Ca(OH)2的物质的量为
有沉淀产生,理论上至少加入Ca(OH)2的物质的量为
您最近一年使用:0次
填空题
|
困难
(0.15)
名校
【推荐1】一种利用电解锰阳极泥(主要成分MnO2、MnO)制备MnO2的工艺流程如下:
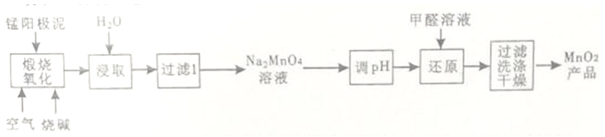
(1)“煅烧氧化”时,1mol MnO煅烧完全转化为Na2MnO4失去电子的物质的量为___________ ;MnO2煅烧反应的化学方程式为__________________ 。
(2)“浸取”时,为提高Na2MnO4的浸取率,可采取的措施有____________ 、____________ (列举2点)
(3)“调pH”是将溶液pH 调至约为10,防止pH较低时Na2MnO4自身发生氧化还原反应,生成MnO2和___________ ;写出用pH试纸测定溶液pH的操作_______________ 。
(4)“还原”时有无机含氧酸盐生成,发生反应的化学方程式为_____________ 。
(5)测定产品中MnO2质量分数的步骤如下:
步骤1. 准确称取mg产品,加入c1mol·L-1Na2C2O4溶液V1mL (过量)及适量的稀硫酸,水浴加热煮沸一段时间。(已知:Na2C2O4+2H2SO4+MnO2=MnSO4+2CO2↑+2H2O+Na2SO4)
步骤2. 然后用c2mol·L-1KMnO4标准溶液滴定剩余的Na2C2O4滴定至终点时消耗KMnO4标准溶液V2mL。(已知:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+10CO2↑+K2SO4+8H2O)
步骤2达滴定终点时判断依据是_____________ ;产品中MnO2的质量分数为ω(MnO2)=____________ (列出计算的表达式即可)。

(1)“煅烧氧化”时,1mol MnO煅烧完全转化为Na2MnO4失去电子的物质的量为
(2)“浸取”时,为提高Na2MnO4的浸取率,可采取的措施有
(3)“调pH”是将溶液pH 调至约为10,防止pH较低时Na2MnO4自身发生氧化还原反应,生成MnO2和
(4)“还原”时有无机含氧酸盐生成,发生反应的化学方程式为
(5)测定产品中MnO2质量分数的步骤如下:
步骤1. 准确称取mg产品,加入c1mol·L-1Na2C2O4溶液V1mL (过量)及适量的稀硫酸,水浴加热煮沸一段时间。(已知:Na2C2O4+2H2SO4+MnO2=MnSO4+2CO2↑+2H2O+Na2SO4)
步骤2. 然后用c2mol·L-1KMnO4标准溶液滴定剩余的Na2C2O4滴定至终点时消耗KMnO4标准溶液V2mL。(已知:5H2C2O4+2KMnO4+3H2SO4=2MnSO4+10CO2↑+K2SO4+8H2O)
步骤2达滴定终点时判断依据是
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐2】四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:
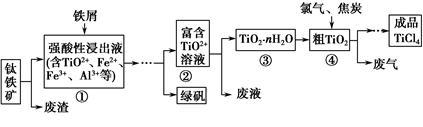
回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe=3Fe2+
2TiO2+(无色)+Fe+4H+=2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O=TiO2+(无色)+Fe2++2H+
加入铁屑的作用是______ 。
(2)在②→③工艺过程中需要控制条件以形成TiO2·nH2O溶胶,该溶胶的分散质颗粒直径大小在______ 范围。
(3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉。已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+Fe3++3H2O的平衡常数K=______ 。
(4)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:______ 。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是______ (只要求写出一项)。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4,可采用______ 方法。

回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe=3Fe2+
2TiO2+(无色)+Fe+4H+=2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O=TiO2+(无色)+Fe2++2H+
加入铁屑的作用是
(2)在②→③工艺过程中需要控制条件以形成TiO2·nH2O溶胶,该溶胶的分散质颗粒直径大小在
(3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉。已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+Fe3++3H2O的平衡常数K=
(4)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4,可采用
| TiCl4 | SiCl4 | |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
您最近一年使用:0次
填空题
|
困难
(0.15)
【推荐3】高纯度的绿矾(FeSO4·7H2O)是治疗缺铁性贫血的特效药。下面是以商品级纯度铁屑(含少量锡等杂质)生产绿矾的一种方法:
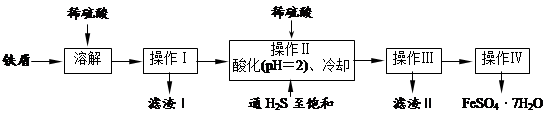
已知:在H2S饱和溶液中,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5。
(1)检验所得绿矾晶体中是否含有Fe3+的实验操作是___________________________ 。
(2)操作Ⅱ在溶液中用硫酸酸化至pH=2的目的是_______________________ ;
通入硫化氢至饱和的目的是:①除去操作I所得溶液中含有的Sn2+等杂质离子;
②除去Fe3+,反应的离子方程式为___________________________ 。
(3)操作IV的顺序依次为:___________ 、降温结晶。
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:
①除去晶体表面附着的硫酸等杂质;②____________________________ 。
(5)测定绿矾产品中Fe2+含量的方法是:
a.称取2.8500g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol·L—1 KMnO4溶液滴定至终点,反应为:
5Fe2++ +8H+=5Fe3++Mn2++4H2O
+8H+=5Fe3++Mn2++4H2O
消耗KMnO4溶液体积的平均值为20.00mL。
计算上述样品中FeSO4·7H2O的质量分数为______________________ 。
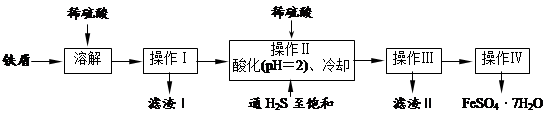
已知:在H2S饱和溶液中,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5。
(1)检验所得绿矾晶体中是否含有Fe3+的实验操作是
(2)操作Ⅱ在溶液中用硫酸酸化至pH=2的目的是
通入硫化氢至饱和的目的是:①除去操作I所得溶液中含有的Sn2+等杂质离子;
②除去Fe3+,反应的离子方程式为
(3)操作IV的顺序依次为:
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:
①除去晶体表面附着的硫酸等杂质;②
(5)测定绿矾产品中Fe2+含量的方法是:
a.称取2.8500g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol·L—1 KMnO4溶液滴定至终点,反应为:
5Fe2++
 +8H+=5Fe3++Mn2++4H2O
+8H+=5Fe3++Mn2++4H2O消耗KMnO4溶液体积的平均值为20.00mL。
计算上述样品中FeSO4·7H2O的质量分数为
您最近一年使用:0次



