T℃时,有甲、乙两个密闭容器,甲容器的体积为1L,乙容器的体积为2L,分别向甲、乙两容器中加入6mol A和3mol B,发生反应如下:3A(g)+b B(g) 3C(g)+2D(g), 4min后甲容器内的反应达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L;t min后乙容器内的反应达到平衡,B的浓度为0.8mol/L。根据题给的信息回答下列问题:
3C(g)+2D(g), 4min后甲容器内的反应达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L;t min后乙容器内的反应达到平衡,B的浓度为0.8mol/L。根据题给的信息回答下列问题:
(1)甲容器中反应的平均速率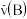 =
=____________________ 。
(2)在温度T℃时,该反应的化学平衡常数为__________________ ,由下表数据可知该反应为______________ (填“吸热”“放热”)反应。
化学平衡常数K和温度t的关系如下表:
(3)T℃时,在另一个体积与乙相同的丙容器中,为了达到平衡时B的浓度仍然为0.8mol/L,起始时,向丙容器中加入C、D的物质的量分别为3mol、2mol,则还需加入A、B的物质的量分别是___________ 、___________ 。
 3C(g)+2D(g), 4min后甲容器内的反应达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L;t min后乙容器内的反应达到平衡,B的浓度为0.8mol/L。根据题给的信息回答下列问题:
3C(g)+2D(g), 4min后甲容器内的反应达到平衡,A的浓度为2.4mol/L,B的浓度为1.8mol/L;t min后乙容器内的反应达到平衡,B的浓度为0.8mol/L。根据题给的信息回答下列问题:(1)甲容器中反应的平均速率
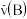 =
=(2)在温度T℃时,该反应的化学平衡常数为
化学平衡常数K和温度t的关系如下表:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(3)T℃时,在另一个体积与乙相同的丙容器中,为了达到平衡时B的浓度仍然为0.8mol/L,起始时,向丙容器中加入C、D的物质的量分别为3mol、2mol,则还需加入A、B的物质的量分别是
11-12高二上·湖南湘西·期末 查看更多[3]
山东省新泰市第一中学(弘文部)2023-2024学年高二上学期第二次月考化学试题(已下线)2011年湖南省湘西州部分高中高二1月期末联考化学试卷2015-2016学年湖北省宜昌金东方高级中学高二上学期期末化学试卷
更新时间:2019-01-30 18:14:09
|
相似题推荐
【推荐1】CH4、CH3OH、CO等都是重要的能源,也是重要的化工原料。
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO和液态水时放出38kJ热量,则该条件下反应的热化学反应方程式___________ 。
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
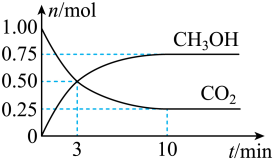
①从反应开始到平衡,CO2的平均反应速率v(CO2)=___________ 。
②达到平衡时,H2的转化率为___________ 。
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g) CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是___________ 。
A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
(1)已知25℃、101kPa时,1g甲烷完全燃烧生成CO和液态水时放出38kJ热量,则该条件下反应的热化学反应方程式
(2)为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量,有效地开发利用CO2,工业上可以用CO2来生产甲醇燃料。在体积为2L的密闭容器中,充入lmolCO2和3molH2,一定条件下发生反应:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CH3OH和CO2的物质的量随时间变化如图所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=
②达到平衡时,H2的转化率为
(3)工业上也可以用CO和H2为原料制备CH3OH,反应方程式为:CO(g)+2H2(g)
 CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
CH3OH(g),在一体积固定的密闭容器中投入一定量的CO和H2气体进行上述反应。下列叙述中能说明上述反应达到平衡状态的是A.反应中CO与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1molCO,同时生成1molCH3OH
D.CH3OH的质量分数在混合气体中保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在一定温度下,4L密闭容器内存在反应2N M,其中气体M、气体N的物质的量随时间变化的曲线如图所示:
M,其中气体M、气体N的物质的量随时间变化的曲线如图所示:
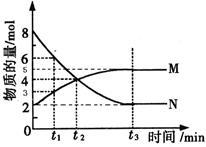
(1)比较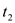 时刻,正逆反应速率大小V正
时刻,正逆反应速率大小V正_____ V逆。
(2)若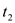 =2min,计算反应开始至
=2min,计算反应开始至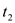 时刻,M的平均化学反应速率为:
时刻,M的平均化学反应速率为:_____________________________ 。
(3)t1与t2相比,反应速率__________ 较慢,其原因是__________________ ;已知该反应是放热反应,则N的能量___________ M的能量(填“大于”、“小于”、“等于”)镁条和盐酸的总能量。
 M,其中气体M、气体N的物质的量随时间变化的曲线如图所示:
M,其中气体M、气体N的物质的量随时间变化的曲线如图所示:
(1)比较
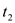 时刻,正逆反应速率大小V正
时刻,正逆反应速率大小V正(2)若
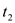 =2min,计算反应开始至
=2min,计算反应开始至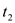 时刻,M的平均化学反应速率为:
时刻,M的平均化学反应速率为:(3)t1与t2相比,反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在体积为2L密闭容器中加入反应物A,B,发生如下反应:A(g)+2B(g)⇌3C(g),该反应为放热反应.经2min后,A的浓度从开始时的1.0mol•L-1降到0.8mol•L-1.已知反应开始时B的浓度是1.2mol•L-1,则2min末B的浓度为 ______ ,C的物质的量为______ .2min内,用A物质的浓度变化来表示该反应的反应速率,即v(A)=______ .当反应达到平衡后,降低温度,平衡将 ______ ,若通入0.5L氩气,平衡将 ______ 。(填“向右移动”、“向左移动”“不移动”)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】合成氨工业对国民经济和社会发展具有重要的意义。其原理为: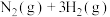


据此回答以下问题:
(1)当有0.5molN2反应完,放出的热量是___________ kJ
(2)此反应能自发进行的条件是___________
(3)某温度下,若把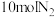 与
与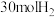 置于体积为
置于体积为 的密闭容器内,反应2min达到平衡状态时,测得混合气体中氨的体积分数为
的密闭容器内,反应2min达到平衡状态时,测得混合气体中氨的体积分数为 ,则用N2表示该反应的平均反应速率为
,则用N2表示该反应的平均反应速率为___________ ,能说明该反应达到化学平衡状态的是___________ (填字母)。
 容器内的密度保持不变
容器内的密度保持不变  容器内压强保持不变
容器内压强保持不变
 υ正
υ正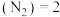 υ逆(NH3) d.混合气体中
υ逆(NH3) d.混合气体中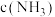 不变
不变
(4)对于合成氨反应而言,下列有关图象一定正确的是(选填序号)___________ 。
a.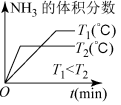 b.
b. c.
c.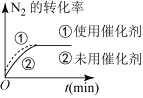
(5)相同温度下,有恒容密闭容器 和恒压密闭容器
和恒压密闭容器 ,两容器中均充入
,两容器中均充入 和
和 ,此时两容器的体积相等。在一定条件下反应达到平衡状态,
,此时两容器的体积相等。在一定条件下反应达到平衡状态, 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量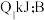 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量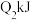 。则:a
。则:a_______ b填“ ”、“
”、“ ”或“
”或“ ”,下同Q1
”,下同Q1______ Q2
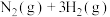


据此回答以下问题:
(1)当有0.5molN2反应完,放出的热量是
(2)此反应能自发进行的条件是
(3)某温度下,若把
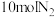 与
与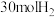 置于体积为
置于体积为 的密闭容器内,反应2min达到平衡状态时,测得混合气体中氨的体积分数为
的密闭容器内,反应2min达到平衡状态时,测得混合气体中氨的体积分数为 ,则用N2表示该反应的平均反应速率为
,则用N2表示该反应的平均反应速率为 容器内的密度保持不变
容器内的密度保持不变  容器内压强保持不变
容器内压强保持不变 υ正
υ正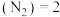 υ逆(NH3) d.混合气体中
υ逆(NH3) d.混合气体中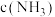 不变
不变(4)对于合成氨反应而言,下列有关图象一定正确的是(选填序号)
a.
 b.
b. c.
c.
(5)相同温度下,有恒容密闭容器
 和恒压密闭容器
和恒压密闭容器 ,两容器中均充入
,两容器中均充入 和
和 ,此时两容器的体积相等。在一定条件下反应达到平衡状态,
,此时两容器的体积相等。在一定条件下反应达到平衡状态, 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量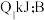 中
中 的体积分数为
的体积分数为 ,放出热量
,放出热量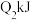 。则:a
。则:a ”、“
”、“ ”或“
”或“ ”,下同Q1
”,下同Q1
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知体积为2L的恒容密闭容器中发生反应:2SO2(g) + O2(g)  2SO3(g),请根据化学反应的有关原理回答下列问题:
2SO3(g),请根据化学反应的有关原理回答下列问题:
(1)一定条件下,充入2molSO2(g)和2molO2(g),20 s后,测得SO2的体积百分含量为12.5%,则用SO2表示该反应在这20s内的反应速率为____ 。
(2)下面的叙述可作为判断(1)中可逆反应达到平衡状态依据的是(填序号)____ 。
①v正(SO2)=2v逆(O2)②混合气体的密度不变③混合气体的平均相对分子质量不变④各气体的浓度都不再发生变化
(3)下图表示该反应的速率(v)随时间(t)的变化的关系。则下列不同时间段中,SO3的百分含量最高的是( )
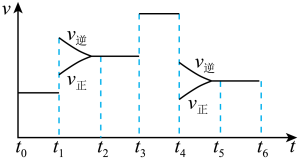
A、t2→t3 ) B、t0→t1 C、t5→t6 D、t3→t4
据图分析:你认为t3时改变的外界条件可能是_____ ; t6时保持体积不变向体系中充人少量SO3,再次平衡后SO2的体积百分含量比t6时____ (填“大”“小”或“等于”)。
(4)下图中P是可自由平行滑动的活塞。在相同温度时,向A容器中充入4 molSO3(g),关闭K,向B容器中充入2 molSO3(g),两容器分别发生反应。已知起始时容器A和B的体积均为aL。试回答:
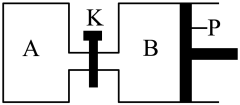
①反应达到平衡时容器B的体积为1.2aL,容器B中SO3转化率为____ 。
②若打开K,一段时间后重新达到平衡,容器B的体积为_____ L(连通管中气体体积忽略不计,且不考虑温度的影响)。
 2SO3(g),请根据化学反应的有关原理回答下列问题:
2SO3(g),请根据化学反应的有关原理回答下列问题:(1)一定条件下,充入2molSO2(g)和2molO2(g),20 s后,测得SO2的体积百分含量为12.5%,则用SO2表示该反应在这20s内的反应速率为
(2)下面的叙述可作为判断(1)中可逆反应达到平衡状态依据的是(填序号)
①v正(SO2)=2v逆(O2)②混合气体的密度不变③混合气体的平均相对分子质量不变④各气体的浓度都不再发生变化
(3)下图表示该反应的速率(v)随时间(t)的变化的关系。则下列不同时间段中,SO3的百分含量最高的是

A、t2→t3 ) B、t0→t1 C、t5→t6 D、t3→t4
据图分析:你认为t3时改变的外界条件可能是
(4)下图中P是可自由平行滑动的活塞。在相同温度时,向A容器中充入4 molSO3(g),关闭K,向B容器中充入2 molSO3(g),两容器分别发生反应。已知起始时容器A和B的体积均为aL。试回答:

①反应达到平衡时容器B的体积为1.2aL,容器B中SO3转化率为
②若打开K,一段时间后重新达到平衡,容器B的体积为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】温度一定时,在密闭容器中发生可逆反应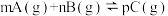 ,达到平衡后,若将混合气体的体积压缩到原来的
,达到平衡后,若将混合气体的体积压缩到原来的 ,当再次达到平衡时,C的浓度是原平衡时的1.9倍,试判断:
,当再次达到平衡时,C的浓度是原平衡时的1.9倍,试判断:
(1)压缩体积时平衡向_______________ (填“正反应”或“逆反应”)方向移动;
(2)反应再次达到平衡后,C气体的体积分数____________ (填“增大”“减小”或“不变”);
(3)反应再次达到平衡后,A气体的转化率____________ (填“增大”“减小”或“不变”);
(4)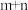
____________ p(填“>”“<”或”=”)。
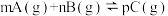 ,达到平衡后,若将混合气体的体积压缩到原来的
,达到平衡后,若将混合气体的体积压缩到原来的 ,当再次达到平衡时,C的浓度是原平衡时的1.9倍,试判断:
,当再次达到平衡时,C的浓度是原平衡时的1.9倍,试判断:(1)压缩体积时平衡向
(2)反应再次达到平衡后,C气体的体积分数
(3)反应再次达到平衡后,A气体的转化率
(4)
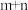
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】温度为 ,在三个容积均为
,在三个容积均为 的恒容密闭容器中仅发生反应
的恒容密闭容器中仅发生反应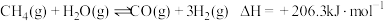 ,该反应中,正反应速率为
,该反应中,正反应速率为 ,逆反应速率为
,逆反应速率为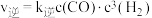 ,
, 、
、 为速率常数,受温度影响。已知
为速率常数,受温度影响。已知 时,
时, ,则该温度下,平衡常数
,则该温度下,平衡常数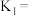
_______ ;当温度改变为 时,若
时,若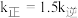 ,则
,则
_______ (填“>”“=”或“<”) 。
。
 ,在三个容积均为
,在三个容积均为 的恒容密闭容器中仅发生反应
的恒容密闭容器中仅发生反应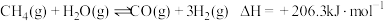 ,该反应中,正反应速率为
,该反应中,正反应速率为 ,逆反应速率为
,逆反应速率为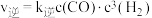 ,
, 、
、 为速率常数,受温度影响。已知
为速率常数,受温度影响。已知 时,
时, ,则该温度下,平衡常数
,则该温度下,平衡常数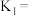
 时,若
时,若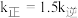 ,则
,则
 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】分在2L密闭容器,800℃时发生如下反应:
2CuO(s)+CO(g) Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
(1)写出该反应的平衡常数表达式______________ 。
已知:K(400℃)>K(350℃),则该反应是___________ 热反应。
(2)右图中表示Cu2O的物质的量随时间变化的曲线是____________ (选填“A”或“B”),800℃时,0~3min内该反应的平均速率v (CO2)=__________ 。
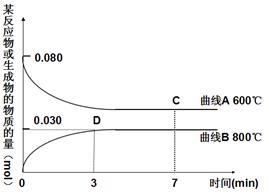
(3) 能说明该反应已达到平衡状态的是__________ 。
a.v(CO)=v(CO2) b.容器内压强保持不变
c.v逆(CO)=v正(CO2) d.容器内气体的密度保持不变
(4)能使该反应的正反应速率增大,且平衡向正反应方向移动的是____________ 。
A.增加CuO的量
B.适当升高温度
C.及时移去CO2
D.增大CO的浓度
E.选择高效催化剂
F.增大压强
2CuO(s)+CO(g)
 Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:
Cu2O(s)+CO2(g),n(CuO)随时间的变化如表:| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CuO)(mol) | 0.080 | 0.060 | 0.040 | 0.020 | 0.020 | 0.020 |
(1)写出该反应的平衡常数表达式
已知:K(400℃)>K(350℃),则该反应是
(2)右图中表示Cu2O的物质的量随时间变化的曲线是

(3) 能说明该反应已达到平衡状态的是
a.v(CO)=v(CO2) b.容器内压强保持不变
c.v逆(CO)=v正(CO2) d.容器内气体的密度保持不变
(4)能使该反应的正反应速率增大,且平衡向正反应方向移动的是
A.增加CuO的量
B.适当升高温度
C.及时移去CO2
D.增大CO的浓度
E.选择高效催化剂
F.增大压强
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】已知:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH=Q。其平衡常数随温度变化如下表所示:
回答下列问题:
(1)上述反应的化学平衡常数表达式为_______ ,该反应的Q_______ (填“>”或“<”)0。
(2)850 ℃时,在体积为10 L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的浓度变化如下图所示,则0~4 min时,平均反应速率v(CO)=_______ 。
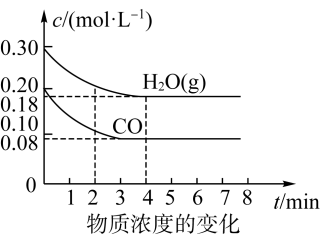
(3)若在500 ℃时进行,且CO、H2O(g)的起始浓度均为0.020 mol·L-1,该条件下,CO的最大转化率为_______ 。(提示:利用平衡常数,三段式计算)
(4)有人提出可以设计反应2CO(g)=2C(s)+O2(g)(ΔH>0)来消除CO的污染。请判断上述反应能否自发进行:_______ (填“能”或“不能”)。理由是_______ 。
| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
(1)上述反应的化学平衡常数表达式为
(2)850 ℃时,在体积为10 L的反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)的浓度变化如下图所示,则0~4 min时,平均反应速率v(CO)=

(3)若在500 ℃时进行,且CO、H2O(g)的起始浓度均为0.020 mol·L-1,该条件下,CO的最大转化率为
(4)有人提出可以设计反应2CO(g)=2C(s)+O2(g)(ΔH>0)来消除CO的污染。请判断上述反应能否自发进行:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】研究CO2的再利用有利于低碳减排的同时获得新的能源物质。如一定条件下,CO2加氢可制得甲醇: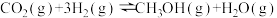
 。回答下列问题:
。回答下列问题:
(1)我国科研人员研究的该反应历程如图,吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态,括号里的数字表示微粒的相对总能量(单位为eV)。
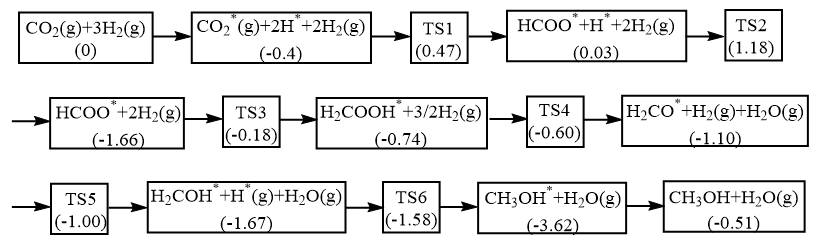
该反应
___________ 0(填“>”或“<”);该历程中总反应的决速步方程式为___________ 。
(2)T℃时,在一容积为2L的恒容密闭容器中充入2mol CO2和6molH2,测得不同时刻容器中的压强关系如下表所示:
①用H2表示该反应0~5min内的平均反应速率为___________ 。
②CO2的平衡转化率为___________ ;T℃时,该反应的平衡常数为___________ (保留一位小数)。
③其它条件不变,下列措施能同时增大反应速率和H2平衡转化率的是___________ (填标号)。
a.升高温度 b.按原比例再充入一定量CO2和H2
c.将 和
和 液化移出 d.缩小容器体积
液化移出 d.缩小容器体积
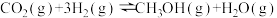
 。回答下列问题:
。回答下列问题:(1)我国科研人员研究的该反应历程如图,吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态,括号里的数字表示微粒的相对总能量(单位为eV)。

该反应

(2)T℃时,在一容积为2L的恒容密闭容器中充入2mol CO2和6molH2,测得不同时刻容器中的压强关系如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
 | 0.80 | 0.72 | 0.66 | 0.62 | 0.60 | 0.60 |
①用H2表示该反应0~5min内的平均反应速率为
②CO2的平衡转化率为
③其它条件不变,下列措施能同时增大反应速率和H2平衡转化率的是
a.升高温度 b.按原比例再充入一定量CO2和H2
c.将
 和
和 液化移出 d.缩小容器体积
液化移出 d.缩小容器体积
您最近一年使用:0次

 H2(g)+
H2(g)+
 )是一种可再生能源,具有广泛的开发和应用前景。
)是一种可再生能源,具有广泛的开发和应用前景。

 充入2L的密闭容器中,充分反应,达到平衡后,测得
充入2L的密闭容器中,充分反应,达到平衡后,测得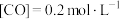 ,则CO的平衡转化率为
,则CO的平衡转化率为

