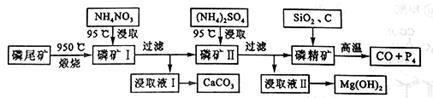
资源的高效利用对保护环境、促进经济持续健康发展具有重要作用。磷尾矿主要含Ca5(PO4)3F和CaCO3·MgCO3。某研究小组提出了磷尾矿综合利用的研究方案,制备具有重要工业用途的CaCO3、Mg(OH)2、P4和H2,其简化流程如下:
已知:①Ca5(PO4)3F在950℃不分解;
②4Ca5(PO4)3F+18SiO2+30C 2CaF2+30CO+18CaSiO3+3P4
2CaF2+30CO+18CaSiO3+3P4
请回答下列问题:
(1)950℃煅烧磷尾矿生成气体的主要成分是___________ 。
(2)实验室过滤所需的玻璃仪器是_____________ 。
(3)NH4NO3溶液能从磷矿Ⅰ中浸取出Ca2+的原因是__________ 。
(4)在浸取液Ⅱ中通入NH3,发生反应的化学方程式是____________ 。
(5)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ΔH=-271kJ/mol
5 CaO(s)+3H3PO4(l)+HF(g)= Ca5(PO4)3F (s)+5H2O(l) ΔH=-937kJ/mol
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是_________________ 。
(6)在一定条件下CO(g)+H2O(g) CO2(g)+H2(g),当CO与H2O(g)的起始物质的量之比为1:5,达平衡时,CO转化了
CO2(g)+H2(g),当CO与H2O(g)的起始物质的量之比为1:5,达平衡时,CO转化了 。若a kg含Ca5(PO4)3F(相对分子质量为504)的质量分数为10%的磷尾矿,在上述过程中有b%的Ca5(PO4)3F转化为P4,将产生的CO与H2O(g)按起始物质的量之比1:3混合,则相同条件下达平衡时能产生H2
。若a kg含Ca5(PO4)3F(相对分子质量为504)的质量分数为10%的磷尾矿,在上述过程中有b%的Ca5(PO4)3F转化为P4,将产生的CO与H2O(g)按起始物质的量之比1:3混合,则相同条件下达平衡时能产生H2________ kg。

已知:①Ca5(PO4)3F在950℃不分解;
②4Ca5(PO4)3F+18SiO2+30C
 2CaF2+30CO+18CaSiO3+3P4
2CaF2+30CO+18CaSiO3+3P4请回答下列问题:
(1)950℃煅烧磷尾矿生成气体的主要成分是
(2)实验室过滤所需的玻璃仪器是
(3)NH4NO3溶液能从磷矿Ⅰ中浸取出Ca2+的原因是
(4)在浸取液Ⅱ中通入NH3,发生反应的化学方程式是
(5)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ΔH=-271kJ/mol
5 CaO(s)+3H3PO4(l)+HF(g)= Ca5(PO4)3F (s)+5H2O(l) ΔH=-937kJ/mol
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是
(6)在一定条件下CO(g)+H2O(g)
 CO2(g)+H2(g),当CO与H2O(g)的起始物质的量之比为1:5,达平衡时,CO转化了
CO2(g)+H2(g),当CO与H2O(g)的起始物质的量之比为1:5,达平衡时,CO转化了 。若a kg含Ca5(PO4)3F(相对分子质量为504)的质量分数为10%的磷尾矿,在上述过程中有b%的Ca5(PO4)3F转化为P4,将产生的CO与H2O(g)按起始物质的量之比1:3混合,则相同条件下达平衡时能产生H2
。若a kg含Ca5(PO4)3F(相对分子质量为504)的质量分数为10%的磷尾矿,在上述过程中有b%的Ca5(PO4)3F转化为P4,将产生的CO与H2O(g)按起始物质的量之比1:3混合,则相同条件下达平衡时能产生H2
2016·四川·高考真题 查看更多[5]
更新时间:2016-12-09 16:08:40
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】电化学原理在医学医疗中有重要应用。
(1)碘可用作心脏起搏器电源—锂碘电池的材料。该电池反应如下:
2Li(s)+I2(s)=2LiI(s) ΔH
已知:4Li(s)+O2(g)=2Li2O(s) ΔH1
4LiI(s)+O2(g)=2I2(s)+2Li2O(s) ΔH2
则ΔH=_______ ;碘电极作为该电池的_______ 极。
(2)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用离子方程式表示:盐碱地产生碱性的原因:_______ 。
(3)已知水存在如下平衡:H2O⇌H++OH-,向水中加入NaHSO4固体,水的电离平衡向_______ 移动(正反应方向,逆反应方向),所得溶液显_______ 性。
(4)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=_______ 。此溶液中离子浓度由大到小的顺序是_______ 。
(5)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;
b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈_______ 性(填“酸”、“碱”或“中”),NH4HCO3溶液中物质的量浓度最大的离子是_______ (填离子符号)。
(1)碘可用作心脏起搏器电源—锂碘电池的材料。该电池反应如下:
2Li(s)+I2(s)=2LiI(s) ΔH
已知:4Li(s)+O2(g)=2Li2O(s) ΔH1
4LiI(s)+O2(g)=2I2(s)+2Li2O(s) ΔH2
则ΔH=
(2)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用离子方程式表示:盐碱地产生碱性的原因:
(3)已知水存在如下平衡:H2O⇌H++OH-,向水中加入NaHSO4固体,水的电离平衡向
(4)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=
(5)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;
b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】油气开采、石油化工、煤化工等行业的废气中均含有硫化氢,需要将其回收处理并加以利用
Ⅰ、高温热分解法: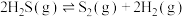
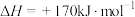
(1)该反应的化学平衡常数表达式为_____ 。
(2)升高温度,该反应的化学平衡常数_____ (填“变大”“变小”或“不变”)。
(3)工业上,通常在等温、等压条件下将 与Ar的混合气体通入反应器,发生
与Ar的混合气体通入反应器,发生 热分解反应,达到平衡状态后,若继续向反应器中通入Ar,
热分解反应,达到平衡状态后,若继续向反应器中通入Ar, 的平衡转化率会
的平衡转化率会_____ (填“增大”“减小”或“不变”)
Ⅱ、克劳斯法:
已知: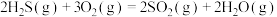
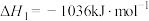

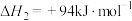
(4)用克劳斯法处理 ,若生成1mol
,若生成1mol ,放出热量
,放出热量_____ kJ。
(5)用克劳斯法处理 时,研究人员对反应条件对
时,研究人员对反应条件对 产率的影响进行了如下研究。
产率的影响进行了如下研究。
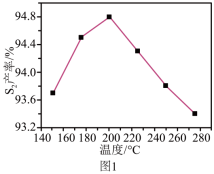
①其他条件相同时,相同时间内, 产率随温度的变化如图1所示。由图1可见,随着温度升高,
产率随温度的变化如图1所示。由图1可见,随着温度升高, 产率先增大后减小,原因是
产率先增大后减小,原因是_____ 。
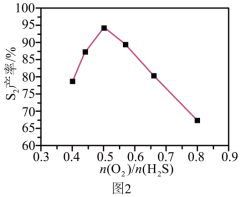
②其他条件相同时,相同时间内, 产率随
产率随 值的变化如图2所示。
值的变化如图2所示。 值过高不利于提高
值过高不利于提高 产率,可能的原因是
产率,可能的原因是_____ 。
Ⅰ、高温热分解法:
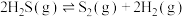
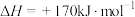
(1)该反应的化学平衡常数表达式为
(2)升高温度,该反应的化学平衡常数
(3)工业上,通常在等温、等压条件下将
 与Ar的混合气体通入反应器,发生
与Ar的混合气体通入反应器,发生 热分解反应,达到平衡状态后,若继续向反应器中通入Ar,
热分解反应,达到平衡状态后,若继续向反应器中通入Ar, 的平衡转化率会
的平衡转化率会Ⅱ、克劳斯法:

已知:
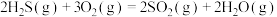
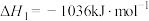

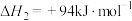
(4)用克劳斯法处理
 ,若生成1mol
,若生成1mol ,放出热量
,放出热量(5)用克劳斯法处理
 时,研究人员对反应条件对
时,研究人员对反应条件对 产率的影响进行了如下研究。
产率的影响进行了如下研究。①其他条件相同时,相同时间内,
 产率随温度的变化如图1所示。由图1可见,随着温度升高,
产率随温度的变化如图1所示。由图1可见,随着温度升高, 产率先增大后减小,原因是
产率先增大后减小,原因是
②其他条件相同时,相同时间内,
 产率随
产率随 值的变化如图2所示。
值的变化如图2所示。 值过高不利于提高
值过高不利于提高 产率,可能的原因是
产率,可能的原因是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划。
(1)催化剂常具有较强的选择性,即专一性。已知:
反应I:4NH3(g)+5O2(g)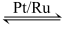 4NO(g)+6H2O(g) ΔH=-905.0kJ·mol-1
4NO(g)+6H2O(g) ΔH=-905.0kJ·mol-1
反应II:4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH=-1266.6kJ·mol-1
2N2(g)+6H2O(g) ΔH=-1266.6kJ·mol-1
写出NO分解生成N2与O2的热化学方程式___ 。
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应I,测得不同时间的NH3和O2的浓度如下表:
则下列有关叙述中正确的是____ 。
A.使用催化剂时,在加快其反应速率的同时,也可以提高反应物的平衡转化率
B.若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内NH3和O2的比例恒定时,说明反应已达平衡
D.前10分钟内的平均速率v(NO)=0.088mol·L-1·min-1
E.在该体系中,当反应达到平衡时,压强为p1;充入少量的NO,达到新平衡时,压强为p2,则p2>p1。
(3)氨催化氧化时会发生上述两个竞争反应I、II。为分析某催化剂对该反应的选择性,在1L密闭容器中充入1molNH3和2molO2,测得有关物质的量关系如图:
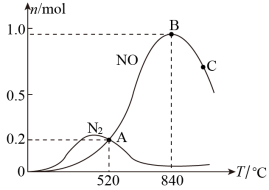
①该催化剂在低温时选择反应____ (填“I”或“II”)。
②520℃时,4NH3(g)+3O2(g) 2N2(g)+6H2O(g)的平衡常数K=
2N2(g)+6H2O(g)的平衡常数K=___ (不要求得出计算结果,只需列出数字计算式)。
③C点比B点所产生的NO的物质的量少的主要原因___ 。
(4)制备催化剂时常产生一定的废液,工业上常利用氢硫酸检测和除去废液中的Cu2+。已知:25℃时,K1(H2S)=1.3×10-7,K2(H2S)=7.1×10-15。
①在计算溶液中的离子浓度时,涉及弱酸的电离通常要进行近似处理。则0.lmol•L-1氢硫酸的pH≈___ (取近似整数)。
②已知,某浓度为0.1mol/LCuSO4溶液,若通入适量的H2S至Cu2+恰好沉淀完全时,此时溶液液中c(H+)为___ mol·L-1。
(1)催化剂常具有较强的选择性,即专一性。已知:
反应I:4NH3(g)+5O2(g)
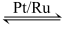 4NO(g)+6H2O(g) ΔH=-905.0kJ·mol-1
4NO(g)+6H2O(g) ΔH=-905.0kJ·mol-1反应II:4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) ΔH=-1266.6kJ·mol-1
2N2(g)+6H2O(g) ΔH=-1266.6kJ·mol-1写出NO分解生成N2与O2的热化学方程式
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应I,测得不同时间的NH3和O2的浓度如下表:
| 时间(min) | 0 | 5 | 10 | 15 | 20 | 25 |
| c(NH3)mol/L | 1.00 | 0.36 | 0.12 | 0.08 | 0.072 | 0.072 |
| c(O2)mol/L | 2.00 | 1.20 | 0.90 | 0.85 | 0.84 | 0.84 |
则下列有关叙述中正确的是
A.使用催化剂时,在加快其反应速率的同时,也可以提高反应物的平衡转化率
B.若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内NH3和O2的比例恒定时,说明反应已达平衡
D.前10分钟内的平均速率v(NO)=0.088mol·L-1·min-1
E.在该体系中,当反应达到平衡时,压强为p1;充入少量的NO,达到新平衡时,压强为p2,则p2>p1。
(3)氨催化氧化时会发生上述两个竞争反应I、II。为分析某催化剂对该反应的选择性,在1L密闭容器中充入1molNH3和2molO2,测得有关物质的量关系如图:

①该催化剂在低温时选择反应
②520℃时,4NH3(g)+3O2(g)
 2N2(g)+6H2O(g)的平衡常数K=
2N2(g)+6H2O(g)的平衡常数K=③C点比B点所产生的NO的物质的量少的主要原因
(4)制备催化剂时常产生一定的废液,工业上常利用氢硫酸检测和除去废液中的Cu2+。已知:25℃时,K1(H2S)=1.3×10-7,K2(H2S)=7.1×10-15。
①在计算溶液中的离子浓度时,涉及弱酸的电离通常要进行近似处理。则0.lmol•L-1氢硫酸的pH≈
②已知,某浓度为0.1mol/LCuSO4溶液,若通入适量的H2S至Cu2+恰好沉淀完全时,此时溶液液中c(H+)为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】甲烷是一种理想的洁净燃料,利用甲烷与水反应制备氢气,因原料廉价,具有推广价值。该反应为CH4(g)+H2O(g)  CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0
(1)若800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表。
则此时正、逆反应速率的关系是v(正)______ v(逆)。(填“>”“<”“=”)
(2)为了探究温度、压强对上述化学反应速率的影响,某同学设计了以下三组对比实验(温度为360℃或480℃、压强为101 kPa或303 kPa,其余实验条件见下表)。
表中P=_________ ; 实验l、2、3中反应的化学平衡常数的大小关系是_________ (用K1、K2、K3表示)
(3)—定温度下,在容积1L且固定的两个密闭容器中,按如下方式加入反应物, 一段时间后达到平衡。
经测定甲容器经过5min达到平衡,平衡后甲中气体的压强为开始的1.2倍,则此条件下的平衡常数=__________ ,若要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则b的取值范围为__________________ 。
 CO(g)+3H2(g) △H>0
CO(g)+3H2(g) △H>0(1)若800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表。
| CH4 | H2O | CO | H2 |
| 2.0 mol·L-1 | 2.0 mol·L-1 | 4.0 mol·L-1 | 1.0 mol·L-1 |
则此时正、逆反应速率的关系是v(正)
(2)为了探究温度、压强对上述化学反应速率的影响,某同学设计了以下三组对比实验(温度为360℃或480℃、压强为101 kPa或303 kPa,其余实验条件见下表)。
| 实验序号 | 温度/℃ | 压强/kPa | CH4初始浓度/mol·L-1 | H2O初始浓度/ mol·L-1 |
| 1 | 360 | 101 | 2.00 | 6.80 |
| 2 | t | 101 | 2.00 | 6.80 |
| 3 | 360 | P | 2.00 | 6.80 |
表中P=
(3)—定温度下,在容积1L且固定的两个密闭容器中,按如下方式加入反应物, 一段时间后达到平衡。
| 容器 | 甲 | 乙 |
| 反应物投入量 | 2molCH4、 2molH2O | amolCH4、 amolH2O、b molCO、b molH2 |
经测定甲容器经过5min达到平衡,平衡后甲中气体的压强为开始的1.2倍,则此条件下的平衡常数=
您最近半年使用:0次
【推荐2】工业废气、汽车尾气排放出的SO2、NOx等,是形成雾霾的重要因素。霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾。
(1)NOx和SO2在空气中存在下列平衡:2NO(g)+O2(g) 2NO2(g)△H=-113.0kJ•mol-1,2SO2(g)+O2(g)
2NO2(g)△H=-113.0kJ•mol-1,2SO2(g)+O2(g) 2SO3(g)△H=-296.6kJ•mol-1,SO2通常在二氧化氮的存在下,进一步被氧化,生成SO3。
2SO3(g)△H=-296.6kJ•mol-1,SO2通常在二氧化氮的存在下,进一步被氧化,生成SO3。
①写出NO2和SO2反应的热化学方程式为______________________________ 。
②随温度降低,该反应化学平衡常数变化趋势是______ (填“增大”或“减小”或“不变”)。
(2)提高2SO2+O2 2SO3反应中SO2的转化率,是减少SO2排放的有效措施。
2SO3反应中SO2的转化率,是减少SO2排放的有效措施。
①T温度时,在10L的密闭容器中加入2.0molSO2和1.0molO2,5min后反应达到平衡,二氧化硫的转化率为50%,该反应的平衡常数是______ 。
②在①中条件下,反应达到平衡后,改变下列条件,能使SO2的转化率提高的是______ (填字母)。
a.温度和容器体积不变,充入1.0molHe
b.温度和容器体积不变,充入1.0molO2
c.在其他条件不变时,改用高效催化剂
d.在其他条件不变时,减少容器的体积
e.在其他条件不变时,升高体系温度
(3)工业上利用氯碱工业产品治理含二氧化硫的废气.如图是氯碱工业中电解饱和食盐水的原理示意图
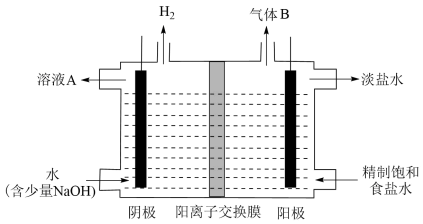
①电解饱和食盐水的化学方程式是__________________________ ;
②若用NaOH溶液吸收含二氧化硫的废气,当二者恰好完全反应生成NaHSO3时,溶液的pH<7,则该溶液中各离子浓度由大到小的顺序为_________________________ ;
③用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是____________ 。
(1)NOx和SO2在空气中存在下列平衡:2NO(g)+O2(g)
 2NO2(g)△H=-113.0kJ•mol-1,2SO2(g)+O2(g)
2NO2(g)△H=-113.0kJ•mol-1,2SO2(g)+O2(g) 2SO3(g)△H=-296.6kJ•mol-1,SO2通常在二氧化氮的存在下,进一步被氧化,生成SO3。
2SO3(g)△H=-296.6kJ•mol-1,SO2通常在二氧化氮的存在下,进一步被氧化,生成SO3。①写出NO2和SO2反应的热化学方程式为
②随温度降低,该反应化学平衡常数变化趋势是
(2)提高2SO2+O2
 2SO3反应中SO2的转化率,是减少SO2排放的有效措施。
2SO3反应中SO2的转化率,是减少SO2排放的有效措施。①T温度时,在10L的密闭容器中加入2.0molSO2和1.0molO2,5min后反应达到平衡,二氧化硫的转化率为50%,该反应的平衡常数是
②在①中条件下,反应达到平衡后,改变下列条件,能使SO2的转化率提高的是
a.温度和容器体积不变,充入1.0molHe
b.温度和容器体积不变,充入1.0molO2
c.在其他条件不变时,改用高效催化剂
d.在其他条件不变时,减少容器的体积
e.在其他条件不变时,升高体系温度
(3)工业上利用氯碱工业产品治理含二氧化硫的废气.如图是氯碱工业中电解饱和食盐水的原理示意图

①电解饱和食盐水的化学方程式是
②若用NaOH溶液吸收含二氧化硫的废气,当二者恰好完全反应生成NaHSO3时,溶液的pH<7,则该溶液中各离子浓度由大到小的顺序为
③用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是
您最近半年使用:0次
【推荐3】煤化工中常需研究反应在不同温度下的平衡常数,C、 与水蒸气之间的相互反应是煤化工中的重要反应。
与水蒸气之间的相互反应是煤化工中的重要反应。
(1)已知在一定温度下:
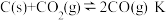
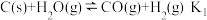

则K、 、
、 之间的关系是
之间的关系是___________ 。
(2)已知反应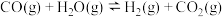 在500℃时的平衡常数为9。在500℃时,若
在500℃时的平衡常数为9。在500℃时,若 、
、 的起始浓度均为
的起始浓度均为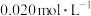 ,则在该条件下,
,则在该条件下, 的最大转化率为
的最大转化率为____________ 。
(3)向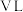 的密闭容器中通入
的密闭容器中通入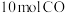 和
和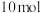 水蒸气,在
水蒸气,在 下达到平衡时,急速除去水蒸气(除水蒸气时其他物质的物质的量不变),将混合气体点燃,测得放出的热量为
下达到平衡时,急速除去水蒸气(除水蒸气时其他物质的物质的量不变),将混合气体点燃,测得放出的热量为 (已知该条件下
(已知该条件下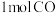 完全燃烧放出
完全燃烧放出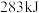 热量,
热量,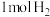 完全燃烧放出
完全燃烧放出 热量),则
热量),则 时该反应的平衡常数
时该反应的平衡常数
________ 。
 与水蒸气之间的相互反应是煤化工中的重要反应。
与水蒸气之间的相互反应是煤化工中的重要反应。(1)已知在一定温度下:
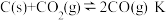
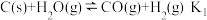

则K、
 、
、 之间的关系是
之间的关系是(2)已知反应
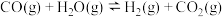 在500℃时的平衡常数为9。在500℃时,若
在500℃时的平衡常数为9。在500℃时,若 、
、 的起始浓度均为
的起始浓度均为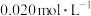 ,则在该条件下,
,则在该条件下, 的最大转化率为
的最大转化率为(3)向
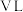 的密闭容器中通入
的密闭容器中通入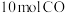 和
和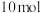 水蒸气,在
水蒸气,在 下达到平衡时,急速除去水蒸气(除水蒸气时其他物质的物质的量不变),将混合气体点燃,测得放出的热量为
下达到平衡时,急速除去水蒸气(除水蒸气时其他物质的物质的量不变),将混合气体点燃,测得放出的热量为 (已知该条件下
(已知该条件下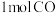 完全燃烧放出
完全燃烧放出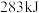 热量,
热量,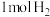 完全燃烧放出
完全燃烧放出 热量),则
热量),则 时该反应的平衡常数
时该反应的平衡常数
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】碘是人类发现的第二个生命体必需微量元素。回答下列问题:
(1)碘与氯是同族元素,它们位于元素周期表的第______ 族;HI的稳定性比HCl________ (填“强”或“弱”,下同),HI的还原性比HCl__________ 。
(2)自然界中的碘有的以NaIO3形态存在于硝石(NaNO3)中,向硝石母液中加入NaHSO3可以制得I2,请写出NaIO3溶液和NaHSO3溶液反应的离子方程式:_________ 。
(3)碘还以碘化物的形态存在于海水中,被海藻类植物吸收而富集,从海带中提取碘的过程如图:
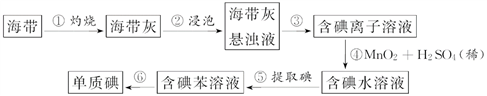
步骤③的操作名称为________________ ;
步骤④发生反应的离子方程式为_______________________________________________ 。
(1)碘与氯是同族元素,它们位于元素周期表的第
(2)自然界中的碘有的以NaIO3形态存在于硝石(NaNO3)中,向硝石母液中加入NaHSO3可以制得I2,请写出NaIO3溶液和NaHSO3溶液反应的离子方程式:
(3)碘还以碘化物的形态存在于海水中,被海藻类植物吸收而富集,从海带中提取碘的过程如图:

步骤③的操作名称为
步骤④发生反应的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】铟是一种稀有贵金属,广泛应用于航空航天、太阳能电池等高科技领域。从铜烟灰酸浸渣(主要含PbO、FeAsO4·2H2O、In2O3)中提取铟和铅的工艺流程如下:

已知:①焙烧后金属元素均以硫酸盐的形式存在;
②In(OH)3性质与Al(OH)3类似。
回答下列问题:
(1)FeAsO4·2H2O中铁元素化合价为_______ 。
(2)生成PbO粗品的化学反应方程式为_______ 。
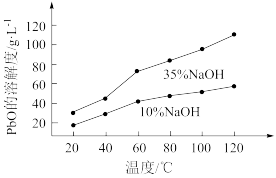
(3)PbO在NaOH溶液中溶解度曲线如图所示,PbO粗品中的杂质难溶于NaOH溶液。结合溶解度曲线,简述提纯PbO粗品的操作_______ 。
(4)“还原铁”反应的离子方程式为________
(5)“萃取除铁”中,发现当溶液pH>1.5后,铟萃取率随pH的升高而下降,原因是_______
(6)为测定PbO产品的纯度,探究小组同学准确称取PbO1.161g,加入稀硝酸使其完全溶解,再加入蒸馏水配制成50.00mL溶液:冷却至25℃,用0.100mol·L-1H2SO4滴定该溶液,滴定曲线如图所示。
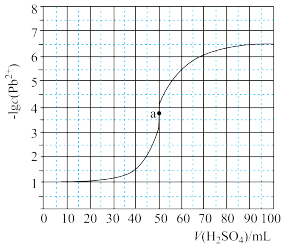
已知: ;a点的坐标为(50,3.8)
;a点的坐标为(50,3.8)
①25℃,PbSO4的Ksp=_______ 。
②PbO产品的纯度为_______ 。

已知:①焙烧后金属元素均以硫酸盐的形式存在;
②In(OH)3性质与Al(OH)3类似。
回答下列问题:
(1)FeAsO4·2H2O中铁元素化合价为
(2)生成PbO粗品的化学反应方程式为
(3)PbO在NaOH溶液中溶解度曲线如图所示,PbO粗品中的杂质难溶于NaOH溶液。结合溶解度曲线,简述提纯PbO粗品的操作

(4)“还原铁”反应的离子方程式为
(5)“萃取除铁”中,发现当溶液pH>1.5后,铟萃取率随pH的升高而下降,原因是
(6)为测定PbO产品的纯度,探究小组同学准确称取PbO1.161g,加入稀硝酸使其完全溶解,再加入蒸馏水配制成50.00mL溶液:冷却至25℃,用0.100mol·L-1H2SO4滴定该溶液,滴定曲线如图所示。

已知:
 ;a点的坐标为(50,3.8)
;a点的坐标为(50,3.8)①25℃,PbSO4的Ksp=
②PbO产品的纯度为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】黄铜灰渣(含有Cu、Zn、CuO、ZnO及少量FeO、Fe3O4、Fe2O3)生产 溶液的流程如下图所示。
溶液的流程如下图所示。
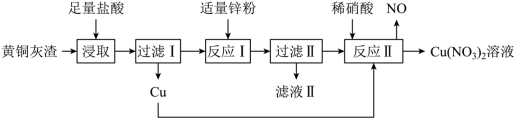
回答下列问题:
(1)写出“浸取”时Fe3O4反应的离子方程式:___________ 。
(2)小明认为“过滤Ⅰ”后所得滤液中不否含Fe3+,理由是:___________ (用离子方程式表示)。
(3)“滤液Ⅱ”中的金属阳离子是___________ 。
(4)“反应Ⅱ”所用稀硝酸可由质量分数为63%、密度为1.40g·cm-3的浓硝酸稀释获得。
①若要获得100mL1.4mol·L-1的稀硝酸,需要用到浓硝酸的体积为___________ mL。另有实验需470mL0.1mol·L-1CuSO4溶液,配制时要用托盘天平称取胆矾___________ g。
②NO是一种无色气体,请依据信息写出“反应Ⅱ”的化学方程式:___________ 。
③ 将绿豆大小的金属钠(Na)放入足量的Cu(NO3)2溶液中,得到的固体产物是___________ (填化学式)
 溶液的流程如下图所示。
溶液的流程如下图所示。
回答下列问题:
(1)写出“浸取”时Fe3O4反应的离子方程式:
(2)小明认为“过滤Ⅰ”后所得滤液中不否含Fe3+,理由是:
(3)“滤液Ⅱ”中的金属阳离子是
(4)“反应Ⅱ”所用稀硝酸可由质量分数为63%、密度为1.40g·cm-3的浓硝酸稀释获得。
①若要获得100mL1.4mol·L-1的稀硝酸,需要用到浓硝酸的体积为
②NO是一种无色气体,请依据信息写出“反应Ⅱ”的化学方程式:
③ 将绿豆大小的金属钠(Na)放入足量的Cu(NO3)2溶液中,得到的固体产物是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】铁及其化合物在生产生活中有广泛应用。
(1) 可用作净水剂,也可用于无线电印刷电路做蚀刻剂。某化学兴趣小组利用如图所示装置向
可用作净水剂,也可用于无线电印刷电路做蚀刻剂。某化学兴趣小组利用如图所示装置向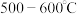 的铁屑中通入
的铁屑中通入 生产无水
生产无水 。已知:
。已知: 固体呈黑棕色、易潮解、
固体呈黑棕色、易潮解、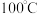 左右时升华。
左右时升华。
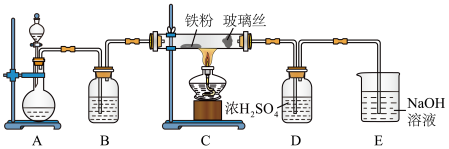
回答下列问题
①写出用高锰酸钾和浓盐酸在装置 中制备氯气的离子方程式
中制备氯气的离子方程式_____ 。
②装置 中加入的试剂是
中加入的试剂是_____ ,装置 中玻璃丝的作用是
中玻璃丝的作用是_____ , 中
中 溶液的作用是
溶液的作用是_____ 。
③有同学认为气体通入装置 前应除去其中含有的
前应除去其中含有的 ,改进措施为
,改进措施为_____ 。
(2)一种新型高效净水剂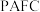 (聚合氯化铁铝
(聚合氯化铁铝 ,广泛用于日常生活用水和工业污水的处理。某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取
,广泛用于日常生活用水和工业污水的处理。某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取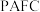 ,设计生产流程如下:
,设计生产流程如下:
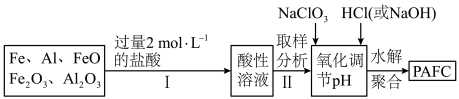
①实验室现需用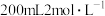 的稀盐酸,欲用
的稀盐酸,欲用 的浓盐酸配制,则所需浓盐酸体积为
的浓盐酸配制,则所需浓盐酸体积为________ 。
②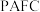 中
中 显
显________ 价,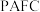 在强酸性和强碱性溶液中均
在强酸性和强碱性溶液中均________ 稳定存在(填“能”或“不能”)。
③步骤Ⅱ中取样分析的目的是________ 。
A.测定溶液中 与
与 的含量比 B.测定原料是否完全溶解
的含量比 B.测定原料是否完全溶解
C.测定溶液中 的含量,以确定加入
的含量,以确定加入 的量 D.测定溶液中
的量 D.测定溶液中 的含量
的含量
(1)
 可用作净水剂,也可用于无线电印刷电路做蚀刻剂。某化学兴趣小组利用如图所示装置向
可用作净水剂,也可用于无线电印刷电路做蚀刻剂。某化学兴趣小组利用如图所示装置向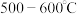 的铁屑中通入
的铁屑中通入 生产无水
生产无水 。已知:
。已知: 固体呈黑棕色、易潮解、
固体呈黑棕色、易潮解、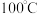 左右时升华。
左右时升华。
回答下列问题
①写出用高锰酸钾和浓盐酸在装置
 中制备氯气的离子方程式
中制备氯气的离子方程式②装置
 中加入的试剂是
中加入的试剂是 中玻璃丝的作用是
中玻璃丝的作用是 中
中 溶液的作用是
溶液的作用是③有同学认为气体通入装置
 前应除去其中含有的
前应除去其中含有的 ,改进措施为
,改进措施为(2)一种新型高效净水剂
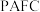 (聚合氯化铁铝
(聚合氯化铁铝 ,广泛用于日常生活用水和工业污水的处理。某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取
,广泛用于日常生活用水和工业污水的处理。某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取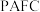 ,设计生产流程如下:
,设计生产流程如下:
①实验室现需用
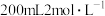 的稀盐酸,欲用
的稀盐酸,欲用 的浓盐酸配制,则所需浓盐酸体积为
的浓盐酸配制,则所需浓盐酸体积为②
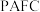 中
中 显
显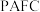 在强酸性和强碱性溶液中均
在强酸性和强碱性溶液中均③步骤Ⅱ中取样分析的目的是
A.测定溶液中
 与
与 的含量比 B.测定原料是否完全溶解
的含量比 B.测定原料是否完全溶解C.测定溶液中
 的含量,以确定加入
的含量,以确定加入 的量 D.测定溶液中
的量 D.测定溶液中 的含量
的含量
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:
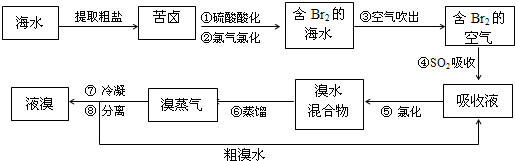
(1)步骤①中叫硫酸酸化可提高Cl2的利用率,理由是_______________ 。
(2)步骤④利用了SO2的还原性,反应的离子方程式为_______________ 。
(3)步骤⑥的蒸馏过程中,温度应控制在80〜90℃。温度过高或过低都不利于生产,请解释原因_______ 。
(4)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是______ 。
(5)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是_____ 。

(1)步骤①中叫硫酸酸化可提高Cl2的利用率,理由是
(2)步骤④利用了SO2的还原性,反应的离子方程式为
(3)步骤⑥的蒸馏过程中,温度应控制在80〜90℃。温度过高或过低都不利于生产,请解释原因
(4)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是
(5)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过“空气吹出”、“SO2吸收”、“氯化”后再蒸馏,这样操作的意义是
您最近半年使用:0次
【推荐3】我国出口球状氯化镁融雪剂时,对产品色度(白度)要求很高,因此研究脱色及显色离子的去除有现实意义。以水氯镁石为原料生产符合白度要求的融雪剂的流程如下。
已知:①水氯镁石的主要成分是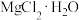 ,还含有少量有色有机物、可溶性
,还含有少量有色有机物、可溶性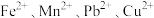 等杂质离子及少量不溶物。
等杂质离子及少量不溶物。
I.去除泥沙及脱除有机物颜色
水氯镁石
 饱和溶液
饱和溶液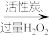 脱色后的
脱色后的 饱和溶液
饱和溶液
(1)操作1的名称是_______ 。
(2)活性炭的作用是_______ 。
(3)部分有机物可与 反应脱氢,在该反应中,
反应脱氢,在该反应中, 体现的性质是
体现的性质是_______ 。
(4)其它条件都不变的情况下,得到温度对脱色率的影响如图所示。 后,随温度升高,脱色率下降的原因是
后,随温度升高,脱色率下降的原因是_______ 。

II.去除显色离子
向脱色处理后的氯化镁溶液中加入氨水反应30分钟,再将溶液升温至 保持30分钟,恢复至室温,最后加入适量的
保持30分钟,恢复至室温,最后加入适量的 溶液反应一段时间,过滤得到氯化镁精制溶液。
溶液反应一段时间,过滤得到氯化镁精制溶液。
(5)过滤得到的滤渣中含有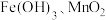 、
、_______ 。
①将横线补充完整_______ 。
②将生成 的离子方程式补充完整:
的离子方程式补充完整:_______ 、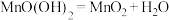
(6)将溶液升温至 的目的是
的目的是_______ 。
III.制备产品
氯化镁精制溶液
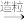 球状氯化镁融雪剂
球状氯化镁融雪剂
(7)操作2是_______ 。
已知:①水氯镁石的主要成分是
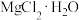 ,还含有少量有色有机物、可溶性
,还含有少量有色有机物、可溶性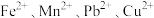 等杂质离子及少量不溶物。
等杂质离子及少量不溶物。| 物质 |  |  |
 | 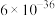 | 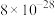 |
水氯镁石

 饱和溶液
饱和溶液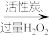 脱色后的
脱色后的 饱和溶液
饱和溶液(1)操作1的名称是
(2)活性炭的作用是
(3)部分有机物可与
 反应脱氢,在该反应中,
反应脱氢,在该反应中, 体现的性质是
体现的性质是(4)其它条件都不变的情况下,得到温度对脱色率的影响如图所示。
 后,随温度升高,脱色率下降的原因是
后,随温度升高,脱色率下降的原因是
II.去除显色离子
向脱色处理后的氯化镁溶液中加入氨水反应30分钟,再将溶液升温至
 保持30分钟,恢复至室温,最后加入适量的
保持30分钟,恢复至室温,最后加入适量的 溶液反应一段时间,过滤得到氯化镁精制溶液。
溶液反应一段时间,过滤得到氯化镁精制溶液。(5)过滤得到的滤渣中含有
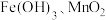 、
、①将横线补充完整
②将生成
 的离子方程式补充完整:
的离子方程式补充完整: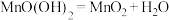
(6)将溶液升温至
 的目的是
的目的是III.制备产品
氯化镁精制溶液

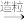 球状氯化镁融雪剂
球状氯化镁融雪剂(7)操作2是
您最近半年使用:0次



