已知:2A(g)+B(g) 2C(g);ΔH =-a kJ/mol(a>0)。在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500℃时充分反应达平衡后C的浓度w mol/L,放出热量b kJ。
2C(g);ΔH =-a kJ/mol(a>0)。在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500℃时充分反应达平衡后C的浓度w mol/L,放出热量b kJ。
(1)比较a____ b(填“>”“=”或“<”)。
(2)若在原来的容器中,只加入2 mol C,500℃时充分反应达到平衡后,吸收热量c kJ,C浓度__________ w mol/L(填“>”“=”或“<”),a、b、c之间满足何种关系_______________ (用a、b、c建立一个等式关系)。
(3)能说明该反应已经达到平衡状态的是____________ (填写字母)。
A.v(C)=2v(B) B.容器内压强保持不变
C.v逆(A)=2v正(B) D.容器内的密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的操作是_______ (填写字母)。
A.及时分离出C气体B.适当升高温度
C.增大B的浓度D.选择高效的催化剂
(5)若将上述容器改为恒压容器(反应前体积、压强相同),起始时加入2 mol A和1 mol B,500℃时充分反应达平衡后,放出热量d kJ,则d________ b(填“>”、“=”或“<”),理由是__________ 。
 2C(g);ΔH =-a kJ/mol(a>0)。在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500℃时充分反应达平衡后C的浓度w mol/L,放出热量b kJ。
2C(g);ΔH =-a kJ/mol(a>0)。在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500℃时充分反应达平衡后C的浓度w mol/L,放出热量b kJ。(1)比较a
(2)若在原来的容器中,只加入2 mol C,500℃时充分反应达到平衡后,吸收热量c kJ,C浓度
(3)能说明该反应已经达到平衡状态的是
A.v(C)=2v(B) B.容器内压强保持不变
C.v逆(A)=2v正(B) D.容器内的密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的操作是
A.及时分离出C气体B.适当升高温度
C.增大B的浓度D.选择高效的催化剂
(5)若将上述容器改为恒压容器(反应前体积、压强相同),起始时加入2 mol A和1 mol B,500℃时充分反应达平衡后,放出热量d kJ,则d
更新时间:2017-10-24 18:56:59
|
相似题推荐
【推荐1】回答下列问题。
(1)在相同温度下,反应①比反应②释放的热量多,为什么?_______
 ①
①
 ②
②
(2)在相同条件下,反应③和反应④释放的热量几乎相等,从化学键的角度分析,原因是什么?_______
 ③
③
 ④
④
(注: 的结构简式为
的结构简式为 ,
, 的结构简式为
的结构简式为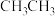 ,
, 的结构简式为
的结构简式为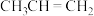 ,
, 的结构简式为
的结构简式为 )
)
(1)在相同温度下,反应①比反应②释放的热量多,为什么?
 ①
① ②
②(2)在相同条件下,反应③和反应④释放的热量几乎相等,从化学键的角度分析,原因是什么?
 ③
③ ④
④(注:
 的结构简式为
的结构简式为 ,
, 的结构简式为
的结构简式为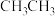 ,
, 的结构简式为
的结构简式为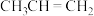 ,
, 的结构简式为
的结构简式为 )
)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:①N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-543kJ/mol
③H2(g)+F2(g)=2HF(g)△H=-538kJ/mol
④H2(g)+ O2(g)=H2O(g)△H=-242kJ/mol
O2(g)=H2O(g)△H=-242kJ/mol
(1)以上四个反应中,属于放热反应的是_____ ,属于吸热反应的是_____ 。
(2)由以上反应可知,等物质的量的N2H4(g)和H2(g)与足量的O2(g)反应,放出能量更多的是_____ (填“N2H4”或“H2”,下同);等质量的N2H4(g)和H2(g)与足量的O2(g)反应,放出能量更多的是____ 。
(3)由反应①和②可求:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) △H=-_____ kJ/mol
(4)有人认为若用氟代替二氧化氮作氧化剂,则反应释放能量更大,由反应②、③、④可求:N2H4(g)+2F2(g)=N2(g)+4HF(g) △H=-_____ kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-543kJ/mol
③H2(g)+F2(g)=2HF(g)△H=-538kJ/mol
④H2(g)+
 O2(g)=H2O(g)△H=-242kJ/mol
O2(g)=H2O(g)△H=-242kJ/mol(1)以上四个反应中,属于放热反应的是
(2)由以上反应可知,等物质的量的N2H4(g)和H2(g)与足量的O2(g)反应,放出能量更多的是
(3)由反应①和②可求:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) △H=-
(4)有人认为若用氟代替二氧化氮作氧化剂,则反应释放能量更大,由反应②、③、④可求:N2H4(g)+2F2(g)=N2(g)+4HF(g) △H=-
您最近一年使用:0次
【推荐3】(1)发射卫星时可用肼 为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:
为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:
① ,
,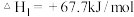
② ,
,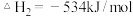 。
。
写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:_______ 。
(2)氢气的燃烧热为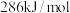 。写出表示氢气燃烧热的热化学方程式
。写出表示氢气燃烧热的热化学方程式_______ 。
(3)等质量的下列物质分别完全燃烧,放出热量较多的是反应过程_______ (填选项字母)。
A.固体硫 B.硫蒸气
(4)已知:通常条件下,强酸、强碱稀溶液中和生成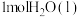 放出的热量为中和热。稀溶液中
放出的热量为中和热。稀溶液中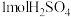 和足量NaOH恰好反应时放出QkJ热量,则其中和热为
和足量NaOH恰好反应时放出QkJ热量,则其中和热为_______  。
。
(5)已知 和
和 反应放热,且断开
反应放热,且断开 键、
键、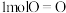 键、
键、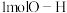 键吸收的能量分别为
键吸收的能量分别为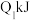 、
、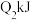 、
、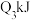 ,由此推知下列关系正确的是
,由此推知下列关系正确的是_______ (填选项字母)。
A.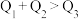
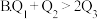
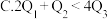
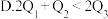
 为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:
为燃料,用二氧化氮为氧化剂,这两种物质反应生成氮气和水蒸气。已知:①
 ,
,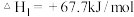
②
 ,
,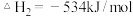 。
。写出肼和二氧化氮反应生成氮气和气态水的热化学方程式:
(2)氢气的燃烧热为
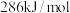 。写出表示氢气燃烧热的热化学方程式
。写出表示氢气燃烧热的热化学方程式(3)等质量的下列物质分别完全燃烧,放出热量较多的是反应过程
A.固体硫 B.硫蒸气
(4)已知:通常条件下,强酸、强碱稀溶液中和生成
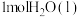 放出的热量为中和热。稀溶液中
放出的热量为中和热。稀溶液中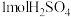 和足量NaOH恰好反应时放出QkJ热量,则其中和热为
和足量NaOH恰好反应时放出QkJ热量,则其中和热为 。
。(5)已知
 和
和 反应放热,且断开
反应放热,且断开 键、
键、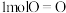 键、
键、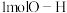 键吸收的能量分别为
键吸收的能量分别为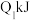 、
、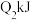 、
、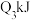 ,由此推知下列关系正确的是
,由此推知下列关系正确的是A.
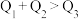
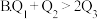
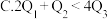
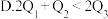
您最近一年使用:0次
【推荐1】煤的气化过程中发生反应:CO(g)+H2O(g) CO2(g)+H2(g),若在恒温恒压容器中充入1molCO和3mol水蒸气发生上述反应,达到平衡时测得反应物与生成物的物质的量之比为5∶3,且吸收热量180kJ,请回答下列问题:
CO2(g)+H2(g),若在恒温恒压容器中充入1molCO和3mol水蒸气发生上述反应,达到平衡时测得反应物与生成物的物质的量之比为5∶3,且吸收热量180kJ,请回答下列问题:
(1)该反应的热化学方程式可写为___ 。
(2)两种反应物的转化率之和为___ 。
(3)该条件下此反应的平衡常数为___ 。
(4)若要在相同的温度下和相同的容器中,按下列物料配比充入,建立平衡后CO的体积百分含量与题干平衡相同,下列选项中可行的是___ 。
 CO2(g)+H2(g),若在恒温恒压容器中充入1molCO和3mol水蒸气发生上述反应,达到平衡时测得反应物与生成物的物质的量之比为5∶3,且吸收热量180kJ,请回答下列问题:
CO2(g)+H2(g),若在恒温恒压容器中充入1molCO和3mol水蒸气发生上述反应,达到平衡时测得反应物与生成物的物质的量之比为5∶3,且吸收热量180kJ,请回答下列问题:(1)该反应的热化学方程式可写为
(2)两种反应物的转化率之和为
(3)该条件下此反应的平衡常数为
(4)若要在相同的温度下和相同的容器中,按下列物料配比充入,建立平衡后CO的体积百分含量与题干平衡相同,下列选项中可行的是
| 物质 选项 | n(CO) | n(H2O) | n(CO2) | n(H2) |
| A | 0mol | 4mol | 2mol | 2mol |
| B | 0.5mol | 2.5mol | 0.5mol | 0.5mol |
| C | 1mol | 4mol | 0.5mol | 0.5mol |
| D | 0mol | 0mol | 1mol | 3mol |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在100℃时,将0.100mol的N2O4气体充入1L抽空密闭容器中,发生反应:N2O4(g)⇌2NO2.现在隔一定时间对该容器内的物质进行分析,得到如下表格:
试回答下列问题:
(1)达到平衡时N2O4的转化率为_____ %,表中c2_____ c3,a_____ b(后两空选填>、<、=)
(2)20 s的N2O4的浓度c1=_____ mol/L在0~20s内N2O4的平均反应速率为_____ mol/(L•s);
(3)若其他反应条件以及初始物质物质的量不变,将反应的温度降低到80℃时,达到平衡时NO2的物质的量为0.100 mol,那么正反应是_____ 反应(选填吸热或放热)
(4)若在相同初始情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度为_____ mol/L。
| t/s c/(mol•L﹣1) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/(mol•L﹣1) | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2)/(mol•L﹣1) | 0 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试回答下列问题:
(1)达到平衡时N2O4的转化率为
(2)20 s的N2O4的浓度c1=
(3)若其他反应条件以及初始物质物质的量不变,将反应的温度降低到80℃时,达到平衡时NO2的物质的量为0.100 mol,那么正反应是
(4)若在相同初始情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度为
您最近一年使用:0次
【推荐3】一定温度下,向如图所示带有可移动活塞的密闭容器中充入2LSO2和1LO2的混合气体,发生如下反应2SO2(g)+O2(g)⇌2SO3(g)。
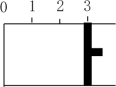
(1)若活塞可自由移动,平衡后,活塞由“3”移动到“2.1”处,则该反应中SO2的转化率为_______ 。
(2)若使活塞固定在“3”处,向容器中充入4LSO2和2LO2,反应进行到某一时刻时,SO2和O2的转化率之比为_______
(3)若使活塞固定在“3”处的三个相同容器,开始时,充入容器的起始物质分别是①2LSO2和1LO2;②2LSO3(g);③1LSO2、1LO2和1LSO3(g)。上述三种投料方式的反应体系均达到平衡后,则三种情况容器中SO3(g)的物质的量浓度大小关系是_______ (用序号和“<”、“=”、“>”表示)。

(1)若活塞可自由移动,平衡后,活塞由“3”移动到“2.1”处,则该反应中SO2的转化率为
(2)若使活塞固定在“3”处,向容器中充入4LSO2和2LO2,反应进行到某一时刻时,SO2和O2的转化率之比为
(3)若使活塞固定在“3”处的三个相同容器,开始时,充入容器的起始物质分别是①2LSO2和1LO2;②2LSO3(g);③1LSO2、1LO2和1LSO3(g)。上述三种投料方式的反应体系均达到平衡后,则三种情况容器中SO3(g)的物质的量浓度大小关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】向一个固定容积为2 L的密闭容器中充入4 mol N2和8 mol H2,在一定温度和压强下,发生反应N2(g)+3H2(g) 2NH3(g),5 s后达到平衡状态,测得N2的物质的量是2 mol。
2NH3(g),5 s后达到平衡状态,测得N2的物质的量是2 mol。
(1)以H2表示的反应速率为___________ ;
(2)下列措施不能使上述化学反应速率加快的是___________。
(3)下列叙述能说明该反应已达到化学平衡状态的是___________ (填标号)。
①单位时间内生成n mol N2的同时,生成3n mol H2 ② 各组分的物质的量浓度不再改变③ N2、H2、NH3物质的量浓度之比为1∶3∶2 ④混合气体的总物质的量保持不变⑤容器内压强保持不变 ⑥混合气体的密度保持不变
 2NH3(g),5 s后达到平衡状态,测得N2的物质的量是2 mol。
2NH3(g),5 s后达到平衡状态,测得N2的物质的量是2 mol。(1)以H2表示的反应速率为
(2)下列措施不能使上述化学反应速率加快的是___________。
| A.及时分离出NH3气体 | B.适当升高温度 | C.增大N2的浓度 | D.选择高效催化剂 |
①单位时间内生成n mol N2的同时,生成3n mol H2 ② 各组分的物质的量浓度不再改变③ N2、H2、NH3物质的量浓度之比为1∶3∶2 ④混合气体的总物质的量保持不变⑤容器内压强保持不变 ⑥混合气体的密度保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)氮是动植物生长不可缺少的元素,合成氨的反应对人类解决粮食问题贡献巨大,反应如下:N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
①合成氨的反应中的能量变化如图所示。该反应是___ 反应(填“吸热”或“放热”),其原因是反应物化学键断裂吸收的总能量___ (填“大于”或“小于”)生成物化学键形成放出的总能量。

②在一定条件下,将一定量的N2和H2的混合气体充入某密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是___ (填序号)。
A.容器中气体密度不变
B.N2、H2、NH3的物质的量之比为1:3:2
C.容器中的压强不随时间变化
D.单位时间内每断裂6 mol N—H键的同时断裂3 mol H﹣H键
(2)某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。2分钟时达到平衡状态,根据图中数据,试填写下列空白:

①该反应的化学方程式为___ 。
②反应开始到平衡建立,用气体Z表示的反应速率为___ ;若反应容器体积可变,则充入氮气会使反应速率___ (填”变快”、”变慢”或”不变”)
 2NH3(g)。
2NH3(g)。①合成氨的反应中的能量变化如图所示。该反应是

②在一定条件下,将一定量的N2和H2的混合气体充入某密闭容器中,一段时间后,下列叙述能说明该反应达到平衡状态的是
A.容器中气体密度不变
B.N2、H2、NH3的物质的量之比为1:3:2
C.容器中的压强不随时间变化
D.单位时间内每断裂6 mol N—H键的同时断裂3 mol H﹣H键
(2)某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。2分钟时达到平衡状态,根据图中数据,试填写下列空白:

①该反应的化学方程式为
②反应开始到平衡建立,用气体Z表示的反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】合成氨工业对国民经济和社会发展具有重要的意义。其原理为:N
 2NH
2NH ;据此回答以下问题:
;据此回答以下问题:
(1)该反应的化学平衡常数表达式为
_______ 。
(2)根据温度对化学平衡的影响规律可知,对于该反应温度越高,其化学平衡常数的值_______ 。(填“越大”、“越小”或“不变”)
(3)某温度下,若把 与
与 置于体积为
置于体积为 的密闭容器内,反应达到平衡状态时,测得混合气体的压强变为开始时的
的密闭容器内,反应达到平衡状态时,测得混合气体的压强变为开始时的 ,则平衡时氢气的转化率
,则平衡时氢气的转化率 =
=_______ (用百分数表示 。能说明该反应达到化学平衡状态的是
。能说明该反应达到化学平衡状态的是_______  填字母
填字母 。
。
a.容器内的密度保持不变 b.容器内压强保持不变
c.v正(N2)=2v逆(NH3) d.混合气体中c(NH3)不变
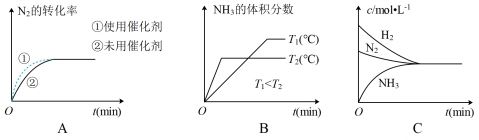
(4)对于合成氨反应而言,下列有关图象一定正确的是 选填序号
选填序号
_______ 。

 2NH
2NH ;据此回答以下问题:
;据此回答以下问题:(1)该反应的化学平衡常数表达式为

(2)根据温度对化学平衡的影响规律可知,对于该反应温度越高,其化学平衡常数的值
(3)某温度下,若把
 与
与 置于体积为
置于体积为 的密闭容器内,反应达到平衡状态时,测得混合气体的压强变为开始时的
的密闭容器内,反应达到平衡状态时,测得混合气体的压强变为开始时的 ,则平衡时氢气的转化率
,则平衡时氢气的转化率 =
= 。能说明该反应达到化学平衡状态的是
。能说明该反应达到化学平衡状态的是 填字母
填字母 。
。a.容器内的密度保持不变 b.容器内压强保持不变
c.v正(N2)=2v逆(NH3) d.混合气体中c(NH3)不变
(4)对于合成氨反应而言,下列有关图象一定正确的是
 选填序号
选填序号

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g) 2SO3(g) ∆H<0。
2SO3(g) ∆H<0。
(1)写出该反应的化学平衡常数表达式K=___________
(2)降低温度,该反应K值___________ ,二氧化硫转化率___________ ,化学反应速率___________ (以上均填增大、减小或不变)。
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态时间是___________ 。
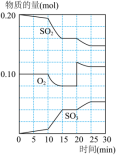
(4)据图判断,反应进行至20min时,曲线发生变化的原因是___________ (用文字表达)。
(5)若该反应的密闭容器为2L,则反应15min时,v(SO2)=___________ (取近似值)。
(6)为使该反应的反应速率增大,且平衡向正反应方向移动的是___________。
 2SO3(g) ∆H<0。
2SO3(g) ∆H<0。(1)写出该反应的化学平衡常数表达式K=
(2)降低温度,该反应K值
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态时间是

(4)据图判断,反应进行至20min时,曲线发生变化的原因是
(5)若该反应的密闭容器为2L,则反应15min时,v(SO2)=
(6)为使该反应的反应速率增大,且平衡向正反应方向移动的是___________。
| A.及时分离出SO3气体 | B.适当升高温度 |
| C.增大O2的浓度 | D.选择高效的催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】水煤气 (主要成分CO、H2 ) 是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:C (s) + H2O(g) CO (g) +H2 (g);△H =+131.3kJ•mol-1
CO (g) +H2 (g);△H =+131.3kJ•mol-1
(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和 1.0mo l水蒸气 (H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。平衡时水蒸气的转化率为___________ ;向该容器中补充 a mol 炭,水蒸气的转化率将____________ (填 “增大”、“减小”、“不变”),再补充 a mol 水蒸气 (H218O), 最终容器中C16O和C18O 的物质的量之比为_____________ 。
 CO (g) +H2 (g);△H =+131.3kJ•mol-1
CO (g) +H2 (g);△H =+131.3kJ•mol-1(1)某温度下,四个容器中均进行着上述反应,各容器中炭足量,其它物质的物质的量浓度及正逆反应速率关系如下表所示。请填写表中相应的空格。
| 容器编号 | c(H2O)/mol·L-1 | c(CO)/mol·L-1 | c(H2)/mol·L-1 | V正、V逆比较 |
| I | 0.06 | 0.60 | 0.10 | V正=V逆 |
| II | 0.06 | 0.50 | 0.40 | |
| III | 0.12 | 0.40 | 0.80 | V正<V逆 |
| IV | 0.12 | 0.30 | V正=V逆 |
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0mol炭和 1.0mo l水蒸气 (H216O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。平衡时水蒸气的转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在密闭容器中,当合成氨的反应N2+3H2 2NH3(正反应是放热反应)达到平衡时,改变如下的一些条件:
2NH3(正反应是放热反应)达到平衡时,改变如下的一些条件:
A.升温 B.加压 C.减压 D.增大c(H2) E.减小c(NH3) F.增大c(NH3)。
若平衡向右移动用“ →”,若平衡向左移动用“←”表示;若值增加用“↑”表示,若值减小用“↓”表示,请根据下表中各项的变化情况,在改变条件栏目中填上相应的编号(每项只改变一个条件)。
 2NH3(正反应是放热反应)达到平衡时,改变如下的一些条件:
2NH3(正反应是放热反应)达到平衡时,改变如下的一些条件:A.升温 B.加压 C.减压 D.增大c(H2) E.减小c(NH3) F.增大c(NH3)。
若平衡向右移动用“ →”,若平衡向左移动用“←”表示;若值增加用“↑”表示,若值减小用“↓”表示,请根据下表中各项的变化情况,在改变条件栏目中填上相应的编号(每项只改变一个条件)。
| 编号 | 改变条件 | 平衡移动方向 | N2的转化率 | c(NH3) | c(N2) | c(H2) |
| ① | → | ↑ | ↓ | ↓ | ↓ | |
| ② | ← | ↓ | ↓ | ↑ | ↑ | |
| ③ | → | ↑ | ↑ | ↓ | ↑ | |
| ④ | ← | ↓ | ↓ | ↓ | ↓ | |
| ⑤ | → | ↑ | ↑ | ↑ | ↑ |
您最近一年使用:0次



