下列有关电解质溶液的叙述中错误的是
A.在T℃时,某溶液中c(H+)=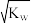 ,则该溶液一定显中性 ,则该溶液一定显中性 |
| B.25℃时,如弱酸与强碱溶液的pH之和等于14,则它们等体积混合液呈酸性 |
| C.常温下,pH相等的NaOH溶液与氨水稀释后保持pH仍然相等,则氨水加水多 |
| D.体积和pH均相等的HCl与CH3COOH溶液分别与足量锌粒反应,放出H2一样多 |
更新时间:2019-01-19 08:30:49
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】有25mL0.1mol•L-1的三种溶液①Na2CO3溶液;②CH3COONa溶液;③NaOH溶液,下列说法正确的是
| 电离平衡常数 | Ka1 | Ka2 |
| H2CO3 | 4.5×10-7 | 4.7×10-11 |
| CH3COOH | 1.75×10-5 | —— |
| A.3种溶液pH的大小顺序是③>②>① |
| B.若将3种溶液稀释相同倍数,pH变化最大的是② |
| C.若分别加入25mL0.1mol•L-1盐酸后,pH最大的是① |
| D.若3种溶液的pH均为9,则物质的量浓度的大小顺序是③>②>① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】羟胺 易溶于水,可看成是
易溶于水,可看成是 中的
中的 被
被 取代的产物,其水溶液是比肼还弱的碱性溶液。下列有关说法正确的是
取代的产物,其水溶液是比肼还弱的碱性溶液。下列有关说法正确的是
 易溶于水,可看成是
易溶于水,可看成是 中的
中的 被
被 取代的产物,其水溶液是比肼还弱的碱性溶液。下列有关说法正确的是
取代的产物,其水溶液是比肼还弱的碱性溶液。下列有关说法正确的是A. 分子稳定性较强是因为分子间含有氢键 分子稳定性较强是因为分子间含有氢键 |
B. 的水溶液显碱性是因为 的水溶液显碱性是因为 溶于水时可电离产生 溶于水时可电离产生 |
C. 与 与 中 中 的键角相同 的键角相同 |
D. 与 与 的中心 的中心 原子的价层电子对数相同 原子的价层电子对数相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
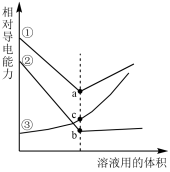
【推荐1】如图所示实验方案不能达到对应实验目的的是


| A.方案①可比较Cu和Ag的金属性强弱 |
| B.方案②可探究室温下醋酸的电离程度 |
| C.方案③可探究浓度对反应速率的影响 |
D.方案④可制备无水 固体 固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】现有常温下体积均为10 mL、 pH=3的两种溶液:① HCl溶液,② CH3COOH溶液。下列说法中,正确的是
| A.溶液中溶质的物质的量浓度:① > ② |
| B.溶液中酸根的物质的量浓度:① = ② |
| C.加水稀释至1 L,溶液的pH:① < ② |
| D.分别加入等浓度NaOH溶液至中性,消耗NaOH的量:① = ② |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】25℃时,将浓度均为0.1mol·L-1,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,且保持 Va+Vb=100mL,Va、Vb 与混合液的 pH 的关系如图所示.下列说法正确的是


| A.Ka(HA)≈1×10-6 |
B.c点时,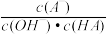 随温度升高而增大 随温度升高而增大 |
| C.a→c过程中水的电离程度始终增大 |
| D.b点时,c(B+)=c(A-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,用0.1mol·L-1的NaOH溶液滴定10mL0.1mol·L-1的H2A溶液,溶液的pH与NaOH溶液体积关系如图所示。下列说法错误的是
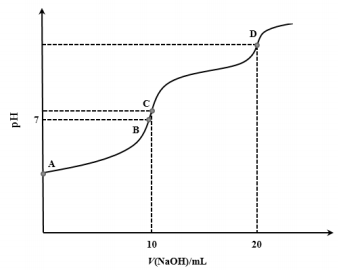

| A.水的电离程度:C>B |
B.向A点溶液中加少量的水: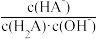 保持不变 保持不变 |
| C.C点:c(Na+)>c(HA-)+2c(A2-) |
| D.D点:2 c(Na+)=c(HA -)+c(H2A)+c(A2-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】25℃时,将浓度均为0.1mol·L-1、体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示。下列说法正确的是
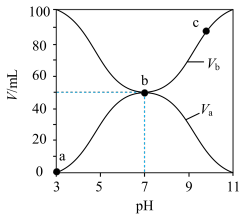

| A.Ka(HA)=1×10-6 |
| B.b点时,水电离出的c(H+)=10-7mo/L |
| C.a→c过程中水的电离程度始终增大 |
D.c点时, 随温度升高而减小 随温度升高而减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列化学用语的表述正确的是
A.NH4Cl的水解常数表达式:K=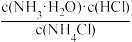 |
B.NaHCO3水解的离子方程式:HCO3-+H2O H3O++CO32- H3O++CO32- |
C.结构示意图为 的阴离子都不能破坏水的电离平衡 的阴离子都不能破坏水的电离平衡 |
D.H2SO3的电离方程式:H2SO3 2H++SO32- 2H++SO32- |
您最近一年使用:0次


 +HCN。以下说法正确的是
+HCN。以下说法正确的是

