常温下,向浓度为0.1 mol·L-1、体积为V L的氨水中逐滴加入一定浓度的盐酸,用pH计测溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。根据图中信息回答下列问题:
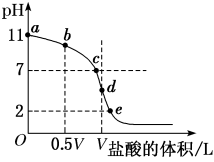
(1)该温度时NH3·H2O的电离常数K=________ 。
(2)滴定过程中所用盐酸的pH=________ 。
(3)比较b、c、d三点时的溶液中,由水电离出的c(OH-)大小顺序为___________ 。(填字母)
(4)滴定时,由b点到c点的过程中,下列各选项中数值变大的是___ (填字母,下同)。
A.c(H+)·c(OH-) B. c(H+)·c(NH3·H2O)/c(NH4+)
C. c(NH4+)·c(OH-)/c(NH3·H2O) D. c(H+)/c(OH-)
(5)根据以上滴定曲线判断下列说法正确的是________ (溶液中N元素只存在NH4+和NH3·H2O两种形式)。
A.点b所示溶液中:c(NH4+)+c(H+)=c(OH-)+c(NH3·H2O)
B.点c所示溶液中:c(Cl-)=c(NH3·H2O)+c(NH4+)
C.点d所示溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.滴定过程中可能有:c(NH3·H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+)
(6)d点之后若继续加入盐酸至图象中的e点(不考虑NH4+水解的影响),则e点对应的横坐标为________ 。

(1)该温度时NH3·H2O的电离常数K=
(2)滴定过程中所用盐酸的pH=
(3)比较b、c、d三点时的溶液中,由水电离出的c(OH-)大小顺序为
(4)滴定时,由b点到c点的过程中,下列各选项中数值变大的是
A.c(H+)·c(OH-) B. c(H+)·c(NH3·H2O)/c(NH4+)
C. c(NH4+)·c(OH-)/c(NH3·H2O) D. c(H+)/c(OH-)
(5)根据以上滴定曲线判断下列说法正确的是
A.点b所示溶液中:c(NH4+)+c(H+)=c(OH-)+c(NH3·H2O)
B.点c所示溶液中:c(Cl-)=c(NH3·H2O)+c(NH4+)
C.点d所示溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.滴定过程中可能有:c(NH3·H2O)>c(NH4+)>c(OH-)>c(Cl-)>c(H+)
(6)d点之后若继续加入盐酸至图象中的e点(不考虑NH4+水解的影响),则e点对应的横坐标为
更新时间:2019-03-25 11:39:07
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知:25℃时,CH3COOH和NH3·H2O的电离常数相等。
(1)25 ℃时,取10mL0.1mol·L-1醋酸溶液测得其pH=3。0.1mol·L-1氨水(NH3·H2O溶液)的pH=___ 。用pH试纸测定该氨水pH的操作方法为_____ 。氨水(NH3·H2O溶液)电离平衡常数表达式Kb=____ ,25℃时,氨水电离平衡常数约为_____ 。
(2)25℃时,现向10mL0.1mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中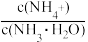
___ (填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1mL0.1mol·L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=-lgc(OH-)。
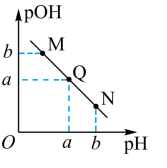
图中M、Q、N三点所示溶液呈中性的点是____ (填字母,下同)。图中M、Q、N三点所示溶液中水的电离程度最大的点是____ 。
(1)25 ℃时,取10mL0.1mol·L-1醋酸溶液测得其pH=3。0.1mol·L-1氨水(NH3·H2O溶液)的pH=
(2)25℃时,现向10mL0.1mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中
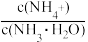
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1mL0.1mol·L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=-lgc(OH-)。

图中M、Q、N三点所示溶液呈中性的点是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)氯化铝水溶液呈___________ 性,原因是(用离子方程式表示):___________ 把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是___________ 。
(2)25℃时,0.5mol•L-1氨水,电离度为0.01,水电离的c(OH-)为___________ ;
(3)25℃时,将c(OH-)=0.2mol•L-1和pH=8的NaOH溶液等体积混合,则混合后溶液的pH=___________ 。
(4)某温度时,纯水电离的c(H+)=10-6mol•L-1,将pH=5的盐酸与pH=8的Ba(OH)2溶液混合,使混合后溶液的pH=7,则盐酸与Ba(OH)2的体积比___________ 。
(1)氯化铝水溶液呈
(2)25℃时,0.5mol•L-1氨水,电离度为0.01,水电离的c(OH-)为
(3)25℃时,将c(OH-)=0.2mol•L-1和pH=8的NaOH溶液等体积混合,则混合后溶液的pH=
(4)某温度时,纯水电离的c(H+)=10-6mol•L-1,将pH=5的盐酸与pH=8的Ba(OH)2溶液混合,使混合后溶液的pH=7,则盐酸与Ba(OH)2的体积比
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.25℃时,三种酸的电离平衡常数如下:
回答下列问题:
(1)一般情况下,当温度升高时,Ka___________ (填“增大”、“减小”或“不变”)。
(2)下列四种离子结合质子能力由大到小的顺序是___________ (填字母)。
a.CO b.ClO- c.CH3COO- d.HCO
b.ClO- c.CH3COO- d.HCO
(3)下列反应不能发生的是___________ (填字母)。
a.2ClO-+CO2+H2O=CO +2HClO
+2HClO
b.ClO-+CH3COOH=CH3COO-+HClO
c.CO +2HClO=CO2↑+H2O+2ClO-
+2HClO=CO2↑+H2O+2ClO-
d.CO +2CH3COOH=2CH3COO-+CO2↑+H2O
+2CH3COOH=2CH3COO-+CO2↑+H2O
(4)用蒸馏水稀释0.10mol·L-1的醋酸,下列各式表示的数值随水量的增加而增大的是___________ 。
a. b.
b. c.
c. d.
d.
(5)体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。则醋酸的电离平衡常数___________ (填“>”、“=”或“<”,下同)HX的电离平衡常数;稀释后,醋酸溶液中水电离出来的c(H+)___________ HX溶液中水电离出来的c(H+);用同浓度的NaOH溶液分别中和上述两种酸溶液,恰好中和时消耗NaOH溶液的体积:醋酸___________ HX。

(6)25℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,则溶液中c(CH3COO-)-c(Na+)=___________ mol·L-1(填精确数值)。
II.下表是不同温度下水的离子积数据:
(7)在t2℃下pH=10的NaOH溶液中,水电离产生的OH-浓度为___________ 。
(8)t2℃下,将pH=11的NaOH溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=___________ 。
| CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | 1.8×10-5 | K1=4.3×10-7K2=5.6×10-11 | 3.0×10-8 |
回答下列问题:
(1)一般情况下,当温度升高时,Ka
(2)下列四种离子结合质子能力由大到小的顺序是
a.CO
 b.ClO- c.CH3COO- d.HCO
b.ClO- c.CH3COO- d.HCO
(3)下列反应不能发生的是
a.2ClO-+CO2+H2O=CO
 +2HClO
+2HClOb.ClO-+CH3COOH=CH3COO-+HClO
c.CO
 +2HClO=CO2↑+H2O+2ClO-
+2HClO=CO2↑+H2O+2ClO-d.CO
 +2CH3COOH=2CH3COO-+CO2↑+H2O
+2CH3COOH=2CH3COO-+CO2↑+H2O(4)用蒸馏水稀释0.10mol·L-1的醋酸,下列各式表示的数值随水量的增加而增大的是
a.
 b.
b. c.
c. d.
d.
(5)体积均为10mL、pH均为2的醋酸溶液与HX溶液分别加水稀释至1000mL,稀释过程中pH变化如图所示。则醋酸的电离平衡常数

(6)25℃时,若测得CH3COOH与CH3COONa的混合溶液的pH=6,则溶液中c(CH3COO-)-c(Na+)=
II.下表是不同温度下水的离子积数据:
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积KW | 1×10-14 | a | 1×10-12 |
(8)t2℃下,将pH=11的NaOH溶液V1L与pH=1的稀硫酸V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1:V2=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡,请根据所学知识回答:
(1)某温度下,纯水中的c(H+)=1.5×10-7,该温度时的水的离子积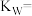
___________ 。保持温度不变,滴入稀盐酸使溶液中的 ,则溶液中的
,则溶液中的
___________  。
。
(2)常温下,一定浓度的CH3COONa溶液的pH=8,已知CH3COOH的电离平衡常数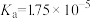 ,则该CH3COONa溶液中:
,则该CH3COONa溶液中: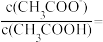
___________ 。
(3)甲酸钠(HCOONa)溶液呈碱性的原因是___________ (用离子方程式表示)。0.02mol/L的HCOONa溶液中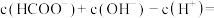
___________ mol/L。
(4)25℃,在0.10mol•L1硫酸铜溶液中加入氢氧化钠稀溶液充分反应,有蓝色氢氧化铜沉淀生成,当溶液的pH=9时,c(Cu2+)=___________ molL1(Ksp[Cu(OH)2]=2.2×1020)。
(1)某温度下,纯水中的c(H+)=1.5×10-7,该温度时的水的离子积
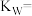
 ,则溶液中的
,则溶液中的
 。
。(2)常温下,一定浓度的CH3COONa溶液的pH=8,已知CH3COOH的电离平衡常数
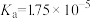 ,则该CH3COONa溶液中:
,则该CH3COONa溶液中: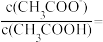
(3)甲酸钠(HCOONa)溶液呈碱性的原因是
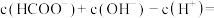
(4)25℃,在0.10mol•L1硫酸铜溶液中加入氢氧化钠稀溶液充分反应,有蓝色氢氧化铜沉淀生成,当溶液的pH=9时,c(Cu2+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硫化氢气体是一种剧毒气体,易溶于水形成酸性溶液。查阅得,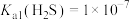 ,
, ;
;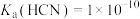 。按所给信息回答下列问题。
。按所给信息回答下列问题。
(1)书写 第二步电离方程式:
第二步电离方程式:_______ 。
(2)向 的
的 溶液中加入等浓度的
溶液中加入等浓度的 时,电离平衡向
时,电离平衡向_______ 移动(填“左”或“右”),混合溶液中
_______ 。(填“增大”、“减小”或“不变”)
(3)能证明 酸性强于
酸性强于 的是:_______。
的是:_______。
(4)下列反应不能发生的是_______ (填字母)。
a. b.
b.
c. d.
d.
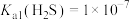 ,
, ;
;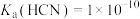 。按所给信息回答下列问题。
。按所给信息回答下列问题。(1)书写
 第二步电离方程式:
第二步电离方程式:(2)向
 的
的 溶液中加入等浓度的
溶液中加入等浓度的 时,电离平衡向
时,电离平衡向
(3)能证明
 酸性强于
酸性强于 的是:_______。
的是:_______。A.相同温度下,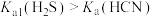 |
| B.溶液能使紫色石蕊试液变红 |
C.等浓度、等体积的 溶液和 溶液和 溶液分别与等浓度的 溶液分别与等浓度的 溶液反应, 溶液反应, 消耗的 消耗的 溶液体积更多 溶液体积更多 |
D.常温下,将 气体通入 气体通入 溶液有 溶液有 生成 生成 |
a.
 b.
b.
c.
 d.
d.
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列有关问题
(1)KW的数学表达式是KW =__________ ,温度升高KW的变化情况是______ (选填“变大”“变小”或“不变”)。
(2)K通常表示化学平衡常数,K值越大表示该反应进行程度越________ ,对于反应2NO2(g)  N2O4(g),其化学平衡常数K的数学表达式为K=[N2O4]/[NO2]2,式中[NO2]2表示的意义是
N2O4(g),其化学平衡常数K的数学表达式为K=[N2O4]/[NO2]2,式中[NO2]2表示的意义是_______________ 。
(3)Kα通常表示弱酸的电离平衡常数,Kα值越大表示该弱酸的酸性_______ ,对于某一元弱酸,当用蒸馏水稀释该酸时,溶液越稀,Kα的变化情况是________ (选填“变大”“变小”或“不变”)
(4)Ksp表示难溶物的溶度积常数,该常数越大表示难溶物在水中的__________ 。
(5)实验室可用NaOH溶液吸收NO2 ,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O.含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1mol/L的CH3COONa溶液,则两溶液中c(NO3-)、c(NO2-) 和c(CH3COO-) 由大到小的顺序为_____________ 。(已知HNO2的电离常数Ka=7.1×10−4 mol/L,CH3COOH的电离常数为:Ka=1.7×10−5 mol/L),可使溶液A和溶液B的pH相等的方法是_____________ 。
A.向溶液A中加适量水 B.向溶液A中加适量NaOH
C.向溶液B中加适量水 D.向溶液B中加适量NaOH.
(1)KW的数学表达式是KW =
(2)K通常表示化学平衡常数,K值越大表示该反应进行程度越
 N2O4(g),其化学平衡常数K的数学表达式为K=[N2O4]/[NO2]2,式中[NO2]2表示的意义是
N2O4(g),其化学平衡常数K的数学表达式为K=[N2O4]/[NO2]2,式中[NO2]2表示的意义是(3)Kα通常表示弱酸的电离平衡常数,Kα值越大表示该弱酸的酸性
(4)Ksp表示难溶物的溶度积常数,该常数越大表示难溶物在水中的
(5)实验室可用NaOH溶液吸收NO2 ,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O.含0.2mol NaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.1mol/L的CH3COONa溶液,则两溶液中c(NO3-)、c(NO2-) 和c(CH3COO-) 由大到小的顺序为
A.向溶液A中加适量水 B.向溶液A中加适量NaOH
C.向溶液B中加适量水 D.向溶液B中加适量NaOH.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】电解质在水溶液中存在各种行为,如电离、水解等,根据所学知识回答:
(1)下列事实一定能证明HNO2是弱电解质的是___________ (填序号)
①向HNO2中加入NaNO2固体后pH增大;
②用HNO2溶液做导电实验,灯泡很暗;
③HNO2和NaCl不能发生反应;
④0.1mol/L HNO2溶液的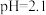 ;
;
⑤NaNO2和H3PO4反应,生成HNO2
(2)t℃时,纯水中c(H+)=1×10-6mol/L,则t℃___________ 25℃(填“>”、“<”或“=”)。
(3)Al2(SO4)3溶液呈___________ 性(填“酸”、“碱”或“中”),原因是(用离子方程式表示):___________
(4)随着“碳达峰”限期的日益临近,捕集CO2后再利用成为环境科学的研究热点。海洋吸收CO2的能力巨大,若室温下测得某地海水的pH≈8,在该溶液中c( )∶c(
)∶c( )=
)=___________ (已知室温下H2CO3的Ka1=4×10-7,Ka2=5×10-11)。
(5)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2。下表是25℃时几种常见弱酸的电离平衡常数
①常温下,物质的量浓度均为0.10mol/L的NaClO2、NaF、NaCN、Na2S四种溶液的pH由大到小的顺序为___________ 。(用化学式表示)
②少量H2S与KCN溶液反应的离子反应方程式:___________ 。
③常温下,CH3COOH和CH3COONa混合溶液中,若溶液pH=6,则溶液中c(CH3COO-)-c(Na+)=___________ mol/L(填精确值)。
(1)下列事实一定能证明HNO2是弱电解质的是
①向HNO2中加入NaNO2固体后pH增大;
②用HNO2溶液做导电实验,灯泡很暗;
③HNO2和NaCl不能发生反应;
④0.1mol/L HNO2溶液的
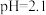 ;
;⑤NaNO2和H3PO4反应,生成HNO2
(2)t℃时,纯水中c(H+)=1×10-6mol/L,则t℃
(3)Al2(SO4)3溶液呈
(4)随着“碳达峰”限期的日益临近,捕集CO2后再利用成为环境科学的研究热点。海洋吸收CO2的能力巨大,若室温下测得某地海水的pH≈8,在该溶液中c(
 )∶c(
)∶c( )=
)=(5)印染工业常用亚氯酸钠(NaClO2)漂白织物,漂白织物时真正起作用的是HClO2。下表是25℃时几种常见弱酸的电离平衡常数
| 弱酸 | HClO2 | HF | HCN | H2S |
| Ka | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10-8 K2=1.1×10-15 |
①常温下,物质的量浓度均为0.10mol/L的NaClO2、NaF、NaCN、Na2S四种溶液的pH由大到小的顺序为
②少量H2S与KCN溶液反应的离子反应方程式:
③常温下,CH3COOH和CH3COONa混合溶液中,若溶液pH=6,则溶液中c(CH3COO-)-c(Na+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】常温下,取 溶液与
溶液与 溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的
溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的 ,试回答以下问题:
,试回答以下问题:
(1)混合溶液中由水电离出的c(H+)______  溶液中由水电离出的
溶液中由水电离出的 (填“
(填“ 、
、 或
或 ”)。
”)。
(2)求出混合物中下列算式的精确计算结果(填具体数字):c(Cl-)-c(M+)=______ 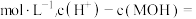
______ mol/L。
(3)若常温下取 溶液与
溶液与 溶液等体积混合,测得混合溶液的pH
溶液等体积混合,测得混合溶液的pH ,说明
,说明 的电离程度
的电离程度_______ (填“ 、
、 或
或 ”)
”) 的水解程度。溶液中各离子浓度由大到小的顺序为
的水解程度。溶液中各离子浓度由大到小的顺序为_______ 。
(4)若常温下 的盐酸与
的盐酸与 的氨水溶液等体积混合,则混合溶液的pH
的氨水溶液等体积混合,则混合溶液的pH_____ 7填(“ 、
、 或
或 ”)。
”)。
 溶液与
溶液与 溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的
溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的 ,试回答以下问题:
,试回答以下问题:(1)混合溶液中由水电离出的c(H+)
 溶液中由水电离出的
溶液中由水电离出的 (填“
(填“ 、
、 或
或 ”)。
”)。(2)求出混合物中下列算式的精确计算结果(填具体数字):c(Cl-)-c(M+)=
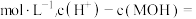
(3)若常温下取
 溶液与
溶液与 溶液等体积混合,测得混合溶液的pH
溶液等体积混合,测得混合溶液的pH ,说明
,说明 的电离程度
的电离程度 、
、 或
或 ”)
”) 的水解程度。溶液中各离子浓度由大到小的顺序为
的水解程度。溶液中各离子浓度由大到小的顺序为(4)若常温下
 的盐酸与
的盐酸与 的氨水溶液等体积混合,则混合溶液的pH
的氨水溶液等体积混合,则混合溶液的pH 、
、 或
或 ”)。
”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)100°C时,KW=1.0×10-12,在该温度下,测得0.1mol/L Na2A溶液pH=6。
①H2A在水溶液中的电离方程式为_____ ;
②体积相等pH=1的盐酸与H2A溶液分别与足量的Zn反应,H2A溶液产生的H2_____ (填“多”、“少”或“一样多”)。
(2)将0.4mol/L HA溶液与0.2mol/L NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-):
①混合溶液中c(A)_____ c(HA)(填“>”、“<”或“=”,下同);
②混合溶液中c(HA)+c(A)_____ 0.2mol/L。
(3)已知在常温下测得浓度均为0.1mol/L的下列5种溶液的pH,如表所示:
①少量二氧化碳通入NaClO溶液中的离子方程式_____ ;
②浓度均为0.01mol/L的下列4种物质的溶液分别加水稀释100倍,pH变化最小的是_____ (填编号);
a.CH3COOH b.HCN c.HClO d.H2CO3
③常温下浓度相同的醋酸和醋酸钠混合液pH=6,则c(CH3COO-)-c(CH3COOH)=_____ mol/L(填准确数值)。
①H2A在水溶液中的电离方程式为
②体积相等pH=1的盐酸与H2A溶液分别与足量的Zn反应,H2A溶液产生的H2
(2)将0.4mol/L HA溶液与0.2mol/L NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-):
①混合溶液中c(A)
②混合溶液中c(HA)+c(A)
(3)已知在常温下测得浓度均为0.1mol/L的下列5种溶液的pH,如表所示:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①少量二氧化碳通入NaClO溶液中的离子方程式
②浓度均为0.01mol/L的下列4种物质的溶液分别加水稀释100倍,pH变化最小的是
a.CH3COOH b.HCN c.HClO d.H2CO3
③常温下浓度相同的醋酸和醋酸钠混合液pH=6,则c(CH3COO-)-c(CH3COOH)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知25℃时部分弱电解质的电离平衡常数数据如表所示:
回答下列问题:
(1)物质的量浓度均为0.1mol·L-1的四种溶液:
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
pH由小到大排列的顺序是________ (用字母编号填写)。
(2)常温下,0.1mol·L-1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是___ (填字母)。
A.c(H+)
B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH-)
D.c(OH-)/c(H+)
E.c(H+)·c(CH3COO-)/c(CH3COOH)
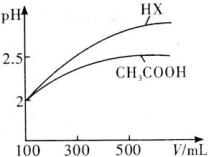
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数________ (填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
(4)标准状况下,将1.12L CO2通入100mL 1mol·L-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:
①c(OH-)=2c(H2CO3)+________ ;
②c(H+)+c(Na+)=________ 。
(5)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=________ mol·L-1(填精确值)。
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
(1)物质的量浓度均为0.1mol·L-1的四种溶液:
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
pH由小到大排列的顺序是
(2)常温下,0.1mol·L-1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.c(H+)
B.c(H+)/c(CH3COOH)
C.c(H+)·c(OH-)
D.c(OH-)/c(H+)
E.c(H+)·c(CH3COO-)/c(CH3COOH)
(3)体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数

(4)标准状况下,将1.12L CO2通入100mL 1mol·L-1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:
①c(OH-)=2c(H2CO3)+
②c(H+)+c(Na+)=
(5)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】将氨气通入水中可制得氨水,也可与酸化合制得铵盐。
(1)写出一水合氨电离平衡常数的表达式___________ 。室温下 的氨水溶液在加水稀释过程中,电离平衡常数
的氨水溶液在加水稀释过程中,电离平衡常数___________ (选填“变大”“变小”或“不变”,下同),
___________ 。
(2)氯化铵溶液中加入镁粉能放出氢气和氨气,请运用平衡移动原理解释该现象产生的原因___________ 。
(3)在25℃时,浓度均为 的
的 、
、 、
、 溶液中,铵根离子浓度由大到小的顺序是
溶液中,铵根离子浓度由大到小的顺序是___________ (填化学式)。
(1)写出一水合氨电离平衡常数的表达式
 的氨水溶液在加水稀释过程中,电离平衡常数
的氨水溶液在加水稀释过程中,电离平衡常数
(2)氯化铵溶液中加入镁粉能放出氢气和氨气,请运用平衡移动原理解释该现象产生的原因
(3)在25℃时,浓度均为
 的
的 、
、 、
、 溶液中,铵根离子浓度由大到小的顺序是
溶液中,铵根离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
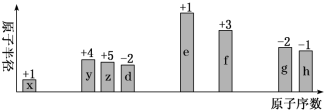
根据判断出的元素回答问题:
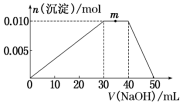
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:
(1)R溶液中,离子浓度由大到小的顺序是___________________________________
(2)写出m点反应的离子方程式:__________________________________________ 。
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为________ mol。

根据判断出的元素回答问题:
上述元素可组成盐R:zx4f(gd4)2。向盛有10mL 1mol·L-1R溶液的烧杯中滴加1mol·L-1NaOH溶液,沉淀物质的量随NaOH溶液体积的变化示意图如下:

(1)R溶液中,离子浓度由大到小的顺序是
(2)写出m点反应的离子方程式:
(3)若在R溶液中改加20mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次



