向0.5L 0.4mol/L的NaClO溶液中缓慢通入0.1mol CO2根据下面表格提供的数据,下列判断不正确的是
| 化学式 | 电离常数 |
| HClO | K1=3×10-8 |
| H2CO3 | K1=4.33×10-7 |
| K2=5.6×10-11 |
| A.原溶液中:c(ClO-)> c(OH-)>c(H+) |
| B.原溶液中:c(OH-)=c(H+)+ c(HClO) |
| C.反应后溶液中:c(HClO)>c(HCO3-)>c(ClO-)>c(CO32-) |
| D.反应后溶液中:c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)+c(ClO-)+c(HClO) |
16-17高三下·上海·阶段练习 查看更多[1]
(已下线)上海市同济中学2017届高三3月月考化学试题
更新时间:2019-10-27 08:44:11
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列事实中能证明 是弱电解质的有几项
是弱电解质的有几项
①常温下, 的氨水中
的氨水中
② 的氨水与
的氨水与 的盐酸恰好完全反应
的盐酸恰好完全反应
③常温下,5mL 的浓氨水中加水至5000mL,
的浓氨水中加水至5000mL,
④用氨水做导电实验,灯泡很暗
 是弱电解质的有几项
是弱电解质的有几项①常温下,
 的氨水中
的氨水中
②
 的氨水与
的氨水与 的盐酸恰好完全反应
的盐酸恰好完全反应③常温下,5mL
 的浓氨水中加水至5000mL,
的浓氨水中加水至5000mL,
④用氨水做导电实验,灯泡很暗
| A.4项 | B.3项 | C.2项 | D.1项 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向醋酸溶液中滴加NaOH溶液,则
| A.醋酸的电离平衡向左移动 | B.溶液的pH减小 |
| C.醋酸的浓度减小 | D.醋酸根离子的物质的量减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】常温下,向某浓度的 溶液中逐滴加入某浓度的KOH溶液,测得溶液中
溶液中逐滴加入某浓度的KOH溶液,测得溶液中 、
、 、
、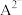 三种微粒的物质的量分数
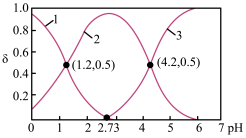
三种微粒的物质的量分数 与溶液pH的关系如图所示。下列说法不正确的是
与溶液pH的关系如图所示。下列说法不正确的是
 溶液中逐滴加入某浓度的KOH溶液,测得溶液中
溶液中逐滴加入某浓度的KOH溶液,测得溶液中 、
、 、
、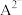 三种微粒的物质的量分数
三种微粒的物质的量分数 与溶液pH的关系如图所示。下列说法不正确的是
与溶液pH的关系如图所示。下列说法不正确的是
A.曲线1代表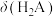 ,曲线3代表 ,曲线3代表 |
B. 的第一步电离常数 的第一步电离常数 |
| C.KHA溶液呈碱性 |
D. 时,溶液中 时,溶液中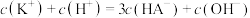 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一般较强酸可制取较弱酸,这是复分解反应的规律之一。已知在常温下测得浓度均为0.1mol/L的下列 3 种溶液的 pH:
下列有关说法正确的是( )
| 溶质 | NaHCO3 | Na2CO3 | NaClO |
| pH | 8.34 | 11.6 | 10.3 |
下列有关说法正确的是( )
| A.以上溶液的 pH 是用广泛 pH 试纸测定的 |
| B.反应CO2+H2O+2NaClO=Na2CO3+2HClO可以发生 |
| C.室温下,电离常数: K2(H2CO3)>K(HClO) |
| D.在新制氯水中加入少量 NaHCO3固体可以提高溶液中 HClO 的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法错误的是
A.将 的 的 溶液加水稀释, 溶液加水稀释, 变大 变大 |
B.常温下,向氨水溶液中滴入 溶液至 溶液至 时: 时: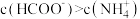 |
C. 的 的 溶液的 溶液的 约为8,该溶液中有 约为8,该溶液中有 |
D.等物质的量浓度的 与 与 混合溶液: 混合溶液: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大.以下是某温度下这四种酸在冰醋酸中的电离常数:
从以上表格中判断以下说明不正确的是
| 酸 | HClO4 | H2SO4 | HCl | HNO3 | |
| Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
| A.在冰醋酸中,高氯酸的酸性最强 |
| B.水对于这四种酸的强弱没有区分能力,但醋酸可以区分这四种酸的强弱 |
| C.在冰醋酸中1mol/L的高氯酸的电离度约为0.4% |
| D.在冰醋酸中硫酸的电离方程式为:H2SO4═2H++SO42- |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】SO2的烟气会形成酸雨,工业上常利用Na2SO3溶液作为吸收液脱除烟气中的SO2。随着SO2的吸收,吸收液的pH不断变化。下列粒子浓度关系一定正确的是
A.Na2SO3溶液中存在:c(Na+)>c(SO )>c(H2SO3)>c(HSO )>c(H2SO3)>c(HSO ) ) |
B.已知NaHSO3溶液pH<7,该溶液中:c(Na+)>c(HSO )>c(H2SO3) >c(SO )>c(H2SO3) >c(SO ) ) |
C.当吸收液呈中性时:c(Na+)=2 c(SO )+c(HSO )+c(HSO ) ) |
D.当吸收液呈酸性时:c(Na+)=c(SO )+c(HSO )+c(HSO )+c(H2SO3) )+c(H2SO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,下列各组离子在指定溶液中一定能大量共存的是
A.加入铝粉能放出氢气的溶液:Na+、Mg2+、Cl-、 |
B.由水电离出的c(OH-)=1.0×10-12mol·L-1的溶液:Fe2+、 、ClO-、 、ClO-、 |
C. =1.0×10-12的溶液:K+、 =1.0×10-12的溶液:K+、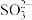 、S2-、Cl- 、S2-、Cl- |
D.c(NH )=c(Cl-)的NH4Cl-NH3·H2O混合液:Al3+、Fe3+、 )=c(Cl-)的NH4Cl-NH3·H2O混合液:Al3+、Fe3+、 、 、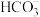 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A.pH=1的NaHSO4溶液:c(H+)=c( )+c(OH-) )+c(OH-) |
B.0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7):c(NH3·H2O)>c( )>c(Cl-)>c(OH-) )>c(Cl-)>c(OH-) |
C.0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c( )+c( )+c( )+c(OH-)=c(Na+)+c(H+) )+c(OH-)=c(Na+)+c(H+) |
D.0.1mol/LNa2CO3与0.1mol/LNaHCO3溶液等体积混合:3c(Na+)=2[c( )+c( )+c( )+c(H2CO3)] )+c(H2CO3)] |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在25mL 0.1mol/L NaOH溶液中逐滴加入0.2mol/L CH3COOH溶液,曲线如图所示,下列有关离子浓度关系的比较,正确的是


| A.在A、B间任一点,溶液中一定都有c(Na+)>c(CH3COO—)>c(OH—)>c(H+) |
| B.在B点,a>12.5,且有c(Na+)=c(CH3COO—)=c(OH—)=c(H+) |
| C.在C点: c(Na+)> c(CH3COO—) > c(OH—)>c(H+) |
| D.在D点:c(CH3COO—)+ c(CH3COOH)=2 c(Na+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列关于电解质溶液的叙述正确的是
A.常温下电离常数为Ka的酸HA溶液中c(H+)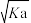 mol·L-1 mol·L-1 |
| B.向0.1 mol·L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3·H2O)增大 |
| C.0.2 mol·L-1CH3COOH溶液与0.1 mol·L-1NaOH溶液等体积混合 2c(H+)-2 c(OH-)=c(CH3COO-)- c(CH3COOH) |
| D.将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]大于Ksp(CaSO4) |
您最近一年使用:0次

 是一种一元弱酸,
是一种一元弱酸, 时,在
时,在 溶液中滴加
溶液中滴加 氢氧化钠溶液
氢氧化钠溶液 ,混合溶液的
,混合溶液的 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是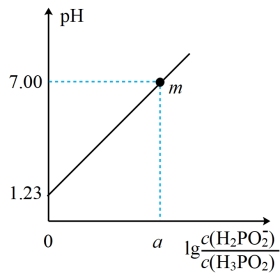


 的数量级为
的数量级为
 时,溶液中存在关系:
时,溶液中存在关系:


