工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g) CH3OH(g)△H
CH3OH(g)△H
(1)该反应的平衡常数表达式为_______ ;
(2)如表所列数据是反应在不同温度下的化学平衡常数(K)
①由表中数据判断该反应的△H______ 0(填“>”、“=”或“<”);
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应10s后达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为____ ,用H2表示反应速率为_____ ,此时的温度为______ ;
(3)要提高CO的转化率,可以采取的措施是______ ;
a.升温 b.加入催化剂 c.增加CO的浓度
d.恒容充入H2 e.恒压充入惰性气体 f.分离出甲醇
 CH3OH(g)△H
CH3OH(g)△H(1)该反应的平衡常数表达式为
(2)如表所列数据是反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
①由表中数据判断该反应的△H
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应10s后达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为
(3)要提高CO的转化率,可以采取的措施是
a.升温 b.加入催化剂 c.增加CO的浓度
d.恒容充入H2 e.恒压充入惰性气体 f.分离出甲醇
更新时间:2019-11-18 09:13:14
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】反应SO2(g)+NO2(g)  SO3(g)+NO(g),若在一定温度下,将物质的量浓度均为2 mol·L-1的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%。则在该温度下:
SO3(g)+NO(g),若在一定温度下,将物质的量浓度均为2 mol·L-1的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%。则在该温度下:
(1)该反应达到平衡状态的标志是___________
A.SO3(g)的生成速率等于SO2(g)的消耗速率
B.混合物的物质的量不再发生变化
C.混合气体的平均摩尔质量不再发生变化
D.混合气体的压强不再发生变化
E.各组分的物质的量分数不再发生变化
(2)此反应在该温度下的平衡常数为___________ 。
(3)在上述温度下,若SO2(g)的初始浓度增大到3 mol·L-1,NO2(g)的初始浓度仍为2 mol·L-1,达到化学平衡状态时,计算下列各物质的平衡浓度及SO2和NO2的平衡转化率。
①c(SO3) =___________ mol·L-1,c(SO2)=___________ mol·L-1。
②SO2的转化率为___________ , NO2的转化率为___________ 。
(4)反应SO2(g)+NO2(g) NO(g)+SO3(g)在一定条件下建立平衡,再加入一定量的O2,下列说法正确的是 ___________ 。
NO(g)+SO3(g)在一定条件下建立平衡,再加入一定量的O2,下列说法正确的是 ___________ 。
①平衡左移,容器内压强不一定增大 ②平衡右移,平衡时容器内压强不一定增大 ③平衡不一定移动,容器内压强一定增大 ④平衡右移,SO2转化率提高
 SO3(g)+NO(g),若在一定温度下,将物质的量浓度均为2 mol·L-1的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%。则在该温度下:
SO3(g)+NO(g),若在一定温度下,将物质的量浓度均为2 mol·L-1的SO2(g)和NO2(g)注入一密闭容器中,当达到平衡状态时,测得容器中SO2(g)的转化率为50%。则在该温度下:(1)该反应达到平衡状态的标志是
A.SO3(g)的生成速率等于SO2(g)的消耗速率
B.混合物的物质的量不再发生变化
C.混合气体的平均摩尔质量不再发生变化
D.混合气体的压强不再发生变化
E.各组分的物质的量分数不再发生变化
(2)此反应在该温度下的平衡常数为
(3)在上述温度下,若SO2(g)的初始浓度增大到3 mol·L-1,NO2(g)的初始浓度仍为2 mol·L-1,达到化学平衡状态时,计算下列各物质的平衡浓度及SO2和NO2的平衡转化率。
①c(SO3) =
②SO2的转化率为
(4)反应SO2(g)+NO2(g)
 NO(g)+SO3(g)在一定条件下建立平衡,再加入一定量的O2,下列说法正确的是 ___________ 。
NO(g)+SO3(g)在一定条件下建立平衡,再加入一定量的O2,下列说法正确的是 ___________ 。①平衡左移,容器内压强不一定增大 ②平衡右移,平衡时容器内压强不一定增大 ③平衡不一定移动,容器内压强一定增大 ④平衡右移,SO2转化率提高
| A.①② | B.②③ | C.③④ | D.②④ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】认识化学反应的快慢和限度规律及影响因素,通过调控更好地满足工农业生产和日常生活的实际需要。
Ⅰ.根据所学知识,完成下列各题:
(1)决定化学反应速率的内在因素是_______。
(2)下列过程中,需要加快反应速率的是_______。
Ⅱ.用相同质量的锌片和铜粉跟相同浓度的足量的稀盐酸反应,得到的实验数据如下表所示:
(3)实验①和②表明_______ ,化学反应速率越快。
(4)能表明固体的表面积对反应速率有影响的实验编号是_______ 。
(5)该实验的目的是探究_______ 等因素对锌和稀盐酸反应速率的影响。
(6)请设计一个实验方案探究盐酸的浓度对反应速率的影响。_______
(7)对于2HBr(g) H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。
H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。
(8)对于平衡体系:FeCl3+3KSCN Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)
Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)
Ⅲ.牙齿表面被一层坚硬的名叫羟基磷酸钙的物质保护着,该物质的组成为Ca5(PO4)3OH,它在唾液中存在下列平衡:Ca5(PO4)3OH(s) 5Ca2+(aq)+3
5Ca2+(aq)+3 (aq)+OH-(aq)
(aq)+OH-(aq)
(9)口腔中的细菌和酶在消化分解食物时,会产生有机酸,从而使羟基磷酸钙溶解。若不及时处理,最终会使牙齿产生蛀洞。适用化学平衡知识解释酸使羟基磷酸钙溶解的原因。_______
Ⅰ.根据所学知识,完成下列各题:
(1)决定化学反应速率的内在因素是_______。
| A.温度和压强 | B.反应物的浓度 |
| C.反应物自身的性质 | D.催化剂 |
| A.钢铁腐蚀 | B.食物腐败 | C.炼钢 | D.塑料老化 |
Ⅱ.用相同质量的锌片和铜粉跟相同浓度的足量的稀盐酸反应,得到的实验数据如下表所示:
| 实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气所需时间/s |
| ① | 薄片 | 15 | 200 |
| ② | 薄片 | 25 | 90 |
| ③ | 粉末 | 25 | 10 |
(4)能表明固体的表面积对反应速率有影响的实验编号是
(5)该实验的目的是探究
(6)请设计一个实验方案探究盐酸的浓度对反应速率的影响。
(7)对于2HBr(g)
 H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。
H2(g)+Br2(g)反应,下列四个图中可以表示该反应在一定条件下为可逆反应的是_______。A. | B. | C. | D. |
 Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)
Fe(SCN)3+3KCl,下列描述正确的是_______。(多选)| A.其他条件不变,增大FeCl3溶液浓度,溶液的血红色加深 |
| B.其他条件不变,增大KSCN溶液的浓度,平衡正向移动 |
| C.其他条件不变,加入一定量的KCl固体,平衡逆向移动,溶液颜色变浅 |
| D.其他条件不变,加入少量的铁粉,振荡,溶液颜色变浅 |
Ⅲ.牙齿表面被一层坚硬的名叫羟基磷酸钙的物质保护着,该物质的组成为Ca5(PO4)3OH,它在唾液中存在下列平衡:Ca5(PO4)3OH(s)
 5Ca2+(aq)+3
5Ca2+(aq)+3 (aq)+OH-(aq)
(aq)+OH-(aq)(9)口腔中的细菌和酶在消化分解食物时,会产生有机酸,从而使羟基磷酸钙溶解。若不及时处理,最终会使牙齿产生蛀洞。适用化学平衡知识解释酸使羟基磷酸钙溶解的原因。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】氯碱工业中电解饱和食盐水的原理示意图如右图所示。

(1)电极b是电源的_________ ;
(2)溶液A的溶质是(填化学式)_________ ;
(3)电解饱和食盐水的化学方程式是_______________________ 。
(4)电解时用盐酸控制阳极区溶液的pH在2~3。用化学平衡移动原理解释盐酸的作用:________________________________________________________________________________ 。
(5)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mol Cl2参与反应时释
放出145kJ热量,写出该反应的热化学方程:________________________ 。

(1)电极b是电源的
(2)溶液A的溶质是(填化学式)
(3)电解饱和食盐水的化学方程式是
(4)电解时用盐酸控制阳极区溶液的pH在2~3。用化学平衡移动原理解释盐酸的作用:
(5)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1mol Cl2参与反应时释
放出145kJ热量,写出该反应的热化学方程:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】自然界的矿物、岩石的成因和变化受到许多条件的影响。地壳内每加深1km,压强增大约25000~30000 kPa。在地壳内SiO2和HF存在以下平衡:SiO2(s) +4HF(g) SiF4(g)+ 2H2O(g)△H =-148.9 kJ·mol-1。
SiF4(g)+ 2H2O(g)△H =-148.9 kJ·mol-1。
根据题意完成下列填空:
(1)在地壳深处容易有________ 气体逸出,在地壳浅处容易有________ 沉积。
(2)如果上述反应的平衡常数K值变大,该反应________ (选填编号)。
a.一定向正反应方向移动b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动d.在平衡移动时逆反应速率先减小后增大
(3)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为___________ 。
 SiF4(g)+ 2H2O(g)△H =-148.9 kJ·mol-1。
SiF4(g)+ 2H2O(g)△H =-148.9 kJ·mol-1。根据题意完成下列填空:
(1)在地壳深处容易有
(2)如果上述反应的平衡常数K值变大,该反应
a.一定向正反应方向移动b.在平衡移动时正反应速率先增大后减小
c.一定向逆反应方向移动d.在平衡移动时逆反应速率先减小后增大
(3)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硫酸工业中通过下列反应使SO2氧化成SO3: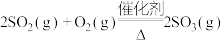
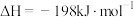 。已知制SO3过程中催化剂是V2O5,它在400~500℃时催化效果最好。
。已知制SO3过程中催化剂是V2O5,它在400~500℃时催化效果最好。
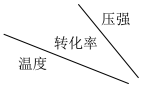
下表为不同温度和压强下SO2的转化率(%):
(1)根据化学原理综合分析,从化学反应速率和原料转化率角度分析,生产中应采取的条件是___________ 。
(2)实际生产中,选定400~500℃作为操作温度,其原因是___________ 。
(3)实际生产中,采用的压强为常压,其原因是___________ 。
(4)在生产中,通入过量空气的目的是___________ 。
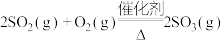
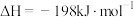 。已知制SO3过程中催化剂是V2O5,它在400~500℃时催化效果最好。
。已知制SO3过程中催化剂是V2O5,它在400~500℃时催化效果最好。下表为不同温度和压强下SO2的转化率(%):
 |  | 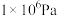 | 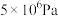 | 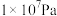 |
| 450℃ | 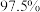 | 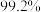 |  | 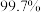 |
| 550℃ |  | 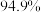 | 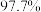 |  |
(1)根据化学原理综合分析,从化学反应速率和原料转化率角度分析,生产中应采取的条件是
(2)实际生产中,选定400~500℃作为操作温度,其原因是
(3)实际生产中,采用的压强为常压,其原因是
(4)在生产中,通入过量空气的目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有反应mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则
(1)该反应的逆反应是________ 热反应,且m+n______ (填“>”“<”或“=”)p。
(2)减压时,A的质量分数________ (填“增大”“减小”或“不变”,下同)。
(3)若加入B(体积不变),则A的转化率________ ,B的转化率________ 。
(4)若升高温度,则平衡时,B、C的浓度之比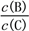 将
将________ 。
 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数减小,则(1)该反应的逆反应是
(2)减压时,A的质量分数
(3)若加入B(体积不变),则A的转化率
(4)若升高温度,则平衡时,B、C的浓度之比
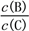 将
将
您最近一年使用:0次
【推荐1】有可逆反应Fe(s)+CO2(g) FeO(s) +CO(g),已知在温度938 K时,平衡常数K=1.5,在1173 K时,K=2.2 。请回答下列问题:
FeO(s) +CO(g),已知在温度938 K时,平衡常数K=1.5,在1173 K时,K=2.2 。请回答下列问题:
(1)能判断该反应达到平衡状态的依据是___________(填字母标号)。
(2)写出该反应的平衡常数表达式________ 。若起始时把Fe和CO2放入体积固定的密闭容器中,CO2的起始浓度为2.0 mol·L-1,某温度时达到平衡,此时容器中CO的浓度为1.0 mol·L-1,则该温度下上述反应的平衡常数K=_____ (保留二位有效数字)。
(3)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,如果改变下列条件,反应混合气体中CO2的物质的量分数如何变化(选填“增大”、“减小”、“不变”)。
①加入催化剂__________ 。
②再通入CO___________ 。
(4)下图描述的是该反应在甲,乙两个容器进行反应时CO2的转化率变化情况。

请问甲乙容器中必定不同的反应条件是什么?___________ 。
 FeO(s) +CO(g),已知在温度938 K时,平衡常数K=1.5,在1173 K时,K=2.2 。请回答下列问题:
FeO(s) +CO(g),已知在温度938 K时,平衡常数K=1.5,在1173 K时,K=2.2 。请回答下列问题:(1)能判断该反应达到平衡状态的依据是___________(填字母标号)。
| A.容器内压强不变了 | B.c(CO)不变了 |
| C.v正(CO2)=v逆(CO) | D.c(CO2)=c(CO) |
(2)写出该反应的平衡常数表达式
(3)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,如果改变下列条件,反应混合气体中CO2的物质的量分数如何变化(选填“增大”、“减小”、“不变”)。
①加入催化剂
②再通入CO
(4)下图描述的是该反应在甲,乙两个容器进行反应时CO2的转化率变化情况。

请问甲乙容器中必定不同的反应条件是什么?
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Cu的化合物在生活及科研中有重要作用,不同反应可制得不同状态的Cu2O
(1)科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂。
①在加热条件下用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时放出N2。当收集的N2体积为3.36L(已换算为标准状况)时,可制备纳米级Cu2O的质量为________ ;
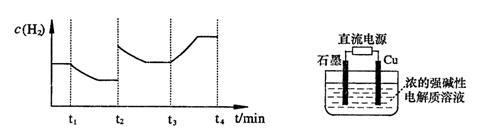
②一定温度下,在2 L密闭容器中加入纳米级Cu2O并通入0.20 mol水蒸气,发生反应:
2H2O(g)=2H2(g)+O2(g)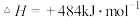 ;测得20 min时O2的物质的量为0.0016 mol,则前20 min的反应速率v(H2O)=
;测得20 min时O2的物质的量为0.0016 mol,则前20 min的反应速率v(H2O)=_________________ ;该温度下,反应的平衡常数表达式K=_________________ ;下图表示在t1时刻达到平衡后,只改变一个条件又达到平衡的不同时段内,H2的浓度随时间变化的情况,则t1时平衡的移动方向为______ ,t2时改变的条件可能为______________ ;若以K1、K2、K3分别表示t1时刻起改变条件的三个时间段内的平衡常数,t3时刻没有加入或减少体系中的任何物质,则K1、K2、K3的关系为________________ ;
(2)已知: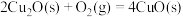 ΔH=-293kJ·mol-1
ΔH=-293kJ·mol-1
 ΔH=-221kJ·mol-1
ΔH=-221kJ·mol-1
请写出用足量炭粉还原CuO(s)制备Cu2O(s)的热化学方程式________ ;
(3)用电解法也可制备Cu2O。原理如右上图所示,则阳极电极反应可以表示为________ 。
(1)科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂。
①在加热条件下用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时放出N2。当收集的N2体积为3.36L(已换算为标准状况)时,可制备纳米级Cu2O的质量为

②一定温度下,在2 L密闭容器中加入纳米级Cu2O并通入0.20 mol水蒸气,发生反应:
2H2O(g)=2H2(g)+O2(g)
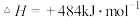 ;测得20 min时O2的物质的量为0.0016 mol,则前20 min的反应速率v(H2O)=
;测得20 min时O2的物质的量为0.0016 mol,则前20 min的反应速率v(H2O)=(2)已知:
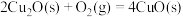 ΔH=-293kJ·mol-1
ΔH=-293kJ·mol-1 ΔH=-221kJ·mol-1
ΔH=-221kJ·mol-1请写出用足量炭粉还原CuO(s)制备Cu2O(s)的热化学方程式
(3)用电解法也可制备Cu2O。原理如右上图所示,则阳极电极反应可以表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在一定体积的密闭容器中进行化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度的关系如表所示:
CO(g)+H2O(g),其化学平衡常数K和温度的关系如表所示:
回答下列问题:
(1)该反应为__ 反应(填“吸热”或“放热”)。
(2)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为__ 。
(3)能判断该反应是否达到化学平衡状态的依据是__ 。
A.容器中物质的量不变
B.混合气体中各物质的浓度不变
C.消耗nmolCO2的同时,生成了2nmolH2
D.c(CO2)=c(H2O)
 CO(g)+H2O(g),其化学平衡常数K和温度的关系如表所示:
CO(g)+H2O(g),其化学平衡常数K和温度的关系如表所示:| t/ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为
(2)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
(3)能判断该反应是否达到化学平衡状态的依据是
A.容器中物质的量不变
B.混合气体中各物质的浓度不变
C.消耗nmolCO2的同时,生成了2nmolH2
D.c(CO2)=c(H2O)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在2L密闭容器内,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)上述反应___ (填“是”或“不是”)可逆反应。
(2)用O2表示从0~2s内该反应的平均速率v=__ 。达到平衡时NO的转化率等于__ 。
(3)如图所示,表示NO2变化曲线的是__ 。

(4)能说明该反应已达到平衡状态的是__ (填序号)。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)用O2表示从0~2s内该反应的平均速率v=
(3)如图所示,表示NO2变化曲线的是

(4)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
您最近一年使用:0次
【推荐2】氨气是一种重要的化工原料,在工农业生产中有广泛的应用。
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:CO+2H2 CH3OH(g)。该可逆反应达到平衡的标志是
CH3OH(g)。该可逆反应达到平衡的标志是________ 。
A.2 v正(H2)= v逆(CH3OH)
B.单位时间生成m molCO的同时生成2m molH2
C.容器内气体的平均相对分子质量不再随时间而变化
D.混合气体的密度不再随时间变化
(2)工业上可用天然气为原料来制取化工原料气氢气,某研究性学习小组的同学模拟工业制取氢气的原理,在一定温度下,体积为2L的恒容密闭容器中,测得如下表所示数据。
请回答下列问题:
①该温度下,上述反应的平衡常数K=________ ;
②反应在7~10 min内,CO的物质的量减少的原因可能是____________ (填字母)。
A.减少CH4的物质的量 B.降低温度
C.升高温度 D.充入H2
③若保持相同的温度,向2L的恒容器密闭容器中同时充入0.2molCH4、0.62molH2O、a molCO和0.5molH2,当a =0.2时,上述反应向_____ (填“正反应”或“逆反应”)方向进行。若要使上述反应开始时向逆反应方向进行,则a的取值范围为__________ 。
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:CO+2H2
 CH3OH(g)。该可逆反应达到平衡的标志是
CH3OH(g)。该可逆反应达到平衡的标志是A.2 v正(H2)= v逆(CH3OH)
B.单位时间生成m molCO的同时生成2m molH2
C.容器内气体的平均相对分子质量不再随时间而变化
D.混合气体的密度不再随时间变化
(2)工业上可用天然气为原料来制取化工原料气氢气,某研究性学习小组的同学模拟工业制取氢气的原理,在一定温度下,体积为2L的恒容密闭容器中,测得如下表所示数据。
| 时间/min | CH4(mol) | H2O(mol) | CO(mol) | H2(mol) |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | a | 0.80 | c | 0.60 |
| 7 | 0.20 | b | 0.20 | d |
| 10 | 0.21 | 0.81 | 0.19 | 0.64 |
①该温度下,上述反应的平衡常数K=
②反应在7~10 min内,CO的物质的量减少的原因可能是
A.减少CH4的物质的量 B.降低温度
C.升高温度 D.充入H2
③若保持相同的温度,向2L的恒容器密闭容器中同时充入0.2molCH4、0.62molH2O、a molCO和0.5molH2,当a =0.2时,上述反应向
您最近一年使用:0次
【推荐3】1905年哈珀开发实现了以氮气和氢气为原料合成氨气,生产的氨制造氮肥服务于农业,养活了地球三分之一的人口,哈珀也因此获得了1918年的诺贝尔化学奖。
(1)工业合成氨的反应如下:N2+3H2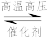 2NH3。已知断裂1 mol N2中的共价键吸收的能量为946 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2和H2生成2 mol NH3 的能量变化为
2NH3。已知断裂1 mol N2中的共价键吸收的能量为946 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2和H2生成2 mol NH3 的能量变化为__________ kJ。 下图能正确表示该反应中能量变化的是__________ (填“A”或“B”)。
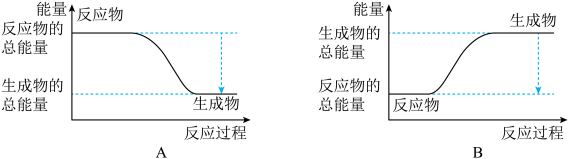
(2)反应2NH3(g)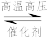 N2(g)+3H2(g)在三种不同条件下进行,N2、H2的起始浓度为 0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
N2(g)+3H2(g)在三种不同条件下进行,N2、H2的起始浓度为 0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
根据上述数据回答:实验①②中,有一个实验使用了催化剂,它是实验_____ (填序号);实验①③对比说明了_________________________________ 。在恒温恒容条件下,判断该反应达到化学平衡状态的标志是_________ (填序号)。
a. NH3的正反应速率等于逆反应速率 b.混合气体的密度不变
c.混合气体的压强不变 d.c(NH3)=c(H2)
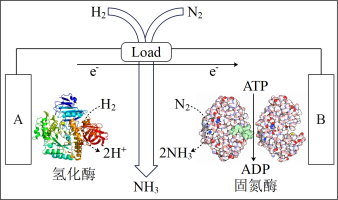
(3)近日美国犹他大学 Minteer教授成功构筑了H2—N2生物燃料电池。该电池类似燃料电池原理,以氮气和氢气为原料、氢化酶和固氮酶为两极催化剂、质子交换膜(能够传递H+)为隔膜,在室温条件下即实现了氨的合成同时还能提供电能。则A电极为_____ 极(填“正”、“负”),该电池放电时溶液中的H+向______ 极移动(填“A”、“B”)。
(1)工业合成氨的反应如下:N2+3H2
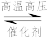 2NH3。已知断裂1 mol N2中的共价键吸收的能量为946 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2和H2生成2 mol NH3 的能量变化为
2NH3。已知断裂1 mol N2中的共价键吸收的能量为946 kJ,断裂1 mol H2中的共价键吸收的能量为436 kJ,形成1 mol N-H键放出的能量为391 kJ,则由N2和H2生成2 mol NH3 的能量变化为
(2)反应2NH3(g)
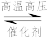 N2(g)+3H2(g)在三种不同条件下进行,N2、H2的起始浓度为 0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。
N2(g)+3H2(g)在三种不同条件下进行,N2、H2的起始浓度为 0,反应物NH3的浓度(mol/L)随时间(min)的变化情况如下表所示。| 实验序号 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| ① | 400℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| ② | 400℃ | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| ③ | 500℃ | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
a. NH3的正反应速率等于逆反应速率 b.混合气体的密度不变
c.混合气体的压强不变 d.c(NH3)=c(H2)
(3)近日美国犹他大学 Minteer教授成功构筑了H2—N2生物燃料电池。该电池类似燃料电池原理,以氮气和氢气为原料、氢化酶和固氮酶为两极催化剂、质子交换膜(能够传递H+)为隔膜,在室温条件下即实现了氨的合成同时还能提供电能。则A电极为

您最近一年使用:0次



