工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g) CH3OH(g)ΔH=akJ/mol下,表所列数据是反应在不同温度下的化学平衡常数(Kc)。
CH3OH(g)ΔH=akJ/mol下,表所列数据是反应在不同温度下的化学平衡常数(Kc)。
(1)写出该反应的压强平衡常数的表达式Kp______ 。
(2)判断该反应达到平衡状态的依据有_________ 。
A.消耗CH3OH的速率与消耗CO的速率相等 B.混合气体的平均相对分子质量不变
C.混合气体的密度不变 D.容器内气压不变
(3)根据上表数据,要同时提高CO的平衡转化率和反应速率,可采取的措施是______ 。
A.升温 B.充入H2 C.分离出甲醇 D.加入催化剂
(4)250℃时,将2 mol CO和一定量的H2充入2 L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol·L-1,则以H2表示的反应速率v(H2)=_____ 。平衡后再向容器中加入0.1 mol CO和 0.4 mol CH3OH,则此时v正___ v逆(填“>”、“<”或“=”)。
(5)CO还可以用做燃料电池的燃料。若电池用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混和气为正极助燃气,电池在650 ℃下工作时,其正极反应式:O2 + 2CO2 + 4e-=2CO32-,则负极反应式为:________ 。
 CH3OH(g)ΔH=akJ/mol下,表所列数据是反应在不同温度下的化学平衡常数(Kc)。
CH3OH(g)ΔH=akJ/mol下,表所列数据是反应在不同温度下的化学平衡常数(Kc)。| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.0 | 0.27 | 0.012 |
(1)写出该反应的压强平衡常数的表达式Kp
(2)判断该反应达到平衡状态的依据有
A.消耗CH3OH的速率与消耗CO的速率相等 B.混合气体的平均相对分子质量不变
C.混合气体的密度不变 D.容器内气压不变
(3)根据上表数据,要同时提高CO的平衡转化率和反应速率,可采取的措施是
A.升温 B.充入H2 C.分离出甲醇 D.加入催化剂
(4)250℃时,将2 mol CO和一定量的H2充入2 L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol·L-1,则以H2表示的反应速率v(H2)=
(5)CO还可以用做燃料电池的燃料。若电池用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混和气为正极助燃气,电池在650 ℃下工作时,其正极反应式:O2 + 2CO2 + 4e-=2CO32-,则负极反应式为:
更新时间:2019-11-18 22:30:53
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某学习小组研究溶液中Fe2+的稳定性,进行如下实验,观察,记录结果。
实验Ⅰ
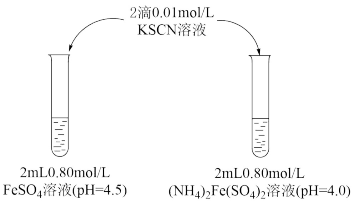
(1)溶液的稳定性:FeSO4_______ (NH4)2Fe(SO4)2(填“>”或“<”)
(2)结合离子方程式解释FeSO4溶液中加入KSCN溶液后变红的原因____________ 。
(3)甲同学提出实验Ⅰ中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+具有还原性。进行实验II,否定了该观点,补全该实验。
(4)乙同学提出实验Ⅰ中两溶液的稳定性差异是溶液酸性不同导致,进行实验III:分别配制0.80 mol·L-1 pH为1、2、3、4的FeSO4溶液,观察,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短。
资料显示:亚铁盐溶液中存在反应:4Fe2++O2+10H2O 4Fe(OH)3+8H+。
4Fe(OH)3+8H+。
由实验III,乙同学可得出的结论是___________ ,原因是__________________ 。
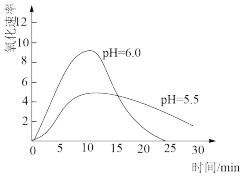
(5)进一步研究在水溶液中Fe2+的氧化机理。测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如下图(实验过程中溶液温度几乎无变化)。反应初期,氧化速率都逐渐增大的原因可能是_____________ 。
(6)综合以上实验,增强Fe2+稳定性的措施有_________________ 。
实验Ⅰ

| 物质 | 0 min | 1min | 1h | 5h |
| FeSO4 | 淡黄色 | 桔红色 | 红色 | 深红色 |
| (NH4)2Fe(SO4)2 | 几乎无色 | 淡黄色 | 黄色 | 桔红色 |
(2)结合离子方程式解释FeSO4溶液中加入KSCN溶液后变红的原因
(3)甲同学提出实验Ⅰ中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+具有还原性。进行实验II,否定了该观点,补全该实验。
| 操作 | 现象 |
| 取 | 与实验Ⅰ中(NH4)2Fe(SO4)2溶液现象相同。 |
资料显示:亚铁盐溶液中存在反应:4Fe2++O2+10H2O
 4Fe(OH)3+8H+。
4Fe(OH)3+8H+。由实验III,乙同学可得出的结论是
(5)进一步研究在水溶液中Fe2+的氧化机理。测定同浓度FeSO4溶液在不同pH条件下,Fe2+的氧化速率与时间的关系如下图(实验过程中溶液温度几乎无变化)。反应初期,氧化速率都逐渐增大的原因可能是

(6)综合以上实验,增强Fe2+稳定性的措施有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ/mol
2NH3(g) ΔH=-92.4 kJ/mol
据此回答:
(1)合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是________ (填序号)。
①20 MPa~50 MPa
②500℃的高温
③铁触媒作催化剂
④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中
(2)一定条件下NH3的平衡体积分数随n(N2)变化如图所示 (T-温度)。
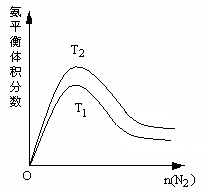
则T2_____ T1 (填>、=、<),判断的依据是:______________________ 。
(3)相同温度下,有恒容密闭容器A、恒压密闭容器B,两容器中均充入1 mol N2和3 mol H2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;B中NH3的体积分数为b,放出热量Q2 kJ。
则:a_____ b(填>、=、<),Q1_____ Q2(填>、=、<),Q1_____ 92.4(填>、=、<)。
N2(g)+3H2(g)
 2NH3(g) ΔH=-92.4 kJ/mol
2NH3(g) ΔH=-92.4 kJ/mol 据此回答:
(1)合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是
①20 MPa~50 MPa
②500℃的高温
③铁触媒作催化剂
④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中
(2)一定条件下NH3的平衡体积分数随n(N2)变化如图所示 (T-温度)。

则T2
(3)相同温度下,有恒容密闭容器A、恒压密闭容器B,两容器中均充入1 mol N2和3 mol H2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;B中NH3的体积分数为b,放出热量Q2 kJ。
则:a
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】煤气中主要的含硫杂质有H2S以及CS2、COS等有机硫,煤气燃烧后含硫杂质会转化成SO2从而引起大气污染。煤气中H2S的脱除程度已成为其洁净度的一个重要指标,脱除煤气中H2S的方法有干法脱硫和湿法脱硫,其中湿法脱硫的原理是利用Na2CO3溶液吸收H2S生成NaHS,再进一步被空气氧化成Na2S2O3。
请回答下列问题:
(1)Na2S2O3的化学名称为___________ 。
(2)脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法以及水解法等。
①COS的分子结构与CO2相似,COS的电子式为___________ 。
②用活性α—Al2O3催化COS水解的反应为COS(g)+ H2 O(g) CO2(g)+ H2S(g)ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,在相同的时间内测得不同温度下COS的转化率(未达平衡)如图1所示;某温度下,COS的平衡转化率与
CO2(g)+ H2S(g)ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,在相同的时间内测得不同温度下COS的转化率(未达平衡)如图1所示;某温度下,COS的平衡转化率与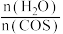 的关系如图2所示。
的关系如图2所示。
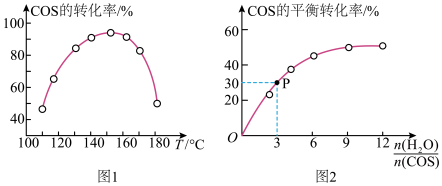
由图1可知,催化剂活性最大时对应的温度约为___________ ;由图2可知,P点时平衡常数K=___________ (保留2位有效数字)。
(3)回收处理燃煤烟气中SO2的方法之一是用氨水先将SO2转化为NH4HSO3,再通入空气将其氧化成(NH4)2SO4.能提高燃煤烟气中SO2去除率的措施有___________ (填字母)。
a.增大氨水浓度 b.增大燃煤烟气的流速 c.升高温度 d.增大压强
请回答下列问题:
(1)Na2S2O3的化学名称为
(2)脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法以及水解法等。
①COS的分子结构与CO2相似,COS的电子式为
②用活性α—Al2O3催化COS水解的反应为COS(g)+ H2 O(g)
 CO2(g)+ H2S(g)ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,在相同的时间内测得不同温度下COS的转化率(未达平衡)如图1所示;某温度下,COS的平衡转化率与
CO2(g)+ H2S(g)ΔH<0,相同投料比、相同流量且在催化剂表面停留相同时间时,在相同的时间内测得不同温度下COS的转化率(未达平衡)如图1所示;某温度下,COS的平衡转化率与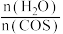 的关系如图2所示。
的关系如图2所示。
由图1可知,催化剂活性最大时对应的温度约为
(3)回收处理燃煤烟气中SO2的方法之一是用氨水先将SO2转化为NH4HSO3,再通入空气将其氧化成(NH4)2SO4.能提高燃煤烟气中SO2去除率的措施有
a.增大氨水浓度 b.增大燃煤烟气的流速 c.升高温度 d.增大压强
您最近一年使用:0次
【推荐1】甲醇是一种重要的化工原料,在生产中有着重要的应用。
(1)已知:①CH3OH(l) + 3/2O2(g)=CO2(g) + 2H2O(g) △H=-638.5 kJ·mol-1
②CO(g) + 1/2O2(g)=CO2(g) △H=-283.0 kJ·mol-1
③H2O(l)=H2O(g) △H=+44.0 kJ·mol-1
则反应CH3OH(l) + O2(g)=CO(g) + 2H2O(l)的△H=______ kJ·mol-1。
(2)工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
I.CO(g) + 2H2(g) ⇌CH3OH(g) △H1
II.CO2(g) + 3H2(g) ⇌CH3OH(g) + H2O(g) △H2<0
III.CO2(g) + H2(g) ⇌CO(g) + H2O(g) △H3>0
①已知升高温度,反应Ⅰ的平衡常数K减小,则该反应的△H1__________ 0(填“>”或“<”)。
②对反应II而言,下列叙述中,能说明该反应达到化学反应平衡状态的是________ 。
a. 单位时间内消耗1 mol CO2的同时生成3 mol H2
b. 反应过程中c(CO2):c(CH3OH)=1:1
c. 恒温恒容时,混合气体的密度保持不变
d. 绝热恒容时,反应的平衡常数不再变化
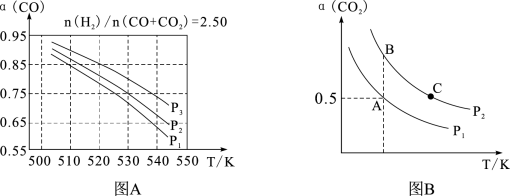
③上述反应体系中,当合成气的组成n(H2)/n(CO + CO2)=2.50时,体系中CO的平衡转化率(α)与温度和压强的关系如下图A所示。则图中压强由大到小的顺序为_____________ ,α(CO)随温度升高而减小的原因是___________________________ 。
(3)用甲醇、二氧化碳可以在一定条件下合成碳酸二甲酯(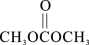 ,简称DMC),其反应的化学方程式为:2CH3OH(g) + CO2(g)
,简称DMC),其反应的化学方程式为:2CH3OH(g) + CO2(g)
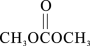 (g) + H2O(g)。在体积为2 L的恒容密闭容器中投入4 mol CH3OH(g) 和2 mol CO2(g) 合成DMC,一定条件下CO2的平衡转化率(α)与温度、压强的变化关系如图B所示。则:
(g) + H2O(g)。在体积为2 L的恒容密闭容器中投入4 mol CH3OH(g) 和2 mol CO2(g) 合成DMC,一定条件下CO2的平衡转化率(α)与温度、压强的变化关系如图B所示。则:
①A点时该反应的平衡常数K=__________ 。
②A、B、C三点的速率v (A)、v (B)、v (C)由快到慢的顺序为____________ 。
(1)已知:①CH3OH(l) + 3/2O2(g)=CO2(g) + 2H2O(g) △H=-638.5 kJ·mol-1
②CO(g) + 1/2O2(g)=CO2(g) △H=-283.0 kJ·mol-1
③H2O(l)=H2O(g) △H=+44.0 kJ·mol-1
则反应CH3OH(l) + O2(g)=CO(g) + 2H2O(l)的△H=
(2)工业上利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主要反应如下:
I.CO(g) + 2H2(g) ⇌CH3OH(g) △H1
II.CO2(g) + 3H2(g) ⇌CH3OH(g) + H2O(g) △H2<0
III.CO2(g) + H2(g) ⇌CO(g) + H2O(g) △H3>0
①已知升高温度,反应Ⅰ的平衡常数K减小,则该反应的△H1
②对反应II而言,下列叙述中,能说明该反应达到化学反应平衡状态的是
a. 单位时间内消耗1 mol CO2的同时生成3 mol H2
b. 反应过程中c(CO2):c(CH3OH)=1:1
c. 恒温恒容时,混合气体的密度保持不变
d. 绝热恒容时,反应的平衡常数不再变化
③上述反应体系中,当合成气的组成n(H2)/n(CO + CO2)=2.50时,体系中CO的平衡转化率(α)与温度和压强的关系如下图A所示。则图中压强由大到小的顺序为

(3)用甲醇、二氧化碳可以在一定条件下合成碳酸二甲酯(
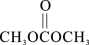 ,简称DMC),其反应的化学方程式为:2CH3OH(g) + CO2(g)
,简称DMC),其反应的化学方程式为:2CH3OH(g) + CO2(g)
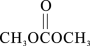 (g) + H2O(g)。在体积为2 L的恒容密闭容器中投入4 mol CH3OH(g) 和2 mol CO2(g) 合成DMC,一定条件下CO2的平衡转化率(α)与温度、压强的变化关系如图B所示。则:
(g) + H2O(g)。在体积为2 L的恒容密闭容器中投入4 mol CH3OH(g) 和2 mol CO2(g) 合成DMC,一定条件下CO2的平衡转化率(α)与温度、压强的变化关系如图B所示。则:①A点时该反应的平衡常数K=
②A、B、C三点的速率v (A)、v (B)、v (C)由快到慢的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】I.某实验小组对H2O2的分解做了如下探究。将等质量的块状MnO2和粉末状MnO2分别加入盛有15ml5%的H2O2溶液的大试管中,并用带火星的木条测试,得结果如下表:
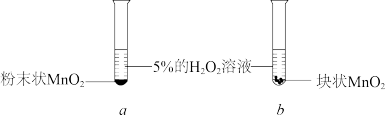
(1)写出上述实验中发生反应的化学方程式:_______ 。
(2)实验结果表明,_______ 催化剂的催化效果更好。(填“块状”或“粉末状”)
(3)根据你的判断t1_______ t2。(填“高于”或“低于”)
(4)在H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如下图所示,则A、B、C三点所表示的即时反应速率最快的是_______ 。
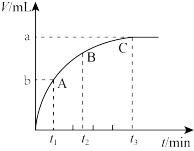
II.某反应在体积为10L的恒容密闭容器中进行,在0~3分钟内各物质的量的变化情况如下图所示(反应中所有物质均为气体,其中X为未知气体)。
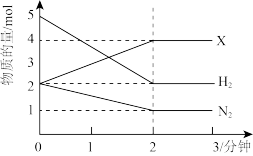
(5)反应开始至2分钟时,N2的平均反应速率为_______ 。
(6)该反应的的化学方程式为_______ 。
(7)能说明该反应已达到平衡状态的是_______ 。
a.2v逆(N2)=v正(X)
b.容器内气体密度保持不变
c.容器内各物质的浓度保持不变
d.容器内各物质的物质的量相等
(8)平衡时,混合气体中X的物质的量的分数为_______ 。
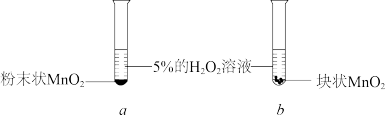
| 组别 | 反应结束时温度 | 现象 | 反应完成所需时间 |
| a | t1 | 剧烈反应,带火星的木条复燃 | 3.5min |
| b | t2 | 反应较慢,火星红亮但木条未复燃 | 30min |
(1)写出上述实验中发生反应的化学方程式:
(2)实验结果表明,
(3)根据你的判断t1
(4)在H2O2溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如下图所示,则A、B、C三点所表示的即时反应速率最快的是

II.某反应在体积为10L的恒容密闭容器中进行,在0~3分钟内各物质的量的变化情况如下图所示(反应中所有物质均为气体,其中X为未知气体)。

(5)反应开始至2分钟时,N2的平均反应速率为
(6)该反应的的化学方程式为
(7)能说明该反应已达到平衡状态的是
a.2v逆(N2)=v正(X)
b.容器内气体密度保持不变
c.容器内各物质的浓度保持不变
d.容器内各物质的物质的量相等
(8)平衡时,混合气体中X的物质的量的分数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】在容积为1.00L的容器中,通入一定量的 ,发生反应
,发生反应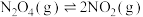 ,随温度升高,混合气体的颜色变深。回答下列问题:
,随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的
___________ 0(填“大于”或“小于”)。100℃时,体系中各物质浓度随时间变化如图所示,在0~60s时段,反应速率
___________ mol⋅L-1⋅s-1;反应的平衡常数
___________ 。

(2)10℃时达到平衡后,改变反应温度为T, 以0.0020 mol⋅L-1⋅s-1的平均速率降低,经10s又达到平衡。
以0.0020 mol⋅L-1⋅s-1的平均速率降低,经10s又达到平衡。
①T___________ 100℃(填“大于”或“小于”)。
②达到新的平衡状态后, 的体积分数为
的体积分数为___________ 。(保留三位有效数字)
③能说明该反应已达到平衡状态的是___________ (填标号)。
A.容器内气体颜色不再变化 B. 与
与 的物质的量比为1∶2
的物质的量比为1∶2
C.混合气体的密度保持不变 D.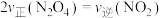
(3)温度T时反应达平衡后,压缩反应容器,平衡向___________ (填“正反应”或“逆反应”)方向移动,混合气体的颜色变化过程为___________ 。
 ,发生反应
,发生反应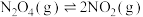 ,随温度升高,混合气体的颜色变深。回答下列问题:
,随温度升高,混合气体的颜色变深。回答下列问题:(1)反应的




(2)10℃时达到平衡后,改变反应温度为T,
 以0.0020 mol⋅L-1⋅s-1的平均速率降低,经10s又达到平衡。
以0.0020 mol⋅L-1⋅s-1的平均速率降低,经10s又达到平衡。①T
②达到新的平衡状态后,
 的体积分数为
的体积分数为③能说明该反应已达到平衡状态的是
A.容器内气体颜色不再变化 B.
 与
与 的物质的量比为1∶2
的物质的量比为1∶2C.混合气体的密度保持不变 D.
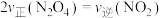
(3)温度T时反应达平衡后,压缩反应容器,平衡向
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】CO2 的资源化利用是“减少碳排放”背景下的科学研究热点。
I.利用 CO2 甲烷化反应:CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g)进行热力学转化。
(1)已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-802kJ/mol
写出 CO2甲烷化反应的热化学方程式___________ 。
(2)CO2 甲烷化反应的平衡常数的表达式:K=___________ 。温度升高,K___________ (填“增大”或“减小”)。
II.CO2 催化加氢合成二甲醚。其过程中主要发生下列反应:
反应i:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41.2kJ·mol−1
反应ii:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ·mol−1
在恒压、CO2 和 H2 的起始量一定的条件下,CO2 平衡转化率和平衡时 CH3OCH3 的选择性随温度的变化如下图所示。

(3)①温度升高,平衡时CH3OCH3的选择性下降的原因是___________ 。
②温度高于300℃时,CO2平衡转化率随温度升高而上升的原因是___________ 。
III.电化学转化
多晶 Cu 可高效催化 CO2 甲烷化,电解 CO2 制备CH4 的原理示意图如下。电解过程中温度控制在 10℃左右,持续通入 CO2.阴、阳极室的 KHCO3 溶液的浓度基本保持不变。
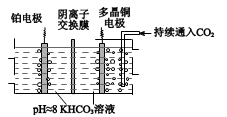
(4)多晶Cu作___________ (填“阴”或“阳”)极。
(5)阳极上发生的电极反应式是___________ 。
(6)阴离子交换膜中传导的离子是___________ ,移动方向是(填“从左向右”或者“从右向左”)___________ 。
I.利用 CO2 甲烷化反应:CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g)进行热力学转化。
(1)已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-802kJ/mol
写出 CO2甲烷化反应的热化学方程式
(2)CO2 甲烷化反应的平衡常数的表达式:K=
II.CO2 催化加氢合成二甲醚。其过程中主要发生下列反应:
反应i:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41.2kJ·mol−1
反应ii:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ·mol−1
在恒压、CO2 和 H2 的起始量一定的条件下,CO2 平衡转化率和平衡时 CH3OCH3 的选择性随温度的变化如下图所示。

(3)①温度升高,平衡时CH3OCH3的选择性下降的原因是
②温度高于300℃时,CO2平衡转化率随温度升高而上升的原因是
III.电化学转化
多晶 Cu 可高效催化 CO2 甲烷化,电解 CO2 制备CH4 的原理示意图如下。电解过程中温度控制在 10℃左右,持续通入 CO2.阴、阳极室的 KHCO3 溶液的浓度基本保持不变。

(4)多晶Cu作
(5)阳极上发生的电极反应式是
(6)阴离子交换膜中传导的离子是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】⑴可逆反应FeO(s)+CO(g)⇌Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如下表:
①写出该反应平衡常数的表达式________ 。
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若升高温度,混合气体的平均相对分子质量________ ;充入氦气,混合气体的密度________ (填“增大”“减小”或“不变”)。
⑵常温下,浓度均为0.1 mol·L-1的下列六种溶液的pH如下表:
①根据表中数据判断,浓度均为0.01 mol·L-1的下列四种物质的溶液中,酸性最强的是________ (填编号)。
A.HCN B.HClO C.H2CO3 D.CH3COOH
②据上表数据,请你判断下列反应不能成立的是________ (填编号)。
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa B.CH3COOH+NaCN=CH3COONa+HCN C.CO2+H2O+2NaClO=Na2CO3+2HClO
| T/K | 938 | 1100 |
| K | 0.68 | 0.40 |
①写出该反应平衡常数的表达式
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,若升高温度,混合气体的平均相对分子质量
⑵常温下,浓度均为0.1 mol·L-1的下列六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
①根据表中数据判断,浓度均为0.01 mol·L-1的下列四种物质的溶液中,酸性最强的是
A.HCN B.HClO C.H2CO3 D.CH3COOH
②据上表数据,请你判断下列反应不能成立的是
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa B.CH3COOH+NaCN=CH3COONa+HCN C.CO2+H2O+2NaClO=Na2CO3+2HClO
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】一氧化碳是一种用途广泛的化工基础原料。有机物加氢反应中镍是常用的催化剂。但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为弄清该方法对催化剂的影响,查得资料如下:
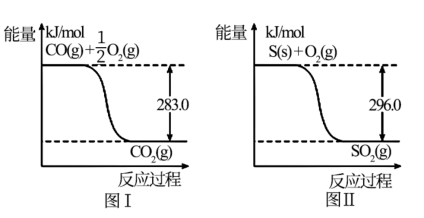
回答下列问题:
(1)SO2(g) + 2CO(g) S(s) + 2CO2(g) △H =
S(s) + 2CO2(g) △H =__________________ ;该反应的平衡常数的表达式是__________________ 。
(2)工业上用一氧化碳制取氢气的反应为:CO(g)+H2O(g)
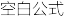 CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为
CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为_____ ,H2的平均生成速率为________________ mol·L-1·min-1。
(3)为减少雾霾、降低大气中有害气体含量,研究机动车尾气中CO、NO及CxHy的排放量意义重大。机动车尾气污染物的含量与空/燃比(空气与燃油气的体积比)的变化关系如图所示。
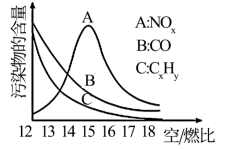
已知:N2与O2生成NO的反应是吸热反应。请解释:
①随空/燃比增大,CO和CxHy的含量减少的原因是__________________________ 。
②当空/燃比达到15后,NO减少的原因可能是___________________________ 。
(4)一定条件下H2与CO合成CH3OH,CH3OH再转化成为CH3OCH3,转化的热化学反应方程式如下:2CH3OH(g) CH3OCH3(g)+H2O(g) ΔH=-24.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-24.5kJ·mol-1
在250℃、压强不变的密闭容器中,加入2mol的CH3OH,一段时间后上述反应达平衡,体系放出热量11 kJ;若同一条件下加入0.2mol CH3OCH3和0.2mol H2O,一段时间后上述反应达平衡,体系的热效应为_________ 。

回答下列问题:
(1)SO2(g) + 2CO(g)
 S(s) + 2CO2(g) △H =
S(s) + 2CO2(g) △H =(2)工业上用一氧化碳制取氢气的反应为:CO(g)+H2O(g)

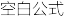 CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为
CO2(g)+H2(g),已知420℃时,该反应的化学平衡常数K=9。如果反应开始时,在2L的密闭容器中充入CO和H2O的物质的量都是0.60mol,5min末达到平衡,则此时CO的转化率为(3)为减少雾霾、降低大气中有害气体含量,研究机动车尾气中CO、NO及CxHy的排放量意义重大。机动车尾气污染物的含量与空/燃比(空气与燃油气的体积比)的变化关系如图所示。

已知:N2与O2生成NO的反应是吸热反应。请解释:
①随空/燃比增大,CO和CxHy的含量减少的原因是
②当空/燃比达到15后,NO减少的原因可能是
(4)一定条件下H2与CO合成CH3OH,CH3OH再转化成为CH3OCH3,转化的热化学反应方程式如下:2CH3OH(g)
 CH3OCH3(g)+H2O(g) ΔH=-24.5kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-24.5kJ·mol-1在250℃、压强不变的密闭容器中,加入2mol的CH3OH,一段时间后上述反应达平衡,体系放出热量11 kJ;若同一条件下加入0.2mol CH3OCH3和0.2mol H2O,一段时间后上述反应达平衡,体系的热效应为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】I.某研究性学习小组根据反应: 2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O。设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。
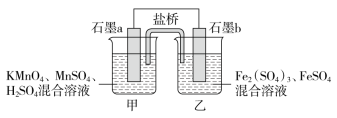
回答下列问题:
(1)此原电池的正极是石墨________ (填“a”或“b”),发生________ 反应。
(2)电池工作时,盐桥中的SO42-移向________ (填“甲”或“乙”)烧杯。
(3)两烧杯中的电极反应式分别为
甲_____________________ ;
乙____________________ 。
(4)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为________ mol。
Ⅱ.次磷酸钴(II)[Co(H2PO2)2]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图。

(5)A、B、C均为离子交换膜,其中为阳离子交换膜的是____________ 。
(6)阳极的电极反应式为________________ 。
(7)电解一段时间后,阴极室溶液的pH______ (填“增大”“减小”或“不变”)。
(8)用Co(H2PO2)2溶液化学镀钴是在强碱性条件下通过发生自身氧化还原反应,反应的同时会生成HPO32-,其离子方程式为__________ 。

回答下列问题:
(1)此原电池的正极是石墨
(2)电池工作时,盐桥中的SO42-移向
(3)两烧杯中的电极反应式分别为
甲
乙
(4)若不考虑溶液的体积变化,MnSO4浓度变为1.5 mol·L-1,则反应中转移的电子为
Ⅱ.次磷酸钴(II)[Co(H2PO2)2]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图。

(5)A、B、C均为离子交换膜,其中为阳离子交换膜的是
(6)阳极的电极反应式为
(7)电解一段时间后,阴极室溶液的pH
(8)用Co(H2PO2)2溶液化学镀钴是在强碱性条件下通过发生自身氧化还原反应,反应的同时会生成HPO32-,其离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】H2O2在工业、农业、医药上都有广泛的用途。
(1)许多物质都可以做H2O2分解的催化剂。一种观点认为:在反应过程中催化剂先被H2O2氧化(或还原),后又被H2O2还原(或氧化)。下列物质都可做H2O2分解的催化剂,在反应过程中先被氧化,后被还原的是___________ 。
a.I- b.Fe3+ c.Cu2+ d.Fe2+
(2)用碱性氢氧燃料电池合成H2O2,具有效率高,无污染等特点。电池总反应为:H2+O2+OH-=H2O+HO 。写出正极反应式:
。写出正极反应式:___________ 。
(3)H2O2是一种环境友好的强氧化剂。电镀废水(主要含Cu2+、Ni2+,还含少量Fe3+、Fe2+、Cr3+等)制备硫酸镍的一种流程如图:

①第(i)步,加入H2O2反应的离子方程式___________ 。
②为测定NiSO4·nH2O的组成,进行如下实验:称取2.627 g样品,配制成250.00 mL溶液。准确量取配制的溶液25.00 mL,用0.04000 mol·L-1的EDTA(Na2H2Y)标准溶液滴定Ni2+(离子方程式为:Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00 mL。则硫酸镍晶体的化学式为___________ 。
(1)许多物质都可以做H2O2分解的催化剂。一种观点认为:在反应过程中催化剂先被H2O2氧化(或还原),后又被H2O2还原(或氧化)。下列物质都可做H2O2分解的催化剂,在反应过程中先被氧化,后被还原的是
a.I- b.Fe3+ c.Cu2+ d.Fe2+
(2)用碱性氢氧燃料电池合成H2O2,具有效率高,无污染等特点。电池总反应为:H2+O2+OH-=H2O+HO
 。写出正极反应式:
。写出正极反应式:(3)H2O2是一种环境友好的强氧化剂。电镀废水(主要含Cu2+、Ni2+,还含少量Fe3+、Fe2+、Cr3+等)制备硫酸镍的一种流程如图:

①第(i)步,加入H2O2反应的离子方程式
②为测定NiSO4·nH2O的组成,进行如下实验:称取2.627 g样品,配制成250.00 mL溶液。准确量取配制的溶液25.00 mL,用0.04000 mol·L-1的EDTA(Na2H2Y)标准溶液滴定Ni2+(离子方程式为:Ni2++H2Y2-=NiY2-+2H+),消耗EDTA标准溶液25.00 mL。则硫酸镍晶体的化学式为
您最近一年使用:0次
【推荐3】当今世界多国相继规划了碳达峰、碳中和的时间节点,中国承诺2030年前,二氧化碳的排放不再增长,达到峰值之后逐步降低。2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。因此,降低空气中二氧化碳含量成为研究热点,其中研发二氧化碳的利用技术,将二氧化碳转化为能源是缓解环境和解决能源问题的方案之一、
Ⅰ.二氧化碳在一定条件下转化为甲烷,其反应过程如下图所示。
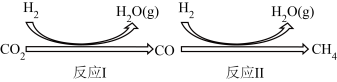
已知:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔHl=-205kJ∙mol-1
反应Ⅱ:CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH2=-246kJ∙mol-1
(1)则反应Ⅰ的热化学方程式为___________ 。
(2)一定条件下,向2L恒容密闭容器中加入1molCO2和5molH2,只发生上述反应Ⅰ和反应Ⅱ;10min后容器内总压强(P)不再变化,容器中CH4为0.6mol,CO2为0.2mol,H2O为1.4mol,10min内H2的平均反应速率
___________ ,CH4的体积分数=___________ 。
Ⅱ.在催化剂作用下CO2加氢还可制得甲醇。
(3)能说明反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=+50kJ∙mol-1已达平衡状态的是___________(填字母)。
Ⅲ.催化重整制备CH3OCH3的过程中存在反应:
①2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ΔH<0;
②CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0。
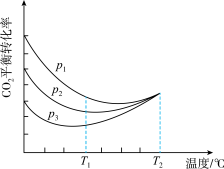
(4)向密闭容器中以物质的量之比为1∶3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图所示。P1、P2、P3由大到小的顺序为___________ ;T2℃时主要发生反应________ (填“①”或“②”)。
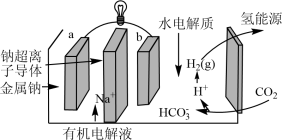
(5)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。系统工作时,a极为________ 极,b极区的电极反应式为___________ 。
Ⅰ.二氧化碳在一定条件下转化为甲烷,其反应过程如下图所示。

已知:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) ΔHl=-205kJ∙mol-1
反应Ⅱ:CO(g)+3H2(g)⇌CH4(g)+H2O(g) ΔH2=-246kJ∙mol-1
(1)则反应Ⅰ的热化学方程式为
(2)一定条件下,向2L恒容密闭容器中加入1molCO2和5molH2,只发生上述反应Ⅰ和反应Ⅱ;10min后容器内总压强(P)不再变化,容器中CH4为0.6mol,CO2为0.2mol,H2O为1.4mol,10min内H2的平均反应速率

Ⅱ.在催化剂作用下CO2加氢还可制得甲醇。
(3)能说明反应CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=+50kJ∙mol-1已达平衡状态的是___________(填字母)。
| A.单位时间内生成1molCH3OH(g)的同时消耗了3molH2(g) |
| B.在恒温恒容的容器中,混合气体的密度保持不变 |
| C.在绝热恒容的容器中,反应的平衡常数不再变化 |
| D.在恒温恒压的容器中,气体的平均摩尔质量不再变化 |
Ⅲ.催化重整制备CH3OCH3的过程中存在反应:
①2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g) ΔH<0;
②CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH>0。
(4)向密闭容器中以物质的量之比为1∶3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图所示。P1、P2、P3由大到小的顺序为

(5)科学家研发出一种新系统,通过“溶解”水中的二氧化碳,以触发电化学反应,有效减少碳的排放,其工作原理如图所示。系统工作时,a极为

您最近一年使用:0次



