Ⅰ.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,二盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
(1)写出二盐酸肼第一步水解反应的离子方程式_____________________ 。
(2)二盐酸肼水溶液中离子浓度的排列顺序正确的是_____ 。
A.c(Cl﹣)>c(N2H62+)>c(H+)>c(OH﹣);
B.c(Cl﹣)>c([N2H5•H2O]+)>c(H+)>c(OH﹣);
C.c(N2H62+)+c([N2H5•H2O]+)+c(H+)=c(Cl﹣)+c(OH﹣);
D.c(N2H62+)>c(Cl﹣)>c(H+)>c(OH﹣);
Ⅱ.某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A=H++HA﹣;HA⇌H++A2﹣则NaHA溶液显_____ (填“酸性”,“中性”,或“碱性”),理由是___________________ ;
Ⅲ.已知HClO的Ka为3.0×10﹣8,H2CO3的 Ka1=4.31×10﹣7 Ka2=5.61×10﹣11,写出向次氯酸钠中通入少量二氧化碳的离子反应方程式:____________________ 。
(1)写出二盐酸肼第一步水解反应的离子方程式
(2)二盐酸肼水溶液中离子浓度的排列顺序正确的是
A.c(Cl﹣)>c(N2H62+)>c(H+)>c(OH﹣);
B.c(Cl﹣)>c([N2H5•H2O]+)>c(H+)>c(OH﹣);
C.c(N2H62+)+c([N2H5•H2O]+)+c(H+)=c(Cl﹣)+c(OH﹣);
D.c(N2H62+)>c(Cl﹣)>c(H+)>c(OH﹣);
Ⅱ.某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A=H++HA﹣;HA⇌H++A2﹣则NaHA溶液显
Ⅲ.已知HClO的Ka为3.0×10﹣8,H2CO3的 Ka1=4.31×10﹣7 Ka2=5.61×10﹣11,写出向次氯酸钠中通入少量二氧化碳的离子反应方程式:
更新时间:2020-01-02 17:19:05
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】有三溶液:a.Ba(OH)2,b.NaOH,c.NH3·H2O
(1)pH值相等时,三种溶液浓度由大到小的顺序为_________________
(2)物质的量浓度相等时,pH值由大到小的顺序为_________________
(3)pH=11时,各100mL与同浓度的HCl中和,消耗HCl体积由多到少的顺序为________________
(4)浓度相等时,各100mL与同浓度HCl中和,消耗HCl体积由多到少的顺序为_______________
(1)pH值相等时,三种溶液浓度由大到小的顺序为
(2)物质的量浓度相等时,pH值由大到小的顺序为
(3)pH=11时,各100mL与同浓度的HCl中和,消耗HCl体积由多到少的顺序为
(4)浓度相等时,各100mL与同浓度HCl中和,消耗HCl体积由多到少的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)某温度时,水的 ,则该温度
,则该温度______ (填“>”“<”或“=")25℃,其理由是______________ 。
(2)该温度下,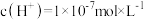 的溶液呈
的溶液呈______ (填“酸性”“碱性”或“中性”);若该溶液中只存在NaOH溶质,则由H2O电离出来的c(OH-)=______ 。
(3)在新制饱和氯水中加入少量NaCl固体,水的电离平衡______ 。(填“向左”“向右”或“不”)移动。
(4)25℃时,pH=4的盐酸中水的电离程度______ (填“大于”“小””或“等于”)pH=10的Ba(OH)2溶液中水的电离程度。
(1)某温度时,水的
 ,则该温度
,则该温度(2)该温度下,
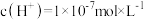 的溶液呈
的溶液呈(3)在新制饱和氯水中加入少量NaCl固体,水的电离平衡
(4)25℃时,pH=4的盐酸中水的电离程度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】连二次硝酸(H2N2O2)是一种二元酸,可用于制N2O气体。
(1)常温下,用0.01mol·L-1的NaOH溶液滴定10mL 0.01mol·L-1的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。
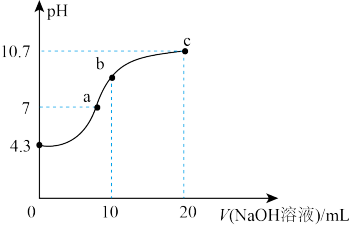
①写出H2N2O2在水溶液中的电离方程式:___ 。
②b点时溶液中c(H2N2O2)__ c(N2O )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。
③a点时溶液中c(Na+)__ c(HN2O )+c(N2O
)+c(N2O )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。
(2)温度为T℃时水的离子积常数为Kw,该温度下,将浓度为a mol·L-1的H2SO4与b mol·L-1的一元碱AOH等体积混合。则可判断溶液呈中性的是__ (填序号)。
①混合溶液的pH=7
②c(SO )=
)= c(A+)
c(A+)
③混合溶液中c(H+)•c(OH-)=Kw
④混合溶液中c(OH-)=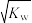
(3)已知常温下CN-的水解常数Kh=1.61×10-5mol·L-1,该温度下若将c mol·L-1盐酸与0.62mol·L-1 KCN溶液等体积混合后恰好得到中性溶液,则c=___ mol·L-1(小数点后保留4位数字)。
(1)常温下,用0.01mol·L-1的NaOH溶液滴定10mL 0.01mol·L-1的H2N2O2溶液,测得溶液pH与NaOH溶液体积的关系如图所示。

①写出H2N2O2在水溶液中的电离方程式:
②b点时溶液中c(H2N2O2)
 )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。③a点时溶液中c(Na+)
 )+c(N2O
)+c(N2O )(填“>”“<”或“=”)。
)(填“>”“<”或“=”)。(2)温度为T℃时水的离子积常数为Kw,该温度下,将浓度为a mol·L-1的H2SO4与b mol·L-1的一元碱AOH等体积混合。则可判断溶液呈中性的是
①混合溶液的pH=7
②c(SO
 )=
)= c(A+)
c(A+)③混合溶液中c(H+)•c(OH-)=Kw
④混合溶液中c(OH-)=
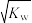
(3)已知常温下CN-的水解常数Kh=1.61×10-5mol·L-1,该温度下若将c mol·L-1盐酸与0.62mol·L-1 KCN溶液等体积混合后恰好得到中性溶液,则c=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度下,部分酸的电离平衡常数如下表:
(1)在温度相同时,各酸的Ka值与酸性的相对强弱的关系为_______ 。
(2)室温下①0.1 mol·L-1 HCOONa、②0.1 mol·L-1 NaClO、③0.1 mol·L-1 Na2CO3、④0.1 mol·L-1 NaHCO3溶液中pH由大到小的顺序为_______ 。
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO 、CO
、CO 、HSO
、HSO 、HCO
、HCO 浓度由大到小的顺序为
浓度由大到小的顺序为_______ 。
(4)下列离子方程式正确的是_______ (填字母)。
a.2ClO-+H2O+CO2=2HClO+CO
b.2HCOOH+CO =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑
c.H2SO3+2HCOO-=2HCOOH+SO
(5)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为_______ 。
| 酸 | HCOOH | HClO | H2CO3 | H2SO3 |
| 电离平衡常数 | Ka=1.77×10-4 | Ka=4.0×10-8 | Ka1=4.3×10-7 Ka2=4.7×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
(1)在温度相同时,各酸的Ka值与酸性的相对强弱的关系为
(2)室温下①0.1 mol·L-1 HCOONa、②0.1 mol·L-1 NaClO、③0.1 mol·L-1 Na2CO3、④0.1 mol·L-1 NaHCO3溶液中pH由大到小的顺序为
(3)浓度均为0.1 mol·L-1的Na2SO3和Na2CO3的混合溶液中,SO
 、CO
、CO 、HSO
、HSO 、HCO
、HCO 浓度由大到小的顺序为
浓度由大到小的顺序为(4)下列离子方程式正确的是
a.2ClO-+H2O+CO2=2HClO+CO

b.2HCOOH+CO
 =2HCOO-+H2O+CO2↑
=2HCOO-+H2O+CO2↑c.H2SO3+2HCOO-=2HCOOH+SO

(5)常温下,pH=3的HCOOH溶液与pH=11的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】雌黄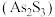 和雄黄
和雄黄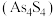 是一对共生矿物,有“矿物鸳鸯”的说法。我国古代书画家曾用其作绘画颜料,因有抗病毒疗效,故在中医治疗中也有非常广泛的用途。
是一对共生矿物,有“矿物鸳鸯”的说法。我国古代书画家曾用其作绘画颜料,因有抗病毒疗效,故在中医治疗中也有非常广泛的用途。
(1)基态砷原子电子排布式为__________ ,砷元素位于周期表的位置__________ 。
(2)同主族元素N、P、As,第一电离能最大的为__________ ;同周期元素Si、P、S,电负性最小的为__________ 。
(3)雌黄可以转化为用于治疗白血病的亚砷酸 ,亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH的关系如图所示:
,亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH的关系如图所示:
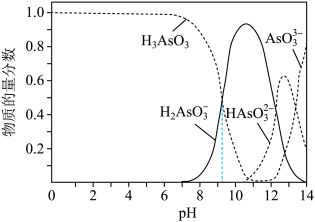
①人体血液的pH为7.35~7.45,用药后人体所含砷元素的主要微粒是__________ 。
②将KOH溶液滴入 溶液中,当pH从11调至12时,反应的离子方程式是
溶液中,当pH从11调至12时,反应的离子方程式是__________ 。
③ 的数量级是
的数量级是_______ 。
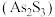 和雄黄
和雄黄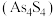 是一对共生矿物,有“矿物鸳鸯”的说法。我国古代书画家曾用其作绘画颜料,因有抗病毒疗效,故在中医治疗中也有非常广泛的用途。
是一对共生矿物,有“矿物鸳鸯”的说法。我国古代书画家曾用其作绘画颜料,因有抗病毒疗效,故在中医治疗中也有非常广泛的用途。(1)基态砷原子电子排布式为
(2)同主族元素N、P、As,第一电离能最大的为
(3)雌黄可以转化为用于治疗白血病的亚砷酸
 ,亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH的关系如图所示:
,亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液pH的关系如图所示:
①人体血液的pH为7.35~7.45,用药后人体所含砷元素的主要微粒是
②将KOH溶液滴入
 溶液中,当pH从11调至12时,反应的离子方程式是
溶液中,当pH从11调至12时,反应的离子方程式是③
 的数量级是
的数量级是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是几种弱电解质的电离平衡常数 (25℃)。
回答下列问题(C6H5OH为苯酚):
(1)由上表分析,若 ① CH3COOH ② HCO3— ③ C6H5OH ④ H2PO4— 均可看作酸,则它们酸性由强到弱的顺序为___________ (填编号);
(2)写出C6H5OH与Na3PO4反应的离子方程式:__________________________ ;
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO—)______ c(NH4+);(填“>”、“=”或“<”)
(4)25℃时,向10 mL 0.01 mol/L苯酚溶液中滴加V mL 0.01 mol/L氨水,混合溶液中粒子浓度关系正确的是______ ;
A.若混合液pH>7,则V≥ 10
B.若混合液pH<7,则c((NH4+) >c (C6H5O—) >c (H+)>c (OH—)
C.V=10时,混合液中水的电离程度小于10 mL 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3·H2O)+ 2 c (NH4+)= c (C6H5O—)+ c (C6H5OH)
(5)水解反应是典型的可逆反应.水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式_______________ 。
| 电解质 | 电离方程式 | 平衡常数K |
| CH3COOH | CH3COOH CH3COO— + H+ CH3COO— + H+ | 1.76 × 10 -5 |
| H2CO3 | H2CO3 HCO3— + H+ HCO3— + H+HCO3—  CO32— + H+ CO32— + H+ | K1=4.31 × 10 -7 K2=5.61 × 10 -11 |
| C6H5OH | C6H5OH C6H5O—+ H+ C6H5O—+ H+ | 1.1 × 10 -10 |
| H3PO4 | H3PO4 H2PO4—+ H+ H2PO4—+ H+H2PO4—  HPO42—+ H+ HPO42—+ H+HPO42—  PO43—+ H+ PO43—+ H+ | K1=7.52 × 10 -3 K2=6.23× 10 -8 K3=2.20× 10 -13 |
| NH3·H2O | NH3·H2O NH4+ + OH— NH4+ + OH— | 1.76× 10 -5 |
回答下列问题(C6H5OH为苯酚):
(1)由上表分析,若 ① CH3COOH ② HCO3— ③ C6H5OH ④ H2PO4— 均可看作酸,则它们酸性由强到弱的顺序为
(2)写出C6H5OH与Na3PO4反应的离子方程式:
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO—)
(4)25℃时,向10 mL 0.01 mol/L苯酚溶液中滴加V mL 0.01 mol/L氨水,混合溶液中粒子浓度关系正确的是
A.若混合液pH>7,则V≥ 10
B.若混合液pH<7,则c((NH4+) >c (C6H5O—) >c (H+)>c (OH—)
C.V=10时,混合液中水的电离程度小于10 mL 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3·H2O)+ 2 c (NH4+)= c (C6H5O—)+ c (C6H5OH)
(5)水解反应是典型的可逆反应.水解反应的化学平衡常数称为水解常数(用Kh表示),类比化学平衡常数的定义,请写出Na2CO3第一步水解反应的水解常数的表达式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)化学中,酸的电离平衡常数(Ka)是评估酸性强弱的重要依据。几种酸的电离常数(25℃)如下表所示。
①写出CH3COOH的电离方程式:__________ 。
②写出H2S的Ka1的表达式:___________ 。
③常温下,浓度相同的三种溶液NaF、Na2CO3、CH3COONa,pH由大到小的顺序是_________ 。
④将过量H2S通入Na2CO3溶液,反应的离子方程式是_________ 。
(2)室温下,用0.100mol/L盐酸溶液滴定20.00mL0.100mol/L的氨水溶液,滴定曲线如图所示(忽略溶液体积的变化,①②填“>”、“<”或“=”)。

①a点所示的溶液中c(NH3·H2O)_________ c(Cl-)。
②b点所示的溶液中c(C1-)_______ c( )。
)。
③室温下pH=11的氨水与pH≈5的NH4Cl溶液中,由水电离出的c(H)之比为_______ 。
(1)化学中,酸的电离平衡常数(Ka)是评估酸性强弱的重要依据。几种酸的电离常数(25℃)如下表所示。
| 弱酸 | HF | CH3COOH | H2CO3 | H2S |
| 电离平衡常数 | Ka=7.2×10-4 | Ka=1.75×10-5 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=9.1×10-8 Ka2=1.1×10-12 |
②写出H2S的Ka1的表达式:
③常温下,浓度相同的三种溶液NaF、Na2CO3、CH3COONa,pH由大到小的顺序是
④将过量H2S通入Na2CO3溶液,反应的离子方程式是
(2)室温下,用0.100mol/L盐酸溶液滴定20.00mL0.100mol/L的氨水溶液,滴定曲线如图所示(忽略溶液体积的变化,①②填“>”、“<”或“=”)。

①a点所示的溶液中c(NH3·H2O)
②b点所示的溶液中c(C1-)
 )。
)。③室温下pH=11的氨水与pH≈5的NH4Cl溶液中,由水电离出的c(H)之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式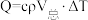 计算获得。
计算获得。
(1)热量的测定:取上述 溶液(
溶液(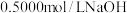 溶液)和盐酸各
溶液)和盐酸各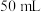 进行反应,测得反应前后体系的温度值(
进行反应,测得反应前后体系的温度值( )分别为
)分别为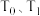 ,则该过程放出的热量为
,则该过程放出的热量为_______  (c和
(c和 分别取
分别取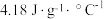 和
和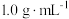 ,忽略水以外各物质吸收的热量,下同)。
,忽略水以外各物质吸收的热量,下同)。
(2)乙同学也借鉴(1)的方法,测量反应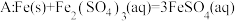 的焓变。
的焓变。
查阅资料:配制 溶液时需加入酸。加酸的目的是
溶液时需加入酸。加酸的目的是_______ 。
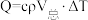 计算获得。
计算获得。(1)热量的测定:取上述
 溶液(
溶液(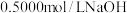 溶液)和盐酸各
溶液)和盐酸各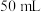 进行反应,测得反应前后体系的温度值(
进行反应,测得反应前后体系的温度值( )分别为
)分别为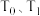 ,则该过程放出的热量为
,则该过程放出的热量为 (c和
(c和 分别取
分别取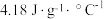 和
和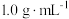 ,忽略水以外各物质吸收的热量,下同)。
,忽略水以外各物质吸收的热量,下同)。(2)乙同学也借鉴(1)的方法,测量反应
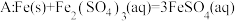 的焓变。
的焓变。查阅资料:配制
 溶液时需加入酸。加酸的目的是
溶液时需加入酸。加酸的目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列填空
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①Na2CO3俗称纯碱,因CO 水解而使其水溶液呈碱性,试写出CO
水解而使其水溶液呈碱性,试写出CO 水解的离子方程式(忽略第二步水解):
水解的离子方程式(忽略第二步水解):___________ ,其水解反应平衡常数(即水解常数)的表达式为Kh=___________ 。
②已知25℃时,Kh=2×10-4mol·L-1,则当溶液中c(HCO ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=___________ 。
③0.1mol·L-1Na2CO3溶液中c(OH-)-c(H+)=___________ [用含c(HCO )、c(H2CO3)的关系式表示]。
)、c(H2CO3)的关系式表示]。
④向Na2CO3溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式:___________ 。
(2)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2molNO2恰好完全反应得1L溶液A,溶液B为0.1mol·L-1的CH3COONa溶液,则两溶液中c(NO )、c(NO
)、c(NO )和c(CH3COO-)由大到小的顺序为
)和c(CH3COO-)由大到小的顺序为___________ (已知HNO2的电离常数Ka=7.1×10-4mol·L-1,CH3COOH的电离常数Ka=1.7×10-5mol·L-1)。可使溶液A和溶液B的pH相等的方法是___________ (填字母)。
a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(3)直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。吸收液(NaOH溶液)吸收SO2的过程中,pH随n(SO ):n(HSO
):n(HSO )的变化关系如下表:
)的变化关系如下表:
①由上表判断NaHSO3溶液显酸性,用化学平衡原理解释:___________ 。
②当吸收液呈中性时,溶液中离子浓度关系正确的是___________ (填字母)。
A.c(Na+)=2c(SO )+c(HSO
)+c(HSO )
)
B.c(Na+)>c(HSO )>c(SO
)>c(SO )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
C.c(Na+)+c(H+)=c(SO )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①Na2CO3俗称纯碱,因CO
 水解而使其水溶液呈碱性,试写出CO
水解而使其水溶液呈碱性,试写出CO 水解的离子方程式(忽略第二步水解):
水解的离子方程式(忽略第二步水解):②已知25℃时,Kh=2×10-4mol·L-1,则当溶液中c(HCO
 ):c(CO
):c(CO )=2:1时,溶液的pH=
)=2:1时,溶液的pH=③0.1mol·L-1Na2CO3溶液中c(OH-)-c(H+)=
 )、c(H2CO3)的关系式表示]。
)、c(H2CO3)的关系式表示]。④向Na2CO3溶液中加入明矾会产生沉淀和气体,请写出相关的离子方程式:
(2)实验室可用NaOH溶液吸收NO2,反应为2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2molNO2恰好完全反应得1L溶液A,溶液B为0.1mol·L-1的CH3COONa溶液,则两溶液中c(NO
 )、c(NO
)、c(NO )和c(CH3COO-)由大到小的顺序为
)和c(CH3COO-)由大到小的顺序为a.向溶液A中加适量水 b.向溶液A中加适量NaOH
c.向溶液B中加适量水 d.向溶液B中加适量NaOH
(3)直接排放含SO2的烟气会形成酸雨,危害环境。利用钠碱循环法可脱除烟气中的SO2。吸收液(NaOH溶液)吸收SO2的过程中,pH随n(SO
 ):n(HSO
):n(HSO )的变化关系如下表:
)的变化关系如下表:n(SO ):n(HSO ):n(HSO ) ) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
①由上表判断NaHSO3溶液显酸性,用化学平衡原理解释:
②当吸收液呈中性时,溶液中离子浓度关系正确的是
A.c(Na+)=2c(SO
 )+c(HSO
)+c(HSO )
)B.c(Na+)>c(HSO
 )>c(SO
)>c(SO )>c(H+)=c(OH-)
)>c(H+)=c(OH-)C.c(Na+)+c(H+)=c(SO
 )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】亚硝酸是一种弱酸,Ka(HNO2)=5.6×10-4,NaNO2可用于滴定分析。
(1)常温下,0.1 mol/L的NaNO2溶液呈__________ (填“酸性”、“中性”或“碱性”);原因是__________ (用离子方程式表示)。
(2)0.1 mol/LNaNO2溶液中部分微粒组分及浓度如图所示,X表示的是_______ (填写微粒化学式)。c(NO2-)+c(HNO2)=__________ mol/L。

(3)NaNO2用于测药物中对氨基苯磺酸(Ar-NH2)的含量。测定原理为:酸性环境中,NaNO2先转化为HNO2:HX + NaNO2 = HNO2 + NaX,HNO2再与Ar-NH2以物质的量比1:1发生反应。
①下列酸中,能作为HX来使用的是_______ 。
A.醋酸(Ka=1.8×10-5) B.盐酸 C.次氯酸(Ka=4.0×10-8)
②反应体系中,Ar-NH2和少量KI共存时,HNO2会先与Ar-NH2完全反应后,再氧化KI。滴定时用KI-淀粉糊剂作指示剂,滴定终点时淀粉糊剂显_______ 色。
③用该法测定含 Ar-NH2(Mr=173)药物样品的纯度,每次取0.400g样品,用0.100mol/L NaNO2标准溶液进行滴定,实验结果如下:
则该样品中对氨基苯磺酸的纯度是__________ 。
第二次实验数据出现异常,造成这种异常的原因可能是________ (填代号)。
a.锥形瓶洗净后未干燥
b.滴定终点时俯视读数
c.装标准溶液的滴定管未用标准溶液润洗
(4)已知298K时,H2CO3的Ka1=4.2×10-7、Ka2=5.61×10-11。将浓度均为0.1mol/L的Na2CO3及 HNO2溶液等体积混合,溶液中阴离子浓度由大到小的顺序为_______ 。
(1)常温下,0.1 mol/L的NaNO2溶液呈
(2)0.1 mol/LNaNO2溶液中部分微粒组分及浓度如图所示,X表示的是

(3)NaNO2用于测药物中对氨基苯磺酸(Ar-NH2)的含量。测定原理为:酸性环境中,NaNO2先转化为HNO2:HX + NaNO2 = HNO2 + NaX,HNO2再与Ar-NH2以物质的量比1:1发生反应。
①下列酸中,能作为HX来使用的是
A.醋酸(Ka=1.8×10-5) B.盐酸 C.次氯酸(Ka=4.0×10-8)
②反应体系中,Ar-NH2和少量KI共存时,HNO2会先与Ar-NH2完全反应后,再氧化KI。滴定时用KI-淀粉糊剂作指示剂,滴定终点时淀粉糊剂显
③用该法测定含 Ar-NH2(Mr=173)药物样品的纯度,每次取0.400g样品,用0.100mol/L NaNO2标准溶液进行滴定,实验结果如下:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗NaNO2溶液体积/mL | 20.12 | 20.90 | 20.00 | 19.88 |
第二次实验数据出现异常,造成这种异常的原因可能是
a.锥形瓶洗净后未干燥
b.滴定终点时俯视读数
c.装标准溶液的滴定管未用标准溶液润洗
(4)已知298K时,H2CO3的Ka1=4.2×10-7、Ka2=5.61×10-11。将浓度均为0.1mol/L的Na2CO3及 HNO2溶液等体积混合,溶液中阴离子浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知氢硫酸是一种二元弱酸,请回答以下问题:
(1)已知 0.1mol/L NaHS 溶液显碱性,则c(S2-)___ c(H2S)(填“>”“<”或“=”)。
(2)常温下,向 0.2mol/L的 H2S溶液中逐滴滴入 0.2mol/L NaOH 溶液至中性,此时溶液中以下所示关系不正确的是___ (填字母)。
(3)已知常温下,CaS饱和溶液中存在平衡CaS(s) ⇌Ca2+(aq)+S2-(aq) △H>0。
①温度升高时,KSP(CaS ) =___ (填“增大”“减少”或“不变”,下同)。
②滴加少量浓盐酸时,c(Ca2+ )___ ,原因是___ (用文字和离子方程式说明)。
③若向CaS 饱和溶液中加入Cu(NO3)2 溶液中,生成一种黑色固体物质,写出该过程中反应的离子方程式:___ 。
(1)已知 0.1mol/L NaHS 溶液显碱性,则c(S2-)
(2)常温下,向 0.2mol/L的 H2S溶液中逐滴滴入 0.2mol/L NaOH 溶液至中性,此时溶液中以下所示关系不正确的是
| A.c(H+)·c(OH-)=1×10-14 |
| B.c(Na+)=c(HS-)+2c(S2-) |
| C.c(Na+)> c(HS-)+c(S2-)+ c(H2S) |
| D.c(H2S)> c(S2-) |
①温度升高时,KSP(CaS ) =
②滴加少量浓盐酸时,c(Ca2+ )
③若向CaS 饱和溶液中加入Cu(NO3)2 溶液中,生成一种黑色固体物质,写出该过程中反应的离子方程式:
您最近一年使用:0次



