已知:25℃时,碳酸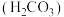 的电离常数
的电离常数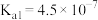 、
、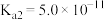 。常温下,向
。常温下,向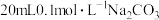 溶液中逐滴加入
溶液中逐滴加入 的盐酸
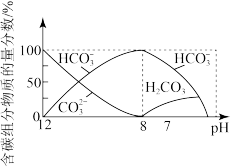
的盐酸 ,溶液中含碳元素各微粒
,溶液中含碳元素各微粒 因逸出未画出
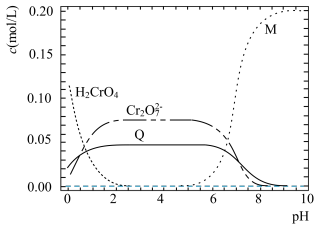
因逸出未画出 的物质的量分数随溶液pH的变化如图所示,下列说法错误的是
的物质的量分数随溶液pH的变化如图所示,下列说法错误的是
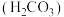 的电离常数
的电离常数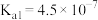 、
、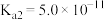 。常温下,向
。常温下,向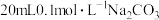 溶液中逐滴加入
溶液中逐滴加入 的盐酸
的盐酸 ,溶液中含碳元素各微粒
,溶液中含碳元素各微粒 因逸出未画出
因逸出未画出 的物质的量分数随溶液pH的变化如图所示,下列说法错误的是
的物质的量分数随溶液pH的变化如图所示,下列说法错误的是
A.随着盐酸的加入,溶液中 的值增大 的值增大 |
B.加入盐酸至溶液 的过程中,水的电离程度逐渐减小 的过程中,水的电离程度逐渐减小 |
C.当 时,溶液中 时,溶液中 |
D.当溶液中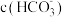 : :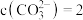 :1时,溶液的 :1时,溶液的 |
更新时间:2020-01-22 10:19:16
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】常温常压下,丙二酸(HOOCCH2COOH)的电离常数为Ka1=1.4×10-3,Ka1=2.0×10-6。向10mL某浓度的丙二酸溶液中滴加0.2mol • L-1NaOH溶液,在滴加过程中下列有关说法不正确的是
| A.在中和反应未完成前随着NaOH溶液的滴加,-OOCCH2COO-的物质的量浓度逐渐升高 |
| B.若滴入的NaOH溶液的体积为10ml时溶液温度最高,则丙二酸的物质的量浓度= 0.1mol·L-1 |
| C.在丙二酸未完全中和前,随着NaOH的滴加,水的电离程度逐渐增大 |
| D.若忽略丙二酸氢根离子的电离和水解,丙二酸根离子的水解常数约为7.14×10-12 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】 时,某酸
时,某酸 溶液中存在的各种含R元素微粒在总浓度中所占分数
溶液中存在的各种含R元素微粒在总浓度中所占分数 随溶液
随溶液 的变化关系如图所示。下列叙述不正确的是
的变化关系如图所示。下列叙述不正确的是

 时,某酸
时,某酸 溶液中存在的各种含R元素微粒在总浓度中所占分数
溶液中存在的各种含R元素微粒在总浓度中所占分数 随溶液
随溶液 的变化关系如图所示。下列叙述不正确的是
的变化关系如图所示。下列叙述不正确的是
A. 的数量级为 的数量级为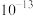 |
B. 溶液中, 溶液中, |
C.若 ,则 ,则 |
D. 易与溶液中的 易与溶液中的 形成沉淀, 形成沉淀, 时 时 恰好沉淀完全 恰好沉淀完全 ,此时 ,此时 ( ( 的 的 为 为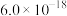 ) ) |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
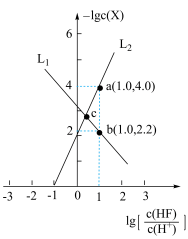
【推荐1】已知 属于难溶于水、可溶于酸的盐。常温下,用HCl调节
属于难溶于水、可溶于酸的盐。常温下,用HCl调节 浊液的pH,测得在不同pH条件下,体系中
浊液的pH,测得在不同pH条件下,体系中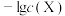 (X为
(X为 或
或 )与
)与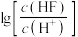 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 属于难溶于水、可溶于酸的盐。常温下,用HCl调节
属于难溶于水、可溶于酸的盐。常温下,用HCl调节 浊液的pH,测得在不同pH条件下,体系中
浊液的pH,测得在不同pH条件下,体系中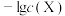 (X为
(X为 或
或 )与
)与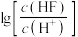 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A. 代表 代表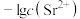 与 与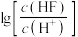 的变化曲线 的变化曲线 |
B.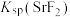 的数量级为 的数量级为 |
C.a、c两点的溶液中均存在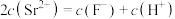 |
D.c点的溶液中存在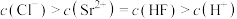 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】室温下,通过下列实验探究Na2CO3的性质。已知:25℃时,H2SO3的Ka1=1.4×10-2、Ka2=1.0×10-7,H2CO3的Ka1=4.3×10-7、Ka2=5.6×10-11。
实验1:配制50mL0.1mol·L-1Na2CO3溶液,测得溶液pH约为12;
实验2:取10mL0.1mol·L-1Na2CO3溶液,向其中加入一定量CaSO4固体充分搅拌,一段时间后过滤,向滤渣中加入足量稀盐酸,固体部分溶解;
实验3:取10mL0.1mol·L-1Na2CO3溶液,向其中缓慢滴入等体积0.1mol·L-1稀盐酸。
下列说法正确的是
实验1:配制50mL0.1mol·L-1Na2CO3溶液,测得溶液pH约为12;
实验2:取10mL0.1mol·L-1Na2CO3溶液,向其中加入一定量CaSO4固体充分搅拌,一段时间后过滤,向滤渣中加入足量稀盐酸,固体部分溶解;
实验3:取10mL0.1mol·L-1Na2CO3溶液,向其中缓慢滴入等体积0.1mol·L-1稀盐酸。
下列说法正确的是
A.实验1所得溶液中,c(Na+)<c(CO )+c(HCO )+c(HCO ) ) |
B.实验2,加入稀盐酸后的上层清液中c(Ca2+)=c(SO ) ) |
C.实验3反应后溶液中存在:c(Na+)=c(CO )+c(HCO )+c(HCO )+c(H2CO3) )+c(H2CO3) |
D.25℃时,反应CO +H2SO3⇌HCO +H2SO3⇌HCO +HSO +HSO 的平衡常数K=2.5×108 的平衡常数K=2.5×108 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A.某弱酸的酸式盐NaHA溶液中一定有:c(OH﹣)+2c(A2﹣)=c(H+)+c(H2A) |
| B.0.2 mol•L﹣1 CH3COONa溶液与0.1 mol•L﹣1盐酸等体积混合后的酸性溶液中:c(CH3COO﹣)>c(CH3COOH)>c(Cl﹣)>c(H+) |
C.室温下,向100ml0.5mol/L的Na2CO3溶液中加入0.05molCaO,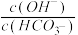 溶液中增大 溶液中增大 |
| D.0.1 mol•L﹣1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3•H2O)+c(Fe2+)=0.3 mol•L﹣1 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】电位滴定法是根据滴定过程中电极电位变化来判断滴定终点的一种滴定分析方法,滴定终点时电极电位发生突变。常温下,利用盐酸滴定某溶液中磷酸钠的含量,其电位滴定曲线与pH曲线如图所示。下列说法不正确的是

已知:磷酸Ka1=6.9×10-3、Ka2=6.2×10-8、Ka3=4.8×10-13

已知:磷酸Ka1=6.9×10-3、Ka2=6.2×10-8、Ka3=4.8×10-13
A.a点溶液中存在:c(Cl-)>c( )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
B.b点对应的溶液中存在:c(H+)+c(H3PO4)=c(OH-)+c( )+2c( )+2c( ) ) |
C.c点对应的溶液中存在:c(H+)=c( )+2c( )+2c( )+3c( )+3c( )+c(OH-) )+c(OH-) |
| D.水的电离程度:a<b<c |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】将 溶液滴加到己二酸
溶液滴加到己二酸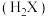 溶液中,混合溶液的
溶液中,混合溶液的 与离子浓度变化的关系如图所示。下列叙述错误的是
与离子浓度变化的关系如图所示。下列叙述错误的是

 溶液滴加到己二酸
溶液滴加到己二酸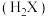 溶液中,混合溶液的
溶液中,混合溶液的 与离子浓度变化的关系如图所示。下列叙述错误的是
与离子浓度变化的关系如图所示。下列叙述错误的是
A.当混合溶液呈中性时,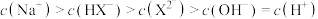 |
B.曲线 表示 表示 与 与 的变化关系 的变化关系 |
C. 溶液中 溶液中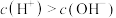 |
D. 的数量级为 的数量级为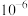 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
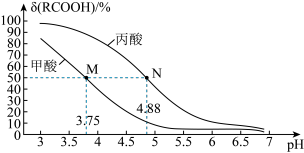
【推荐3】25 ℃时,改变0.1 mol/L弱酸RCOOH溶液的pH,溶液中RCOOH分子的物质的量分数δ(RCOOH)随之改变[已知δ(RCOOH)=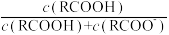 ],甲酸(HCOOH)与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是
],甲酸(HCOOH)与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是
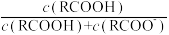 ],甲酸(HCOOH)与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是
],甲酸(HCOOH)与丙酸(CH3CH2COOH)溶液中δ(RCOOH)与pH的关系如图所示。下列说法正确的是
| A.若弱酸pH增大是通过向弱酸中加入NaOH固体实现的,则图中M、N两点对应溶液中的c(Na+)相等 |
| B.对于甲酸和丙酸,当lg[c(RCOOH)/c(RCOO-)]>0时,溶液都为酸性 |
| C.等浓度的HCOONa和CH3CH2COONa两种溶液中的c(NaOH)相等 |
| D.将0.1 mol/L的HCOOH溶液与0.1 mol/L的HCOONa溶液等体积混合,所得溶液中:c(Na+)>c(HCOOH)>c(HCOO-)>c(OH-)>c(H+) |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐1】常温下,将0.1mol·L-1NaOH溶液滴加到一定浓度的二元酸(H2R)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
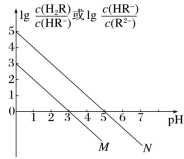

A.线N表示pH与lg 的变化关系 的变化关系 |
| B.当溶液中c(HR-)=c(R2-)时,pH=3 |
| C.NaHR溶液中c(H+)>c(OH-) |
| D.当混合溶液呈中性时,c(Na+)<c(H2R)+c(HR-)+c(R2-) |
您最近半年使用:0次
单选题
|
较难
(0.4)
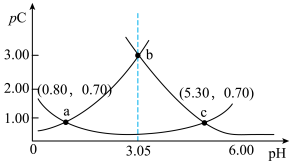
【推荐2】常温下,某浓度 溶液中滴加
溶液中滴加 溶液,若定义
溶液,若定义 ,则测得
,则测得 、
、 、
、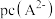 变化如图所示。下列说法
变化如图所示。下列说法不正确 的是。
 溶液中滴加
溶液中滴加 溶液,若定义
溶液,若定义 ,则测得
,则测得 、
、 、
、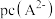 变化如图所示。下列说法
变化如图所示。下列说法
A.曲线Ⅱ表示 随pH的变化 随pH的变化 |
B.常温下,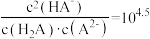 |
C.将等浓度等体积的 与 与 溶液混合后,溶液显酸性 溶液混合后,溶液显酸性 |
D.a、b、c三点对应的溶液,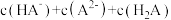 始终不变 始终不变 |
您最近半年使用:0次

 ,简记为
,简记为 ]为二元弱酸。常温下,在含
]为二元弱酸。常温下,在含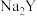 、
、 的溶液中滴加盐酸,混合液pX[pX=-lgX,
的溶液中滴加盐酸,混合液pX[pX=-lgX, 、
、 、
、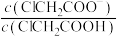 、
、 ]与pH关系如图所示。直线
]与pH关系如图所示。直线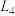 代表
代表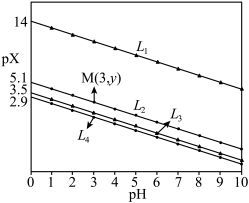
 、
、 分别代表
分别代表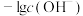 、
、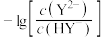 与pH关系
与pH关系 电离常数的数量级为
电离常数的数量级为 ,M点的坐标为
,M点的坐标为
 溶液中:
溶液中:
 的平衡常数K约为
的平衡常数K约为
 、
、 和
和 的分布曲线如图所示。
的分布曲线如图所示。