常温下有H2RO4=H++HRO4-、HRO4-⇌H++RO42-,现有物质的量浓度都为0.1mol∙L-1的三种溶液:①NaHRO4溶液;②H2RO4溶液;③Na2RO4溶液。下列说法中正确的是( )
| A.②和③等体积混合后的溶液中:c(Na+)=c(HRO4-)+c(H2RO4)+c(RO42-) |
| B.100mL①溶液中:n(HRO4-)+n(RO42-)+n(OH-) -n(H+)=0.01mol |
| C.①和②等体积混合后的溶液中离子浓度大小顺序为c(H+)>c(HRO4-)>c(Na+) |
| D.若①和③等体积混合后,会抑制水的电离,则HRO4-的电离程度肯定大于RO42-的水解程度 |
更新时间:2020-02-07 18:04:26
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加德罗常数的值,下列说法正确的是
A.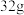 甲醇分子中含有的 甲醇分子中含有的 键数为4NA 键数为4NA |
B.电解精炼铜,若阳极质量减少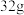 ,转移电子数一定为NA ,转移电子数一定为NA |
C. 羟基含有的电子数为10NA 羟基含有的电子数为10NA |
D.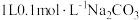 溶液中阴离子数大于0.1NA 溶液中阴离子数大于0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】等物质的量浓度的下列五种溶液:①CH3COONa,②NH4Cl,③NaHSO4,④Na2CO3,⑤Ba(OH)2,溶液的pH由小到大正确的是
| A.②③①④⑤ | B.③②①④⑤ | C.③①②④⑤ | D.③②④①⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】通过滴加相同浓度的盐酸或KOH溶液来调节0.01 mol·L-1 Na2HAsO3溶液的pH,实验测得含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与溶液pH的关系如图所示。

下列有关说法正确的是

下列有关说法正确的是
A.NaH2AsO3溶于水,所得溶液中H2AsO 的水解程度小于其电离程度 的水解程度小于其电离程度 |
| B.K1(H3AsO3)的数量级为10-9 |
| C.水的电离程度:a点大于b点 |
D.c点溶液中存在:c(Na+)=2c(H2AsO )+4c(HAsO )+4c(HAsO )+2c(AsO )+2c(AsO ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知:Ka1(H2SO3)=1.0×10-1.85、Ka2(H2SO3)=1.0×10-7。通过0.1mol·L−1NaOH溶液滴定20 mL0.1mol·L−1H2SO3溶液实验探究H2SO3、Na2SO3、NaHSO3溶液的性质。
实验1:滴入10 mL 0.1mol·L−1NaOH溶液时测得溶液的pH=1.85。
实验2:向实验1所得溶液中继续滴入10 mL 0.1mol·L−1NaOH溶液时无明显现象。
实验3:向实验2所得溶液中通入NH3至溶液pH=7(通入气体对溶液体积的影响可忽略)。
实验4:向实验2所得溶液中滴加HNO3酸化的Ba(NO3)2溶液,产生白色沉淀。
下列说法正确的是
实验1:滴入10 mL 0.1mol·L−1NaOH溶液时测得溶液的pH=1.85。
实验2:向实验1所得溶液中继续滴入10 mL 0.1mol·L−1NaOH溶液时无明显现象。
实验3:向实验2所得溶液中通入NH3至溶液pH=7(通入气体对溶液体积的影响可忽略)。
实验4:向实验2所得溶液中滴加HNO3酸化的Ba(NO3)2溶液,产生白色沉淀。
下列说法正确的是
A.实验1溶液中存在:2c(H2SO3)+ c(SO )=0.1 mol·L−1 )=0.1 mol·L−1 |
B.实验2溶液中存在:c(Na+)>c(HSO )>c(SO )>c(SO )>c(H2SO3) )>c(H2SO3) |
C.实验3溶液中存在:c(Na+)>c(NH )>c(SO )>c(SO ) ) |
D.实验4反应后静置所得上层清液中一定有:c(Ba2+)×c(SO )=Ksp(BaSO3) )=Ksp(BaSO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列溶液中各微粒的浓度关系不正确的是
| A.0.1mol·L-1HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) |
B.1L0.1mol•L-1CuSO4•(NH4)2SO4•6H2O溶液中:c( )>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) )>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) |
| C.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
D.0.1mol·L-1NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)>c( )+c( )+c( )+c(OH-) )+c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温时,向20mL0.1mol•L-1的两种酸HA、HB中分别滴加0.1mol•L-1NaOH溶液,其pH变化分别对应如图中的I、II。下列说法正确的是


| A.a点溶液中微粒浓度:c(A-)>c(Na+)>c(HA) |
| B.HB的酸性比HA强,HA的电离常数Ka约为10-7 |
| C.滴加NaOH溶液至pH=7时,两种溶液中c(A-)=c(B-) |
| D.滴加至20mLNaOH溶液时,II中H2O的电离程度大于I |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据下表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是
| 化学式 | 电离常数 |
| HClO | Ka=3×10-8mol·L-1 |
| H2CO3 | Ka1=4.3×10-7mol·L-1 |
| Ka2=5.6×10-11mol·L-1 |
A.c( )>c(ClO-)>c(OH-) )>c(ClO-)>c(OH-) | B. c(HClO)+c(ClO-)=c( )+c(H2CO3) )+c(H2CO3) |
C.c(ClO-)>c( )>c(H+) )>c(H+) | D.c(Na+)+c(H+)=c( )+c(ClO-)+c(OH-) )+c(ClO-)+c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,下列溶液中的微粒浓度关系正确的是:
| A.pH=3的盐酸和pH=11的氨水等体积混合:c(NH4+)=c(Cl-)>c(H+)=c(OH-) |
| B.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+ c(OH-) |
| C.pH=8.3的NaHCO3溶液c(Na+)>c(HCO3-)> c(H2CO3) > c(CO32-) |
| D.0.2mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合:2c(H+)—c(OH-)=c(CH3COO-)—c(CH3COOH) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】复分解反应存在这样一个规律:较强酸可制取较弱酸。盐类的水解也是复分解反应,弱酸强碱盐对应的弱酸越弱,其盐越容易发生水解。已知在常温下测得浓度均为0.1mol·L-1的5种溶液的pH:
请根据上述信息判断下列反应不能发生的是 ( )
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.1 | 8.8 | 11.6 | 10.3 | 11.1 |
请根据上述信息判断下列反应不能发生的是 ( )
| A.CO2+H2O+2NaClO=Na2CO3+2HClO |
| B.CO2+H2O+ NaClO= NaHCO3+HClO |
| C.CH3COOH+ NaCN= CH3COONa+ HCN |
| D.CH3COOH+Na2CO3=NaHCO3+CH3COONa |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关说法正确的是
| A.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
| B.等物质的量浓度的CH3COOH溶液和HCl溶液中,水的电离程度相同 |
| C.0.1 mol/LNa2CO3溶液:c(OH-)=c(H2CO3)+c(HCO3-)+c(H+) |
D.对于反应2SO2+O2  2SO3,使用催化剂能加快反应速率和提高SO2平衡转化率 2SO3,使用催化剂能加快反应速率和提高SO2平衡转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用0.1000 mol·L−1NaOH溶液滴定20.00 mL 0.1000 mol·L−1的H3A溶液的滴定曲线如图所示。已知H3A的pKa1、pKa2、pKa3分别为2、7和12(pKa=-lgKa),下列说法正确的是
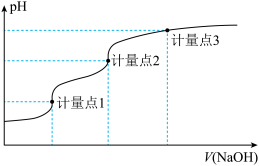

| A.滴定前溶液pH值约为3 |
| B.计量点1时,可以用甲基橙作为指示剂 |
| C.到达计量点2时,溶液中存在c(Na+)=c(H2A-)+2c(HA2-)+3c(A3-) |
D.到达计量点3时,微热溶液, 会增大 会增大 |
您最近一年使用:0次

 的值减小
的值减小

