制取水煤气反应C(s)+H2O(g)⇌CO(g)+H2(g),化学平衡常数表示为K=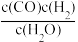 ,有关化学平衡常数说法正确的是( )
,有关化学平衡常数说法正确的是( )
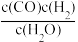 ,有关化学平衡常数说法正确的是( )
,有关化学平衡常数说法正确的是( )| A.由表达式可知c(CO)与c(CO)增大时,K值增大 |
| B.其他条件不变时,温度升高,K值增大 |
| C.化学平衡向右移动,K值增大 |
| D.K值变化,化学平衡一定发生了移动 |
更新时间:2020-03-11 09:57:47
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】已知: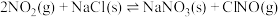
 ,下列说法正确的是
,下列说法正确的是
A.该反应的平衡常数可表达为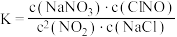 |
| B.该反应一定能自发进行 |
C.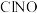 分子的VSEPR模型名称为平面三角形 分子的VSEPR模型名称为平面三角形 |
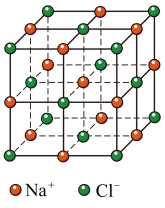
D. 晶胞(如图所示)中每个 晶胞(如图所示)中每个 周围与其距离最近的 周围与其距离最近的 有12个 有12个 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】在密闭容器中充入足量的FeO(s)和适量O2(g),在一定条件下发生反应6FeO(s)+O2(g) 2Fe3O4(s) ΔH<0,达到平衡时,测得O2浓度为a mol·L-1;保持温度不变,缩小体积至原来的四分之一,重新达到平衡时,测得O2浓度为c mol·L-1,下列有关说法正确的是
2Fe3O4(s) ΔH<0,达到平衡时,测得O2浓度为a mol·L-1;保持温度不变,缩小体积至原来的四分之一,重新达到平衡时,测得O2浓度为c mol·L-1,下列有关说法正确的是
 2Fe3O4(s) ΔH<0,达到平衡时,测得O2浓度为a mol·L-1;保持温度不变,缩小体积至原来的四分之一,重新达到平衡时,测得O2浓度为c mol·L-1,下列有关说法正确的是
2Fe3O4(s) ΔH<0,达到平衡时,测得O2浓度为a mol·L-1;保持温度不变,缩小体积至原来的四分之一,重新达到平衡时,测得O2浓度为c mol·L-1,下列有关说法正确的是| A.上述反应为熵减反应,在较低温度下能自发进行 |
| B.恒温恒容条件下平衡后,再充入O2,O2的平衡转化率减小 |
| C.当FeO(s)或Fe3O4(s)的物质的量保持不变时达到平衡状态 |
| D.温度不变,达到新平衡时,c=4a |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】298K温度下,CuSO4·5H2O脱水的平衡压力为:
平衡关系表明:若p(H2O)>1.04kPa,CuSO4·5H2O不分解;p(H2O)=1.04kPa表明CuSO4·5H2O和CuSO4·3H2O处于平衡。则当
| 化 学 反 应 | p(H2O)/kPa |
(1)CuSO4·5H2O(s) CuSO4·3H2O(s)+2H2O(g) CuSO4·3H2O(s)+2H2O(g) | 1.04 |
(2)CuSO4·3H2O(s) CuSO4·H2O(s)+2H2O(g) CuSO4·H2O(s)+2H2O(g) | 0.75 |
(3)CuSO4·H2O(s) CuSO4(s)+H2O(g) CuSO4(s)+H2O(g) | 0.11 |
| A.p(H2O)=0.75 kPa时,CuSO4·3H2O不分解 |
| B.p(H2O)≤0.11 kPa时,CuSO4·H2O和CuSO4处于平衡 |
| C.0.75kPa>p(H2O)>0.11kPa时,是CuSO4·H2O的稳定区 |
| D.1.04kPa>p(H2O)>0.75kPa时,体系中不存在CuSO4·5H2O、CuSO4·H2O和CuSO4 |
您最近一年使用:0次
【推荐1】近日,北京航空航天大学教授团队与中科院高能物理研究所合作,合成了Y、Sc(Y1/NC,Sc1/NC)单原子催化剂,用于常温常压下的电化学催化氢气还原氮气的反应。反应历程与相对能量模拟计算结果如图所示(*表示稀土单原子催化剂)。下列说法错误的是
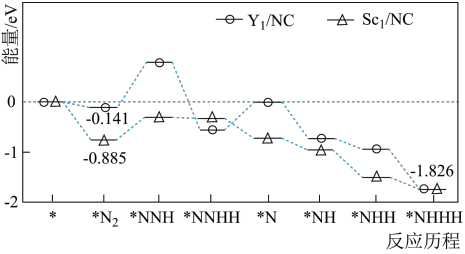

| A.相同条件下,两种催化反应的焓变相同 |
| B.实际生产中将催化剂的尺寸处理成纳米级颗粒可提高氨气的平衡转化率 |
| C.使用Sc1/NC单原子催化剂的反应历程中,最大能垒的反应过程可表示为*N2+H→*NNH |
| D.升高温度一定可以提高氨气单位时间内的产率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】目前,常利用催化技术将汽车尾气中的 和
和 转化为
转化为 和
和 。为研究反应条件对该化学反应的影响,某课题组按下表数据进行了实验探究。实验中使用了等质量的同种催化剂,测得
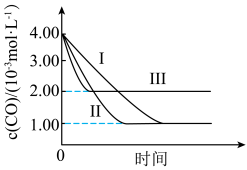
。为研究反应条件对该化学反应的影响,某课题组按下表数据进行了实验探究。实验中使用了等质量的同种催化剂,测得 的浓度随时间的变化如图所示。下列说法不正确的是
的浓度随时间的变化如图所示。下列说法不正确的是
 和
和 转化为
转化为 和
和 。为研究反应条件对该化学反应的影响,某课题组按下表数据进行了实验探究。实验中使用了等质量的同种催化剂,测得
。为研究反应条件对该化学反应的影响,某课题组按下表数据进行了实验探究。实验中使用了等质量的同种催化剂,测得 的浓度随时间的变化如图所示。下列说法不正确的是
的浓度随时间的变化如图所示。下列说法不正确的是
| 编号 | 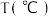 | 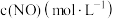 | 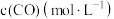 | 催化剂的比表面积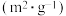 |
| Ⅰ | 280 | 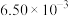 | 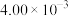 | 80.0 |
| Ⅱ | 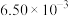 | 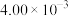 | 120 | |
| Ⅲ | 360 | 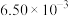 | 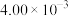 | 80.0 |
A.实验Ⅱ的反应温度为 |
| B.由实验Ⅰ、Ⅱ可知,增大催化剂的比表面积,该化学反应速率增大 |
C.实验Ⅰ达到平衡时, 的浓度为 的浓度为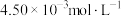 |
D.该反应的反应热 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
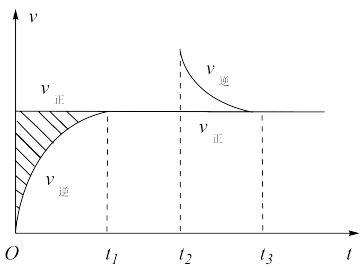
【推荐1】恒温密闭容器发生可逆反应:Z(?)+W(?) X(g)+Y(?) △H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后不再改变条件。下列有关说法中,正确的是
X(g)+Y(?) △H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后不再改变条件。下列有关说法中,正确的是
 X(g)+Y(?) △H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后不再改变条件。下列有关说法中,正确的是
X(g)+Y(?) △H,在t1时刻反应达到平衡,在t2时刻缩小容器体积,t3时刻再次达到平衡状态后不再改变条件。下列有关说法中,正确的是
| A.该条件下,Z和W中的一种可能为气态 |
| B.t1~t2时间段与t3时刻后,两时间段反应体系中气体的平均摩尔质量相等 |
| C.若在该温度此反应平衡常数表达式为K=c(X),则t1~t2时间段与t3时刻后的X浓度不相等 |
| D.若该反应△H>0,则该反应的平衡常数K随温度升高而增大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】Bodensteins 研究了反应 2HI(g) I2(g)+H2(g),某温度下的上述反应中,正反应速率为υ正=k正c2(HI),逆反应速率为υ逆=k逆c(I2)·c(H2),k=A·e-Ea/RT,其中k正、k逆为速率常数,根据以上内容得出的结论,正确的是
I2(g)+H2(g),某温度下的上述反应中,正反应速率为υ正=k正c2(HI),逆反应速率为υ逆=k逆c(I2)·c(H2),k=A·e-Ea/RT,其中k正、k逆为速率常数,根据以上内容得出的结论,正确的是
 I2(g)+H2(g),某温度下的上述反应中,正反应速率为υ正=k正c2(HI),逆反应速率为υ逆=k逆c(I2)·c(H2),k=A·e-Ea/RT,其中k正、k逆为速率常数,根据以上内容得出的结论,正确的是
I2(g)+H2(g),某温度下的上述反应中,正反应速率为υ正=k正c2(HI),逆反应速率为υ逆=k逆c(I2)·c(H2),k=A·e-Ea/RT,其中k正、k逆为速率常数,根据以上内容得出的结论,正确的是| A.反应物浓度越大,正反应速率越大 |
| B.使用催化剂,反应的υ正增大、υ逆减小 |
C.该反应的平衡常数K =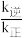 |
| D.由k=A·e-Ea/RT可知,速率常数的大小与温度、活化能有关 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】为了模拟汽车尾气的净化,向密闭容器中投入一定量的CO和O2,在催化剂(I型、II型)和不同温度下发生反应:2CO(g)+O2(g) 2CO2(g),反应进行相同时间t(s),测得CO转化率与温度的关系曲线如图所示。下列说法正确的是
2CO2(g),反应进行相同时间t(s),测得CO转化率与温度的关系曲线如图所示。下列说法正确的是
 2CO2(g),反应进行相同时间t(s),测得CO转化率与温度的关系曲线如图所示。下列说法正确的是
2CO2(g),反应进行相同时间t(s),测得CO转化率与温度的关系曲线如图所示。下列说法正确的是
| A.该反应在a、b两点对应的平衡常数大小关系:Ka>Kb |
| B.b点转化率明显下降最主要原因是温度升高催化剂失活 |
| C.在实验中CO平衡转化率达到阴影部分数值只能采用延长反应时间的方案 |
D.50℃、t s时容器中O2浓度为0.01 mol/L,该温度下反反应平衡常数为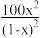 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】SO2的氧化是工业制硫酸中的一步重要反应:2SO2(g)+O2(g)=2SO3(g) △H(△H<0)。如果反应在密闭容器中进行,达到平衡后,以下说法中,正确的是
| A.升高温度,正反应速率增大,化学平衡常数增大 |
| B.增加压强,平衡会向右移动 |
| C.加入催化剂后,正逆反应速率均不变,平衡不移动 |
| D.达到平衡状态时,SO2的消耗速率与SO2的生成速率相等 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】在同一温度下,在3个容积均为1.0 L的恒容密闭容器中发生反应:PCl5(g) PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是
 PCl3(g)+Cl2(g)。下列说法错误的是
PCl3(g)+Cl2(g)。下列说法错误的是| 容器编号 | 物质的起始浓度/(mol/L) | 物质的平衡浓度/(mol/L) | ||
| c(PCl5) | c(PCl3) | c(Cl2) | c(Cl2) | |
| I | 0.4 | 0 | 0 | 0.2 |
| II | 0.6 | 0 | 0.2 | |
| III | 0.8 | 0 | 0 | |
A.反应达到平衡时,容器I中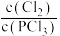 比容器II中的大 比容器II中的大 |
| B.反应达到平衡时,容器I与容器II中的总压强之比为3∶4 |
C.反应达到平衡时,容器III中Cl2的体积分数小于 |
| D.反应达到平衡时,容器III中0.4 mol/L<c(PCl5)<0.8 mol/L |
您最近一年使用:0次

 3C(?)+D(?)
3C(?)+D(?)



