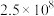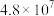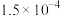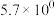雾霾由多种污染物形成,包含颗粒物(PM2.5)、氮氧化物(NOx)、CO、SO2等。化学在解决雾霾污染中有着重要的作用。
(1)已知:①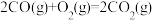 ΔH1=-566.0 kJ·mol-1②
ΔH1=-566.0 kJ·mol-1②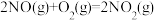 ΔH2=-116.5 kJ·mol-1③
ΔH2=-116.5 kJ·mol-1③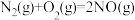 ΔH3=+180.5 kJ·mol-1,废气中NO2与CO 转化成无污染气体的热化学方程式为
ΔH3=+180.5 kJ·mol-1,废气中NO2与CO 转化成无污染气体的热化学方程式为____ 。
(2)研究发现利用NH3可除去硝酸工业尾气中的NO。NH3与NO的物质的量之比分别为1∶2、1∶1.5、3∶1时,NO脱除率随温度变化的曲线如图所示。
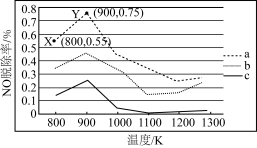
①曲线a中,NO的起始浓度为6×10-4mg·m-3,从X点到Y点经过10 s,则该时间段内NO的脱除速率为___________ mg· m-3·s-1。
②曲线c对应的NH3与NO的物质的量之比是___ ,其理由是___ 。
(3)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化氧可以快速氧化SO2。活化过程的能量变化模拟计算结果如图所示。

无水情况下,一个氧分子的活化能为__ ,容易活化氧分子的条件是___ (填“有水”或“无水”)。
(4)利用反应 构成的电池既能有效消除氮氧化物的排放,减轻雾霾污染,又能充分利用化学能,装置如图所示。
构成的电池既能有效消除氮氧化物的排放,减轻雾霾污染,又能充分利用化学能,装置如图所示。

①B极的电极反应式为___ 。
②若反应转移1.2 mol电子,A极生成N2的体积为___ L(标准状况)。
(1)已知:①
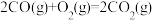 ΔH1=-566.0 kJ·mol-1②
ΔH1=-566.0 kJ·mol-1②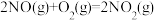 ΔH2=-116.5 kJ·mol-1③
ΔH2=-116.5 kJ·mol-1③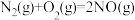 ΔH3=+180.5 kJ·mol-1,废气中NO2与CO 转化成无污染气体的热化学方程式为
ΔH3=+180.5 kJ·mol-1,废气中NO2与CO 转化成无污染气体的热化学方程式为(2)研究发现利用NH3可除去硝酸工业尾气中的NO。NH3与NO的物质的量之比分别为1∶2、1∶1.5、3∶1时,NO脱除率随温度变化的曲线如图所示。

①曲线a中,NO的起始浓度为6×10-4mg·m-3,从X点到Y点经过10 s,则该时间段内NO的脱除速率为
②曲线c对应的NH3与NO的物质的量之比是
(3)炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化氧可以快速氧化SO2。活化过程的能量变化模拟计算结果如图所示。

无水情况下,一个氧分子的活化能为
(4)利用反应
 构成的电池既能有效消除氮氧化物的排放,减轻雾霾污染,又能充分利用化学能,装置如图所示。
构成的电池既能有效消除氮氧化物的排放,减轻雾霾污染,又能充分利用化学能,装置如图所示。
①B极的电极反应式为
②若反应转移1.2 mol电子,A极生成N2的体积为
更新时间:2020-04-06 09:00:45
|
相似题推荐
【推荐1】氢能是一种极具发展潜力的清洁能源。
(1)氢气的制取与储存是氢能源利用领域的研究热点.
已知:①CH4的燃烧热为890KJ·mol-1; ②H2的热值为50.2kJ·g-1
则甲烷部分氧化生成CO2和H2的热化学方程式为___________________________________ ;该反应自发进行的条件是___________ 。
(2)Bodensteins研究了如下反应:2HI(g) H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
①根据上述实验结果,该反应的平衡常数K的计算式为:___________ 。
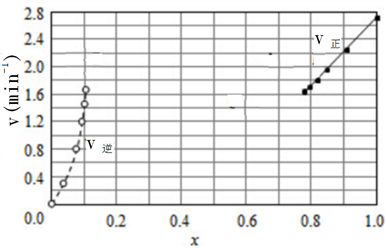
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,若k正=9.00min-1,在t=20min时,v逆=__________ min-1(保留三位有效数字)
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。在上述平衡基础上,缓慢升高到某一温度,反应重新达到平衡,请在下图中画出此过程的趋势图。______________
(3)一种可超快充电的新型铝电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,放电时负极Al的电极反应式为______________________ 。
(1)氢气的制取与储存是氢能源利用领域的研究热点.
已知:①CH4的燃烧热为890KJ·mol-1; ②H2的热值为50.2kJ·g-1
则甲烷部分氧化生成CO2和H2的热化学方程式为
(2)Bodensteins研究了如下反应:2HI(g)
 H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
H2(g)+I2(g)△H=+11kJ/mol在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| X(HI) | 1.00 | 0.910 | 0.850 | 0.815 | 0.795 | 0.784 |
| X(HI) | 0.00 | 0.600 | 0.730 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,若k正=9.00min-1,在t=20min时,v逆=
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。在上述平衡基础上,缓慢升高到某一温度,反应重新达到平衡,请在下图中画出此过程的趋势图。

(3)一种可超快充电的新型铝电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其它离子不参与电极反应,放电时负极Al的电极反应式为
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】载氧体化学链燃烧技术(CLC)是一种燃烧效率更高的新技术。以 为燃料气,
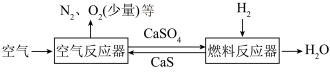
为燃料气, 为载氧体的CLC体系的工作原理如图所示。
为载氧体的CLC体系的工作原理如图所示。
已知:“燃料反应器”中发生反应的热化学方程式为
反应1
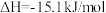 。
。
(1)该CLC体系反应条件下: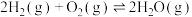
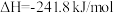 ,则“空气反应器”中发生反应
,则“空气反应器”中发生反应 的
的 为
为______ 。
(2)随着温度的升高,“燃料反应器”中还可能发生如下副反应:
反应2: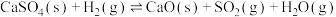

武汉某大学教育部重点实验室利用HSC软件绘制出1mol 和1mol
和1mol  在不同温度下反应平衡体系中部分物质的组成如图所示:
在不同温度下反应平衡体系中部分物质的组成如图所示:
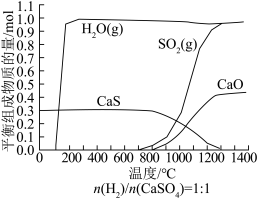
①该CLC体系工作时,“燃料反应器”中应该采用______ (填标号),否则不但会影响燃烧效率而且会有污染物生成。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
②在标准状态下,“ ”是化学反应等温式的一种表达形式,其中
”是化学反应等温式的一种表达形式,其中 、
、 可以视为与温度无关的定值,R是常数。我国研究人员根据化学反应等温式利用HSC软件计算出不同温度下反应1的平衡常数
可以视为与温度无关的定值,R是常数。我国研究人员根据化学反应等温式利用HSC软件计算出不同温度下反应1的平衡常数 和反应2的平衡常数
和反应2的平衡常数 如下:
如下:
ⅰ.比较
______ 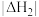 (填“>”或“<”)理由是
(填“>”或“<”)理由是______ 。
ⅱ.1000℃时,平衡体系中 和
和 的物质的量分别为
的物质的量分别为______ mol和______ mol。
ⅲ.保持1000℃不变,将“燃料反应器”的容积压缩,重新达到平衡后, 、
、 的物质的量的变化情况为:
的物质的量的变化情况为:
______ ,
______ (填“增大”“减小”或“不变”)。
 为燃料气,
为燃料气, 为载氧体的CLC体系的工作原理如图所示。
为载氧体的CLC体系的工作原理如图所示。
已知:“燃料反应器”中发生反应的热化学方程式为
反应1

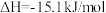 。
。(1)该CLC体系反应条件下:
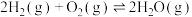
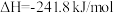 ,则“空气反应器”中发生反应
,则“空气反应器”中发生反应 的
的 为
为(2)随着温度的升高,“燃料反应器”中还可能发生如下副反应:
反应2:
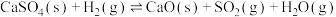

武汉某大学教育部重点实验室利用HSC软件绘制出1mol
 和1mol
和1mol  在不同温度下反应平衡体系中部分物质的组成如图所示:
在不同温度下反应平衡体系中部分物质的组成如图所示:
①该CLC体系工作时,“燃料反应器”中应该采用
A.高温高压 B.高温低压 C.低温高压 D.低温低压
②在标准状态下,“
 ”是化学反应等温式的一种表达形式,其中
”是化学反应等温式的一种表达形式,其中 、
、 可以视为与温度无关的定值,R是常数。我国研究人员根据化学反应等温式利用HSC软件计算出不同温度下反应1的平衡常数
可以视为与温度无关的定值,R是常数。我国研究人员根据化学反应等温式利用HSC软件计算出不同温度下反应1的平衡常数 和反应2的平衡常数
和反应2的平衡常数 如下:
如下:温度/℃ | 600 | 800 | 1000 | 1200 |
|
|
|
|
|
|
|
|
|
|

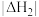 (填“>”或“<”)理由是
(填“>”或“<”)理由是ⅱ.1000℃时,平衡体系中
 和
和 的物质的量分别为
的物质的量分别为ⅲ.保持1000℃不变,将“燃料反应器”的容积压缩,重新达到平衡后,
 、
、 的物质的量的变化情况为:
的物质的量的变化情况为:

您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】研究大气污染物SO2、CH3OH与H2O之间的反应,有利于揭示雾霾的形成机理。
反应i: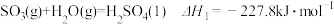
反应ii:
(1)CH3OSO3H发生水解: △H=
△H=______ kJ/mol。
(2)T℃时,反应ii的CH3OH(g)、SO3(g)的初始浓度分别为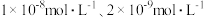 ,平衡时SO3转化率为0.04%,则K=
,平衡时SO3转化率为0.04%,则K=_____________ 。
(3)我国科学家利用计算机模拟计算,分别研究反应ii在无水和有水条件下的反应历程,如图所示,其中分子间的静电作用力用“…”表示。

①分子间的静电作用力最强的是_____________ (填“a”、“b”或“c”)。
②水将反应ii的最高能垒由_____________ eV降为_____________ eV。
③d到f转化的实质为质子转移,该过程断裂的化学键为____ (填标号)。
A.CH3OH中的氢氧键B.CH3OH中的碳氧键
C.H2O中的氢氧键D.SO3中的硫氧键
(4)分别研究大气中H2O、CH3OH的浓度对反应i、反应ii产物浓度的影响,结果如图所示。
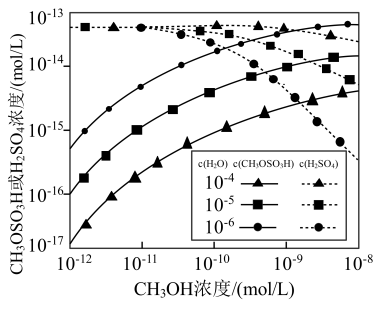
①当c(CH3OH)大于10-11mol.L-1时,c(CH3OH)越大,c(H2SO4)越小的原因是_____________ 。
②当c(CH3OH)小于10-11mol.L-1时,c(H2O)越大,c(CH3OSO3H)越小的原因是_____________ 。
反应i:
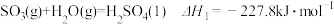
反应ii:

(1)CH3OSO3H发生水解:
 △H=
△H=(2)T℃时,反应ii的CH3OH(g)、SO3(g)的初始浓度分别为
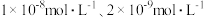 ,平衡时SO3转化率为0.04%,则K=
,平衡时SO3转化率为0.04%,则K=(3)我国科学家利用计算机模拟计算,分别研究反应ii在无水和有水条件下的反应历程,如图所示,其中分子间的静电作用力用“…”表示。

①分子间的静电作用力最强的是
②水将反应ii的最高能垒由
③d到f转化的实质为质子转移,该过程断裂的化学键为
A.CH3OH中的氢氧键B.CH3OH中的碳氧键
C.H2O中的氢氧键D.SO3中的硫氧键
(4)分别研究大气中H2O、CH3OH的浓度对反应i、反应ii产物浓度的影响,结果如图所示。

①当c(CH3OH)大于10-11mol.L-1时,c(CH3OH)越大,c(H2SO4)越小的原因是
②当c(CH3OH)小于10-11mol.L-1时,c(H2O)越大,c(CH3OSO3H)越小的原因是
您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验。
(1)请完成以下实验设计表(表中不要留空格)。
[数据处理]实验测得p-CP的浓度随时间变化的关系如下图。
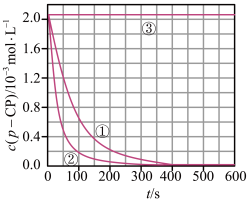
(2)请根据右上图实验①曲线,计算降解反应在50-150s内的反应速率:v(p-CP)=_______________ 。
[解释与结论]
(3)实验①、②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:_____________________ 。
(4)实验③得出的结论是:pH等于10时,_________________________ 。
(5)根据题意:在一定条件下H2O2和Fe2+的离子反应式____________________ 。
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验。
(1)请完成以下实验设计表(表中不要留空格)。
| 实验编号 | 实验目的 | T/K | pH | c/10-3 mol·L-1 | |
| H2O2 | Fe2+ | ||||
① | 为以下实验作参照 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | ||||
| ③ | 298 | 10 | 6.0 | 0.30 | |

(2)请根据右上图实验①曲线,计算降解反应在50-150s内的反应速率:v(p-CP)=
[解释与结论]
(3)实验①、②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:
(4)实验③得出的结论是:pH等于10时,
(5)根据题意:在一定条件下H2O2和Fe2+的离子反应式
您最近半年使用:0次
【推荐2】在一定温度下将2molA气体和4molB气体在2L密闭容器中混合并发生反应:A(g)+2B(g) 3C(g)+D(g)(吸热反应)。若经2min后达到平衡,测得C的平衡浓度为0.6mol/L,回答下列问题:
3C(g)+D(g)(吸热反应)。若经2min后达到平衡,测得C的平衡浓度为0.6mol/L,回答下列问题:
(1)用物质A表示的反应速率为_________ 。
(2)2min时物质B的浓度为________ ,B的平衡转化率为________ 。
(3)当下列哪些项不再发生变化时,表明上述反应已达到平衡状态_______ 。
A. 混合气体的压强
B. 混合气体的密度
C. 混合气体的总物质的量
D. 单位时间内消耗1molB同时生成1.5molC
E. 混合气体的平均相对分子质量
F. 用A、B、C表示的速率比为1:2:3
(4)提高A的转化率,可以采取的措施有_______________ 。
NO2(红棕色)和N2O4(无色)之间发生反应:N2O4(g) NO2(g)。将一定量N2O4气体充入体积为2L的恒容密闭容器中,控制反应温度为T。
NO2(g)。将一定量N2O4气体充入体积为2L的恒容密闭容器中,控制反应温度为T。
(5)该反应为吸热反应,则反应物的化学键断裂要吸收的能量______ (填“>”“<”或“=”)生成物的化学键形成要放出的能量。
(6)下列可以说明该反应达到平衡的是______。
(7)在温度为T的条件下,向该恒容密闭容器中充入0.04mol/L ,
,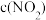 随时间的变化曲线如图所示:
随时间的变化曲线如图所示:
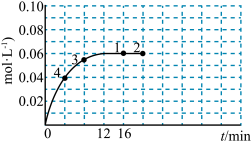
①在图中画出0~16min时间段内, 随时间的变化曲线。
随时间的变化曲线。
②1~4四个点中,v正=v逆的点有__________ 。
 3C(g)+D(g)(吸热反应)。若经2min后达到平衡,测得C的平衡浓度为0.6mol/L,回答下列问题:
3C(g)+D(g)(吸热反应)。若经2min后达到平衡,测得C的平衡浓度为0.6mol/L,回答下列问题:(1)用物质A表示的反应速率为
(2)2min时物质B的浓度为
(3)当下列哪些项不再发生变化时,表明上述反应已达到平衡状态
A. 混合气体的压强
B. 混合气体的密度
C. 混合气体的总物质的量
D. 单位时间内消耗1molB同时生成1.5molC
E. 混合气体的平均相对分子质量
F. 用A、B、C表示的速率比为1:2:3
(4)提高A的转化率,可以采取的措施有
NO2(红棕色)和N2O4(无色)之间发生反应:N2O4(g)
 NO2(g)。将一定量N2O4气体充入体积为2L的恒容密闭容器中,控制反应温度为T。
NO2(g)。将一定量N2O4气体充入体积为2L的恒容密闭容器中,控制反应温度为T。(5)该反应为吸热反应,则反应物的化学键断裂要吸收的能量
(6)下列可以说明该反应达到平衡的是______。
A.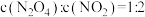 | B.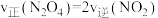 |
| C.容器内气体的颜色不再变化 | D.混合气体的压强不再变化 |
 ,
,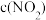 随时间的变化曲线如图所示:
随时间的变化曲线如图所示:
①在图中画出0~16min时间段内,
 随时间的变化曲线。
随时间的变化曲线。②1~4四个点中,v正=v逆的点有
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】(1)利用某些有机物之间的相互转换可以贮存太阳能,如原降冰片二烯(NBD)经过太阳光照转化成为四环烷(Q)的反应为
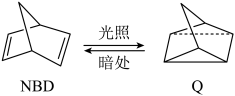 △H=+88.62 kJ/mol
△H=+88.62 kJ/mol
以下叙述错误的是_____ (填序号)
a NBD的能量比Q的能量高b NBD和Q互为同分异构体
c NBD的分子式为C7H8d NBD能使溴水褪色e NBD及Q的一氯代物均为三种
(2)如图是在一定温度下,某固定容积的密闭容器中充入一定量的NO2气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是_____ 。
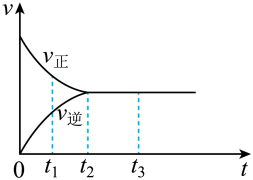
a t1时,反应未达到平衡,NO2浓度在减小
b t2时,反应达到平衡,反应不再进行
c t2~t3,各物质浓度不再变化
d t2~t3,各物质的浓度相等
e 0~t2,N2O4浓度增大
f.反应过程中气体的颜色不变
(3)某研究性学习小组欲研究影响锌和稀硫酸反应速率的外界条件,如表是其实验设计的有关数据:
①在此5组实验中,判断锌和稀硫酸反应速率大小,最简单的方法可通过定量测定锌完全消失所需的时间进行判断,其速率最快的实验是_____ (填实验序号)。
②对锌和稀硫酸反应,实验1和2表明,_____ 对反应速率有影响,实验1和3表明,_____ 对反应速率有影响
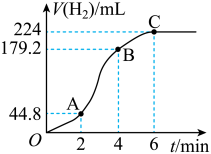
③进行实验2时,小组同学根据实验过程绘制的标准状况下的气体体积V与时间t的图象如图所示。在OA、AB、BC三段中反应速率最快的是_____ ,2~4min内以硫酸的浓度变化表示的反应速率(假设溶液的体积不变)=_____ 。
 △H=+88.62 kJ/mol
△H=+88.62 kJ/mol以下叙述错误的是
a NBD的能量比Q的能量高b NBD和Q互为同分异构体
c NBD的分子式为C7H8d NBD能使溴水褪色e NBD及Q的一氯代物均为三种
(2)如图是在一定温度下,某固定容积的密闭容器中充入一定量的NO2气体后,反应速率(v)与时间(t)的关系曲线。下列叙述正确的是

a t1时,反应未达到平衡,NO2浓度在减小
b t2时,反应达到平衡,反应不再进行
c t2~t3,各物质浓度不再变化
d t2~t3,各物质的浓度相等
e 0~t2,N2O4浓度增大
f.反应过程中气体的颜色不变
(3)某研究性学习小组欲研究影响锌和稀硫酸反应速率的外界条件,如表是其实验设计的有关数据:
| 实验 序号 | 锌的质量/g | 锌的 状态 | c(H2SO4)/mol•L﹣1 | V(H2SO4) /mL | 反应前溶液的温度/℃ | 添加剂 |
| 1 | 0.65 | 粒状 | 0.5 | 50 | 20 | 无 |
| 2 | 0.65 | 粉末 | 0.5 | 50 | 20 | 无 |
| 3 | 0.65 | 粒状 | 0.5 | 50 | 20 | 2滴CuSO4溶液 |
| 4 | 0.65 | 粉末 | 0.8 | 50 | 20 | 无 |
| 5 | 0.65 | 粉末 | 0.8 | 50 | 35 | 2滴CuSO4溶液 |
①在此5组实验中,判断锌和稀硫酸反应速率大小,最简单的方法可通过定量测定锌完全消失所需的时间进行判断,其速率最快的实验是
②对锌和稀硫酸反应,实验1和2表明,
③进行实验2时,小组同学根据实验过程绘制的标准状况下的气体体积V与时间t的图象如图所示。在OA、AB、BC三段中反应速率最快的是

您最近半年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】文献表明:相同条件下,草酸根(C2O42-)的还原性强于Fe2+。为检验这一结论, 完成如下实验。
资料:i.草酸(H2C2O4)为二元弱酸。
ii.三水三草酸合铁酸钾K3 Fe(C2O4)3·3H2O为翠绿色晶体,光照易分解。其水溶液中存在:
[Fe(C2O4)3]3- Fe3++3C2O42- K=6.3×10-21
Fe3++3C2O42- K=6.3×10-21
iii. FeC2O4·2H2O为黄色固体,微溶于水,可溶于强酸。
[实验1]通过Fe3+和C2O42-在溶液中的反应比较Fe2+和C2O42-的还原性强弱。
(l) C2O42-中碳元素的化合价是____ 。
(2)取实验1中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红,说明晶体中含有+3价的铁元素。加硫酸后溶液变红的原因是____ 。
(3)经检验,翠绿色晶体为K3 Fe(C2O4)3·3H2O设计实验,确认实验1中没有发生氧化还原反应的操作和现象是____ 。实验l中未发生氧化还原反应的原因是____ 。
(4)取实验1中的翠绿色溶液光照一段时间,产生黄色浑浊且有气泡产生。补全反应的离子方程式:
_____ [Fe(C2O4)3]3-+_____ H2O
____ FeC2O4·2H2O↓+_____ +________ 。
[实验2]通过比较H2O2与Fe2+、C2O42-反应的难易,判断二者还原性的强弱。
(5)证明Fe2+被氧化的实验现象是____ 。
(6)以上现象能否说明C2O42-没有被氧化。请判断并说明理由:________
(7)用FeC13溶液、K2C2O4溶液和其他试剂,设计实验方案比较Fe2+和C2O42-的还原性强弱。画出装置图并描述预期现象:____ 。
资料:i.草酸(H2C2O4)为二元弱酸。
ii.三水三草酸合铁酸钾K3 Fe(C2O4)3·3H2O为翠绿色晶体,光照易分解。其水溶液中存在:
[Fe(C2O4)3]3-
 Fe3++3C2O42- K=6.3×10-21
Fe3++3C2O42- K=6.3×10-21iii. FeC2O4·2H2O为黄色固体,微溶于水,可溶于强酸。
[实验1]通过Fe3+和C2O42-在溶液中的反应比较Fe2+和C2O42-的还原性强弱。
| 操作 | 现象 |
| 在避光处,向10 mL 0.5 mol·L-1 FeCl3溶液中缓慢加入0.5 mol·L-1 K2C2O4溶液至过量,搅拌,充分反应后,冰水浴冷却,过滤 | 得到翠绿色溶液和翠绿色晶体 |
(2)取实验1中少量晶体洗净,配成溶液,滴加KSCN溶液,不变红。继续加入硫酸,溶液变红,说明晶体中含有+3价的铁元素。加硫酸后溶液变红的原因是
(3)经检验,翠绿色晶体为K3 Fe(C2O4)3·3H2O设计实验,确认实验1中没有发生氧化还原反应的操作和现象是
(4)取实验1中的翠绿色溶液光照一段时间,产生黄色浑浊且有气泡产生。补全反应的离子方程式:
[实验2]通过比较H2O2与Fe2+、C2O42-反应的难易,判断二者还原性的强弱。
| 步骤 | 操作 | 现象 |
| I | 向l mL 0.5 mol·L-1 FeSO4溶液中加入1 mL 0.5 mol·L-1 K2C2O4溶液,过滤 | 立即产生黄色沉淀 |
| II | 洗涤Ⅰ中的黄色沉淀,向其中加入过量的6%H2O2溶液,振荡,静置 | 剧烈放热,产生大量的红褐色沉淀和无色气体 |
| III | 待充分反应后,向其中加入稀硫酸,调节pH约为4 | 得到翠绿色溶液 |
(6)以上现象能否说明C2O42-没有被氧化。请判断并说明理由:
(7)用FeC13溶液、K2C2O4溶液和其他试剂,设计实验方案比较Fe2+和C2O42-的还原性强弱。画出装置图并描述预期现象:
您最近半年使用:0次
【推荐2】氮和硫的氧化物是造成大气污染的主要物质。研究它们的反应机理,对于消除环境污染有重要意义。
(1)2NO(g)+O2(g) 2NO2(g)的反应历程由两步基元反应组成,相关信息如下(E为活化能,v为反应速率,k为速率常数):
2NO2(g)的反应历程由两步基元反应组成,相关信息如下(E为活化能,v为反应速率,k为速率常数):
2NO(g) N2O2(g)E1=82kJ/molv=k1c2(NO)
N2O2(g)E1=82kJ/molv=k1c2(NO)
N2O2(g)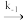 2NO(g)E-1=205kJ/molv=k-1c(N2O2)
2NO(g)E-1=205kJ/molv=k-1c(N2O2)
N2O2(g)+O2(g) 2NO2(g)E2=82kJ/molv=k2c(N2O2)·c(O2)
2NO2(g)E2=82kJ/molv=k2c(N2O2)·c(O2)
2NO2(g)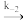 N2O2(g) +O2(g)E-2=72kJ/molv=k-2c2(NO2)
N2O2(g) +O2(g)E-2=72kJ/molv=k-2c2(NO2)
则2NO(g) N2O2(g)△H1=
N2O2(g)△H1=_______ kJ·mol-1,其平衡常数K与上述速率常数k1、k-1的关系式为K=_______ 。2NO(g)+O2(g) 2NO2(g)△H=
2NO2(g)△H=_______ kJ·mol-1。
(2)已知反应NO2(g)+SO2(g) NO(g)+SO3(g)△H<0,某研究小组研究不同温度T1℃、T2℃下的平衡态中lgp(NO2)和lgp(SO3)两个压强对数的关系如图所示,实验初始时体系中的p(NO2)和p(SO2)相等、p(NO)和p(SO3)相等。
NO(g)+SO3(g)△H<0,某研究小组研究不同温度T1℃、T2℃下的平衡态中lgp(NO2)和lgp(SO3)两个压强对数的关系如图所示,实验初始时体系中的p(NO2)和p(SO2)相等、p(NO)和p(SO3)相等。
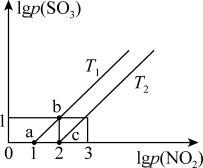
①a、b两点体系压强pa与pb的比值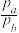 =
=_______ ;同一温度下图象呈线性变化的理由是_______ 。
②温度为T1时化学平衡常数KP=_______ ,T1_______ T2(填“>”“<”或者“=”)。
(1)2NO(g)+O2(g)
 2NO2(g)的反应历程由两步基元反应组成,相关信息如下(E为活化能,v为反应速率,k为速率常数):
2NO2(g)的反应历程由两步基元反应组成,相关信息如下(E为活化能,v为反应速率,k为速率常数):2NO(g)
 N2O2(g)E1=82kJ/molv=k1c2(NO)
N2O2(g)E1=82kJ/molv=k1c2(NO)N2O2(g)
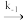 2NO(g)E-1=205kJ/molv=k-1c(N2O2)
2NO(g)E-1=205kJ/molv=k-1c(N2O2)N2O2(g)+O2(g)
 2NO2(g)E2=82kJ/molv=k2c(N2O2)·c(O2)
2NO2(g)E2=82kJ/molv=k2c(N2O2)·c(O2)2NO2(g)
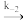 N2O2(g) +O2(g)E-2=72kJ/molv=k-2c2(NO2)
N2O2(g) +O2(g)E-2=72kJ/molv=k-2c2(NO2)则2NO(g)
 N2O2(g)△H1=
N2O2(g)△H1= 2NO2(g)△H=
2NO2(g)△H=(2)已知反应NO2(g)+SO2(g)
 NO(g)+SO3(g)△H<0,某研究小组研究不同温度T1℃、T2℃下的平衡态中lgp(NO2)和lgp(SO3)两个压强对数的关系如图所示,实验初始时体系中的p(NO2)和p(SO2)相等、p(NO)和p(SO3)相等。
NO(g)+SO3(g)△H<0,某研究小组研究不同温度T1℃、T2℃下的平衡态中lgp(NO2)和lgp(SO3)两个压强对数的关系如图所示,实验初始时体系中的p(NO2)和p(SO2)相等、p(NO)和p(SO3)相等。
①a、b两点体系压强pa与pb的比值
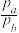 =
=②温度为T1时化学平衡常数KP=
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理实现绿色环保、废物利用。
Ⅰ.脱硝:已知:H2的燃烧热为285.8 kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133 kJ·mol-1
H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
(1)催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为___________ 。
Ⅱ.脱碳:
(2)向2 L密闭容器中加入1mol CO2和3 mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g) CH3OH(l)+H2O(l) ΔH<0
CH3OH(l)+H2O(l) ΔH<0
①该反应自发进行的条件是___________ (填“低温”“高温”或“任意温度”)
②下列叙述能说明此反应达到平衡状态的是___________ (填字母)。
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1 mol CO2生成的同时有3 mol H-H键断裂
f. CO2和H2的物质的量之比保持不变 g. v正(CO2) = 3v逆(H2)
(3)工业上使用水煤气(CO与H2的混合气体)转化成甲醇,反应为CO(g)+2H2(g) CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
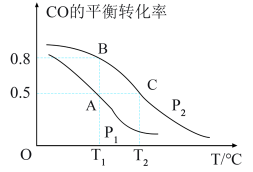
①p1、p2的大小关系是p1___________ p2(填“>”“<"或"=”)。
②A、B、C三点的平衡常数KA、KB、Kc的大小关系是___________ 。
(4)在T2℃、p2压强时,往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。
①平衡时H2的体积分数是___________ ;平衡后再加入1.0molCO后重新到达平衡,则CO的转化率___________ (填“增大""不变”成“减小”),CO与CH3OH的浓度比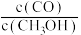
___________ (填"增大”“不变"或“减小")。
②若以不同比例投料,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)___________ v(逆)(填“”“<"或“=”)。
③若p2压强恒定为p,则平衡常数Kp=___________ (Kp用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,整理出含p的最简表达式)。
Ⅰ.脱硝:已知:H2的燃烧热为285.8 kJ·mol-1
N2(g)+2O2(g)=2NO2(g) ΔH=+133 kJ·mol-1
H2O(g)=H2O(l) ΔH=-44 kJ·mol-1
(1)催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为
Ⅱ.脱碳:
(2)向2 L密闭容器中加入1mol CO2和3 mol H2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g)
 CH3OH(l)+H2O(l) ΔH<0
CH3OH(l)+H2O(l) ΔH<0①该反应自发进行的条件是
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变 b.CO2和H2的体积分数保持不变
c.CO2和H2的转化率相等 d.混合气体的密度保持不变
e.1 mol CO2生成的同时有3 mol H-H键断裂
f. CO2和H2的物质的量之比保持不变 g. v正(CO2) = 3v逆(H2)
(3)工业上使用水煤气(CO与H2的混合气体)转化成甲醇,反应为CO(g)+2H2(g)
 CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。CO的平衡转化率与温度、压强的关系如图所示。
①p1、p2的大小关系是p1
②A、B、C三点的平衡常数KA、KB、Kc的大小关系是
(4)在T2℃、p2压强时,往一容积为2L的密闭容器内,充入0.3molCO与0.4molH2发生反应。
①平衡时H2的体积分数是
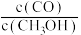
②若以不同比例投料,测得某时刻各物质的物质的量如下,CO:0.1mol、H2:0.2mol、CH3OH:0.2mol,此时v(正)
③若p2压强恒定为p,则平衡常数Kp=
您最近半年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐1】三氧化二砷(As2O3)可用于治疗急性早幼粒细胞白血病。利用某酸性含砷废水(含H3AsO3、H2SO4)可提取As2O3,提取工艺流程如下:
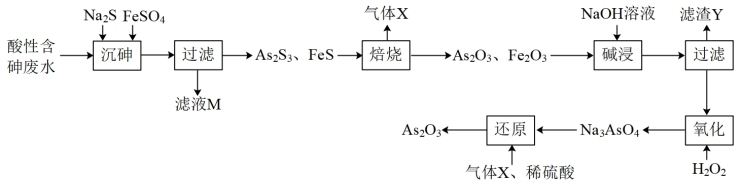
已知:①As2O3为酸性氧化物;②As2S3易溶于过量的Na2S溶液中,故加入FeSO4,的目的是除去过量的S2-。
回答下列问题:
(1)废水中H3AsO3中砷元素的化合价为____
(2)“焙烧”操作中,As2S3参与反应的化学方程式为_____
(3)“碱浸”的目的___________ ,“滤渣Y”的主要成分是___________ 。(写化学式)。
(4)“氧化”操作的目的是___________ (用离子方程式表示)。
(5)“还原”过程中H3AsO4转化为H3AsO3然后将“还原”后溶液加热,H3AsO3分解为As2O3。某次“还原”过程中制得了1.98kgAs2O3,则消耗标准状况下气体X的体积是___________ L。
(6)砷酸钠(Na3AsO4)可用于可逆电池,装置如图1所示,其反应原理为AsO +2H++2I-=AsO
+2H++2I-=AsO +I2+H2O。探究pH对AsO
+I2+H2O。探究pH对AsO 氧化性的影响,测得输出电压与pH的关系如图2所示。则a点时,盐桥中K+
氧化性的影响,测得输出电压与pH的关系如图2所示。则a点时,盐桥中K+___________ (填“向左”“向右”或“不”)移动,c点时,负极的电极反应为___________ 。


已知:①As2O3为酸性氧化物;②As2S3易溶于过量的Na2S溶液中,故加入FeSO4,的目的是除去过量的S2-。
回答下列问题:
(1)废水中H3AsO3中砷元素的化合价为
(2)“焙烧”操作中,As2S3参与反应的化学方程式为
(3)“碱浸”的目的
(4)“氧化”操作的目的是
(5)“还原”过程中H3AsO4转化为H3AsO3然后将“还原”后溶液加热,H3AsO3分解为As2O3。某次“还原”过程中制得了1.98kgAs2O3,则消耗标准状况下气体X的体积是
(6)砷酸钠(Na3AsO4)可用于可逆电池,装置如图1所示,其反应原理为AsO
 +2H++2I-=AsO
+2H++2I-=AsO +I2+H2O。探究pH对AsO
+I2+H2O。探究pH对AsO 氧化性的影响,测得输出电压与pH的关系如图2所示。则a点时,盐桥中K+
氧化性的影响,测得输出电压与pH的关系如图2所示。则a点时,盐桥中K+
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】I. 甲烷和水蒸气催化制氢主要存在如下两个反应:
①CH4(g)+ H2O (g) CO(g)+3H2(g) ∆H= +206kJ•mol-1
CO(g)+3H2(g) ∆H= +206kJ•mol-1
②CO(g)+ H2O (g) CO2 (g)+H2(g) ∆H= —41kJ•mol-1
CO2 (g)+H2(g) ∆H= —41kJ•mol-1
恒定压强为P0时,将n(CH4):n(H2O)=1 :3的混合气体投入反应器中,平衡时各组分的物质的量分数与温度的关系如图所示。
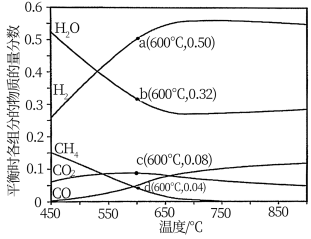
回答下列问题:
(1)写出CH4与CO2生成H2和CO的热化学方程式:___________ 。
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是___________ (填字母)。
A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快
B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快
C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快
D.加入合适的催化剂,同时降低反应温度,相同时间内的转化率可能不变
(3)恒定压强为P0,投料比n(CH4): n(H2O)=1 :3时,从提高氢气产率角度考虑反应温度应控制在___________ ℃左右。
(4) 600°C时,CH4的平衡转化率为___________ (保留2位有效数字),反应①的平衡常数的计算式为Kp=___________ (Kp是以分压表示的平衡常数,分压=总压×物质的量分数)。
II.我国科学家最近发明了一种Zn-PbO2电池,电解质为K2SO4、H2SO4和KOH,由a和b两种离子交换膜隔开,形成A、B、C三个电解质溶液区域,反应后B中溶液浓度变大,结构示意图如下:

回答下列问题:
(5)电池中,Zn 极上发生的电极反应式为___________ 。
(6)电池放电过程中,每消耗6.5gZn,理论上PbO2电极质量增重___________ g。
①CH4(g)+ H2O (g)
 CO(g)+3H2(g) ∆H= +206kJ•mol-1
CO(g)+3H2(g) ∆H= +206kJ•mol-1②CO(g)+ H2O (g)
 CO2 (g)+H2(g) ∆H= —41kJ•mol-1
CO2 (g)+H2(g) ∆H= —41kJ•mol-1恒定压强为P0时,将n(CH4):n(H2O)=1 :3的混合气体投入反应器中,平衡时各组分的物质的量分数与温度的关系如图所示。

回答下列问题:
(1)写出CH4与CO2生成H2和CO的热化学方程式:
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是
A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快
B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快
C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快
D.加入合适的催化剂,同时降低反应温度,相同时间内的转化率可能不变
(3)恒定压强为P0,投料比n(CH4): n(H2O)=1 :3时,从提高氢气产率角度考虑反应温度应控制在
(4) 600°C时,CH4的平衡转化率为
II.我国科学家最近发明了一种Zn-PbO2电池,电解质为K2SO4、H2SO4和KOH,由a和b两种离子交换膜隔开,形成A、B、C三个电解质溶液区域,反应后B中溶液浓度变大,结构示意图如下:

回答下列问题:
(5)电池中,Zn 极上发生的电极反应式为
(6)电池放电过程中,每消耗6.5gZn,理论上PbO2电极质量增重
您最近半年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】SO2是一种污染性气体,减少SO2在大气中的排放是环境保护的重要内容回答下列问题:
(1)已知:S(s)+O2(g)=SO2(g) ∆H=—297.2kJ·mol-1,CH4(g)+2SO2(g)=CO2(g)+2S(s)+2H2O(l) ∆H=—295.9kJ·mol-1,若CH4(g)+2O2(g)=CO2(g)+2H2O(l)反应物的能量为E1,则生成物的能量E2是___________
(2)利用反应:C(s)+SO2(g) CO2(g)+S(g),可减少SO2在大气中的排放,在密闭容器中投入足量的反应物,不同实验条件下达到平衡,测得T=600℃下的x(SO2)—p和p=105Pa下—1gKc—t如图所示[x(SO2)表示SO2平衡时含量,Kc表示平衡常数]。该反应的正反应是
CO2(g)+S(g),可减少SO2在大气中的排放,在密闭容器中投入足量的反应物,不同实验条件下达到平衡,测得T=600℃下的x(SO2)—p和p=105Pa下—1gKc—t如图所示[x(SO2)表示SO2平衡时含量,Kc表示平衡常数]。该反应的正反应是___________ 反应(填“放热”、“吸热”),理由是___________ 。
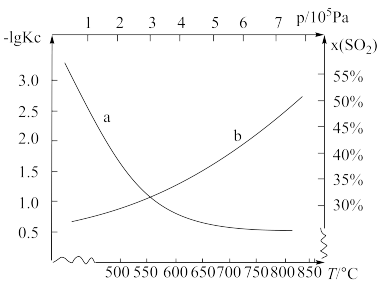
(3)恒温恒容条件下,下列事实不能说明反应C(s)+SO2(g) CO2(g)+S(g)达到平衡状态的是___________(填字母)
CO2(g)+S(g)达到平衡状态的是___________(填字母)
(4)800℃,在1.0L的恒容密闭容器中投入1.0molSO2和120gC,容器中压强为p0kPa,发生反应C(s)+SO2(g) CO2(g)+S(g),5min时容器中CO2的体积分数为20%,10min时达平衡,容器中压强为pkPa时。0~5minv(SO2)
CO2(g)+S(g),5min时容器中CO2的体积分数为20%,10min时达平衡,容器中压强为pkPa时。0~5minv(SO2)___________ kPa·min-1,800℃的化学平衡常数Kc=___________ mol/L。
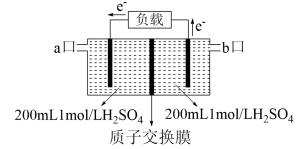
(5)用电化学原理吸收烟道气中SO2以减少其排放,其装置示意图。H2O2从___________ 口进入,电路中通过1mol电子时,正极区溶液的c(H+)将___________ ,负极区n(H2SO4)=___________ 。
(1)已知:S(s)+O2(g)=SO2(g) ∆H=—297.2kJ·mol-1,CH4(g)+2SO2(g)=CO2(g)+2S(s)+2H2O(l) ∆H=—295.9kJ·mol-1,若CH4(g)+2O2(g)=CO2(g)+2H2O(l)反应物的能量为E1,则生成物的能量E2是
(2)利用反应:C(s)+SO2(g)
 CO2(g)+S(g),可减少SO2在大气中的排放,在密闭容器中投入足量的反应物,不同实验条件下达到平衡,测得T=600℃下的x(SO2)—p和p=105Pa下—1gKc—t如图所示[x(SO2)表示SO2平衡时含量,Kc表示平衡常数]。该反应的正反应是
CO2(g)+S(g),可减少SO2在大气中的排放,在密闭容器中投入足量的反应物,不同实验条件下达到平衡,测得T=600℃下的x(SO2)—p和p=105Pa下—1gKc—t如图所示[x(SO2)表示SO2平衡时含量,Kc表示平衡常数]。该反应的正反应是
(3)恒温恒容条件下,下列事实不能说明反应C(s)+SO2(g)
 CO2(g)+S(g)达到平衡状态的是___________(填字母)
CO2(g)+S(g)达到平衡状态的是___________(填字母)A. 不变 不变 |
| B.v(CO2)正=v(SO2)逆 |
| C.混合气体的总压强不再改变 |
| D.混合气体的密度不再改变 |
 CO2(g)+S(g),5min时容器中CO2的体积分数为20%,10min时达平衡,容器中压强为pkPa时。0~5minv(SO2)
CO2(g)+S(g),5min时容器中CO2的体积分数为20%,10min时达平衡,容器中压强为pkPa时。0~5minv(SO2)(5)用电化学原理吸收烟道气中SO2以减少其排放,其装置示意图。H2O2从

您最近半年使用:0次