解题方法
1 . 嫦娥四号使用的月背探测器发动机,是利用 Sr(锶)等放射性同位素衰变产生的能量发电;已知:38Sr(锶)在周期表中与37Rb(铷如)、20Ca(钙)相邻。下列有关Sr(锶)的说法不正确的是
Sr(锶)等放射性同位素衰变产生的能量发电;已知:38Sr(锶)在周期表中与37Rb(铷如)、20Ca(钙)相邻。下列有关Sr(锶)的说法不正确的是
 Sr(锶)等放射性同位素衰变产生的能量发电;已知:38Sr(锶)在周期表中与37Rb(铷如)、20Ca(钙)相邻。下列有关Sr(锶)的说法不正确的是
Sr(锶)等放射性同位素衰变产生的能量发电;已知:38Sr(锶)在周期表中与37Rb(铷如)、20Ca(钙)相邻。下列有关Sr(锶)的说法不正确的是| A.碱性:Sr(OH)2<Ca(OH)2 | B.常温下,Sr能与水反应 |
| C.SrCO3难溶于水 | D.Sr在纯氧中点燃可燃烧 |
您最近一年使用:0次
2 . 下列离子检验或除杂方法错误的是
| A.除去Fe粉中混有的少量铝粉:加入过量NaOH溶液,过滤 |
| B.除去Na2CO3溶液中混有的少量NaHCO3:加入适量NaOH溶液 |
C.向某溶液中加入过量稀盐酸无明显现象,再加入BaCl2溶液,有白色沉淀生成,该溶液中一定含有SO |
| D.向某溶液中加入AgNO3溶液,有白色沉淀生成,该溶液中一定含有Cl- |
您最近一年使用:0次
名校
解题方法
3 . 在无色酸性溶液中能大量共存的离子组是
| A.Na+、Cu2+、ClO-、Br- | B.K+、Br-、NO 、OH- 、OH- |
C.Al3+、Ca2+、CO 、Cl- 、Cl- | D.Mg2+、Na+、I-、SO |
您最近一年使用:0次
2023-03-09更新
|
147次组卷
|
2卷引用:吉林省延边州2022-2023学年高一上学期期末学业质量检测化学试题
4 . 随着原子序数的递增,A~G七种短周期元素的最高正价或最低负价与原子序数的关系如图所示。

(1)C元素在周期表中的位置为_____ 。
(2)B元素原子与氢原子组成含10电子的分子的化学式为_____ ,D、E两种元素的离子半径大小关系为_____ (填元素符号)。
(3)E元素的最高价氧化物与氢氧化钠溶液反应的离子方程式是_____ 。
(4)D元素与G元素形成的最简单化合物的电子式为_____ ,所含的化学键类型为_____ 。
(5)下列表述中,能证明B元素比A元素的非金属性强的是_____ (填字母)。
a.B元素的简单气态氢化物的热稳定性比A的强
b.B元素的最高价氧化物对应的水化物的酸性比A的强
c.B元素的最高正价为+5,A元素的最高正价为+4

(1)C元素在周期表中的位置为
(2)B元素原子与氢原子组成含10电子的分子的化学式为
(3)E元素的最高价氧化物与氢氧化钠溶液反应的离子方程式是
(4)D元素与G元素形成的最简单化合物的电子式为
(5)下列表述中,能证明B元素比A元素的非金属性强的是
a.B元素的简单气态氢化物的热稳定性比A的强
b.B元素的最高价氧化物对应的水化物的酸性比A的强
c.B元素的最高正价为+5,A元素的最高正价为+4
您最近一年使用:0次
名校
解题方法
5 . 为探究“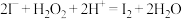 ”碘离子氧化过程进行如下实验.
”碘离子氧化过程进行如下实验.
下列说法不正确的是
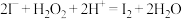 ”碘离子氧化过程进行如下实验.
”碘离子氧化过程进行如下实验.编号 | 1 | 2 |
实验内容 |
|
|
实验现象 | 随着液体不断滴入,产生大量气体;溶液变黄并不断加深至棕黄色后又变浅 | 随着液体不断滴入,溶液变黄,摇匀后又褪色,不断重复直至析出紫色沉淀 |
A.实验1中溶液变浅是因为 |
B.实验2中出现紫色沉淀是因为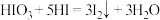 |
C.实验1中产生大量气体的原因是 被氧化的过程大量放热 被氧化的过程大量放热 |
| D.实验2相较于实验1,可节约H2O2用量且有利于反应终点观察 |
您最近一年使用:0次
2023-03-08更新
|
800次组卷
|
3卷引用:2024届吉林省延边州高三教学质量检测(一模)化学试题
名校
解题方法
6 . 向含废水中加入 ,铁元素会形成如图所示的
,铁元素会形成如图所示的 胶团,在静电吸附作用下,胶团可以除去废水中的
胶团,在静电吸附作用下,胶团可以除去废水中的 价砷元素,下列说法正确的是
价砷元素,下列说法正确的是

 ,铁元素会形成如图所示的
,铁元素会形成如图所示的 胶团,在静电吸附作用下,胶团可以除去废水中的
胶团,在静电吸附作用下,胶团可以除去废水中的 价砷元素,下列说法正确的是
价砷元素,下列说法正确的是
| A.废水中的含砷微粒是带正电荷的离子 |
B.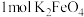 可以形成的胶团数目小于 可以形成的胶团数目小于 |
C.增大废水的 , , 胶粒的吸附絮凝效能提升 胶粒的吸附絮凝效能提升 |
D. 可以还原废水中的含砷微粒到 可以还原废水中的含砷微粒到 价 价 |
您最近一年使用:0次
2022-12-09更新
|
1232次组卷
|
5卷引用:吉林省延边第一中学2023届高三下学期第七次模拟考试理科综合化学试题
名校
7 . 某课外活动小组设计实验验证二氧化碳跟过氧化钠反应时需要与水接触。下列说法中正确的是
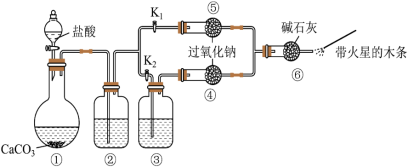

| A.装置①中盐酸不能换成硫酸 |
B.装置②中的试剂是饱和 溶液 溶液 |
C.打开弹簧夹 ,关闭 ,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处,木条复燃 |
| D.上述实验不足以证明有水存在时过氧化钠跟二氧化碳发生了化学反应 |
您最近一年使用:0次
2022-12-07更新
|
193次组卷
|
2卷引用:吉林省延边州2022-2023学年高一上学期期末学业质量检测化学试题
名校
解题方法
8 . 某同学设计用如图所示装置制备少量的AlCl3(易水解)。下列说法正确的是


| A.装置B中所装试剂为饱和NaHCO3溶液,其作用是除去氯气中的HCl气体 |
| B.装置C和F中的试剂均为浓硫酸,其作用是防止水蒸气进入装置D和E中 |
| C.用50mL12mol•L-1的盐酸与足量的MnO2反应,所得氯气可以制取26.7gAlCl3 |
| D.实验过程中应先点燃D处酒精灯预热Al粉,达到反应温度再点燃A处酒精灯 |
您最近一年使用:0次
2022-10-29更新
|
164次组卷
|
3卷引用:吉林省延边第二中学2022-2023学年高三上学期10月月考化学试题
名校
解题方法
9 . 草酸亚铁晶体(FeC2O4•2H2O)常用作生产锂电池、涂料、着色剂以及感光材料的原材料,难溶于水,受热易分解。
I.制备草酸亚铁晶体:
①称取硫酸亚铁铵晶体5g,放入250mL三颈烧瓶中,加入10滴左右1.0mol•L-1H2SO4溶液和15mL蒸馏水加热溶解;
②加入25mL饱和草酸溶液,加热搅拌至沸腾停止加热,静置;
③待黄色晶体FeC2O4•2H2O沉淀后倾析,洗涤,加入约20mL蒸馏水搅拌并温热5min,静置,弃去上层清液,即得黄色草酸亚铁晶体。

(1)B的名称是____ ;B的出水口是____ (填“上口”或“下口”)。
(2)硫酸亚铁铵晶体中可能混有Fe3+,检验其是否含有Fe3+的试剂是____ 溶液,若混有Fe3+,观察到的现象是____ 。
II.将一定质量的草酸亚铁晶体(FeC2O4•2H2O)在氩气气氛中进行热重分析示意图(TG%表示残留固体质量占原样品总质量的百分数)。

(3)B处时残留物的化学式为____ 。
(4)取上述分解得到的600℃时的固体放在空气中继续加热时其质量增加,发生反应的化学方程式为____ 。
I.制备草酸亚铁晶体:
①称取硫酸亚铁铵晶体5g,放入250mL三颈烧瓶中,加入10滴左右1.0mol•L-1H2SO4溶液和15mL蒸馏水加热溶解;
②加入25mL饱和草酸溶液,加热搅拌至沸腾停止加热,静置;
③待黄色晶体FeC2O4•2H2O沉淀后倾析,洗涤,加入约20mL蒸馏水搅拌并温热5min,静置,弃去上层清液,即得黄色草酸亚铁晶体。

(1)B的名称是
(2)硫酸亚铁铵晶体中可能混有Fe3+,检验其是否含有Fe3+的试剂是
II.将一定质量的草酸亚铁晶体(FeC2O4•2H2O)在氩气气氛中进行热重分析示意图(TG%表示残留固体质量占原样品总质量的百分数)。

(3)B处时残留物的化学式为
(4)取上述分解得到的600℃时的固体放在空气中继续加热时其质量增加,发生反应的化学方程式为
您最近一年使用:0次
2022-10-29更新
|
177次组卷
|
4卷引用:吉林省延边第二中学2022-2023学年高三上学期10月月考化学试题
名校
10 . 2012年IUPAC命名116号元素为Lv,Lv的原子核外最外层电子数是6,下列说法错误的是
| A.Lv是第七周期第VIA族元素 |
| B.Lv的同位素原子具有不同的电子数 |
| C.Lv在同族元素中非金属性最弱 |
D.中子数为177的Lv核素符号是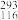 Lv Lv |
您最近一年使用:0次
2022-10-29更新
|
121次组卷
|
3卷引用:吉林省延边第二中学2022-2023学年高三上学期10月月考化学试题





