名校
解题方法
1 . 氧化铍(BeO)在航天航空等领域有着广泛的应用。一种以预处理后的硅铍矿(主要含BeO、Fe2O3、SiO2和FeO等)为原料提取BeO的流程如下图所示:

已知:Be(OH)2具有两性,在强碱性溶液中可转化为BeO 。下列说法错误的是
。下列说法错误的是

已知:Be(OH)2具有两性,在强碱性溶液中可转化为BeO
 。下列说法错误的是
。下列说法错误的是| A.“酸浸”步骤所得“滤渣①”的主要成分为Si |
| B.“滤液②”经处理后可获得副产品Na2SO4·10H2O |
C.“碱溶”时,主要反应为Be(OH)2+2OH-=BeO +2H2O +2H2O |
| D.“水解”时,适当增大溶液pH有利于提高BeO的提取率 |
您最近一年使用:0次
2022-05-23更新
|
1296次组卷
|
9卷引用:湖南省株洲市九方中学2022届高三下学期第二次模拟考试化学试题
湖南省株洲市九方中学2022届高三下学期第二次模拟考试化学试题湖南株洲南方中学2022-2023学年高三第四次月考化学试题广东省深圳市2021届高三4月第二次调研考试化学试题(已下线)卷05 工艺流程型选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)专题13 物质的反应和转化-2022年高考真题模拟题分项汇编福建省福州第三中学2021-2022学年高一下学期期末考试化学试题(已下线)第九章 化学实验基础及综合实验(测)-2023年高考化学一轮复习讲练测(全国通用)新疆喀什地区英吉沙县2022-2023学年高三上学期11月期中考试化学试题湖北省十堰市郧阳中学2023届高三11月月考化学训练题
2 . 铂钌催化剂是甲醇燃料电池的阳极催化剂。一种以钌矿石[主要含Ru(CO3)2,还含少量的FeO、MgO、RuO4、CaO、SiO2]为原料制备钌(Ru)的流程如图。回答下列问题:
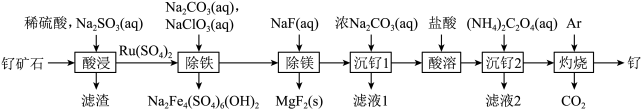
(1)Na2Fe4(SO4)6(OH)2中Fe的化合价为____ 。
(2)“酸浸”时,Na2SO3的作用____ 。“滤渣”的主要成分有SiO2和____ (填化学式)。“酸浸”中钌的浸出率与浸出温度、pH的关系如图所示,“酸浸”的最佳条件是____ 。
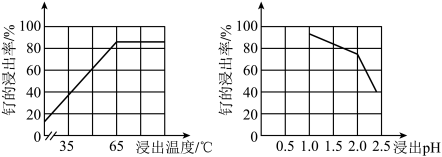
(3)“除铁”的离子方程式为____ 。(提示:1molNaClO3参与反应,转移6mol电子)
(4)从“滤液2”中可提取一种化肥,其电子式为____ 。
(5)“灼烧”时Ar的作用是____ 。
(6)某工厂用10t钌矿石[含8.84tRu(CO3)2、165kgRuO4],最终制得3636kgRu,则Ru的产率为____ 。(保留三位有效数字)

(1)Na2Fe4(SO4)6(OH)2中Fe的化合价为
(2)“酸浸”时,Na2SO3的作用

(3)“除铁”的离子方程式为
(4)从“滤液2”中可提取一种化肥,其电子式为
(5)“灼烧”时Ar的作用是
(6)某工厂用10t钌矿石[含8.84tRu(CO3)2、165kgRuO4],最终制得3636kgRu,则Ru的产率为
您最近一年使用:0次
2022-05-10更新
|
1867次组卷
|
15卷引用:湖南省株洲市北附高级中学2022-2023学年高三上学期第五次月考化学试题
湖南省株洲市北附高级中学2022-2023学年高三上学期第五次月考化学试题河南省新乡市2022届高三第三次模拟理科综合化学试题河北省保定市2022届高三第二次模拟考试化学试题河南省名校联盟2022届高三下学期5月大联考理科综合化学试题(已下线)专题15工艺流程题-2022年高考真题+模拟题汇编(全国卷)(已下线)专题16工艺流程题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16工艺流程题-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题15 工艺流程题-2022年高考真题模拟题分项汇编广东省广州市海珠外国语实验中学2022-2023学年高三上学期第二次阶段性考试化学试题福建省福州第一中学2022-2023学年高三上学期检考前适应性考试化学试题(已下线)专题29 无机化工流程综合分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)考前特训 [综合大题分类规范练](已下线)专题01 工艺流程专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)山东新高考2022-2023学年高一上学期质量测评模拟演练化学试题 四川省泸州市泸县第一中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
3 . 大多数离子液体含有体积很大的阴、阳离子(如图所示)。其中X、Y、Z为原子序数依次增大的短周期非金属元素,X、Z同主族。下列说法正确的是
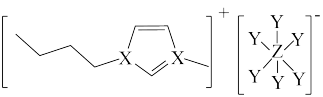

| A.原子半径:Z>X>Y | B.气态氢化物的稳定性:Z>X>Y |
| C.Z的氯化物的分子式一定为ZCl3 | D.此阴离子中Y、Z均满足8电子稳定结构 |
您最近一年使用:0次
2022-07-10更新
|
1337次组卷
|
7卷引用:湖南省株洲市攸县第二中学2022-2023学年高三上学期第三次月考化学试题
名校
解题方法
4 . 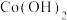 在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用
在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用 盐酸将其恰好完全溶解,得到
盐酸将其恰好完全溶解,得到 溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是
溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是

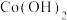 在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用
在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用 盐酸将其恰好完全溶解,得到
盐酸将其恰好完全溶解,得到 溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是
溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是
A.290℃时,若固体中只含有两种元素,则为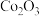 |
B.400℃时, |
| C.500℃时,固体中氧元素质量分数约为26.6% |
| D.生成的黄绿色气体可用于工业上生产“84”消毒液 |
您最近一年使用:0次
2022-10-18更新
|
529次组卷
|
3卷引用:湖南省株洲市九方中学2022-2023学年高一上学期第三次月考化学试题
名校
解题方法
5 . 下列有关物质的性质与用途具有对应关系的是
A. 是红棕色粉末,可用作油漆的颜料 是红棕色粉末,可用作油漆的颜料 |
B. 能溶于水,可用于生产盐酸 能溶于水,可用于生产盐酸 |
C. 为白色固体,可用于游泳池杀菌消毒 为白色固体,可用于游泳池杀菌消毒 |
D. 能与碱反应,可用作焙制糕点的膨松剂 能与碱反应,可用作焙制糕点的膨松剂 |
您最近一年使用:0次
2023-01-10更新
|
311次组卷
|
4卷引用:湖南省株洲市渌口区第三中学2022-2023学年高一上学期期末考试化学试题
湖南省株洲市渌口区第三中学2022-2023学年高一上学期期末考试化学试题江苏省南通市通州区2022-2023学年高一上学期期末考试化学试题山东省曹县第一中学2022-2023学年高一上学期期末考试化学试题(已下线)题型02 重要元素及其化合物的性质和转化-学易金卷:备战2023-2024学年高一化学期末真题分类汇编(江苏专用)
名校
解题方法
6 . 2022年1月10日上午10时15分,一辆装载76桶、共计22吨硫酰氯(SO2Cl2)的箱式危化品车在杭金衢高速衢向K328处发生事故,导致4桶破损,部分硫酰氯流出,与潮湿空气接触后,现场散发出刺鼻性的烟雾,情况十分危急。硫酰氯是一种重要的化工试剂,常温下为无色液体,熔点为-54.1℃,沸点为69.1℃。如今,氯化法是合成硫酰氯的常用方法。实验室合成硫酰氯的实验装置如图所示(部分夹持装置未画出]:

已知:①

②100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。回答下列问题:
(1)硫酰氯(SO2Cl2)中S的化合价为_______ 。
(2)实验室常用高锰酸钾和浓盐酸来制备氯气,请写出装置A中制氯气的离子方程式_______ 。
(3)装置B盛装的试剂为_______ ;装置F的作用为_______ 。
(4)二氧化硫是合成硫酰氯的关键试剂之一,下列有关 的描述正确的是_______。
的描述正确的是_______。
(5)合成的硫酰氯在空气中不稳定,能与空气中的水蒸气生成两种常见的强酸,并产生白雾。请写出相应的化学方程式_______ 。
(6)若装置A中排出氯气4.48L(已折算成标准状况),用仪器检测到装置D中放出12kJ的热量,则氯气的转化率为_______ 。

已知:①


②100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。回答下列问题:
(1)硫酰氯(SO2Cl2)中S的化合价为
(2)实验室常用高锰酸钾和浓盐酸来制备氯气,请写出装置A中制氯气的离子方程式
(3)装置B盛装的试剂为
(4)二氧化硫是合成硫酰氯的关键试剂之一,下列有关
 的描述正确的是_______。
的描述正确的是_______。A.实验室常用稀硫酸和亚硫酸钠溶液反应来制备 |
| B.二氧化硫是一种酸性氧化物,与水反应生成硫酸,是造成酸雨的主要原因 |
| C.二氧化硫能够抑制细菌和真菌的滋生,因此,某些食品也可以用二氧化硫来防腐 |
| D.二氧化硫具有漂白性,能使湿润的蓝色石蕊试纸先变红后褪色 |
(6)若装置A中排出氯气4.48L(已折算成标准状况),用仪器检测到装置D中放出12kJ的热量,则氯气的转化率为
您最近一年使用:0次
2022-11-05更新
|
155次组卷
|
3卷引用:湖南省株洲市九方中学2022-2023学年高一上学期第三次月考化学试题
7 . 某实验小组在实验室制备干燥纯净的氯气,并探究其性质。所用仪器及药品如图所示:

回答下列问题:
(1)根据实验设计上述制取氯气装置时,按照各装置的功能,连接顺序为:气体发生装置→___________ →收集装置→___________ 。
(2)A中盛放浓盐酸的仪器名称为___________ ,反应的化学方程式为___________ 。
(3)E中反应的离子方程式为_______ 。
(4)若要验证干燥的氯气不具有漂白性,可将如图所示装置连接到原实验装置中,连接的最佳位置是____ (填选项序号)。
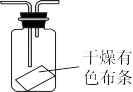
①A、B间 ②B、C间 ③C、D间
(5)该小组同学将制得的氯气配制成氯水,以探究 的还原性。进行了如下实验:取一定量的
的还原性。进行了如下实验:取一定量的 溶液,向其中滴加少量新制氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
溶液,向其中滴加少量新制氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
假设1: 被
被 氧化
氧化
假设2: 被
被 氧化
氧化
请你完成下表,验证假设。
(6)若要产生常温常压下 ,理论上需要
,理论上需要 的质量为
的质量为___________ g。(已知常温常压下气体的摩尔体积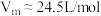 ;计算结果保留两位小数)
;计算结果保留两位小数)

回答下列问题:
(1)根据实验设计上述制取氯气装置时,按照各装置的功能,连接顺序为:气体发生装置→
(2)A中盛放浓盐酸的仪器名称为
(3)E中反应的离子方程式为
(4)若要验证干燥的氯气不具有漂白性,可将如图所示装置连接到原实验装置中,连接的最佳位置是

①A、B间 ②B、C间 ③C、D间
(5)该小组同学将制得的氯气配制成氯水,以探究
 的还原性。进行了如下实验:取一定量的
的还原性。进行了如下实验:取一定量的 溶液,向其中滴加少量新制氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:
溶液,向其中滴加少量新制氯水,振荡后溶液呈黄色。某同学对产生黄色的原因提出了假设:假设1:
 被
被 氧化
氧化假设2:
 被
被 氧化
氧化请你完成下表,验证假设。
| 实验步骤 | 预期现象 | 结论 |
| ①取少量黄色溶液于试管中,滴加几滴 | 假设1正确 | |
| ②取少量黄色溶液于试管中,滴加几滴 | 假设2正确 |
 ,理论上需要
,理论上需要 的质量为
的质量为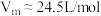 ;计算结果保留两位小数)
;计算结果保留两位小数)
您最近一年使用:0次
2022-01-24更新
|
174次组卷
|
3卷引用: 湖南省株洲市第八中学2022-2023学年高三上学期第三次月考化学试题
名校
解题方法
8 . 某种化合物的结构如图所示,其中 X、Y、Z、Q、W 为原子序数依次增大的五种短周期元素,X 的原子半径是元素周期表中所有元素中最小的,Q 的核外最外层电子数与 Y 的核外电子总数相同。下列叙述正确的是
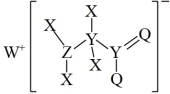

| A.Z 的氧化物对应的水化物是强酸 |
| B.W+的半径大于 Q 的简单离子半径 |
| C.元素非金属性的顺序为 Y>Z>Q |
| D.该化合物中 Z 满足 8 电子稳定结构 |
您最近一年使用:0次
2021-01-11更新
|
482次组卷
|
2卷引用:湖南省株洲市2021届高三教学质量统一检测(一)化学试题
名校
9 . 室温下进行下列实验,根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 用洁净的铂丝蘸取某溶液在火焰上灼烧,火焰呈黄色 | 溶液中不含 |
| B | 室温下,向 溶液中滴加少量KI溶液,再滴加2滴淀粉溶液,溶液变蓝色 溶液中滴加少量KI溶液,再滴加2滴淀粉溶液,溶液变蓝色 |  的氧化性比 的氧化性比 的强 的强 |
| C | 将Fe与水蒸气在高温条件下产生的气体通入肥皂泡中,用火柴点燃,肥皂泡燃烧 | 该气体是 |
| D | 向蓝色石蕊试纸上滴加新制氨水,试纸边缘呈红色,中间为白色 | 氯水既有酸性又有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-19更新
|
212次组卷
|
5卷引用:湖南省株洲市第二中学2021-2022学年高一上学期期中化学试题
10 . 如图所示实验装置用于验证某些物质的性质。在A试管中装入足量的固体NaHCO3。试回答下列问题:
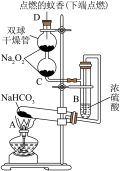
(1)在A试管内发生反应的化学方程式是_____________ ;
(2)B装置的作用是_____________________ ;
(3)在双球干燥管内发生反应的化学方程式为_________ ;
(4)实验时在C装置中观察到的现象是_______________ ;
(5)若将双球干燥管内的Na2O2换成Na2O,则实验时观察到的现象是___________________________________ 。

(1)在A试管内发生反应的化学方程式是
(2)B装置的作用是
(3)在双球干燥管内发生反应的化学方程式为
(4)实验时在C装置中观察到的现象是
(5)若将双球干燥管内的Na2O2换成Na2O,则实验时观察到的现象是
您最近一年使用:0次
2019-12-18更新
|
357次组卷
|
17卷引用:湖南省醴陵市第一中学2017-2018学年高一上学期第二次月考(12月)化学试题
湖南省醴陵市第一中学2017-2018学年高一上学期第二次月考(12月)化学试题2015-2016学年贵州省遵义航天中学高一上期末化学试卷2015-2016学年内蒙古集宁一中高一上第二次月考化学试卷2016-2017学年广西桂林中学高一上学期段考化学卷2018版化学(苏教版)高考总复习课时跟踪训练:钠、镁及其重要化合物内蒙古通辽实验中学2017-2018学年高一上学期期末考试化学试题云南省中央民大附中芒市国际学校2017-2018学年高一上学期末考试化学试卷广西桂梧高中2017-2018学年高一下学期第一次月考化学试题(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第1讲 钠及其氧化物【押题专练】(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第1讲 钠及化合物 (题型专练)湖南省邵东县第一中学2019-2020学年高一上学期第三次月考化学试题内蒙古自治区乌兰察布市北京八中乌兰察布分校2019-2020学年高一上学期期末考试化学试题山东省泰安市宁阳一中2020-2021学年高一上学期第一次阶段性考试化学试题(已下线)【镇江新东方】高一上期中考试河北省唐山市十县一中联盟2022-2023学年高一上学期期中考试化学试题河北省唐山市2022—2023学年高一上学期期中考试化学试题北京市通州区2022-2023学年高一上学期期中考试化学试题



