名校
1 . 按照要求填空
(1)现有下列各组物质:① 和
和 、②
、②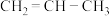 和
和 、③
、③ 和
和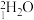 、④
、④ 和
和 、⑤
、⑤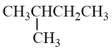 和
和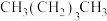 、⑥
、⑥ 和
和 、⑦
、⑦ 和
和
属于同系物的是___________ (填序号)。
(2)把下列物质的沸点按由高到低的顺序排列___________ 。(填入编号)
①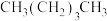 ②
②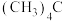 ③十一烷④
③十一烷④
(3)戊烷的同分异构体有___________ 种
(4)已知乳酸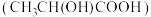 是身体代谢产物之一,该物质所含官能团的名称
是身体代谢产物之一,该物质所含官能团的名称___________ 。 乳酸分别与足量
乳酸分别与足量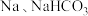 反应产生气体体积之比为:
反应产生气体体积之比为:___________ 。
(5)某有机物的键线式为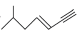 该分子最多有
该分子最多有___________ 个碳原子共面,最多有___________ 个碳原子共线。
(1)现有下列各组物质:①
 和
和 、②
、②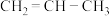 和
和 、③
、③ 和
和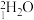 、④
、④ 和
和 、⑤
、⑤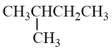 和
和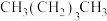 、⑥
、⑥ 和
和 、⑦
、⑦ 和
和
属于同系物的是
(2)把下列物质的沸点按由高到低的顺序排列
①
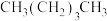 ②
②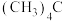 ③十一烷④
③十一烷④
(3)戊烷的同分异构体有
(4)已知乳酸
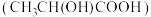 是身体代谢产物之一,该物质所含官能团的名称
是身体代谢产物之一,该物质所含官能团的名称 乳酸分别与足量
乳酸分别与足量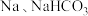 反应产生气体体积之比为:
反应产生气体体积之比为:(5)某有机物的键线式为
 该分子最多有
该分子最多有
您最近一年使用:0次
名校
解题方法
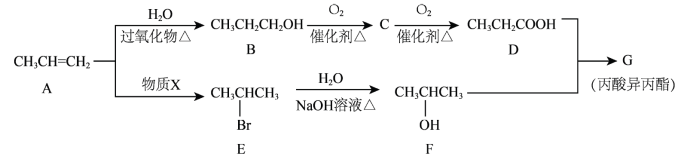
2 . 化合物G(丙酸异丙酯)可用作食品香料。现可通过下列转化制取(部分反应条件略去):___________ 。
(2)写出B→C的化学方程式___________ 。
(3)A→E是加成反应,写出该反应的化学方程式___________ 。
(4)写出D+F→G的化学方程式___________ 。
(5)G的同分异构体中能与碳酸氢钠溶液反应产生CO2的共有___________ 种。
(6)F的同分异构体中能被催化氧化成醛的是___________ (写出结构简式)。
(2)写出B→C的化学方程式
(3)A→E是加成反应,写出该反应的化学方程式
(4)写出D+F→G的化学方程式
(5)G的同分异构体中能与碳酸氢钠溶液反应产生CO2的共有
(6)F的同分异构体中能被催化氧化成醛的是
您最近一年使用:0次
名校
解题方法
3 . 科学家利用氧化锆锌作催化剂,在一定温度下将CO2和H2转化为重要有机原料甲醇(CH3OH),其原理为: (即正反应为放热反应)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2发生上述反应。CO2和CH3OH的物质的量随时间变化如图所示。回答下列问题:
(即正反应为放热反应)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2发生上述反应。CO2和CH3OH的物质的量随时间变化如图所示。回答下列问题:
___________ 。
(2)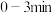 内,H2的反应速率为
内,H2的反应速率为___________ 。
(3)下列叙述正确的是___________ 。
a. 时
时 的生成速率等于其分解速率
的生成速率等于其分解速率
b.由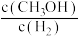 保持不变,可判断该反应达到平衡状态
保持不变,可判断该反应达到平衡状态
c.当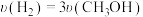 时,该反应一定达到平衡状态
时,该反应一定达到平衡状态
d.当CO2的体积分数不再变化,可判断该反应达到平衡状态
(4)该温度下达到平衡,此时体系压强与开始时的压强之比为___________ 。
(5)其他条件不变时,下列措施不能使生成CH3OH的反应速率增大的是___________ (填序号)。
a.增大CO2的浓度 b.将容器的容积变为4L
c.恒容条件下充入一定量Ne d.将恒温恒容容器改为绝热恒容容器
(6)CH4燃料电池的工作原理如图所示,a、b均为铂电极,A、B为燃料或氧气入口。_______ 。
 (即正反应为放热反应)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2发生上述反应。CO2和CH3OH的物质的量随时间变化如图所示。回答下列问题:
(即正反应为放热反应)。在容积为2L的恒温密闭容器中,充入1molCO2和3molH2发生上述反应。CO2和CH3OH的物质的量随时间变化如图所示。回答下列问题: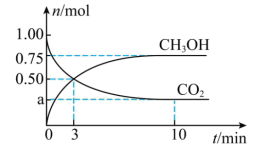

(2)
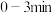 内,H2的反应速率为
内,H2的反应速率为(3)下列叙述正确的是
a.
 时
时 的生成速率等于其分解速率
的生成速率等于其分解速率b.由
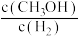 保持不变,可判断该反应达到平衡状态
保持不变,可判断该反应达到平衡状态c.当
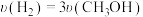 时,该反应一定达到平衡状态
时,该反应一定达到平衡状态d.当CO2的体积分数不再变化,可判断该反应达到平衡状态
(4)该温度下达到平衡,此时体系压强与开始时的压强之比为
(5)其他条件不变时,下列措施不能使生成CH3OH的反应速率增大的是
a.增大CO2的浓度 b.将容器的容积变为4L
c.恒容条件下充入一定量Ne d.将恒温恒容容器改为绝热恒容容器
(6)CH4燃料电池的工作原理如图所示,a、b均为铂电极,A、B为燃料或氧气入口。

您最近一年使用:0次
名校
4 . 工业上以有机物a、一氧化碳和乙醇为原料催化合成有机物d的反应机理如图所示,下列有关叙述正确的是
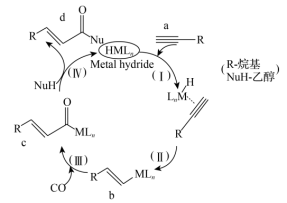
| A.a、b、c、d均存在顺反异构 |
| B.该反应的催化剂为NuH |
| C.反应(Ⅳ)是生成酮的取代反应 |
D.总反应式为  |
您最近一年使用:0次
名校
解题方法
5 . 化学用语是学习化学的重要工具,下列化学用语表述错误的是
A. 的空间填充模型为 的空间填充模型为 | B.2-甲基-2-戊烯的键线式为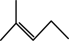 |
C.基态 的价电子排布式为 的价电子排布式为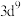 | D. 的电子式为 的电子式为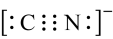 |
您最近一年使用:0次
7日内更新
|
376次组卷
|
2卷引用:吉林省长春市东北师范大学附属实验学校2023-2024学年高三下学期七模化学试题
6 . 卡维地洛类药物(丁)可用于治疗原发性高血压、有症状的充血性心力衰竭。以甲为原料合成丁的方法如下图所示。下列说法正确的是

| A.试剂X可以是足量的NaOH溶液 |
| B.乙、丙、丁均能与盐酸反应 |
| C.丙、丁互为同系物 |
| D.戊的同分异构体有3种 |
您最近一年使用:0次
名校
7 . 按要求回答下列问题:
(1)现有六种有机物,回答下列问题:_______ 。
②上述化合物中互为同分异构体的是_______ (填标号)。
(2)青蒿素(分子式为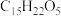 )是目前最有效的抗疟疾药物,可从黄花蒿茎叶中提取。它是无色针状晶体,可溶于乙醇、乙醚等有机溶剂,难溶于水,熔点为156℃~157℃,热稳定性差。常见的提取方法如下:
)是目前最有效的抗疟疾药物,可从黄花蒿茎叶中提取。它是无色针状晶体,可溶于乙醇、乙醚等有机溶剂,难溶于水,熔点为156℃~157℃,热稳定性差。常见的提取方法如下:_______ (填标号),操作Ⅱ为_______ 。_______ (填“共价”或“离子”)化合物。它们的晶体结构与金刚石相似,其熔点如下表所示,试分析GaN、GaP、GaAs的熔点依次降低的原因:_______ 。
(4)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方品格的八面体空隙中,晶胞结构如图所示,其中氮化钼晶胞参数anm,阿伏加德罗常数的值为 ,该晶体的密度为
,该晶体的密度为_______  (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示)。
的代数式表示)。
(1)现有六种有机物,回答下列问题:
A.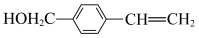 ;B.
;B.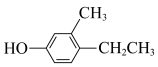 ;C.
;C. ;D.
;D. ;E.
;E. ;F.
;F. 。
。
②上述化合物中互为同分异构体的是
(2)青蒿素(分子式为
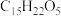 )是目前最有效的抗疟疾药物,可从黄花蒿茎叶中提取。它是无色针状晶体,可溶于乙醇、乙醚等有机溶剂,难溶于水,熔点为156℃~157℃,热稳定性差。常见的提取方法如下:
)是目前最有效的抗疟疾药物,可从黄花蒿茎叶中提取。它是无色针状晶体,可溶于乙醇、乙醚等有机溶剂,难溶于水,熔点为156℃~157℃,热稳定性差。常见的提取方法如下: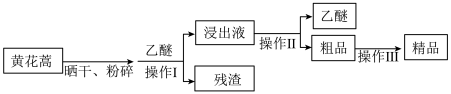
| 物质 | GaN | GaP | GaAs |
| 熔点/℃ | 1700 | 1480 | 1238 |
(4)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方品格的八面体空隙中,晶胞结构如图所示,其中氮化钼晶胞参数anm,阿伏加德罗常数的值为
 ,该晶体的密度为
,该晶体的密度为 (设阿伏加德罗常数的值为
(设阿伏加德罗常数的值为 ,用含a、
,用含a、 的代数式表示)。
的代数式表示)。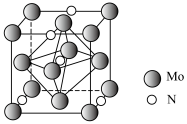
您最近一年使用:0次
名校
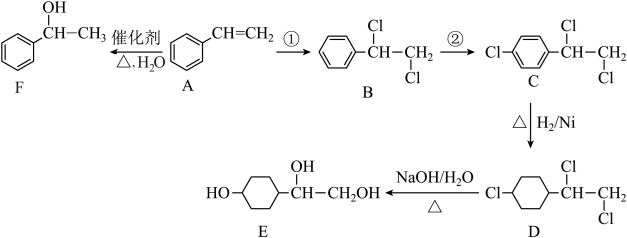
8 . 苯乙烯(A)是一种重要化工原料,以苯乙烯为原料可以制备一系列化工产品,如图所示。
(1)E中所含官能团的名称是______ ,F在一定条件下也可以得到A,则F→A的反应类型是_______ 。
(2)第②步反应所需的试剂是_______ (填化学式)。
(3)写出D→E的化学方程式:_______ 。
(4)G是F的同分异构体,其中属于酚类的G有_______ 种,其中符合核磁共振氢谱有四组峰且峰面积之比为6∶2∶1∶1的结构简式为_______ (任写一种)。
(5)X为2-甲基丙烯,以它为原料合成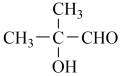 ,可利用题干信息设计如下一条合成路线。
,可利用题干信息设计如下一条合成路线。_______ 、_______ 。
(1)E中所含官能团的名称是
(2)第②步反应所需的试剂是
(3)写出D→E的化学方程式:
(4)G是F的同分异构体,其中属于酚类的G有
(5)X为2-甲基丙烯,以它为原料合成
 ,可利用题干信息设计如下一条合成路线。
,可利用题干信息设计如下一条合成路线。
您最近一年使用:0次
名校
解题方法
9 . 中国科学家参与的国际阿伏加德罗组织以高纯单晶 为样品高精度地测定了
为样品高精度地测定了 。
。
Ⅰ.高纯单晶 的制备流程如下
的制备流程如下

(1)写出基态 原子的电子排布式
原子的电子排布式___________ 。
(2) 分子的空间构型是
分子的空间构型是___________ 。
(3)③中发生分解反应,判断 的分解温度
的分解温度___________ (填“大于”或“小于”) 的分解温度,理由是
的分解温度,理由是___________ 。
Ⅱ. 的测定
的测定
(4)单晶硅的晶胞结构如图所示,X射线衍射测定其边长为apm。 以及缺陷修正值
以及缺陷修正值 (晶胞内实际原子数=理论原子数
(晶胞内实际原子数=理论原子数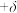 )。用上述物理量列出
)。用上述物理量列出 的计算表达式
的计算表达式___________ 。
 为样品高精度地测定了
为样品高精度地测定了 。
。Ⅰ.高纯单晶
 的制备流程如下
的制备流程如下
(1)写出基态
 原子的电子排布式
原子的电子排布式(2)
 分子的空间构型是
分子的空间构型是(3)③中发生分解反应,判断
 的分解温度
的分解温度 的分解温度,理由是
的分解温度,理由是Ⅱ.
 的测定
的测定(4)单晶硅的晶胞结构如图所示,X射线衍射测定其边长为apm。
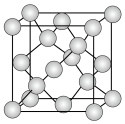
 以及缺陷修正值
以及缺陷修正值 (晶胞内实际原子数=理论原子数
(晶胞内实际原子数=理论原子数 )。用上述物理量列出
)。用上述物理量列出 的计算表达式
的计算表达式
您最近一年使用:0次
名校
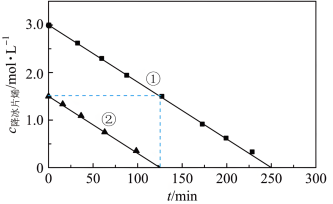
10 . 某温度下,降冰片烯( )在一定条件下聚合,反应物浓度与时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法正确的是
)在一定条件下聚合,反应物浓度与时间关系如图。已知反应物消耗一半所需的时间称为半衰期,下列说法正确的是
| A.降冰片烯与乙烯互为同系物 |
| B.其他条件相同时,降冰片烯浓度越大,反应速率越大 |
C.条件①,降冰片烯起始浓度为 时,半衰期为62.5min 时,半衰期为62.5min |
D.条件②,反应速率为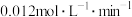 |
您最近一年使用:0次



