1 . 阿斯巴甜是市场上主流甜味剂之一,以下是以天门冬氨酸为原料合成阿斯巴甜的路线。
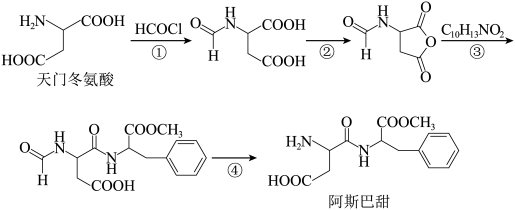
| A.天门冬氨酸难溶于乙醇、乙醚 |
| B.①④的目的是为了保护氨基 |
| C.反应过程中包含了取代反应、消去反应 |
| D.相同物质的量的阿斯巴甜分别与盐酸和氢氧化钠充分反应,消耗HCl与NaOH的物质的量之比为2∶3 |
您最近一年使用:0次
2 . 某实验小组用以下方法探究难溶物 的溶解度s(单位:
的溶解度s(单位: )。
)。
方法一,25℃时,用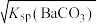 计算溶解度为
计算溶解度为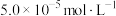 ;
;
方法二,25℃时,实验测量 的溶解度
的溶解度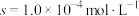 。
。
已知: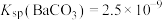 ,
, 的电离常数
的电离常数 ,
, 。
。
下列说法不正确的是
 的溶解度s(单位:
的溶解度s(单位: )。
)。方法一,25℃时,用
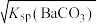 计算溶解度为
计算溶解度为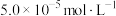 ;
;方法二,25℃时,实验测量
 的溶解度
的溶解度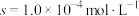 。
。已知:
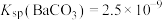 ,
, 的电离常数
的电离常数 ,
, 。
。下列说法不正确的是
A.计算值小于实验测量值的主要原因是 发生水解 发生水解 |
B. 饱和溶液中存在: 饱和溶液中存在: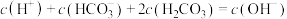 |
C. 饱和溶液中存在: 饱和溶液中存在: |
D.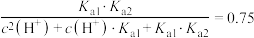 |
您最近一年使用:0次
3 . 化学反应A+B→C(放出能量)分两步进行:①A+B→X(吸收能量),②X→C(放出能量)。下列示意图中表示总反应过程中能量变化的是
A.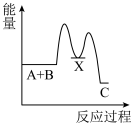 | B. |
C.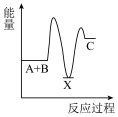 | D.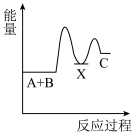 |
您最近一年使用:0次
2024-04-28更新
|
203次组卷
|
10卷引用:浙江省台州市台州八校联盟2022-2023学年高二上学期11月期中联考化学试题
浙江省台州市台州八校联盟2022-2023学年高二上学期11月期中联考化学试题辽宁省葫芦岛市2022-2023学年高一下学期7月期末考试化学试题(已下线)第04讲 化学反应与能量变化-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)山东省济宁市第一中学2023-2024学年高一下学期4月月考化学试题江苏省盐城市五校联考2023-2024学年高一下学期3月月考化学试题江苏省扬州市树人中学2023-2024学年高一下学期第一次月考化学 试题(已下线)清单03 化学反应与能量(考点清单)(讲+练)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)广西来宾市忻城县高级中学2023-2024学年高一下学期期中考试化学试卷江西省景德镇市乐平中学2023-2024学年高一下学期4月期中考试化学试题北京景山学校2023-2024学年高一下学期期中考试化学试题
4 . 下列说法不正确的是
| A.护肤品、医用软膏中的“凡士林”,其主要成分是烷烃,有润滑作用 |
| B.为了获得支链较少的聚乙烯,应选择在低压低温的情况下进行加聚反应 |
| C.利用核磁共振氢谱无法鉴别丙烯和丙醛 |
| D.可用新制氢氧化铜悬浊液鉴别甲酸、乙醛和葡萄糖溶液 |
您最近一年使用:0次
解题方法
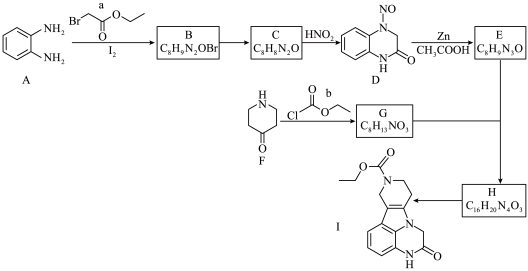
5 . 有机物I是某精神类药物的重要中间体,其合成路径如下:
(1)有机物F中的官能团名称为_____________ 。
(2)有机物B的结构简式为____________ 。
(3)下列说法正确的是 。
(4)写出E+G→H的化学方程式______________ 。
(5)重要的络合剂EDTA的结构为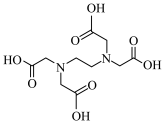 ,请以乙烯为原料,设计合成EDTA的路线(用流程图表示,无机试剂任选,最终产物可用EDTA表示)
,请以乙烯为原料,设计合成EDTA的路线(用流程图表示,无机试剂任选,最终产物可用EDTA表示)_________________ 。
(6)写出3种同时满足下列条件的化合物C的同分异构体的结构简式___________ 。
① 谱表明分子中只有3种不同化学环境的氢原子;
谱表明分子中只有3种不同化学环境的氢原子;
②分子中存在苯环,且是苯环的邻位二取代物。
①
②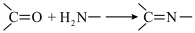
(1)有机物F中的官能团名称为
(2)有机物B的结构简式为
(3)下列说法正确的是 。
A.有机物A在水中的溶解度比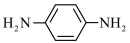 大 大 |
| B.a、b在酸性条件下水解生成的酸的酸性:a>b |
| C.A→D的三步反应均为取代反应 |
| D.H→I在适当的酸性条件下,可以提高有机物I的平衡产率 |
(4)写出E+G→H的化学方程式
(5)重要的络合剂EDTA的结构为
 ,请以乙烯为原料,设计合成EDTA的路线(用流程图表示,无机试剂任选,最终产物可用EDTA表示)
,请以乙烯为原料,设计合成EDTA的路线(用流程图表示,无机试剂任选,最终产物可用EDTA表示)(6)写出3种同时满足下列条件的化合物C的同分异构体的结构简式
①
 谱表明分子中只有3种不同化学环境的氢原子;
谱表明分子中只有3种不同化学环境的氢原子;②分子中存在苯环,且是苯环的邻位二取代物。
您最近一年使用:0次
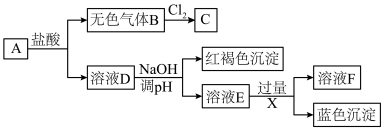
6 . 某固体混合物A由FeSO4、ZnCl2和Cu(NO3)2组成,3种物质的物质的量之比为1∶1∶1。进行如下实验:
②一些阳离子的开始沉淀至完全沉淀的范围:Fe2+(6.3~8.3)、Fe3+(1.5~2.8)、Zn2+(5.4~8.0)、Cu2+(4.7~6.2)。
③Ag2SO4微溶于硝酸。
请回答:
(1)气体B的主要成分为_____________ ,2mol气体B与1mol Cl2化合生成2mol C,C的空间构型为_____________ 。
(2)溶液F中除OH-、Cl-外的阴离子还有_____________ 。
(3)下列说法正确的是 。
(4)请设计实验检验A中的氯离子_______________ 。
(5)新制蓝色沉淀的悬浊液中通入SO2,产生紫红色固体,写出该反应离子方程式:_____________ 。
②一些阳离子的开始沉淀至完全沉淀的范围:Fe2+(6.3~8.3)、Fe3+(1.5~2.8)、Zn2+(5.4~8.0)、Cu2+(4.7~6.2)。
③Ag2SO4微溶于硝酸。
请回答:
(1)气体B的主要成分为
(2)溶液F中除OH-、Cl-外的阴离子还有
(3)下列说法正确的是 。
A.根据实验中的转化关系可得: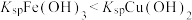 |
| B.调pH范围应控制在2.8~5.4 |
| C.X可以使用氨水或NaOH |
| D.气体B是形成光化学烟雾的罪魁祸首之一 |
(4)请设计实验检验A中的氯离子
(5)新制蓝色沉淀的悬浊液中通入SO2,产生紫红色固体,写出该反应离子方程式:
您最近一年使用:0次
解题方法
7 . 二氧化硫脲[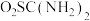 ](
](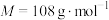 )为氮化合物的重要中间体,微溶于冷水,有还原性(碱性条件下增强)、热稳定性好。某同学利用废石膏制取二氧化硫脲,实验过程如下:
)为氮化合物的重要中间体,微溶于冷水,有还原性(碱性条件下增强)、热稳定性好。某同学利用废石膏制取二氧化硫脲,实验过程如下:
①滤液b主要成份为硫脲[ ](
](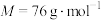 ),该物质易溶于水、有还原性。
),该物质易溶于水、有还原性。
②当pH<2时,硫脲与双氧水发生反应只生成甲脒化二硫。
③二氧化硫脲粗产品中存在尿素[ ]。
]。
请回答:
(1)仪器Y的名称是________________ 。
(2)下列说法正确的是 。
(3)装置A的气密性检查操作为___________ 。
(4)请写出溶液b生成二氧化硫脲的化学方程式_____________ 。
(5)步骤5中将溶液温度下降到5℃的目的是______________ 。
(6)为了检验产品中二氧化硫脲的含量(主要杂质为硫脲,其他杂质不参与反应),该同学设计了如下实验:
①称取5.000g产品,配制成100mL溶液。取10.00mL待测液于碘量瓶中,加入20.00mL 1.500 NaOH溶液,再加入25.00mL 0.5000
NaOH溶液,再加入25.00mL 0.5000 I2标准溶液,静置一段时间,加入适量硫酸进行酸化,改用0.5000
I2标准溶液,静置一段时间,加入适量硫酸进行酸化,改用0.5000
 溶液进行滴定,测得消耗
溶液进行滴定,测得消耗 溶液体积为10.00mL。
溶液体积为10.00mL。
涉及到的反应有:
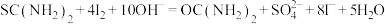
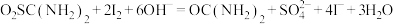

②另取0.1000g产品,加入50.00mL 0.1000 NaOH溶液,再加入30.00mL 3.000%
NaOH溶液,再加入30.00mL 3.000%  溶液,静置2分钟。改用0.1000
溶液,静置2分钟。改用0.1000
 溶液进行滴定,测得消耗
溶液进行滴定,测得消耗 溶液为16.00mL。
溶液为16.00mL。
涉及到的反应有:
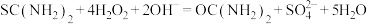


该产品中二氧化硫脲的质量分数为____________ 。
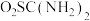 ](
](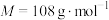 )为氮化合物的重要中间体,微溶于冷水,有还原性(碱性条件下增强)、热稳定性好。某同学利用废石膏制取二氧化硫脲,实验过程如下:
)为氮化合物的重要中间体,微溶于冷水,有还原性(碱性条件下增强)、热稳定性好。某同学利用废石膏制取二氧化硫脲,实验过程如下: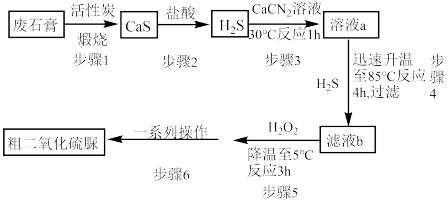

①滤液b主要成份为硫脲[
 ](
](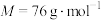 ),该物质易溶于水、有还原性。
),该物质易溶于水、有还原性。②当pH<2时,硫脲与双氧水发生反应只生成甲脒化二硫。
③二氧化硫脲粗产品中存在尿素[
 ]。
]。请回答:
(1)仪器Y的名称是
(2)下列说法正确的是 。
A.装置B中装的X溶液为饱和 溶液 溶液 |
B.装置E中的 与 与 发生氧化还原反应,起到尾气处理的作用 发生氧化还原反应,起到尾气处理的作用 |
| C.装置F中可分多次加入碳酸氢铵,以提高二氧化硫脲的产率 |
| D.步骤6“一系列操作”可为减压过滤,用冷水洗涤沉淀2-3次,一定温度下烘干沉淀 |
(3)装置A的气密性检查操作为
(4)请写出溶液b生成二氧化硫脲的化学方程式
(5)步骤5中将溶液温度下降到5℃的目的是
(6)为了检验产品中二氧化硫脲的含量(主要杂质为硫脲,其他杂质不参与反应),该同学设计了如下实验:
①称取5.000g产品,配制成100mL溶液。取10.00mL待测液于碘量瓶中,加入20.00mL 1.500
 NaOH溶液,再加入25.00mL 0.5000
NaOH溶液,再加入25.00mL 0.5000 I2标准溶液,静置一段时间,加入适量硫酸进行酸化,改用0.5000
I2标准溶液,静置一段时间,加入适量硫酸进行酸化,改用0.5000
 溶液进行滴定,测得消耗
溶液进行滴定,测得消耗 溶液体积为10.00mL。
溶液体积为10.00mL。涉及到的反应有:
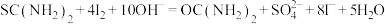
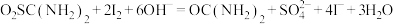

②另取0.1000g产品,加入50.00mL 0.1000
 NaOH溶液,再加入30.00mL 3.000%
NaOH溶液,再加入30.00mL 3.000%  溶液,静置2分钟。改用0.1000
溶液,静置2分钟。改用0.1000
 溶液进行滴定,测得消耗
溶液进行滴定,测得消耗 溶液为16.00mL。
溶液为16.00mL。涉及到的反应有:
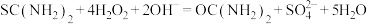


该产品中二氧化硫脲的质量分数为
您最近一年使用:0次
解题方法
8 . P可形成许多结构和性质特殊的化合物。请回答下列问题:
(1)P元素位于周期表的第15列。
①基态P原子的价电子轨道表示式为___________ 。
②下列说法不正确的是________ 。
A.非金属性:As<P<N
B.第二电离能( )大小:
)大小: (Si)<
(Si)< (P)<
(P)< (S)<
(S)< (Na)
(Na)
C.电负性:P<As<O
D.O-H键的键能: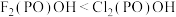
(2)常温下,五氯化磷为白色固体,熔融状态下能导电,气态时以PCl5分子存在。
①气态PCl5分子结构如图所示,O位于等边三角形ABC的中心,DOE垂直于ABC的平面,黑球为P,白球为Cl,比较键长大小:键长OD________ OA(填“>”“<”或“=”)。__________ 。
③PCl5不能与金属Ni反应,而PCl3能与金属Ni反应,解释PCl3能与金属Ni反应的原因_____________ 。
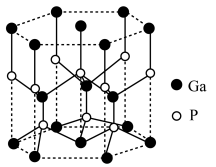
(3)Ga与P形成的某化合物晶体的结构如图。该化合物的化学式为____________ ,P的配位数为____________ 。
(1)P元素位于周期表的第15列。
①基态P原子的价电子轨道表示式为
②下列说法不正确的是
A.非金属性:As<P<N
B.第二电离能(
 )大小:
)大小: (Si)<
(Si)< (P)<
(P)< (S)<
(S)< (Na)
(Na)C.电负性:P<As<O
D.O-H键的键能:
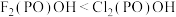
(2)常温下,五氯化磷为白色固体,熔融状态下能导电,气态时以PCl5分子存在。
①气态PCl5分子结构如图所示,O位于等边三角形ABC的中心,DOE垂直于ABC的平面,黑球为P,白球为Cl,比较键长大小:键长OD
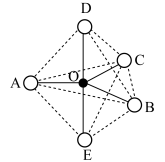
③PCl5不能与金属Ni反应,而PCl3能与金属Ni反应,解释PCl3能与金属Ni反应的原因
(3)Ga与P形成的某化合物晶体的结构如图。该化合物的化学式为
您最近一年使用:0次
9 . 根据实验目的,下列实验方案、现象和结论都正确的是.
选项 | 实验目的 | 实验方案 | 实验现象 | 实验结论 |
A | 测定中和热 | 分别量取50mL 0.5 的盐酸和50mL 0.55 的盐酸和50mL 0.55 的NaOH溶液,迅速加入量热器中,测量起始温度,盖上杯盖,搅棒器搅拌 的NaOH溶液,迅速加入量热器中,测量起始温度,盖上杯盖,搅棒器搅拌 | 温度计温度上升,记录最高温度 | 多次试验后,根据温度差和比热容可计算反应热 |
B | 不同催化剂对双氧水的催化效率 | 5%的 分为A、B两组,分别加入4滴0.1 分为A、B两组,分别加入4滴0.1 的 的 溶液和 溶液和 溶液,记录单位时间内产生的气体量 溶液,记录单位时间内产生的气体量 | A组产生气体更多 |  的催化效果强于 的催化效果强于 |
C | 对比蛋白质的盐析和变性 | 取两组鸡蛋清溶液,分为A、B组,分别加入饱和氯化钠溶液和浓硝酸,之后加入清水 | 均有白色沉淀产生,加入清水后,A组溶液沉淀溶解,B组沉淀不变 | 盐析产生的沉淀会重新溶解而变性不会 |
D | 比较 、 、 与 与 的配位能力 的配位能力 | 在 溶液中,加入足量NaCl固体 溶液中,加入足量NaCl固体 | 溶液红色变浅 |  与 与 的配位能力强于 的配位能力强于 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 某实验小组利用下列装置来降低某硬水中 、
、 和
和 的含量,
的含量,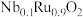 和
和 为极板催化剂。下列说法不正确的是
为极板催化剂。下列说法不正确的是
 、
、 和
和 的含量,
的含量,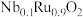 和
和 为极板催化剂。下列说法不正确的是
为极板催化剂。下列说法不正确的是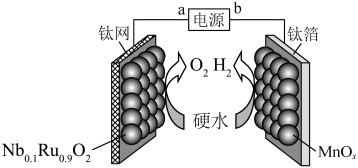
| A.a端电势高于b端电势 |
B.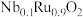 可加快 可加快 失去电子的速率 失去电子的速率 |
C.其它条件不变,适当减小两极的极板间距, 、 、 沉淀速率增大 沉淀速率增大 |
D.阳极区收集的气体中只含有 |
您最近一年使用:0次



