名校
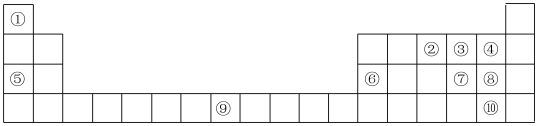
1 . (Ⅰ)如表为元素周期表的部分,列出了10种元素在元素周期表中的位置,试回答下列问题:_______ 。
(2)元素⑤和③的单质加热生成产物中含有的化学键类型为_______ 。
(3)元素⑨在周期表中的位置是_______ 。
(Ⅱ)L、M、N、Q、R、T分别代表上述十种元素之一,其原子半径及主要化合价关系如表:
(4)写出M最高价氧化物对应的水化物与N的最高价含氧酸反应的化学方程式:________ 。
(5)用一个离子方程式证明N和Q两元素的非金属性强弱:_______ 。
(6)R与T形成的简单氢化物的沸点较高的是:_______ (填化学式)。
(7)L、M、Q、R四种元素形成的简单离子半径从大到小的顺序为_______ (用相应的离子符号表示)。
(2)元素⑤和③的单质加热生成产物中含有的化学键类型为
(3)元素⑨在周期表中的位置是
(Ⅱ)L、M、N、Q、R、T分别代表上述十种元素之一,其原子半径及主要化合价关系如表:
| 元素代号 | L | M | N | Q | R | T |
| 原子半径/nm | 0.186 | 0.143 | 0.099 | 0.114 | 0.104 | 0.066 |
| 主要化合价 | +1 | +3 | +7、-1 | +7、-1 | +6、-2 | -2 |
(4)写出M最高价氧化物对应的水化物与N的最高价含氧酸反应的化学方程式:
(5)用一个离子方程式证明N和Q两元素的非金属性强弱:
(6)R与T形成的简单氢化物的沸点较高的是:
(7)L、M、Q、R四种元素形成的简单离子半径从大到小的顺序为
您最近一年使用:0次
2024-02-01更新
|
261次组卷
|
2卷引用:河南省洛阳市宜阳县第一高级中学2023-2024学年高一下学期期中考试化学试卷(研学班)
名校
解题方法
2 . 现有部分短周期主族元素的性质或原子结构如表所示:
A、B、D三种单质(单质分别由X、Y、Z元素组成)和甲、乙、丙、丁四种化合物之间的转化关系如图所示(某些条件已略去)。其中丁是一种高能燃料,常用于火箭推进剂,1个丁分子中含有18个电子,其组成元素与丙相同。
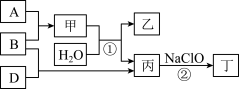
请回答:
(1)元素X在周期表中的位置是_______ ,元素Y的原子结构示意图为_______ 。
(2)单质B电子式为_______ ,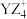 中心原子杂化类型为
中心原子杂化类型为_______ ,空间结构为_______ 。
(3)分子中的大π键可以用符号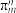 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则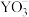 中中心原子价层电子对数为
中中心原子价层电子对数为_______ ,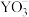 的大π键可表示为
的大π键可表示为_______ 。
(4)丙中所包含的化学键类型有_______ (填字母序号)。
A.离子键 B.极性共价键 C.非极性共价键
(5)反应①的化学方程式为_______ 。
(6)反应②中,0.5molNaClO参加反应时,转移1mol电子,反应②的离子方程式为:_______ 。
| 元素编号 | 元素性质或原子结构 |
| X | 其电子层上M层与K层上的电子数相等 |
| Y | 其最简单氢化物丙的水溶液呈碱性 |
| Z | 其原子半径在所有原子中最小 |

请回答:
(1)元素X在周期表中的位置是
(2)单质B电子式为
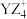 中心原子杂化类型为
中心原子杂化类型为(3)分子中的大π键可以用符号
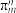 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则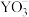 中中心原子价层电子对数为
中中心原子价层电子对数为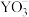 的大π键可表示为
的大π键可表示为(4)丙中所包含的化学键类型有
A.离子键 B.极性共价键 C.非极性共价键
(5)反应①的化学方程式为
(6)反应②中,0.5molNaClO参加反应时,转移1mol电子,反应②的离子方程式为:
您最近一年使用:0次
2023-01-13更新
|
167次组卷
|
2卷引用:河南省洛阳市洛宁县第一高级中学2022-2023学年高二下学期2月月考化学试题
3 . 芳香族化合物A(C9H12O)可用于医药及香料的合成,A有如下转化关系:
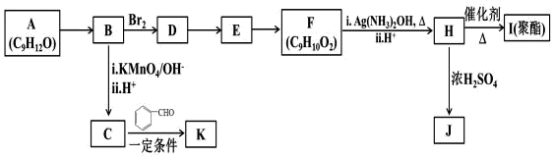
已知:
①A除苯环上的氢以外,核磁共振氢谱还有二组峰,且峰面积之比为1:6;
②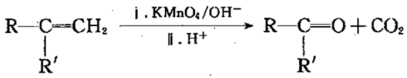 ;
;
③RCOCH3+RCHO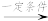 R'COCH=CHR'
R'COCH=CHR'
回答下列问题:
(1)由D生成E的反应类型为_____ ,F所含官能团的名称为_____ 。
(2)请写出B的结构简式________ 。
(3)由E生成F的反应方程式为_________ 。
(4)J为一种具有3个六元环的酯,则其结构简式为_____________ 。
(5)F的同分异构体中,苯环上的一氯代物有3种,且能与NaHCO3反应生成CO2的结构有_______ 种。
(6)糖叉丙酮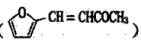 是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁基氯[(CH3)3CCl]和糠醛
是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁基氯[(CH3)3CCl]和糠醛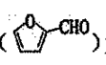 为原料制备糖叉丙酮的合成路线
为原料制备糖叉丙酮的合成路线______ (无机试剂任用)。合成流程图示例如下: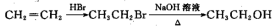

已知:
①A除苯环上的氢以外,核磁共振氢谱还有二组峰,且峰面积之比为1:6;
②
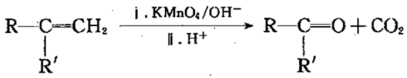 ;
;③RCOCH3+RCHO
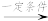 R'COCH=CHR'
R'COCH=CHR'回答下列问题:
(1)由D生成E的反应类型为
(2)请写出B的结构简式
(3)由E生成F的反应方程式为
(4)J为一种具有3个六元环的酯,则其结构简式为
(5)F的同分异构体中,苯环上的一氯代物有3种,且能与NaHCO3反应生成CO2的结构有
(6)糖叉丙酮
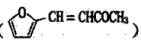 是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁基氯[(CH3)3CCl]和糠醛
是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁基氯[(CH3)3CCl]和糠醛 为原料制备糖叉丙酮的合成路线
为原料制备糖叉丙酮的合成路线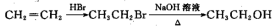
您最近一年使用:0次
名校
解题方法
4 . 芳香族化合物A(C9H12O)常用于药物及香料的合成,A有如下转化关系:
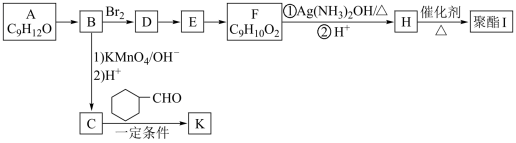
已知:
①A的苯环上只有一个支链,支链上有两种不同环境的氢原子
②
③RCOCH3+R'CHO RCOCH=CHR'+H2O
RCOCH=CHR'+H2O
回答下列问题:
(1)A生成B的反应类型为__________ ,由D生成E的反应条件为_______________ 。
(2)H中含有的官能团名称为______________ 。
(3)I的结构简式为__________________________ 。
(4)由E生成F的化学方程式为____________________________________________ 。
(5)F有多种同分异构体,写出一种符合下列条件的同分异构体的结构简式为:___________________ 。
①能发生水解反应和银镜反应
②属于芳香族化合物且分子中只有一个甲基
③具有5组核磁共振氢谱峰
(6)糠叉丙酮(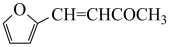 )是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇[(CH3)3COH]和糠醛(
)是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇[(CH3)3COH]和糠醛(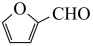 )为原料制备糠叉丙酮的合成路线(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):
)为原料制备糠叉丙酮的合成路线(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):___________________ 。

已知:
①A的苯环上只有一个支链,支链上有两种不同环境的氢原子
②

③RCOCH3+R'CHO
 RCOCH=CHR'+H2O
RCOCH=CHR'+H2O回答下列问题:
(1)A生成B的反应类型为
(2)H中含有的官能团名称为
(3)I的结构简式为
(4)由E生成F的化学方程式为
(5)F有多种同分异构体,写出一种符合下列条件的同分异构体的结构简式为:
①能发生水解反应和银镜反应
②属于芳香族化合物且分子中只有一个甲基
③具有5组核磁共振氢谱峰
(6)糠叉丙酮(
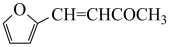 )是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇[(CH3)3COH]和糠醛(
)是一种重要的医药中间体,请参考上述合成路线,设计一条由叔丁醇[(CH3)3COH]和糠醛(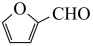 )为原料制备糠叉丙酮的合成路线(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):
)为原料制备糠叉丙酮的合成路线(无机试剂任选,用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件):
您最近一年使用:0次
2018-04-03更新
|
1061次组卷
|
13卷引用:河南省洛阳市第一高级中学2019-2020学年高二下学期5月月考化学试题
河南省洛阳市第一高级中学2019-2020学年高二下学期5月月考化学试题江西省南昌市2018届高三第一次模拟考试理科综合化学试题吉林省实验中学2018届高三第八次月考(第四次模拟)理科综合化学试题【全国市级联考】山西省太原市2018届高三模拟考试理综化学试题备考突破2020高三化学专题强化集训——化学有机推断题2019年四川省内江市高三上学期第一次模拟考试化学试题【全国百强校】安徽省六安市第一中学2020届高三下学期自测(二)化学试题四川省成都市树德中学 2020届高三三诊模拟考试理科综合化学试题河南省南阳市六校2021-2022学年高二下学期5月份联考化学试题湖北省麻城市实验高级中学2021-2022学年高三下学期第一次联考化学试题四川省内江市高中2020届高三上学期第一次模拟考试 理综化学黑龙江省牡丹江市第二高级中学2022-2023学年高二下学期7月期末化学试题河南省济源一中2022-2023学年高二下学期6月月考化学试题
名校
解题方法
5 . 已知氮元素及其化合物的转化关系如图所示,回答下列问题。

(1)①~④各步转化中,属于氮的固定的是_______ (填标号)。
(2)工业生产中利用N2和H2合成氨,一定的温度下,在容积不变的密闭容器中发生反应N2 (g)+3 H2 (g) 2 NH3 (g), 下列说法能说明反应已经达到化学平衡状态的是_______ (填标号)。
2 NH3 (g), 下列说法能说明反应已经达到化学平衡状态的是_______ (填标号)。
(3)某化学兴趣小组利用如图所示的装置探究干燥的氯气与干燥的氨气之间的反应。

回答下列问题:
①若装置A圆底烧瓶中的固体为生石灰,则试剂a的名称为_______ ,盛装试剂a的仪器的名称为_____
②装置F用于制取氯气,当制得2.24 L(已折合成标准状况)氯气时,转移的电子的物质的量为_______ mol 。
③装置B中盛装的试剂X(固体混合物)的主要成分为_______ (填化学式),能否用无水CaCl2代替?_______ (填“能”或“不能”)。
④反应过程中,装置C的集气瓶中有大量白烟产生,同时还生成一种气体单质,则反应的化学方程式为______ 。

(1)①~④各步转化中,属于氮的固定的是
(2)工业生产中利用N2和H2合成氨,一定的温度下,在容积不变的密闭容器中发生反应N2 (g)+3 H2 (g)
 2 NH3 (g), 下列说法能说明反应已经达到化学平衡状态的是_______ (填标号)。
2 NH3 (g), 下列说法能说明反应已经达到化学平衡状态的是_______ (填标号)。| A.容器内气体的密度不再发生变化 |
| B.容器内N2和NH3的物质的量之比不再发生变化 |
| C.单位时间内断开n mol N≡N键,同时生成6n mol N—H键 |
| D.容器内气体的压强不再发生变化 |

回答下列问题:
①若装置A圆底烧瓶中的固体为生石灰,则试剂a的名称为
②装置F用于制取氯气,当制得2.24 L(已折合成标准状况)氯气时,转移的电子的物质的量为
③装置B中盛装的试剂X(固体混合物)的主要成分为
④反应过程中,装置C的集气瓶中有大量白烟产生,同时还生成一种气体单质,则反应的化学方程式为
您最近一年使用:0次
2023-06-03更新
|
100次组卷
|
2卷引用:南省洛阳创新发展联盟2022-2023学年高一下学期6月阶段性考试化学试题
名校
6 . 填空。
(1)下列各烷烃的沸点由高到低的顺序为_______ (用字母表示)
A.正戊烷 B.异戊烷 C.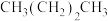 D.新戊烷 E.
D.新戊烷 E.
(2)某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。下列物质中,与该物质互为同系物的是(填序号)_______ ,互为同分异构体的是(填序号)_______ 。

A. B.
B.
C.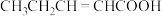 D.
D.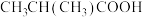
(3)已知端炔烃在催化剂存在下可发生偶联反应: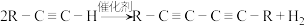 称为Glaser反应,已知:
称为Glaser反应,已知: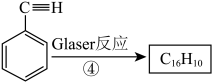 ,该转化关系的产物E(
,该转化关系的产物E(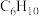 )的结构简式是
)的结构简式是_______ ,用1molE合成1,4-二苯基丁烷,理论上需要消耗_______ mol氢气。
(4)已知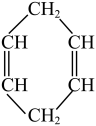 可简写为
可简写为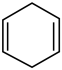 ,现有某化合物W的分子结构可表示为
,现有某化合物W的分子结构可表示为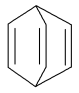
①W的一氯代物有_______ 种;
②下列有关W的说法不正确的是_______ (填编号);
a.能发生还原反应
b.能发生氧化反应
c.等质量的W与苯分别完全燃烧所消耗的氧气量,前者大
d.与苯互为同分异构体
③写出W的芳香族同分异构体(能发生聚合反应)的结构简式_______ ;该聚合反应的化学方程式为_______
④W属于_______ (填编号)。
a.芳香烃b.环烃c.不饱和烃d.炔烃
(1)下列各烷烃的沸点由高到低的顺序为
A.正戊烷 B.异戊烷 C.
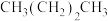 D.新戊烷 E.
D.新戊烷 E.
(2)某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。下列物质中,与该物质互为同系物的是(填序号)

A.
 B.
B.
C.
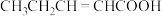 D.
D.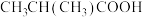
(3)已知端炔烃在催化剂存在下可发生偶联反应:
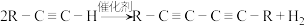 称为Glaser反应,已知:
称为Glaser反应,已知: ,该转化关系的产物E(
,该转化关系的产物E(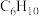 )的结构简式是
)的结构简式是(4)已知
 可简写为
可简写为 ,现有某化合物W的分子结构可表示为
,现有某化合物W的分子结构可表示为
①W的一氯代物有
②下列有关W的说法不正确的是
a.能发生还原反应
b.能发生氧化反应
c.等质量的W与苯分别完全燃烧所消耗的氧气量,前者大
d.与苯互为同分异构体
③写出W的芳香族同分异构体(能发生聚合反应)的结构简式
④W属于
a.芳香烃b.环烃c.不饱和烃d.炔烃
您最近一年使用:0次
2023-03-06更新
|
376次组卷
|
2卷引用:河南省洛阳市第一高级中学2022-2023学年高二下学期4月月考化学试题
解题方法
7 . 氮是一种重要的元素,含氮化合物是化工、能源、环保等领域的研究热点。回答下列问题:
(1)已知:
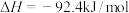

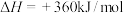

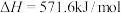
试写出表示氨气的燃烧热的热化学方程式:_______ 。
(2)已知:合成尿素 的反应为
的反应为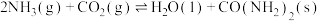
 。向恒容密闭容器中按物质的量之比4:1充入
。向恒容密闭容器中按物质的量之比4:1充入 和
和 ,使反应进行,保持温度不变,测得
,使反应进行,保持温度不变,测得 的转化率随时问的变化情况如图所示。
的转化率随时问的变化情况如图所示。

①若用 的浓度变化表示反应速率,则A点的逆反应速率
的浓度变化表示反应速率,则A点的逆反应速率_______ (填“>”“<”或“=”) B点的正反应速率。
②下列叙述中不能说明该反成达到平衡状态的是_______ (填选项字母)。
A.体系压强不再变化
B.气体平均摩尔质量不再变化
C. 的消耗速率和
的消耗速率和 的消耗速率之比为2:1
的消耗速率之比为2:1
D.固体质量不再发生变化
③工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有_______ (填选项字母)。
A.升高温度 B.充入氮气 C.将尿素及时分离出去 D.增大反应体系的压强
(3)传统的尿素生产,以二氧化碳和氨在高温、高压下,合成、转化得到,工艺耗能较高,且产率较低。最近我国科学家发现 纳米片负载的Pd-Cu合金纳米颗粒电催化剂可以将水溶液中的
纳米片负载的Pd-Cu合金纳米颗粒电催化剂可以将水溶液中的 和
和 直接转化为尿素(反应机理如下图所示,*表示催化剂活性中心原子)。
直接转化为尿素(反应机理如下图所示,*表示催化剂活性中心原子)。

根据以上反应机理,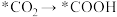 的过程中,断裂的是
的过程中,断裂的是_______ (填“极性键”或“非极性键”,下同),形成的是_______ 。与传统生产工艺相比,这种新方法的优点是_______ (答出一点即可)。
(4)氨催化氧化时会发生下列两个竞争反应I、II。
反应I: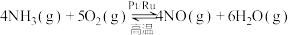 ;
;
反应II: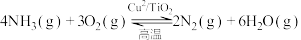 。
。
为分析某催化剂对该反成的选择性,在1L密闭容器中充入1mol 和2mol
和2mol ,测得有关物质的量关系如下图:
,测得有关物质的量关系如下图:
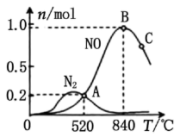
该催化剂在高温时选择反应_______ (填“I”或“II”)。
(1)已知:

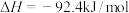

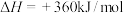

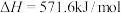
试写出表示氨气的燃烧热的热化学方程式:
(2)已知:合成尿素
 的反应为
的反应为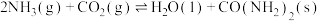
 。向恒容密闭容器中按物质的量之比4:1充入
。向恒容密闭容器中按物质的量之比4:1充入 和
和 ,使反应进行,保持温度不变,测得
,使反应进行,保持温度不变,测得 的转化率随时问的变化情况如图所示。
的转化率随时问的变化情况如图所示。
①若用
 的浓度变化表示反应速率,则A点的逆反应速率
的浓度变化表示反应速率,则A点的逆反应速率②下列叙述中不能说明该反成达到平衡状态的是
A.体系压强不再变化
B.气体平均摩尔质量不再变化
C.
 的消耗速率和
的消耗速率和 的消耗速率之比为2:1
的消耗速率之比为2:1 D.固体质量不再发生变化
③工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有
A.升高温度 B.充入氮气 C.将尿素及时分离出去 D.增大反应体系的压强
(3)传统的尿素生产,以二氧化碳和氨在高温、高压下,合成、转化得到,工艺耗能较高,且产率较低。最近我国科学家发现
 纳米片负载的Pd-Cu合金纳米颗粒电催化剂可以将水溶液中的
纳米片负载的Pd-Cu合金纳米颗粒电催化剂可以将水溶液中的 和
和 直接转化为尿素(反应机理如下图所示,*表示催化剂活性中心原子)。
直接转化为尿素(反应机理如下图所示,*表示催化剂活性中心原子)。
根据以上反应机理,
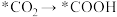 的过程中,断裂的是
的过程中,断裂的是(4)氨催化氧化时会发生下列两个竞争反应I、II。
反应I:
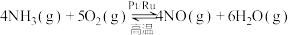 ;
;反应II:
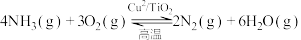 。
。为分析某催化剂对该反成的选择性,在1L密闭容器中充入1mol
 和2mol
和2mol ,测得有关物质的量关系如下图:
,测得有关物质的量关系如下图:
该催化剂在高温时选择反应
您最近一年使用:0次



