解题方法
1 . 实验室用如图装置制备 并验证相关物质的性质。下列有关试剂A说法正确的是
并验证相关物质的性质。下列有关试剂A说法正确的是
 并验证相关物质的性质。下列有关试剂A说法正确的是
并验证相关物质的性质。下列有关试剂A说法正确的是
A.若为 水溶液,可验证 水溶液,可验证 的还原性 的还原性 |
B.若为 溶液,则发生氧化还原反应 溶液,则发生氧化还原反应 |
| C.若为溴水,观察到溶液出现淡黄色浑浊 |
D.若为含 和AgCl的浊液,可证明 和AgCl的浊液,可证明 : :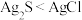 |
您最近一年使用:0次
2 . 实验室利用铁粉与葡萄糖酸制备补铁剂葡萄糖酸亚铁,实验装置如图所示(夹持和加热仪器已省略)。下列相关说法正确的是
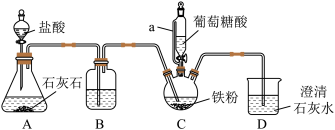

| A.A装置中盐酸可以换成硫酸 |
B.B装置利用饱和的碳酸钠溶液除去二氧化碳气体中混有的 |
| C.C装置中葡萄糖酸滴下一段时间后再打开A装置滴下盐酸 |
| D.D装置中出现白色浑浊,证明装置内的空气已排尽 |
您最近一年使用:0次
名校
3 . 盐碱地是土壤表层集聚过多盐碱成分,对农作物有害的土地。回答下列问题:
(1)盐碱地(含较多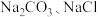 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为___________ (用离子方程式说明);已知 时,
时, 的
的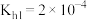 ,则当
,则当 溶液中
溶液中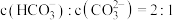 时,溶液的
时,溶液的
___________ 。
(2) 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液___________ (填“喷在叶片上”或“随水灌入土壤中”),主要理由是___________ 。
(3)已知:常温下,碳酸的电离平衡常数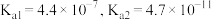 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加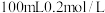 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
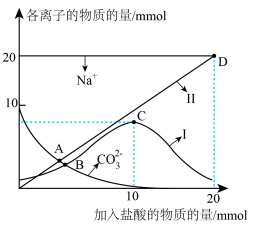
①曲线Ⅰ代表的离子是_______ 。
②A、B两点水的电离程度大小为A_______ B。
③根据上图,下列有关说法不正确的是_______ 。
a.滴加至 点时,
点时,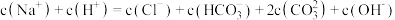
b.滴加至 点时,
点时,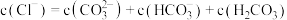
c.滴加至 点时,溶液
点时,溶液
④已知 电离平衡常数约为
电离平衡常数约为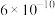 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱_______ 。
⑤证明 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是_______ 。
(1)盐碱地(含较多
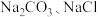 )不利于植物生长,盐碱地呈碱性的原因为
)不利于植物生长,盐碱地呈碱性的原因为 时,
时, 的
的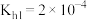 ,则当
,则当 溶液中
溶液中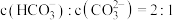 时,溶液的
时,溶液的
(2)
 是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液
是农作物生长过程中不可缺少的微量元素。常用的铜肥是胆矾,在盐碱地施用胆矾时宜将其溶液(3)已知:常温下,碳酸的电离平衡常数
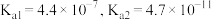 。常温下,向
。常温下,向 溶液中缓慢滴加
溶液中缓慢滴加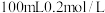 盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸,溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。根据图回答下列问题:
未画出)。根据图回答下列问题:
①曲线Ⅰ代表的离子是
②A、B两点水的电离程度大小为A
③根据上图,下列有关说法不正确的是
a.滴加至
 点时,
点时,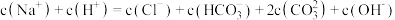
b.滴加至
 点时,
点时,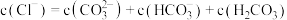
c.滴加至
 点时,溶液
点时,溶液
④已知
 电离平衡常数约为
电离平衡常数约为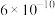 ,用一个离子方程式说明
,用一个离子方程式说明 和
和 结合
结合 能力的相对强弱
能力的相对强弱⑤证明
 是弱电解质,你的设计方案是
是弱电解质,你的设计方案是
您最近一年使用:0次
2023-12-13更新
|
65次组卷
|
2卷引用:广东省佛山市H7教育共同体2023-2024学年高二上学期联考化学试题
名校
解题方法
4 . 下列有关钠的化合物的说法正确的是
| A.用加热法除去NaHCO3固体中混有的Na2CO3 |
| B.Na2O2与H2O的反应中有氢氧化钠生成,Na2O2是典型的碱性氧化物 |
| C.向酚酞溶液中加入过量的过氧化钠粉末,可以观察到溶液的颜色变化:先变红,后褪色 |
| D.某溶液样品的焰色试验火焰呈黄色,证明原溶液中有钠元素,一定没有钾元素 |
您最近一年使用:0次
2023-11-07更新
|
249次组卷
|
2卷引用:广东省部分名校2023-2024学年高一上学期期中联合考试化学试题
5 . 某实验小组用下列装置制备溴苯,下列说法错误的是
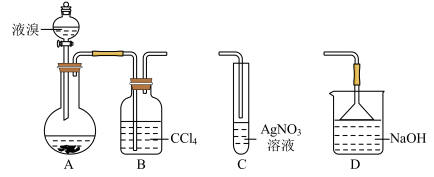
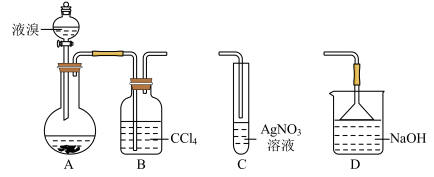
| A.若装置B后连接装置C,装置C中生成淡黄色沉淀,可证明装置A中发生取代反应 |
B.装置A中长玻璃导管仅起冷凝回流作用,装置B中的实验现象是 由无色变橙色 由无色变橙色 |
| C.若装置B后连接装置D,则装置D的作用是吸收尾气 |
| D.向反应后的装置A中加入NaOH溶液,振荡静置,下层为无色油状液体 |
您最近一年使用:0次
名校
6 . I.如图是乙酸乙酯的绿色合成路线之一:
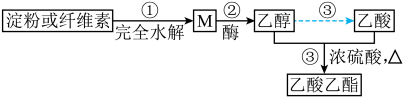
(1)M的分子式为___________ ,作为营养剂供给人体能量,在体内发生的主要反应类型是___________ ;
(2)下列说法不正确的是___________(填字母序号)。
Ⅱ.实验室制取乙酸乙酯的主要步骤如下:
①在甲试管(如图)中加入 浓硫酸、
浓硫酸、 乙醇和
乙醇和 乙酸的混合溶液。
乙酸的混合溶液。
②按如图连接好装置(装置气密性良好)并加入混合液,小火均匀地加热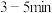 。
。
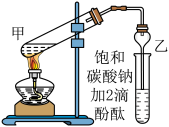
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
(3)若实验中用乙酸和含 的乙醇作用,该反应的化学方程式是:
的乙醇作用,该反应的化学方程式是:___________ ;
(4)上述实验中饱和碳酸钠溶液的作用是___________ (填字母代号);
A.反应掉乙酸并吸收乙醇
B.加速酯的生成,提高其产率
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
(5)欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器是___________ ,分液时,乙酸乙酯应该从仪器___________ (填:“下口放”或“上口倒”)出;
(6)生成乙酸乙酯的反应是可逆反应,反应一段时间后,下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有___________ (填序号);
①混合物中各物质的浓度不再变化;
②单位时间里,生成 乙醇,同时生成
乙醇,同时生成 乙酸;
乙酸;
③单位时间里,生成 乙酸乙酯,同时生成
乙酸乙酯,同时生成 乙酸。
乙酸。
④单位时间里,生成 乙酸乙酯,同时生成
乙酸乙酯,同时生成 水
水
(7)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热 ,再加热使之微微沸腾
,再加热使之微微沸腾 。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
①实验D的目的是与实验C相对照,证明 对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是
对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是___________ mL和___________  。
。
②分析实验___________ (填实验编号)的数据,可以推测出浓 的吸水性提高了乙酸乙酯的产率;
的吸水性提高了乙酸乙酯的产率;
(8)若现有乙酸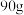 ,乙醇
,乙醇 发生酯化反应得到
发生酯化反应得到 乙酸乙酯,试计算该反应的产品产率为
乙酸乙酯,试计算该反应的产品产率为___________ (产率%= ×100%)。
×100%)。

(1)M的分子式为
(2)下列说法不正确的是___________(填字母序号)。
| A.淀粉和纤维素都属于天然高分子化合物 |
| B.M可与银氨溶液发生银镜反应 |
| C.所有的糖类都有甜味,都可以发生水解反应 |
| D.用KI溶液可以检验淀粉 |
Ⅱ.实验室制取乙酸乙酯的主要步骤如下:
①在甲试管(如图)中加入
 浓硫酸、
浓硫酸、 乙醇和
乙醇和 乙酸的混合溶液。
乙酸的混合溶液。②按如图连接好装置(装置气密性良好)并加入混合液,小火均匀地加热
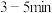 。
。
③待试管乙收集到一定量产物后停止加热,撤出试管并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
(3)若实验中用乙酸和含
 的乙醇作用,该反应的化学方程式是:
的乙醇作用,该反应的化学方程式是:(4)上述实验中饱和碳酸钠溶液的作用是
A.反应掉乙酸并吸收乙醇
B.加速酯的生成,提高其产率
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中更小,有利于分层析出
(5)欲将乙试管中的物质分离以得到乙酸乙酯,必须使用的仪器是
(6)生成乙酸乙酯的反应是可逆反应,反应一段时间后,下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有
①混合物中各物质的浓度不再变化;
②单位时间里,生成
 乙醇,同时生成
乙醇,同时生成 乙酸;
乙酸;③单位时间里,生成
 乙酸乙酯,同时生成
乙酸乙酯,同时生成 乙酸。
乙酸。④单位时间里,生成
 乙酸乙酯,同时生成
乙酸乙酯,同时生成 水
水(7)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热
 ,再加热使之微微沸腾
,再加热使之微微沸腾 。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:| 实验编号 | 试管I中试剂 | 试管II中试剂 | 有机层的厚度/cm |
| A |  乙醇、 乙醇、 乙酸、 乙酸、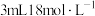 浓硫酸 浓硫酸 | 饱和 溶液 溶液 | 3.0 |
| B |  乙醇、 乙醇、 乙酸、 乙酸、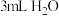 | 0.1 | |
| C |  乙醇、 乙醇、 乙酸、 乙酸、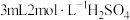 | 0.6 | |
| D |  乙醇、 乙醇、 乙酸、盐酸 乙酸、盐酸 | 0.6 |
 对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是
对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是 。
。②分析实验
 的吸水性提高了乙酸乙酯的产率;
的吸水性提高了乙酸乙酯的产率;(8)若现有乙酸
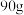 ,乙醇
,乙醇 发生酯化反应得到
发生酯化反应得到 乙酸乙酯,试计算该反应的产品产率为
乙酸乙酯,试计算该反应的产品产率为 ×100%)。
×100%)。
您最近一年使用:0次
名校
解题方法
7 . HNO3是重要的化工原料,浓HNO3与Cu反应的装置如图1所示:
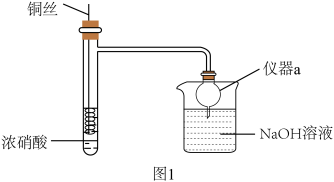
回答下列问题:
(1)仪器a的名称是_______ ,在该实验中的作用为_______ 。
(2)关于该实验下列说法错误的是_______。
(3)某小组同学发现Cu与浓HNO3反应所得混合溶液为绿色,Cu与稀HNO3反应所得混合溶液为蓝色,针对绿色产生的原因展开探究。
【提出猜想】
猜想a:Cu(NO3)2浓度大
猜想b:NO2溶解在Cu(NO3)2溶液中
【实验验证】
实验i:配制饱和Cu(NO3)2溶液,溶液呈_______ 色,证明猜想a不成立。
实验ii:取适量Cu与浓HNO3反应后的溶液,置于图2所示装置中,鼓入空气后,溶液上方可观察到_______ ,5min后,溶液完全变为蓝色,证明猜想b成立。
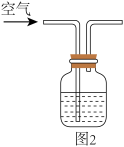
(4)另一组同学查阅资料发现:NO2能与水反应生成HNO2,进而发生下述反应:
①由此该组同学认为通过实验说明猜想b成立不严谨,理由是_______ 。
②写出NO2与水反应生成HNO2的化学方程式_______ 。
③该组同学改进后设计了新的实验:
实验iii:取适量Cu与浓HNO3反应后的溶液,置于图2所示装置中,鼓入氮气后,溶液上方现象与实验ii相同,但5min后,溶液仍为绿色。对比实验ii与实验iii,可推测Cu(NO3)2溶液为绿色的原因主要是_______ 。

回答下列问题:
(1)仪器a的名称是
(2)关于该实验下列说法错误的是_______。
| A.该反应需要加热才能进行 | B.可通过抽动铜丝控制反应开始和停止 |
| C.反应后迅速生成大量红棕色气体 | D.烧杯中仅发生中和反应 |
【提出猜想】
猜想a:Cu(NO3)2浓度大
猜想b:NO2溶解在Cu(NO3)2溶液中
【实验验证】
实验i:配制饱和Cu(NO3)2溶液,溶液呈
实验ii:取适量Cu与浓HNO3反应后的溶液,置于图2所示装置中,鼓入空气后,溶液上方可观察到

(4)另一组同学查阅资料发现:NO2能与水反应生成HNO2,进而发生下述反应:

①由此该组同学认为通过实验说明猜想b成立不严谨,理由是
②写出NO2与水反应生成HNO2的化学方程式
③该组同学改进后设计了新的实验:
实验iii:取适量Cu与浓HNO3反应后的溶液,置于图2所示装置中,鼓入氮气后,溶液上方现象与实验ii相同,但5min后,溶液仍为绿色。对比实验ii与实验iii,可推测Cu(NO3)2溶液为绿色的原因主要是
您最近一年使用:0次
2023-02-09更新
|
1338次组卷
|
3卷引用:广东省佛山市2023届普通高中教学质量检测(一)化学试题
名校
8 . 有关下列实验的说法正确的是
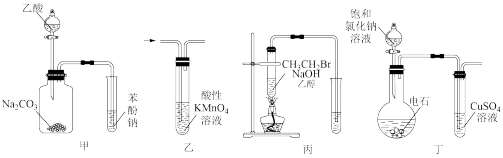
| A.甲装置可用于比较乙酸、碳酸与苯酚的酸性 |
B.乙装置可用于提纯混有少量 的 的 |
C.丙装置中,若右侧试管内的酸性 溶液褪色,证明溴乙烷发生了消去反应 溶液褪色,证明溴乙烷发生了消去反应 |
D.丁是实验室制乙炔的发生和净化装置, 溶液用于除去反应产生的 溶液用于除去反应产生的 杂质 杂质 |
您最近一年使用:0次
2023-01-14更新
|
274次组卷
|
4卷引用:广东省佛山市南海区桂城中学2022-2023学年高二下学期第三次段考(6月)化学试题
(已下线)广东省佛山市南海区桂城中学2022-2023学年高二下学期第三次段考(6月)化学试题浙江省衢州五校联盟2022-2023学年高二上学期创新班期末联考化学试卷(已下线)选择题11-15湖南省长沙市南雅中学2023-2024学年高二下学期5月第三次月考化学试题
名校
解题方法
9 . 下面有关说法正确的是
| A.C3H7Cl表示的一定是纯净物 |
| B.乙醇和丙三醇都有羟基,互为同系物 |
| C.可用酸性高锰酸钾溶液除去乙烷中混有的乙烯 |
| D.甲烷的二氯代物只有一种证明甲烷为正四面体结构 |
您最近一年使用:0次
名校
解题方法
10 . 北京市施行的《北京市小规模食品生产经营管理规定》中明确规定:小规模食品生产经营者不得购进、存放、使用亚硝酸盐等易滥用的食品添加剂。
(1)根据物质组成上分类,亚硝酸钠(NaNO2)属于___________ (填序号)
A.钠盐 B.硝酸盐 C.氧化物
写出其电离方程式为___________ 。
(2)实验室中,亚硝酸钠可用来处理过量的叠氮化钠,有关反应的化学方程式如下:
a.NaNO2+H2SO4=HNO2+NaHSO4
b.2NaN3+2HNO2=3N2↑+2NO↑+2NaOH
①上述两个反应中,属于氧化还原反应的是___________ (填“a”或“b”)。
②其中的氧化还原反应的氧化剂是___________ (填化学式),用双线桥法表示该氧化还原反应中电子转移情况:___________ 。
(3)亚硝酸钠外观与食盐相似,且均有咸味。
①若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是___________ 。
A.亚硝酸钠是还原剂 B.维生素C是氧化剂
C.维生素C能把铁离子还原成为亚铁离子 D.亚硝酸钠被还原
②鉴别方法如下:将样品盐放入稀硫酸与另外一种溶液(溶质为X)的混合液中,振荡,再滴加淀粉溶液如果溶液显蓝色,则可以证明该样品盐是亚硝酸钠;如果溶液无变化,则可以证明该样品盐为氯化钠。X与亚硝酸钠发生的反应可表示为2NaNO2+2X+2H2SO4=2NO↑+I2+K2SO4+Na2SO4+2H2O(已配平),其中X是___________ (填化学式),该反应的离子方程式为___________ 。
③含NaNO2的废水必须经处理后才能排放,可用铵盐来处理亚硝酸钠生成一种无毒气体,写出该反应的离子方程式___________ 。
(1)根据物质组成上分类,亚硝酸钠(NaNO2)属于
A.钠盐 B.硝酸盐 C.氧化物
写出其电离方程式为
(2)实验室中,亚硝酸钠可用来处理过量的叠氮化钠,有关反应的化学方程式如下:
a.NaNO2+H2SO4=HNO2+NaHSO4
b.2NaN3+2HNO2=3N2↑+2NO↑+2NaOH
①上述两个反应中,属于氧化还原反应的是
②其中的氧化还原反应的氧化剂是
(3)亚硝酸钠外观与食盐相似,且均有咸味。
①若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是
A.亚硝酸钠是还原剂 B.维生素C是氧化剂
C.维生素C能把铁离子还原成为亚铁离子 D.亚硝酸钠被还原
②鉴别方法如下:将样品盐放入稀硫酸与另外一种溶液(溶质为X)的混合液中,振荡,再滴加淀粉溶液如果溶液显蓝色,则可以证明该样品盐是亚硝酸钠;如果溶液无变化,则可以证明该样品盐为氯化钠。X与亚硝酸钠发生的反应可表示为2NaNO2+2X+2H2SO4=2NO↑+I2+K2SO4+Na2SO4+2H2O(已配平),其中X是
③含NaNO2的废水必须经处理后才能排放,可用铵盐来处理亚硝酸钠生成一种无毒气体,写出该反应的离子方程式
您最近一年使用:0次



