1 . 某研究性学习小组学生根据氧化还原反应规律,探究 、
、 与
与 反应的情况,提出假设并进行相关实验。
反应的情况,提出假设并进行相关实验。
Ⅰ.从理论上分析 和
和 都既有氧化性又有还原性,于是提出如下假设:
都既有氧化性又有还原性,于是提出如下假设:
假设1: 氧化
氧化 ;
;
假设2: 氧化
氧化 。
。
(1)甲同学设计如图装置进行实验:___________ 。
②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B,向其中加入适量 粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是___________ 。乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星的木条未复燃,得出结论:假设Ⅰ正确。则 和
和 反应的化学方程式是
反应的化学方程式是___________ 。
Ⅱ.该研究性学习小组同学还认为易与 发生反应,应该更易被氧化。查阅资料:
发生反应,应该更易被氧化。查阅资料: ;
;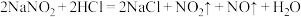 ;酸性条件下,能与
;酸性条件下,能与 反应生成
反应生成 和
和 。
。
(3)丙同学用下图所示装置(部分夹持装置略)探究 与
与 的反应。
的反应。 ,目的是
,目的是___________ 。
②B中观察到的主要现象的是___________ (填字母编号)。
a.铜片逐渐溶解,溶液变为蓝色
b.有红棕色气泡产生
c.有无色气泡产生
③C、E中所盛装的试剂不能是___________ (填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④充分反应后,检验D装置中产物的方法是:取D装置中产物少许,___________ ,则产物是 。
。
 、
、 与
与 反应的情况,提出假设并进行相关实验。
反应的情况,提出假设并进行相关实验。Ⅰ.从理论上分析
 和
和 都既有氧化性又有还原性,于是提出如下假设:
都既有氧化性又有还原性,于是提出如下假设:假设1:
 氧化
氧化 ;
;假设2:
 氧化
氧化 。
。(1)甲同学设计如图装置进行实验:

②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B,向其中加入适量
 粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是
 和
和 反应的化学方程式是
反应的化学方程式是Ⅱ.该研究性学习小组同学还认为易与
 发生反应,应该更易被氧化。查阅资料:
发生反应,应该更易被氧化。查阅资料: ;
;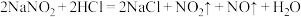 ;酸性条件下,能与
;酸性条件下,能与 反应生成
反应生成 和
和 。
。(3)丙同学用下图所示装置(部分夹持装置略)探究
 与
与 的反应。
的反应。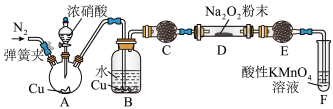
 ,目的是
,目的是②B中观察到的主要现象的是
a.铜片逐渐溶解,溶液变为蓝色
b.有红棕色气泡产生
c.有无色气泡产生
③C、E中所盛装的试剂不能是
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④充分反应后,检验D装置中产物的方法是:取D装置中产物少许,
 。
。
您最近一年使用:0次
2024-04-08更新
|
628次组卷
|
5卷引用:四川省自贡市蜀光中学2023-2024学年高一下学期4月月考化学试题
解题方法
2 . 84消毒液是一种常见的含氯消海剂。如图为某品牌84消毒液的说明书中的部分内容。
(1)常温将氯气通入氢氧化钠溶液可制得84消毒液的主要成分,写出相应离子方程式______________ 。
(2)某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映水溶液中所有物质表现出来的氧化-还原性,ORP值越大,氧化性越强。
Ⅰ.向2 mL 84消毒液中加入2 mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.向2 mL 84消毒液中加入2 mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.测得84消毒液在不同温度时ORP随时间的变化曲线如下。
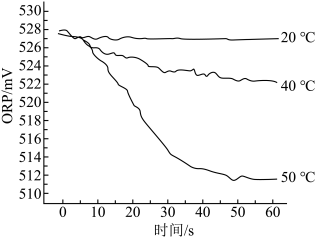
①已知白醋显酸性,不具有漂白性。实验Ⅰ、Ⅱ现象不同的原因是_______________________ 。
②实验Ⅲ不同温度时ORP值不同的原因可能是____________________ 。
(3)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO将H2O2氧化产生O2的促进藻类快速生长。写出该反应的化学方程式_________________ 。
(4)某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液(已知氯气和NaOH在一定温度下能发生如下反应: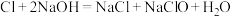 ;
; 。经测定ClO-与
。经测定ClO-与 的数目之比为1∶3,则氯气与氢氧化钠溶液反应时,被还原的氯元素和被氧化的氯元素的质量之比为
的数目之比为1∶3,则氯气与氢氧化钠溶液反应时,被还原的氯元素和被氧化的氯元素的质量之比为___________ 。
| 产品特点: 本品是以次氯钠为主要成分的液体消毒剂。可杀灭肠道致病菌、化脓性球菌、致病性酵母菌,并能灭活病毒。 注意事项: 1.本品易使有色衣脱色,禁止用于丝、毛、麻织物的消毒。 2.不得将本品与酸性产品(如洁厕类清洁产品)同时使用。 3.置于避光、阴凉处保存。 |
(1)常温将氯气通入氢氧化钠溶液可制得84消毒液的主要成分,写出相应离子方程式
(2)某同学研究84消毒液的漂白性,实验如下。
资料:84消毒液中含氯微粒主要有ClO-、Cl-、HClO;相同浓度时,HClO的氧化性强于ClO-;ORP是反映水溶液中所有物质表现出来的氧化-还原性,ORP值越大,氧化性越强。
Ⅰ.向2 mL 84消毒液中加入2 mL水后,放入红色纸片,观察到纸片慢慢褪色。
Ⅱ.向2 mL 84消毒液中加入2 mL白醋后,放入红色纸片,观察到纸片迅速褪色。
Ⅲ.测得84消毒液在不同温度时ORP随时间的变化曲线如下。

①已知白醋显酸性,不具有漂白性。实验Ⅰ、Ⅱ现象不同的原因是
②实验Ⅲ不同温度时ORP值不同的原因可能是
(3)2016年巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO将H2O2氧化产生O2的促进藻类快速生长。写出该反应的化学方程式
(4)某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液(已知氯气和NaOH在一定温度下能发生如下反应:
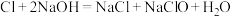 ;
; 。经测定ClO-与
。经测定ClO-与 的数目之比为1∶3,则氯气与氢氧化钠溶液反应时,被还原的氯元素和被氧化的氯元素的质量之比为
的数目之比为1∶3,则氯气与氢氧化钠溶液反应时,被还原的氯元素和被氧化的氯元素的质量之比为
您最近一年使用:0次
3 . 某实验小组用下列装置制备高铁酸钾( K2FeO4 )并探究其性质,制备原理为:3Cl2+2Fe(OH)3+ 10KOH=2K2FeO4+6KCl+8H2O。(夹持装置略)
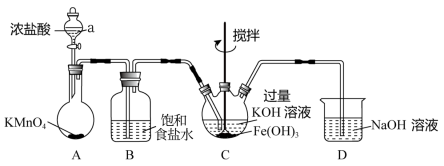
查阅资料:①K2FeO4 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2。②ClO-能将盐酸氧化成氯气。
I. K2FeO4的制备
(1)仪器a的名称为___________ ,D中的NaOH溶液可以用___________ 代替(填入对应字母)。
A.蒸馏水 B.澄清石灰水 C.石灰乳 D.饱和食盐水
(2)检验气体发生装置A气密性的方法是___________ ; 该装置中生成黄绿色气体的化学反应方程式为___________ 。
(3)制备K2FeO4需要在___________ (填“酸性”“碱性”或“中性”)环境中进行,根据上述K2FeO4的制备实验得出:氧化性Cl2___________ FeO (填“>”或“<”)。装置C中Cl2还会与过量的KOH发生反应,请写出其离子反应方程式
(填“>”或“<”)。装置C中Cl2还会与过量的KOH发生反应,请写出其离子反应方程式___________ 。
II.探究K2FeO4的性质
(4)实验方案:用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液。取少量该溶液于试管中,滴加过量盐酸后发现有Cl2产生。
①为确保氧化Cl-的物质只能是FeO ,则用KOH溶液洗涤的目的是
,则用KOH溶液洗涤的目的是___________ 。
②由(4)的实验得出Cl2和FeO 的氧化性强弱关系与I中制备K2FeO4实验时得出的结论相反,其可能的原因是
的氧化性强弱关系与I中制备K2FeO4实验时得出的结论相反,其可能的原因是___________ 。

查阅资料:①K2FeO4 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2。②ClO-能将盐酸氧化成氯气。
I. K2FeO4的制备
(1)仪器a的名称为
A.蒸馏水 B.澄清石灰水 C.石灰乳 D.饱和食盐水
(2)检验气体发生装置A气密性的方法是
(3)制备K2FeO4需要在
 (填“>”或“<”)。装置C中Cl2还会与过量的KOH发生反应,请写出其离子反应方程式
(填“>”或“<”)。装置C中Cl2还会与过量的KOH发生反应,请写出其离子反应方程式II.探究K2FeO4的性质
(4)实验方案:用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液。取少量该溶液于试管中,滴加过量盐酸后发现有Cl2产生。
①为确保氧化Cl-的物质只能是FeO
 ,则用KOH溶液洗涤的目的是
,则用KOH溶液洗涤的目的是②由(4)的实验得出Cl2和FeO
 的氧化性强弱关系与I中制备K2FeO4实验时得出的结论相反,其可能的原因是
的氧化性强弱关系与I中制备K2FeO4实验时得出的结论相反,其可能的原因是
您最近一年使用:0次
2022-01-15更新
|
332次组卷
|
2卷引用:四川省资阳市2021-2022学年高一上学期期末考试化学试题
4 . I.完成下列氧化还原反应相关问题。
(1)误食NaNO2会使人体血红蛋白中的Fe2+转化为Fe3+而导致中毒,该过程中NaNO2表现出___________ (填“氧化性”或“还原性”)。
(2)已知NaNO2可以与NH4Cl反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:___________ 。
Ⅱ.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物ClO2。其反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(3)该反应中的氧化产物为___________ (填化学式)。
(4)浓盐酸在该反应中显示出来的性质是___________ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(5)在碱性条件下加入NaClO3,可将NaCrO2转化为Na2CrO4,ClO 被还原为Cl−,其离子方程式为
被还原为Cl−,其离子方程式为___________ 。还原性:
___________ Cl−(填“>”“<”或“=”)。
(1)误食NaNO2会使人体血红蛋白中的Fe2+转化为Fe3+而导致中毒,该过程中NaNO2表现出
(2)已知NaNO2可以与NH4Cl反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:
Ⅱ.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物ClO2。其反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(3)该反应中的氧化产物为
(4)浓盐酸在该反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(5)在碱性条件下加入NaClO3,可将NaCrO2转化为Na2CrO4,ClO
 被还原为Cl−,其离子方程式为
被还原为Cl−,其离子方程式为
您最近一年使用:0次
9-10高一下·云南曲靖·期末
名校
解题方法
5 . 苹果汁是人们喜爱的饮料,由于此饮料中含有Fe2+,在空气中易转变为Fe3+。若榨汁时加入维生素C,可有效防止这种现象的发生。这说明维生素C具有
| A.还原性 | B.氧化性 | C.碱性 | D.酸性 |
您最近一年使用:0次
2024-03-06更新
|
212次组卷
|
238卷引用:2012-2013学年四川成都二十中高一上学期期中考试理科化学试卷
(已下线)2012-2013学年四川成都二十中高一上学期期中考试理科化学试卷四川省攀枝花市2017-2018学年高一上学期调研检测化学试题四川省成都市成都外国语学校2019-2020学年高一上学期期中考试化学试题四川省成都三中2019-2020学年高一11月月考化学试题四川省成都市蒲江县蒲江中学2019-2020学年高一上学期12月月考化学试题四川省成都市第二十中学2021-2022学年高一上学期期中考试化学试题四川省眉山市仁寿第一中学北校区2021-2022学年高一上学期半期化学试题(已下线)09-10学年云南会泽一中高一下期末考试化学卷(已下线)2010年浙江省杭州市七校高一上学期期中考试化学卷(已下线)2011-2012年河北省大名县第三中学高一上学期期中检测化学试卷(已下线)2011-2012学年江苏省常熟中学高一上学期期中考试化学试卷(已下线)2011-2012学年贵州省湄潭中学高一上学期期末考试化学试卷(已下线)2011-2012学年广东汕头市达濠中学高一第一学期期中考试化学试卷(已下线)2011-2012学年安徽省亳州二中高一第一学期期末考试化学试卷(已下线)2012-2013学年山东省日照市某高中高一上学期期中考试化学试卷(已下线)2012年鲁科版高中化学必修1 2.3氧化剂和还原剂练习卷(已下线)2012-2013学年陕西省三原县北城中学高一上学期期中考试化学试卷(已下线)2012-2013学年天津市天津一中高一上学期期末考试化学试卷(已下线)2012-2013学年广东省深圳科学高中高一第一学期期末考试化学试卷B(已下线)2014届河南省平顶山市部分高中高一上学期期中联考化学试卷(已下线)2014-2015学年江苏江阴高一上暑期学习反馈(开学检测)化学试卷(已下线)2014-2015学年河南省实验中学高一上学期期中考试化学试卷(已下线)2014秋浙江省杭州地区六校高一上学期期中考试化学试卷2014-2015学年江苏省大丰市南阳中学高一下学期期中考试化学试卷2015-2016学年浙江省温州市龙湾中学高一上学期期中测试化学试卷2015-2016学年河北省唐山市迁安二中高一上学期期末化学试卷2015-2016学年湖南省衡阳县高一上学期期末质检化学试卷2015-2016学年山西省临汾二中高一上学期期末化学试卷2016-2017学年云南省昆明三中高一上期中化学试卷2016-2017学年福建省四地六校高一上学期12月月考化学试卷2016-2017学年广东省惠州市高一上学期期末化学试卷2016-2017学年北京市怀柔区高一上学期期末考试化学试卷2016-2017学年黑龙江省鸡西市第十九中学高一上学期期末考试化学试卷2016-2017学年河南省商丘市第一高级中学高一上学期期末考试化学试卷云南省大理市下关一中2017-2018学年高一上学期期中考试化学试题甘肃省兰州市第一中学2017-2018学年高一上学期期中考试化学试题甘肃省兰州新舟中学2017-2018学年高一上学期第二次月考化学试题河北省辛集中学2017-2018学年高一上学期12月月考化学试题江苏省东台市创新学校2017-2018学年高一11月月考化学试题辽宁省抚顺市第十九中学2016-2017学年高一上学期期中考试化学试题内蒙古商都县高级中学2017-2018学年高一上学期期中考试化学试题青海省西宁二十一中2017-2018学年高一上学期12月月考化学试题安徽省六安市第一中学2017-2018学年高一下学期开学考试化学试题【全国百强校】江苏省南菁高级中学2017-2018学年高一(1、2班)上学期期中考试化学试题云南省楚雄州南华县第一中学2018-2019学年高一上学期期中考试化学试题【全国百强校】福建省师范大学附属中学2018-2019学年高一上学期期中考试化学试题辽宁省辽河油田第二高级中学2018-2019学年高一上学期期中考试化学试题【全国百强校】河北省石家庄市辛集中学2018-2019学年高一上学期第二次月考化学试题【市级联考】云南省大理市2017-2018学年高一上学期期中考试化学试题甘肃省岷县二中2018-2019学年高一上学期第三次月考化学试题甘肃省武威第十八中学2018-2019学年高一上学期期末考试化学试题新疆石河子市兵团八师一四三团第一中学2018-2019学年高一上学期期末考试化学试题【市级联考】浙江省台州市2018-2019学年高一下学期期中考试化学试题【市级联考】贵州省遵义市2018-2019学年高一下学期期中考试化学试题山东省聊城第二中学2019-2020学年高一上学期第二次考试(9月)化学试题天津市六校(静海一中,杨村中学,宝坻一中,大港一中等)2019-2020学年高一上学期期中联考化学试题陕西省吴起高级中学2019-2020学年高一上学期期末考试化学试题(已下线)【新东方】2019新中心五地087高中化学云南省陇川县民族中学2019-2020学年高一上学期期末考试化学试题山东省济南市历城第二中学2019-2020学年高一上学期期末考试化学试题云南省昭通市彝良县一中2019—2020学年高一上学期期末考试化学试题2019-2020学年高一上学期期末复习《新题速递·化学》12月(考点12-15)甘肃省永昌四中2019-2020学年高一上学期期末考试化学试题云南省大理市下关第一中学2019-2020学年高一上学期期中考试化学试题山西省河津市第二中学2019-2020学年高一上学期11月月考化学试题(已下线)【新东方】高中化学X004山西省运城市2019-2020学年高一上学期期末调研测试化学试题(已下线)【南昌新东方】莲塘一中化学高一10月份(已下线)衔接点07 氧化剂和还原剂-2020年【衔接教材·暑假作业】初高中衔接化学(已下线)第01章 物质及其变化(A卷基础强化篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)吉林省长春市榆树市实验高级中学2020-2021学年高一上学期第一次月考化学试题吉林省长春市养正高级中学2020-2021学年高一第一次月考化学试题吉林省吉林市第五十五中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】32(已下线)3.1.2 铁的氢氧化物 铁盐和亚铁盐(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)广东省东莞市东莞中学2020-2021学年高一上学期第一次月考化学试题江苏省南京师范大学附属中学2020-2021学年高一上学期期中考试化学试题北京市第三十五中学2020-2021学年高一上学期期中考试化学试题安徽省安庆市2020-2021学年高一上学期期中考试化学试题辽宁省开原市第二高级中学2020-2021学年高一上学期期中考试化学试题河北省张家口市涿鹿中学2020-2021学年高一10月调研考试化学试题(已下线)【浙江新东方】双师 (59).吉林省油田高级中学2019-2020学年高一上学期期中考试化学试题山西省阳泉市盂县第三中学校2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】76.(已下线)【浙江新东方】71.西藏自治区林芝市第二高级中学2020-2021学年高一上学期第二学段(期末)考试化学试题吉林省吉化第一高级中学校2020-2021学年高一上学期第一次月考化学试题(已下线)练习7 氧化还原反应-2020-2021学年【补习教材·寒假作业】高一化学(鲁科版2019)海南省东方市八所中学2020-2021学年高一上学期第三次月考化学试题福建省莆田第十五中学2019-2020学年高一12月月考化学试题上海市黄浦区向明中学2020-2021学年高一上学期期末化学试题广东省台山市华侨中学2020-2021学年高一上学期期中考试化学试题海南省万宁市北京师范大学万宁附属中学2020-2021学年高一下学期开学考试化学试题浙江省之江教育评价2020-2021学年高一下学期返校联考化学试题(已下线)【浙江新东方】在线化学61高一下福建省莆田第七中学2020-2021学年高一下学期第一次月考化学试题浙江省金华市云富高级中学2020-2021学年高一10月月考化学试题云南省峨山彝族自治县第一中学2020-2021学年高一下学期3月月考化学试题云南省普洱市第一中学天有实验学校2020—2021学年高一下学期 (文科)月考化学试题(已下线)衔接点07 氧化剂和还原剂-2021年初升高化学无忧衔接(已下线)专题1.3.3 氧化剂、还原剂(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)江苏省南京市金陵中学河西分校2020-2021学年高一上学期10月月考化学试题(已下线)专题六 铁及其化合物(A卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)(已下线)【苏州新东方】04 十中江西省南昌市进贤县第二中学2021-2022高一上学期第一次月考化学广东省广州市祈福教育管理有限公司2021-2022学年高一上学期10月月考化学试题云南省玉溪市江川区第二中学2020-2021学年高一下学期期末考试化学试卷甘肃省天水市田家炳中学2021-2022学年高一上学期第一阶段考试化学试卷云南省玉溪市江川区第二中学2021-2022学年高一上学期第一次月考化学试题广东省茂名市电白区水东中学2021-2022学年高一10月测试化学试题浙江省杭州市富阳区实验中学2021-2022学年高一上学期10月月考化学试题广东省深圳市红岭中学 2021-2022学年高一上学期期中考试化学试题辽宁省阜新市第二高级中学2021-2022学年高一化学上学期第一次月考试题新疆吐鲁番市高昌区第二中学2021-2022学年高一上学期期中考试化学试题湖南省宁乡市第七高级中学2021-2022学年高一10月月考化学试题广东省梅州市大埔县虎山中学2021-2022学年高一上学期第一次段考(11月)化学试题广东省湛江市第二十一中学2021-2022学年高一上学期期中考试化学试题湖南省衡阳市田家炳实验中学2021-2022学年高一上学期期中考试化学试题北京市顺义区第一中学2021-2022学年高一上学期中阶段质量检测化学试题江苏省徐州市2021-2022学年高一上学期12月月考化学试题甘肃省秦安县第一中学2021-2022学年高一上学期期中考试化学试题吉林省长春市第二十九中学2021-2022学年高一上学期第二学程考试化学(文)试题河南省郑州市第四十七高级中学2021-2022学年高一上学期第二次月考化学试题广东省普宁市华侨中学2021—2022学年高一上学期第三次月考化学试题黑龙江省哈尔滨市阿城区第一中学校2021-2022学年高一上学期10月月考化学试题新疆喀什地区疏附县2021-2022学年高一上学期1月测试化学试题湖南省长沙市湖南师范大学附属中学2021-2022学年高一上学期期末考试化学试题吉林省长春外国语学校2021-2022学年高一上学期期末考试化学试题(学考)新疆生产建设兵团第二师八一中学2021-2022学年高一上学期期中考试化学试题(已下线)衔接点12 氧化剂和还原剂-2022年初升高化学无忧衔接?(已下线)1.3 氧化还原反应-同步学习必备知识天津市红桥区2019-2020学年高一上学期期末考试化学试题甘肃省兰州市西固区三校2021-2022学年高一上学期期中联考化学试题江苏省金湖中学、涟水中学等七校2021-2022学年高一上学期期中大联考化学试题山西省灵丘县第四中学校2021-2022学年高一上学期期中考试化学试题湖北省宜城市第三中学2021-2022学年高一上学期期中化学试题安徽省怀宁县第二中学2021-2022学年高一上学期期中考试化学试题福建省仙游县枫亭中学2021-2022学年高一上学期期末考试化学试题安徽省青阳县第一中学2021-2022学年高一下学期3月月考化学试题西藏林芝市第二高级中学2021-2022学年高一上学期期末考试化学试题上海市格致中学2022-2023学年高一上学期第一次月考化学试题黑龙江省牡丹江市第三高级中学2022-2023学年高一上学期第一次月考化学试题河北省唐山市十县一中联盟2022-2023学年高一上学期期中考试化学试题河北省唐山市2022—2023学年高一上学期期中考试化学试题江苏省海门中学2021--2022学年高一上学期期中考试化学试题天津市武清区2022-2023学年高一上学期期中考试化学试题天津市第三中学2022-2023学年高一上学期期中考试化学试题北京市北京一零一中学2022-2023学年高一上学期期中考试化学试题重庆市礼嘉中学校2022-2023学年高一上学期第一次月考化学试题浙江省杭州市S9联盟2022-2023学年高一上学期期中联考化学试题新疆巴楚县第一中学2021-2022学年高一上学期期中考试化学试题湖北省襄阳四中2021-2022学年高一上学期10月考试化学试题北京市月坛中学2022-2023学年高一上学期期中考试化学试题安徽省合肥市庐巢八校联考2022-2023学年高一上学期12月集中练习2化学试题浙江省宁波市奉化二中2021-2022学年高一上学期期中考试化学试题河北省保定市蠡县第二中学2022-2023学年高一上学期12月月考化学试题广东省东莞市翰林高级中学2022-2023学年高一上学期期中考试化学试题新疆阿瓦提县第四中学2022-2023学年高一上学期9月份测试化学B试题湖南省衡阳市第八中学2022-2023学年高一上学期期末考试化学试题上海市育才中学2022-2023学年高一上学期期末调研化学试题云南省玉溪第一中学2022-2023学年高一上学期第一月考化学试题 【精品卷】1.3.2 氧化剂和还原剂课堂例题-人教版2023-2024学年必修第一册江苏省无锡市市北高级中学2022-2023学年高一上学期期中检测化学试题辽宁省鞍山市普通高中2022-2023学年高一上学期期中测试化学(A卷)试题贵州省三新联盟校2023-2024学年高一上学期10月联考化学试题广西柳州高级中学2023-2024学年高一上学期10月月考化学试题甘肃省庆阳市华池县第一中学2022-2023学年高一上学期期中考试化学试题天津市部分区2023-2024学年高一上学期期中考试化学试题福建省厦门市海沧中学2022-2023学年高一上学期11月期中考试化学试题江苏省连云港高级中学2023-2024学年高一上学期11月期中考试化学试题江苏省苏州大学附属中学2023-2024学年高一上学期10月检测化学试题辽宁省朝阳市建平县实验中学2023-2024学年高一上学期10月月考化学试题福建省福清西山学校2023-2024学年高一上学期12月月考化学试题广西桂林市平乐县平乐中学2023-2024学年高一上学期10月月考化学试题湖南省长沙市雨花区2023-2024学年高一上学期期末质量监测化学试题甘肃省兰州市第五十五中学2023-2024学年高一下学期开学测试化学试卷陕西省延安市延川县中学2023-2024学年高一上学期第一次月考化学试题北京市月坛中学2023-2024学年高一上学期期中考试化学试题贵州省毕节市金沙县精诚中学2023-2024学年高一上学期期末考试化学试题内蒙古呼伦贝尔市满洲里远方中学2023-2024学年高一上学期期末考试化学试题(已下线)江苏省2011届高三化学一轮过关测试(8)(已下线)2010年湖南省浏阳一中高二上学期第三次阶段性测试化学卷(已下线)2011-2012学年湖南省衡阳八中高二上学期期中考试化学(文)试卷(已下线)2011-2012学年福建省南安一中高二上学期期中考试化学(文)试卷(已下线)2011-2012学年山东省日照一中高二上学期期中考试化学(文)试卷(已下线)2011-2012学年甘肃省白银市平川中恒学校高二上学期期末考试化学(文)试卷(已下线)2011-2012年浙江宁波万里国际中学高二上学期期中考试文科化学试卷(已下线)2011-2012学年黑龙江省庆安三中高二下学期期末考试化学试卷(已下线)2011-2012学年浙江省嘉兴八校高二上学期期中联考文科化学试卷(已下线)2012-2013学年江苏泰州二中高二上学期期中考试化学(必修)试卷(已下线)2012-2013学年浙江省桐乡一中高二上学期期中考试文科化学试卷(已下线)2012年苏教版高中化学选修1 2.2提供能量与营养的食物练习卷(已下线)2013-2014学年江西省景德镇市高二上学期期中质量检测文科化学试卷(已下线)2014秋贵州省遵义市第四中学高二上学期期中化学(文)试卷(已下线)2014-2015江西省景德镇市高二上学期期中化学(文)试卷2016届福建省四地六校高三上学期第一次联考化学试卷2015-2016学年湖南省株洲十八中高二上学期期中(文)化学试卷2015-2016学年广西武鸣高级中学高二上段考文化学试卷2015-2016学年上海市虹口区度高二上学期期终考试化学试卷2015-2016学年广东省惠州市高二上学期期末文化学试卷2016届广西普通高中高三上学期模拟考试化学试卷2015-2016学年广西桂林十八中高二下开学测化学试卷2016-2017学年广东省清远三中高二上第二次月考化学卷2016-2017学年海南省琼海嘉积中学高二上期中文化学卷2016-2017学年广西桂林十八中高二上期中文化学卷上海市金山中学2016-2017学年高二上学期期末合格考试化学试题陕西省岐山县2017-2018学年高二上学期期末质量检测(文科)化学试题天津市武清区城关中学2019届高三上学期月考(一)化学试题2018-2019学年鲁科版高二化学选修一:模块检测题江苏省东台市创新学校2018-2019学年高二上学期9月月考化学(必修)试题【全国百强校】陕西省西安市第一中学2019届高三上学期第一次月考化学试题安徽省巢湖市柘皋中学2018-2019学年高二(文)上学期期中考试化学试题【校级联考】广西壮族自治区南宁市马山县金伦中学“4+ N”高中联合体2018-2019学年高二上学期期中考试化学试题福建省晋江市季延中学2018-2019学年高二(文)上学期期中考试化学试题湖南省醴陵市第一中学2018-2019学年高二(文)上学期期末考试化学试题【全国百强校】上海市金山中学2017-2018学年高二上学期期末考试(合格考)化学试题云南省元江县一中2020届高三上学期开学考试化学试题上海第二工业大学附属龚路中学2018-2019学年高二上学期第一次阶段测试化学试题河南省郑州市106中学2019-2020学年高二9月月考化学(文)试题黑龙江省哈尔滨市第六中学2019-2020学年高二上学期期中考试化学(文)试题甘肃省庆阳市宁县第二中学2019-2020学年高二上学期期中考试化学(文)试题湖南省常德市2018-2019学年高二下学期期末考试化学试题(文科)山西省太原市第五十三中学2019-2020学年高二上学期12月月考化学(文)试题湖南省邵东县创新实验学校2019-2020学年高二上学期期末考试(学考)化学试题安徽省合肥市六校2019-2020学年高二上学期期末考试化学(文)试题湖南省常德市石门县第二中学2019-2020学年高二上学期第一次月考化学试题(学考)广西2015-2016学年上学期普通高中学业水平考试仿真模拟化学试题云南省2019年7月普通高中学业水平考试化学试题陕西省宝鸡市金台区2019-2020学年高二上学期期中检测化学试题(文)甘肃省会宁县第一中学2020-2021学年高二上学期期中考试化学(文)试题上海市吴淞中学2021-2022学年高二上学期第一次月考化学试题甘肃省永昌县第一高级中学2021-2022学年高三上学期期中考试化学试题新疆和田地区皮山县高级中学2021-2022学年高二下学期期末考试化学试题重庆市永川北山中学校2022-2023学年高三上学期期中质量监测化学试题(已下线)考点巩固卷02 化学物质及其变化(3大考点44题)?-2024年高考化学一轮复习考点通关卷(新高考通用)天津市南开中学2023-2024学年高三上学期第二次考试化学试题上海市第三女子中学2023-2024学年高二上学期期末化学合格考试题
6 . 人体必需的一些元素在周期表中的分布情况如下:

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是___________ 。H2O2是一种绿色氧化剂,电子式为___________ 。
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为___________ 。
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是___________ ,原子序数为___________ 。
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为___________ 。
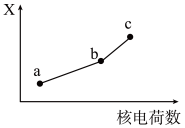
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

(1)碳、氢、氧、氮是人体内的主要元素。碳有多种同位素,其中考古时用于测定文物年代的是
(2)钠离子和氯离子可以帮助我们维持机体的电解质平衡。常温下,将Cl2通入NaOH溶液中,可以得到一种漂白液,上述反应的化学方程式为
(3)硒(Se)具有抗氧化、增强人体抵抗力的功效。Se在元素周期表中的位置是
(4)铁、铬、锰在人体内含量微乎其微,但对维持内分泌平衡和身体基础代谢有重要作用。向少量酸性H2O2溶液中加入FeSO4溶液,发生反应的离子方程式为
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________(填字母)。

| A.若a、b、c表示氧族元素,则X表示对应氢化物的稳定性 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示第IA族元素,则X表示对应离子的氧化性 |
| D.若a、b、c表示第IIA族元素,则X表示最高价氧化物对应水化物的碱性 |
您最近一年使用:0次
2023-12-05更新
|
264次组卷
|
3卷引用:四川省眉山北外附属东坡外国语学校2023-2024学年高一下学期开学化学试题
名校
7 . 回答下列问题:
(一).KClO3和浓盐酸在一定温度下反应会生成黄绿色的有毒气体氯气。其变化可表示为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
(1)请用“双线桥”表示上述反应电子转移的方向和数目_______ 。
(2)请将上述反应改写成离子方程式_______ 。
(3)浓盐酸在反应中体现出来的性质有_______ (填序号)。
①还原性 ②酸性 ③氧化性 ④碱性
(4)若反应生成21.3g氯气,则消耗还原剂的质量为_______ g。
(二).高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是_______ 。(填化学式)
(6)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:_______ 。
②每生成1mol FeO 转移
转移_______ 个电子。
(一).KClO3和浓盐酸在一定温度下反应会生成黄绿色的有毒气体氯气。其变化可表示为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
(1)请用“双线桥”表示上述反应电子转移的方向和数目
(2)请将上述反应改写成离子方程式
(3)浓盐酸在反应中体现出来的性质有
①还原性 ②酸性 ③氧化性 ④碱性
(4)若反应生成21.3g氯气,则消耗还原剂的质量为
(二).高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是
(6)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。
、Cl-、H2O。①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成1mol FeO
 转移
转移
您最近一年使用:0次
名校
8 . 木炭与浓硫酸在加热条件下可发生化学反应,为检验反应的产物,某学生设计了如下图所示的实验,请回答下列问题:___________________ (填装置序号甲、乙等,每个装置仅限使用一次);
(2)甲装置中发生反应的化学方程式为_______________________ ,其中木炭被_________ (填“氧化”或“还原”),浓硫酸体现____________ (填“氧化性”或“还原性”或“酸性”);
(3)两次使用品红溶液的作用分别是________________ ,___________ (按连接先后顺序作答);
(4)丁装置中应该盛装的试剂是酸性_____________ ,写出该反应的离子方程式_______________ ;
(5)丙装置中出现的现象是________________ ,该装置的作用是______________ ;
(6)己装置中的现象是___________ ,能否将己的位置调换到丙的后面?______________ ,原因是_______________________ ;

(2)甲装置中发生反应的化学方程式为
(3)两次使用品红溶液的作用分别是
(4)丁装置中应该盛装的试剂是酸性
(5)丙装置中出现的现象是
(6)己装置中的现象是
您最近一年使用:0次
2024-04-30更新
|
120次组卷
|
2卷引用:四川省成都市安宁河联盟2023-2024学年高一下学期期中联考化学试题
名校
解题方法
9 . 为研究含硫化合物的性质,某兴趣小组在老师的指导下设计了如下实验。
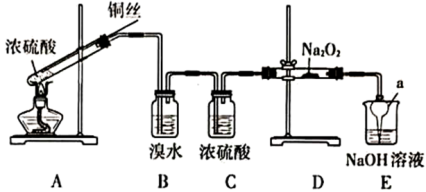
回答以下问题:
(1)A装置试管中主要反应的化学方程式是___________ 。反应中,浓硫酸表现出的性质是___________ (填正确选项的字母)。
A.酸性 B.氧化性 C.脱水性 D.吸水性
(2)仪器a的名称是___________ ,在本实验中的作用是___________ 。
(3)B中溴水出现的现象是___________ ,说明 具有的性质是
具有的性质是___________ 。
(4)D中 与
与 反应生成
反应生成 ,反应的化学方程式是
,反应的化学方程式是___________ 。
(5)同学们发现,A装置试管中铜和硫酸均有剩余时反应却自动停止了,由此推测反应与硫酸的浓度有关。同学们通过查阅资料知, 和浓硫酸反应会同时生成多种含硫化合物。在老师的指导下,同学们按如下步骤测定硫酸能与铜反应的最低浓度。
和浓硫酸反应会同时生成多种含硫化合物。在老师的指导下,同学们按如下步骤测定硫酸能与铜反应的最低浓度。
①在盛有过量铜粉的试管中加入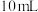 ,
, 浓硫酸进行反应。
浓硫酸进行反应。
②反应自动停止时,收集到 ,测得其他生成物中硫元素的质量共
,测得其他生成物中硫元素的质量共 ,由此可计算出硫酸能与铜反应的最低浓度是
,由此可计算出硫酸能与铜反应的最低浓度是___________  (忽略反应前后溶液体积的变化,计算结果保留一位小数)。
(忽略反应前后溶液体积的变化,计算结果保留一位小数)。

回答以下问题:
(1)A装置试管中主要反应的化学方程式是
A.酸性 B.氧化性 C.脱水性 D.吸水性
(2)仪器a的名称是
(3)B中溴水出现的现象是
 具有的性质是
具有的性质是(4)D中
 与
与 反应生成
反应生成 ,反应的化学方程式是
,反应的化学方程式是(5)同学们发现,A装置试管中铜和硫酸均有剩余时反应却自动停止了,由此推测反应与硫酸的浓度有关。同学们通过查阅资料知,
 和浓硫酸反应会同时生成多种含硫化合物。在老师的指导下,同学们按如下步骤测定硫酸能与铜反应的最低浓度。
和浓硫酸反应会同时生成多种含硫化合物。在老师的指导下,同学们按如下步骤测定硫酸能与铜反应的最低浓度。①在盛有过量铜粉的试管中加入
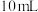 ,
, 浓硫酸进行反应。
浓硫酸进行反应。②反应自动停止时,收集到
 ,测得其他生成物中硫元素的质量共
,测得其他生成物中硫元素的质量共 ,由此可计算出硫酸能与铜反应的最低浓度是
,由此可计算出硫酸能与铜反应的最低浓度是 (忽略反应前后溶液体积的变化,计算结果保留一位小数)。
(忽略反应前后溶液体积的变化,计算结果保留一位小数)。
您最近一年使用:0次
2021-01-07更新
|
441次组卷
|
4卷引用:四川省南充高级中学2020-2021学年高一下学期3月阶段性检测化学试题
四川省南充高级中学2020-2021学年高一下学期3月阶段性检测化学试题广西桂林市2019-2020学年高一上学期期末质量检测化学试题安徽省淮北市树人高级中学2020-2021学年高一上学期期末考试化学试题(已下线)周末培优1 硫、氮及其化合物的相互转化-2021-2022学年高一化学课后培优练(人教版2019必修第二册)
解题方法
10 . 某同学用下列各装置设计一个实验,验证氯气的性质。
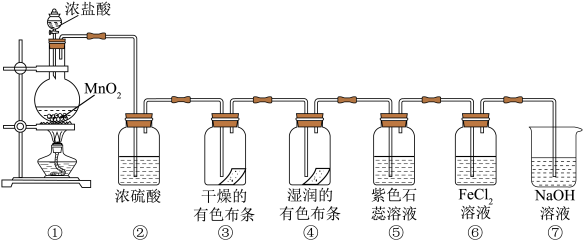
请回答:
(1)盛浓盐酸的仪器名称为___________ 。
(2)①中的化学方程式为___________ ;浓盐酸在反应中显示出来的性质是___________ 。(用字母填空)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②中浓硫酸的作用是___________ 。
(3)③中的实验现象是___________ ;④中的实验现象是___________ ;上述实验现象说明起漂白作用的是___________ (填分子式)。
(4)⑤中的现象是___________
(5)⑥中发生反应的离子方程式是___________
(6)⑦中NaOH溶液的作用是___________ ,试写出反应的离子方程式:___________ 。

请回答:
(1)盛浓盐酸的仪器名称为
(2)①中的化学方程式为
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②中浓硫酸的作用是
(3)③中的实验现象是
(4)⑤中的现象是
(5)⑥中发生反应的离子方程式是
(6)⑦中NaOH溶液的作用是
您最近一年使用:0次



