名校
解题方法
1 . 细菌可以促使含铁、氮的物质发生氧化还原反应,实现铁、氮两种元素的循环。部分转化如图,下列说法正确的是

| A.硝化过程属于氮的固定 |
| B.反硝化过程含氮物质发生氧化反应 |
| C.亚硝态氮只能通过反硝化过程转化为氮气 |
| D.土壤中的铁循环可将氮元素从水体中还原除去 |
您最近一年使用:0次
名校
解题方法
2 . 实验室制乙烯的反应原理为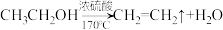 。甲同学为了探究乙烯和溴水的反应。设计了如图所示的实验装置,并进行了实验。甲同学观察到当温度升至
。甲同学为了探究乙烯和溴水的反应。设计了如图所示的实验装置,并进行了实验。甲同学观察到当温度升至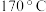 左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速退去。乙同学仔细观察了甲同学的整个实验过程,发现当温度升到
左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速退去。乙同学仔细观察了甲同学的整个实验过程,发现当温度升到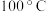 左右时,无色液体开始变色,到
左右时,无色液体开始变色,到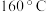 左右时,混合液全呈黑色,在
左右时,混合液全呈黑色,在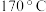 超过后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有杂质,可能影响乙烯的检出,必须除去。据此回答下列问题:
超过后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有杂质,可能影响乙烯的检出,必须除去。据此回答下列问题:___________ 。
(2)仪器a的名称是___________ 。
(3)写出乙烯与溴水反应的化学方程式___________ 。
(4)乙同学认为刺激性气味的气体也能使溴水褪色,理由是___________ (用离子方程表示)。
(5)为证明反应既有乙烯生成,又有上述刺激性气味气体,有人设计下列实验:
(6)丙烯在引发剂作用下能发生加聚反应,产物的结构简式为___________ 。
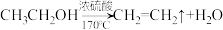 。甲同学为了探究乙烯和溴水的反应。设计了如图所示的实验装置,并进行了实验。甲同学观察到当温度升至
。甲同学为了探究乙烯和溴水的反应。设计了如图所示的实验装置,并进行了实验。甲同学观察到当温度升至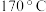 左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速退去。乙同学仔细观察了甲同学的整个实验过程,发现当温度升到
左右时,有大量气体产生,产生的气体通入溴水中,溴水的颜色迅速退去。乙同学仔细观察了甲同学的整个实验过程,发现当温度升到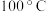 左右时,无色液体开始变色,到
左右时,无色液体开始变色,到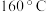 左右时,混合液全呈黑色,在
左右时,混合液全呈黑色,在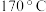 超过后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有杂质,可能影响乙烯的检出,必须除去。据此回答下列问题:
超过后生成气体速度明显加快,生成的气体有刺激性气味。由此他推出,产生的气体中应有杂质,可能影响乙烯的检出,必须除去。据此回答下列问题:
(2)仪器a的名称是
(3)写出乙烯与溴水反应的化学方程式
(4)乙同学认为刺激性气味的气体也能使溴水褪色,理由是
(5)为证明反应既有乙烯生成,又有上述刺激性气味气体,有人设计下列实验:
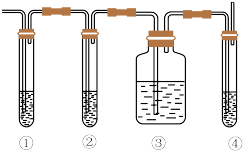
| A.品红溶液 | B.氢氧化钠溶液 | C.浓硫酸 | D.酸性高锰酸钾溶液 |
(6)丙烯在引发剂作用下能发生加聚反应,产物的结构简式为
您最近一年使用:0次
名校
解题方法
3 . 硫酸是工农业生产的重要化工原料。以黄铁矿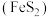 为原料生产硫酸的工艺流程如下图所示。
为原料生产硫酸的工艺流程如下图所示。___________ 。
(2)黄铁矿燃烧主要经过以下两个过程:
I.分解: ;
;
Ⅱ.燃烧: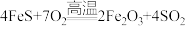 、
、___________ 。
(3)实验发现,在二氧化硫与氧气的反应中,无论怎样改变条件都不能使二氧化硫全部转化为三氧化硫,原因是___________ 。
(4)空气中二氧化硫的简易测定方法如下图所示。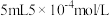 碘溶液,注入测定装置的试管中,加入
碘溶液,注入测定装置的试管中,加入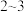 滴淀粉溶液,此时溶液呈
滴淀粉溶液,此时溶液呈___________ 色。
②连接仪器,在测定地点慢慢抽气,每次抽气 ,直到溶液的颜色全部褪尽为止,共抽气n次。空气中二氧化硫的含量为
,直到溶液的颜色全部褪尽为止,共抽气n次。空气中二氧化硫的含量为___________ 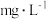 。
。
③若空气中二氧化硫的允许含量以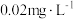 为标准,则抽气次数
为标准,则抽气次数
___________ 次才符合标准,否则超标。
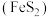 为原料生产硫酸的工艺流程如下图所示。
为原料生产硫酸的工艺流程如下图所示。
(2)黄铁矿燃烧主要经过以下两个过程:
I.分解:
 ;
;Ⅱ.燃烧:
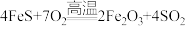 、
、(3)实验发现,在二氧化硫与氧气的反应中,无论怎样改变条件都不能使二氧化硫全部转化为三氧化硫,原因是
(4)空气中二氧化硫的简易测定方法如下图所示。
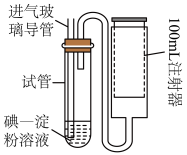
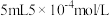 碘溶液,注入测定装置的试管中,加入
碘溶液,注入测定装置的试管中,加入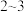 滴淀粉溶液,此时溶液呈
滴淀粉溶液,此时溶液呈②连接仪器,在测定地点慢慢抽气,每次抽气
 ,直到溶液的颜色全部褪尽为止,共抽气n次。空气中二氧化硫的含量为
,直到溶液的颜色全部褪尽为止,共抽气n次。空气中二氧化硫的含量为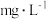 。
。③若空气中二氧化硫的允许含量以
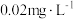 为标准,则抽气次数
为标准,则抽气次数
您最近一年使用:0次
名校
解题方法
4 .  的捕集利用已成为科学家们研究的重要课题。
的捕集利用已成为科学家们研究的重要课题。 加氢可转化为二甲醚
加氢可转化为二甲醚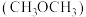 ,反应原理为
,反应原理为 。该反应的能量变化如图1所示。
。该反应的能量变化如图1所示。
(1)该反应为___________ (填“放热”或“吸热”)反应。
(2)在固定体积的密闭容器中发生该反应,能说明该反应达到平衡状态的是___________ (填字母)。
a. 的含量保持不变
的含量保持不变
b.混合气体的密度不变
c.混合气体的平均相对分子质量不变
d.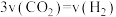
e.四种物质的浓度比为
f.每消耗 ,同时生成
,同时生成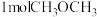
(3)在体积为 密闭容器中充入
密闭容器中充入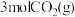 和
和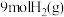 ,测得
,测得 的物质的量随时间变化如图2所示。
的物质的量随时间变化如图2所示。 时,
时,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②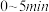 内,
内,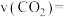
___________ 。
③反应达到平衡状态时,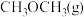 的体积分数为
的体积分数为___________  (保留1位小数)。
(保留1位小数)。
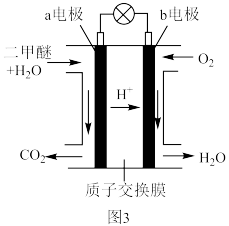
④二甲醚酸性燃料电池的工作原理示意图如图3所示。___________ (填“正”或“负”)极:b电极的电极反应式为___________ 。
 的捕集利用已成为科学家们研究的重要课题。
的捕集利用已成为科学家们研究的重要课题。 加氢可转化为二甲醚
加氢可转化为二甲醚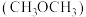 ,反应原理为
,反应原理为 。该反应的能量变化如图1所示。
。该反应的能量变化如图1所示。
(1)该反应为
(2)在固定体积的密闭容器中发生该反应,能说明该反应达到平衡状态的是
a.
 的含量保持不变
的含量保持不变 b.混合气体的密度不变
c.混合气体的平均相对分子质量不变
d.
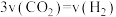
e.四种物质的浓度比为

f.每消耗
 ,同时生成
,同时生成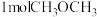
(3)在体积为
 密闭容器中充入
密闭容器中充入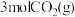 和
和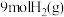 ,测得
,测得 的物质的量随时间变化如图2所示。
的物质的量随时间变化如图2所示。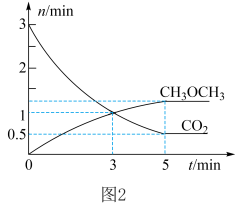
 时,
时,
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②
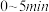 内,
内,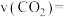
③反应达到平衡状态时,
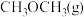 的体积分数为
的体积分数为 (保留1位小数)。
(保留1位小数)。④二甲醚酸性燃料电池的工作原理示意图如图3所示。
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题:
(1)等质量的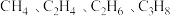 完全燃烧时耗去
完全燃烧时耗去 的量最多的是
的量最多的是___________ (填化学式)。
(2)相对分子质量为72的烷烃的分子式是___________ ;它可能的结构有___________ 种。
(3)一种有机物Y的键线式如图所示: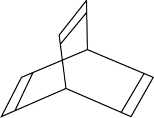 ,Y的分子式为
,Y的分子式为___________ 。
(4)硅烷即硅与氢的化合物,其的组成、结构与相应的烷烃相似,但化学性质活泼。乙硅烷可在空气中自燃,其化学反应方程式为___________ 。
(5)烷烃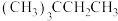 由某烯烃加氢而来,该烯烃的结构简式为
由某烯烃加氢而来,该烯烃的结构简式为___________ 。
(6)碳原子数不大于10的链状烷烃中,一氯代物只有一种结构的物质有___________ 种。
(1)等质量的
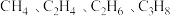 完全燃烧时耗去
完全燃烧时耗去 的量最多的是
的量最多的是(2)相对分子质量为72的烷烃的分子式是
(3)一种有机物Y的键线式如图所示:
 ,Y的分子式为
,Y的分子式为(4)硅烷即硅与氢的化合物,其的组成、结构与相应的烷烃相似,但化学性质活泼。乙硅烷可在空气中自燃,其化学反应方程式为
(5)烷烃
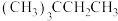 由某烯烃加氢而来,该烯烃的结构简式为
由某烯烃加氢而来,该烯烃的结构简式为(6)碳原子数不大于10的链状烷烃中,一氯代物只有一种结构的物质有
您最近一年使用:0次
名校
6 . 以反应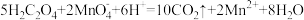 为例,通过测定溶液紫红色褪去所需时间,探究外界条件对化学反应速率的影响。设计实验如下:
为例,通过测定溶液紫红色褪去所需时间,探究外界条件对化学反应速率的影响。设计实验如下:
下列说法错误的是
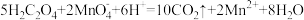 为例,通过测定溶液紫红色褪去所需时间,探究外界条件对化学反应速率的影响。设计实验如下:
为例,通过测定溶液紫红色褪去所需时间,探究外界条件对化学反应速率的影响。设计实验如下:| 实验序号 | 实验温度/℃ | 酸性KMnO4溶液 | H2C2O4溶液 | H2O | 溶液褪至无色所需时间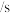 | ||
| V/mL |  | V/mL |  | V/mL | |||
| ① | 20 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
| ② | 20 | 2 | 0.02 | 2 | 0.1 | 2 | t2 |
| ③ | 45 | 2 | 0.02 | 2 | 0.1 | 2 | t3 |
| A.溶液褪至无色所需时间:t1<t2 |
| B.实验①③的目的是探究温度对化学反应速率的影响 |
| C.实验①②③均应先将酸性KMnO4溶液置于相应温度的水浴中 |
| D.每生成1 mol CO2,转移电子1 mol |
您最近一年使用:0次
名校
解题方法
7 . 下列操作中,不会明显降低溶液中K+、Fe3+、Ba2+、Cl-、 等离子浓度的是
等离子浓度的是
 等离子浓度的是
等离子浓度的是| A.通入NH3 | B.加入Cu粉 | C.加入FeCl2 | D.加入ZnSO4 |
您最近一年使用:0次
名校
解题方法
8 . 下列化学用语表示正确的是
A.异戊烷的分子式: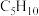 | B. 的结构式: 的结构式: |
C.甲烷的球棍模型: | D.聚乙烯的结构简式: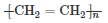 |
您最近一年使用:0次
名校
解题方法
9 . 化学与生产生活密切相关,下列说法正确的是
| A.SO2有毒,不能用作食品添加剂 |
| B.为防止月饼等富脂食品氧化变质,可在包装食品袋中放入生石灰 |
| C.“红瓷候火,还乍识、冰环玉指”所描述的红瓷,其成分为四氧化三铁 |
| D.铵态氮肥不宜与碱液混合使用 |
您最近一年使用:0次
名校
10 . 向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)⇌SO3(g)+NO(g),正反应速率随时间变化的示意图如下所示。下列叙述不正确的是
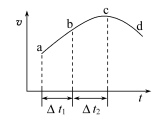
| A.反应物浓度:a点大于b点 |
| B.从a点到c点,正反应速率逐渐增大,说明该反应是放热反应 |
| C.从c点到d点,正反应速率逐渐减小,说明浓度的变化对反应速率的影响程度大于温度的变化对反应速率的影响 |
| D.反应在c点达到平衡状态 |
您最近一年使用:0次
2024-04-23更新
|
307次组卷
|
2卷引用:四川省自贡市蜀光中学2023-2024学年高一下学期期中考试化学试题



