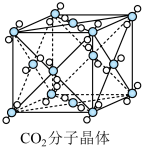
1 . 如图为干冰的晶胞结构:
(1)观察图形,确定在干冰中每个CO2分子周围有_______ 个与之紧邻且等距离的CO2分子,该结构单元平均占有_______ 个CO2分子。
(2)在干冰中撒入镁粉,用红热的铁棒引燃后,再盖上另一块干冰,出现的现象为_______ ,反应的化学方程式是_______ 。_______ CS2,填“>”或“<”),其原因是_______ 。
(4)在40GPa高压下,用激光器加热到1800K时,人们成功制得原子晶体干冰,其结构和性质与SiO2原子晶体相似,下列说法正确的是_______ 。
A.原子晶体干冰易升华,可用作制冷剂
B.原子晶体干冰有很高的熔点和沸点
C.原子晶体干冰的硬度小,不能用作耐磨材料
D.原子晶体干冰在一定条件下可与氢氧化钠反应
E.每摩尔原子晶体干冰中含有4molC—O键
(1)观察图形,确定在干冰中每个CO2分子周围有
(2)在干冰中撒入镁粉,用红热的铁棒引燃后,再盖上另一块干冰,出现的现象为
(4)在40GPa高压下,用激光器加热到1800K时,人们成功制得原子晶体干冰,其结构和性质与SiO2原子晶体相似,下列说法正确的是
A.原子晶体干冰易升华,可用作制冷剂
B.原子晶体干冰有很高的熔点和沸点
C.原子晶体干冰的硬度小,不能用作耐磨材料
D.原子晶体干冰在一定条件下可与氢氧化钠反应
E.每摩尔原子晶体干冰中含有4molC—O键
您最近一年使用:0次
解题方法
2 . I.铁(26Fe)、镍(28Ni)的单质及其化合物在医药、材料等领域有广泛的应用。回答下列问题:
(1)基态Fe原子价电子排布图为_______ ,Ni位于元素周期表的_______ 区。
(2)乳酸亚铁口服液是缺铁人群补铁保健品,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度分析,Fe2+易被氧化成Fe3+的原因是_______ 。
II.回答下列问题:
(3)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为_______ ,中心原子的杂化方式为_______ ,COCl2中心原子的VSEPR模型为_______ ,COCl2分子的空间构型为_______ 。
(4)AlH 中,Al原子的轨道杂化方式为
中,Al原子的轨道杂化方式为_______ ;列举与AlH 空间构型相同的一种离子和一种分子:
空间构型相同的一种离子和一种分子:_______ 、_______ (填化学式)。
(5)用价层电子对互斥理论推断SnBr2分子中,Sn原子的轨道杂化方式为_______ ,SnBr2分子中Br-Sn-Br的键角_______ 120°(填“>”“<”或“=”)。
(1)基态Fe原子价电子排布图为
(2)乳酸亚铁口服液是缺铁人群补铁保健品,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度分析,Fe2+易被氧化成Fe3+的原因是
II.回答下列问题:
(3)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为
(4)AlH
 中,Al原子的轨道杂化方式为
中,Al原子的轨道杂化方式为 空间构型相同的一种离子和一种分子:
空间构型相同的一种离子和一种分子:(5)用价层电子对互斥理论推断SnBr2分子中,Sn原子的轨道杂化方式为
您最近一年使用:0次
3 . Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种_______ (填字母)。
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是_______ (填序号)。
a.1s22s22p43s13p 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p d.1s22s22p63s2
d.1s22s22p63s2
(3)Ti原子位于元素周期表中的_______ 区,其价电子排布式为_______ 。
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+_______ Fe2+(填“大于”或“小于”)。
(5)下列各组多电子原子的能级能量比较不正确的是_______。
①2p=3p②4s>2s③4p>4f④4d>3d
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱 B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.1s22s22p43s13p
 3p
3p 3p
3p b.1s22s22p33s23p
b.1s22s22p33s23p 3p
3p 3p
3p
c.1s22s22p63s13p
 d.1s22s22p63s2
d.1s22s22p63s2(3)Ti原子位于元素周期表中的
(4)Fe3+与Fe2+的离子半径大小关系为Fe3+
(5)下列各组多电子原子的能级能量比较不正确的是_______。
①2p=3p②4s>2s③4p>4f④4d>3d
| A.①④ | B.①③ | C.③④ | D.②③ |
您最近一年使用:0次
名校
解题方法
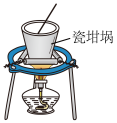
4 . 下列实验装置(部分夹持装置略)能达到相应实验目的的是
|
|
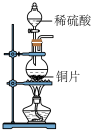
| A.加热熔NaOH固体 | B.制取SO2 |
|
|
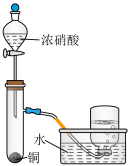
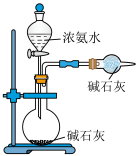
| C.制取并收集NO2 | D.制取并干燥NH3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:_______ ,硅的氧化物属于_______ (选填“酸性”“两性”或“碱性”)氧化物。
(2)整个制备过程必须严格控制无水无氧。在有氧环境下,除了有不安全因素外还可能使产品中混有杂质_______ 。整个过程中可以循环利用的物质是_______ (填化学式)。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程式:_______ 。
(3)已知H2SiO3是白色沉淀,酸性比H2CO3弱。若要证明非金属性:C>Si,方法是_______ 。
(4)关于硅及其相关化合物的叙述正确的是_______ 。
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于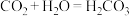 ,用类比法得知
,用类比法得知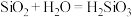
C.Na[AlSi3O8]用氧化物形式表示为Na2O·Al2O3·6SiO2
D.硅元素在金属与非金属的分界线处,因此具有弱导电性,一般可用于作为半导体材料
E.玻璃、水泥、陶瓷都是传统的硅酸盐产品
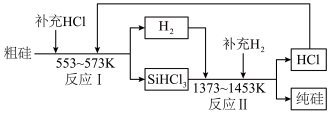
(2)整个制备过程必须严格控制无水无氧。在有氧环境下,除了有不安全因素外还可能使产品中混有杂质
(3)已知H2SiO3是白色沉淀,酸性比H2CO3弱。若要证明非金属性:C>Si,方法是
(4)关于硅及其相关化合物的叙述正确的是
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于
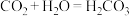 ,用类比法得知
,用类比法得知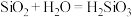
C.Na[AlSi3O8]用氧化物形式表示为Na2O·Al2O3·6SiO2
D.硅元素在金属与非金属的分界线处,因此具有弱导电性,一般可用于作为半导体材料
E.玻璃、水泥、陶瓷都是传统的硅酸盐产品
您最近一年使用:0次
名校
6 . 按要求完成问题。
(1)已知浓硫酸具有以下性质:a强氧化性b吸水性c酸性d脱水性,在下列现象中,分别体现了浓硫酸的什么性质,请把选项填在相应的横线上:
①浓硫酸与铜加热反应_______ ;
②浓硫酸与氧化亚铁反应_______ ;
③浓硫酸使蔗糖碳化_______ ;
④浓硫酸与碳单质反应_______ 。
(2)请写出热的强碱NaOH除去试管内壁附着的硫的化学方程式:_______ 。
(3)实验室用固固加热制取氨气的化学方程式:_______ 。
(4)用氢氟酸雕刻玻璃的化学方程式:_______ 。
(5)用氢氧化钠溶液吸收NO2的化学方程式:_______ 。
(1)已知浓硫酸具有以下性质:a强氧化性b吸水性c酸性d脱水性,在下列现象中,分别体现了浓硫酸的什么性质,请把选项填在相应的横线上:
①浓硫酸与铜加热反应
②浓硫酸与氧化亚铁反应
③浓硫酸使蔗糖碳化
④浓硫酸与碳单质反应
(2)请写出热的强碱NaOH除去试管内壁附着的硫的化学方程式:
(3)实验室用固固加热制取氨气的化学方程式:
(4)用氢氟酸雕刻玻璃的化学方程式:
(5)用氢氧化钠溶液吸收NO2的化学方程式:
您最近一年使用:0次
名校
解题方法
7 . 工业上以软锰矿(主要成分是MnO2,含有SiO2、Fe2O3等少量杂质)为主要原料制备高性能的磁性材料碳酸锰(MnCO3),其工业流程如图。下列说法错误的是
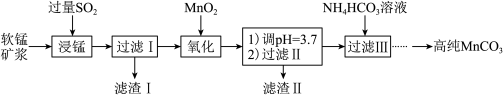
A.浸锰过程中 与 与 反应的离子方程式为: 反应的离子方程式为: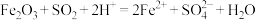 |
B.过滤I所得滤液中主要存在的金属阳离子为 和 和 |
C.滤渣Ⅱ的主要成分含有 |
D.加入 溶液发生反应的主要离子方程式为: 溶液发生反应的主要离子方程式为: |
您最近一年使用:0次
名校
解题方法
8 . 将盛有1.2molNO和NO2混合气体的试管倒立于盛满水的水槽中,再通入0.6molO2,充分反应后,整个试管充满水。则原混合气体中NO与NO2体积比为
| A.1∶2 | B.1∶1 | C.3∶7 | D.无法确定 |
您最近一年使用:0次
名校
解题方法
9 . 下列离子方程式符合题意且正确的是
A.在烧碱溶液中滴几滴 溶液: 溶液: |
B.在 溶液中加入过量 溶液中加入过量 溶液: 溶液: |
C.少量三氧化硫与氨水反应: |
D.向硅酸钠溶液中加入醋酸: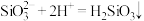 |
您最近一年使用:0次
10 . 设NA表示阿伏加德罗常数,下列叙述中正确的是
A.标准状况下,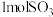 的分子数为 的分子数为 |
B. 和 和 充分反应,生成 充分反应,生成 |
C.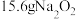 与过量 与过量 反应时,转移的电子数为 反应时,转移的电子数为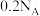 |
D.标准状况下,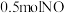 和 和 组成的混合气体,体积约为 组成的混合气体,体积约为 |
您最近一年使用:0次