解题方法
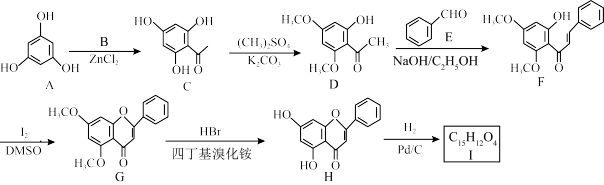
1 . 化合物Ⅰ是一种具有多种药理学活性的黄烷酮类药物。由化合物A制备Ⅰ的合成路线如图:
回答下列问题:
(1)A中官能团的名称为___________ 。
(2)若B为乙酸则由A生成C的化学方程式为___________ 。
(3)由C生成D的反应类型是___________ ,E的化学名称是___________ 。
(4)Ⅰ的结构简式为___________ 。
(5)芳香化合物X是C的同分异构体,同时满足如下条件的X有___________ 种,其中核磁共振氢谱峰面积比为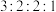 的X的结构简式是
的X的结构简式是___________ 、___________ (写出两种)。
条件:
a.苯环上只有三个取代基,且甲基不与苯环直接相连;
b.能与 溶液发生显色反应;
溶液发生显色反应;
c. 可与
可与 反应。
反应。

回答下列问题:
(1)A中官能团的名称为
(2)若B为乙酸则由A生成C的化学方程式为
(3)由C生成D的反应类型是
(4)Ⅰ的结构简式为
(5)芳香化合物X是C的同分异构体,同时满足如下条件的X有
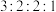 的X的结构简式是
的X的结构简式是条件:
a.苯环上只有三个取代基,且甲基不与苯环直接相连;
b.能与
 溶液发生显色反应;
溶液发生显色反应;c.
 可与
可与 反应。
反应。
您最近一年使用:0次
解题方法
2 . 氮化物应用广泛,如叠氮化钠(NaN3)是典型的高能量密度含能材料,氮化硼是特殊的耐磨和切削材料,氮化铬、氮化钼等过渡金属氮化物常用作高强度材料。回答下列问题:
(1)Na、N、B中,原子半径由大到小的顺序是___________ 。
(2)基态N原子价层电子的电子排布图为___________ 。基态铬原子核外未成对电子数为___________ 。
(3)NaN3中阴离子N 是直线型离子。1个N
是直线型离子。1个N 中的σ键数目为
中的σ键数目为___________ 。分子或离子中的大π键可用符号Π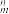 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π ),则N
),则N 中的大π键应表示为
中的大π键应表示为___________ 。
(4)石墨型(BN)x转变为金刚石型(BN)x时,B原子的杂化轨道类型由___________ 变为___________ 。金刚石型(BN)x的硬度比金刚石大,推测其原因是___________ 。
(5)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。
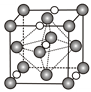
氮化钼的化学式为___________ ,如果让Li+填入氮化钼晶体的八面体空隙,一个晶胞最多可以填入___________ 个Li+。氮化钼晶胞边长为a nm,晶体的密度ρ=___________ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)Na、N、B中,原子半径由大到小的顺序是
(2)基态N原子价层电子的电子排布图为
(3)NaN3中阴离子N
 是直线型离子。1个N
是直线型离子。1个N 中的σ键数目为
中的σ键数目为 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π ),则N
),则N 中的大π键应表示为
中的大π键应表示为(4)石墨型(BN)x转变为金刚石型(BN)x时,B原子的杂化轨道类型由
(5)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。

氮化钼的化学式为
您最近一年使用:0次
名校
3 . 钪是地壳中含量极少的稀土元素,但在照明、合金和陶瓷材料、催化化学等领域具有重要应用价值。钛铁矿主要成分为TiO2、FeO、Fe2O3,还含有Mg、Si、Sc等元素,从钛铁矿中提取Sc2O3的流程如下:

回答下列问题:
(1)“酸浸”时,为提高浸取效率,可以采取的措施有___________ (答两个)。滤渣1的主要成分是___________ 。
(2)“酸浸”后Ti元素转化为TiOSO4,其水解反应的化学方程式是___________ 。
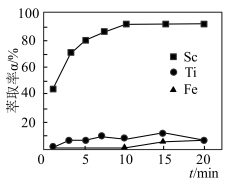
(3)“萃取”时,使用10%P2O4+5%TBP+煤油作为萃取剂,一定条件下萃取率α受振荡时间的影响如图,萃取时适宜的振荡时间为___________ min。“洗钛”所得[TiO(H2O2)]2+为橘黄色的稳定离子,其中氧的化合价有-2、-1两种,则Ti的化合价为___________ 。
(4)“酸溶”后滤液中存在的金属阳离子Sc3+、TiO2+、Fe3+浓度均小于0.01 mol/L,再用氨水调节溶液pH使TiO2+、Fe3+沉淀完全而Sc3+不沉淀,则调pH应控制的pH范围是___________ 。
已知:当离子浓度减小至10-5 mol/L时可认为沉淀完全。lg2=0.3;室温下TiO2+完全沉淀的pH为1.05,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Sc(OH)3]=1.25×10-33。
(5)加草酸“沉钪”的离子方程式为___________ 。
(6)“沉钪”后获得Sc2O3的方法是___________ ,该反应产生的气体必须回收利用,其意义是___________ 。

回答下列问题:
(1)“酸浸”时,为提高浸取效率,可以采取的措施有
(2)“酸浸”后Ti元素转化为TiOSO4,其水解反应的化学方程式是
(3)“萃取”时,使用10%P2O4+5%TBP+煤油作为萃取剂,一定条件下萃取率α受振荡时间的影响如图,萃取时适宜的振荡时间为

(4)“酸溶”后滤液中存在的金属阳离子Sc3+、TiO2+、Fe3+浓度均小于0.01 mol/L,再用氨水调节溶液pH使TiO2+、Fe3+沉淀完全而Sc3+不沉淀,则调pH应控制的pH范围是
已知:当离子浓度减小至10-5 mol/L时可认为沉淀完全。lg2=0.3;室温下TiO2+完全沉淀的pH为1.05,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Sc(OH)3]=1.25×10-33。
(5)加草酸“沉钪”的离子方程式为
(6)“沉钪”后获得Sc2O3的方法是
您最近一年使用:0次
2021-01-07更新
|
1947次组卷
|
7卷引用:四川省自贡市田家炳中学2021届高三12月月考化学试题
四川省自贡市田家炳中学2021届高三12月月考化学试题(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练四川省绵阳南山中学2021-2022学年高三上学期入学考试理综化学试题四川省泸州市泸县第四中学2022届高三三诊模拟考试理科综合化学试题四川省绵阳市梓潼中学校2023-2024学年高三上学期入学考试理科综合化学试题(已下线)工业流程题
解题方法
4 . 化合物H是重要的有机物,可由E和F在一定条件下合成:(部分反应物或产物省略,另请注意箭头的指向方向)

已知如下信息:①A属于芳香烃,H属于酯类化合物。
(1) B的结构简式______________ ,C的官能团名称______________ .
(2)B→C__________________ ;G→J两步的反应类型__________ ,
(3)①E+F→H的化学方程式__________________ .
②I→G的化学方程式__________________ .
(4)H的同系物K比H相对分子质量小28,K的同分异构体中能同时满足如下条件:
①K的一个同分异构体能发生银镜反应,也能使FeCl3溶液显紫色,苯环上有两个支链,苯环上的氢的核磁共振氢谱为二组峰,且峰面积比为1:1,写出K的这种同分异构体的结构简式______________ .
②若K的同分异构体属于芳香族化合物,又能和饱和NaHCO3溶液反应放出CO2,共有__________ 种(不考虑立体异构)。

已知如下信息:①A属于芳香烃,H属于酯类化合物。
②I的核磁共振氢谱为两组峰,且峰面积为6∶1 。
(1) B的结构简式
(2)B→C
(3)①E+F→H的化学方程式
②I→G的化学方程式
(4)H的同系物K比H相对分子质量小28,K的同分异构体中能同时满足如下条件:
①K的一个同分异构体能发生银镜反应,也能使FeCl3溶液显紫色,苯环上有两个支链,苯环上的氢的核磁共振氢谱为二组峰,且峰面积比为1:1,写出K的这种同分异构体的结构简式
②若K的同分异构体属于芳香族化合物,又能和饱和NaHCO3溶液反应放出CO2,共有
您最近一年使用:0次
5 . 氰化钠(NaCN)是一种重要的化工原料、有剧毒,一旦泄漏可以通过喷洒双氧水或硫代硫酸钠溶液来处理。
已知:氰化钠与硫代硫酸钠的反应为:NaCN+Na2S2O3==NaSCN+Na2SO3回答下列问题:
(1)氰化物中碳的化合价为___________ ;用硫代硫酸钠处理1mol NaCN时,反应中转移电子的物质的量为___________ 。
(2)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是_____________ 。
(3)某化学兴趣小组在实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】制备Na2S2O3,其实验室装置如下:
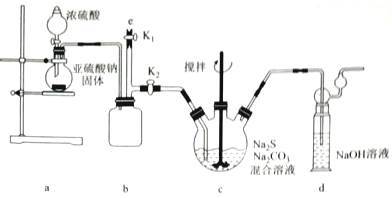
b装置的作用是___________ ;c装置中的产物有Na2S2O3和CO2等,d装置中的溶质有NaOH、Na2CO3,还可能有_____________ 。
实验结束后,在e处最好连接盛____________ (填化学式)的注射器,再关闭K2打开K1,以防拆除装置过程中的有害气体污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50mg/L;
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先于Ag+反应。
实验如下:取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
滴定时1.000×10-4mol/L的标准AgNO3溶液应用_________ (填仪器名称)盛装;滴定终点时的现象是___________ 。
处理后的废水是否达到排放标准:__________ (填“是”或“否”),其依据是__________ (用实验数据说明)。
已知:氰化钠与硫代硫酸钠的反应为:NaCN+Na2S2O3==NaSCN+Na2SO3回答下列问题:
(1)氰化物中碳的化合价为
(2)NaCN用双氧水处理后,产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,该反应的离子方程式是
(3)某化学兴趣小组在实验室制备硫代硫酸钠(Na2S2O3),并检测用硫代硫酸钠溶液处理后的氰化钠废水能否达标排放。
【实验一】制备Na2S2O3,其实验室装置如下:

b装置的作用是
实验结束后,在e处最好连接盛
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。
已知:①废水中氰化钠的最高排放标准为0.50mg/L;
②Ag++2CN-=[Ag(CN)2]-,Ag++I-=AgI↓,AgI呈黄色,且CN-优先于Ag+反应。
实验如下:取20.00mL处理后的氰化钠废水于锥形瓶中,并滴加几滴KI溶液作指示剂,用1.00×10-4mol/L的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为1.50mL。
滴定时1.000×10-4mol/L的标准AgNO3溶液应用
处理后的废水是否达到排放标准:
您最近一年使用:0次
6 . 甲醇是重要的绿色能源之一,目前科学家用水煤气(CO+H2)合成甲醇,其反应为:
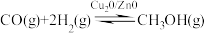 △H=-128.1kJ·mol-1,回答下列问题:
△H=-128.1kJ·mol-1,回答下列问题:
(1)该反应是可逆反应,为使化学反应速率和CO的转化率都同时提高的措施有_____________ (写两条)。
(2)恒温恒容条件能说明该可逆反应达平衡的是______________ ;
A.2v正(H2)=v逆(CH3OH)
B.n(CO):n(H2):n(CH3OH)=1:2:1
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
(3)若上述可逆反应在恒温恒容的密闭容器进行,起始时间向该容器中冲入1molCO(g)和2molH2(g)。实验测得H2的平衡转化率随温度(T)、压强(P)的变化如图所示。
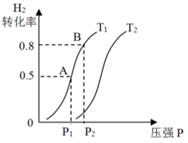
该反应的△S____________ 0,图中的T1___________ T2(填“<”“>”或“=”)
②T1下到达平衡状态A时,容器的体积为2L,此时该反应的平衡常数为_____________ ,若达到平衡状态B时,则容器的体积V(B)=________ L。
(4)已知:H2(g)燃烧热△H=-285.8kJ·mol-1、和CO(g)燃烧热△H=-283.0kJ·mol-1,则CH3OH(g)燃烧热的热化学方程式是为____________ 。
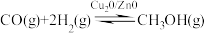 △H=-128.1kJ·mol-1,回答下列问题:
△H=-128.1kJ·mol-1,回答下列问题:(1)该反应是可逆反应,为使化学反应速率和CO的转化率都同时提高的措施有
(2)恒温恒容条件能说明该可逆反应达平衡的是
A.2v正(H2)=v逆(CH3OH)
B.n(CO):n(H2):n(CH3OH)=1:2:1
C.混合气体的密度不变
D.混合气体的平均相对分子质量不变
(3)若上述可逆反应在恒温恒容的密闭容器进行,起始时间向该容器中冲入1molCO(g)和2molH2(g)。实验测得H2的平衡转化率随温度(T)、压强(P)的变化如图所示。

该反应的△S
②T1下到达平衡状态A时,容器的体积为2L,此时该反应的平衡常数为
(4)已知:H2(g)燃烧热△H=-285.8kJ·mol-1、和CO(g)燃烧热△H=-283.0kJ·mol-1,则CH3OH(g)燃烧热的热化学方程式是为
您最近一年使用:0次



