1 . 常温下,PdCO3和Pd(OH)2的沉淀溶解平衡曲线如图所示。下列说法正确的是
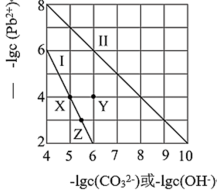
| A.向Z点对应溶液中加入适量的NaOH溶液,有可能得到X点对应溶液 |
| B.Y点对应的PdCO3分散系中,v(溶解)>v(沉淀),固体仍在溶解 |
C.PbCO3(s)+2OH-(aq) Pb(OH)2(s)+ Pb(OH)2(s)+ K=0.01 K=0.01 |
| D.由两者的Ksp可知,Pd(OH)2的溶解度更小 |
您最近一年使用:0次
解题方法
2 . 肼为二元弱碱,在水中的电离方式与氨相似。常温下,向一定浓度肼 水溶液中通入
水溶液中通入 (忽略溶液体积变化),测得
(忽略溶液体积变化),测得 与
与 [X为
[X为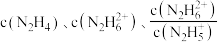 ]的变化关系如图所示。下列说法正确的是
]的变化关系如图所示。下列说法正确的是
 水溶液中通入
水溶液中通入 (忽略溶液体积变化),测得
(忽略溶液体积变化),测得 与
与 [X为
[X为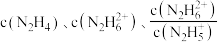 ]的变化关系如图所示。下列说法正确的是
]的变化关系如图所示。下列说法正确的是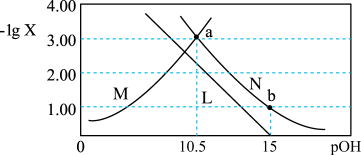
A.曲线N表示 与 与 的变化关系 的变化关系 |
B.常温下,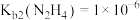 |
C.a点溶液中: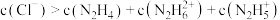 |
D.b点溶液中: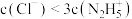 |
您最近一年使用:0次
2024-04-16更新
|
298次组卷
|
2卷引用:2024届四川省雅安市天全中学高三下学期模拟预测化学试题
真题
名校
3 . 元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如图所示。

①在1个晶胞中,X离子的数目为_____ 。
②该化合物的化学式为_________ 。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是_______ 。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是______________ 。
(4)Y 与Z 可形成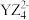
①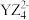 的空间构型为
的空间构型为__________ (用文字描述)。
②写出一种与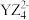 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:_________ 。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为___ 。
(1)X与Y所形成化合物晶体的晶胞如图所示。

①在1个晶胞中,X离子的数目为
②该化合物的化学式为
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是
(4)Y 与Z 可形成
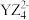
①
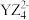 的空间构型为
的空间构型为②写出一种与
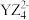 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为
您最近一年使用:0次
2019-01-30更新
|
2183次组卷
|
12卷引用:四川省雅安市2017-2018学年高二上学期期末考试化学试题
四川省雅安市2017-2018学年高二上学期期末考试化学试题2013年全国普通高等学校招生统一考试化学(江苏卷)(已下线)2012-2013学年福建省师大附中高二下学期期末考试化学试卷(已下线)2014届高考化学二轮专题冲刺第16讲 物质结构与性质练习卷2016届安徽省六安一中高三上第四次月考化学试卷2015-2016学年福建省师大附中高二上期末理化学试卷2016届福建省福州八中高三上学期第六次质检化学试卷2017届甘肃省定西市通渭县高三上学期期末化学试卷2016-2017学年山东省滨州市高二下学期第一次阶段性测试化学试卷宁夏回族自治区吴忠市吴忠中学2019-2020学年高二下学期期末考试化学试题(已下线)模块同步卷08 分子晶体与原子晶体-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)(已下线)2020年海南卷化学高考真题变式题15-19
4 . 某蓄电池反应为NiO2+Fe+2H2O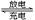 Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2
(1)该蓄电池充电时,发生还原反应的物质是_______ (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是_____________ 。
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常把船体与浸在海水里的Zn块相连,或与该蓄电池这样的直流电源的______ 极(填“正”或“负”)相连。
(3)以该蓄电池做电源,用下图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示__________________________________ 。

(4)精炼铜时,粗铜应与直流电源的________ 极(填“正”或“负”)相连,精炼过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解,甲同学设计如下除杂方案:

已知各离子沉淀时的情况如下表:
则加入H2O2的目的是__________________________________________________ ,
发生反应的离子方程式为_________ 。乙同学认为应将方案中的pH调节到8,你认为此观点______ (填“正确”或“不正确”),理由是______________________________ 。
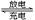 Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2(1)该蓄电池充电时,发生还原反应的物质是
| A.NiO2 | B.Fe | C.Fe(OH)2 | D.Ni(OH)2 |
(3)以该蓄电池做电源,用下图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示

(4)精炼铜时,粗铜应与直流电源的

已知各离子沉淀时的情况如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
| 完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |
发生反应的离子方程式为
您最近一年使用:0次
5 . Ⅰ.CO可用于合成甲醇。在压强为0.1MPa条件下,在体积为bL的密闭容器中充入a mol CO和2a mol H2,在催化剂作用下合成甲醇:
CO(g)+2H2(g) CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
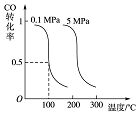
(1)该反应属于_________ 反应(填“吸热”或“放热”)。
(2)100℃时,该反应的平衡常数:K=___________ (用a、b 的代数式表示)。
(3)在温度和容积不变的情况下,再向平衡体系中充入a mol CO,2a mol H2,达到平衡时CO转化率_____ (填“增大”“不变”或“减小”)
Ⅱ.T ℃时,纯水中c(OH-)为10-6 mol·L-1,则该温度时
(1)将pH=3 的H2SO4溶液与pH=10的NaOH溶液按体积比9:2 混合,所得混合溶液的pH为_______ 。
(2)若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是__________ 。
Ⅲ. 在25mL的氢氧化钠溶液中逐滴加入0.2 mol/ L醋酸溶液,滴定曲线如图所示。
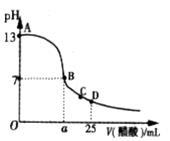
(1)该氢氧化钠溶液浓度为________________ 。
(2)在B点,a_________ 12.5 mL(填“<”“>”或“=”)。若由体积相等的氢氧化钠溶液和醋酸溶液混合且恰好呈中性,则混合前c(NaOH)___________ c(CH3COOH)
(3)在D点,溶液中离子浓度大小关系为_____________________ 。
CO(g)+2H2(g)
 CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
CH3OH(g)平衡时CO的转化率与温度、压强的关系如下图:
(1)该反应属于
(2)100℃时,该反应的平衡常数:K=
(3)在温度和容积不变的情况下,再向平衡体系中充入a mol CO,2a mol H2,达到平衡时CO转化率
Ⅱ.T ℃时,纯水中c(OH-)为10-6 mol·L-1,则该温度时
(1)将pH=3 的H2SO4溶液与pH=10的NaOH溶液按体积比9:2 混合,所得混合溶液的pH为
(2)若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是
Ⅲ. 在25mL的氢氧化钠溶液中逐滴加入0.2 mol/ L醋酸溶液,滴定曲线如图所示。

(1)该氢氧化钠溶液浓度为
(2)在B点,a
(3)在D点,溶液中离子浓度大小关系为
您最近一年使用:0次
名校
6 . 为了探究FeSO4和Cu(NO3)2的混合物中各组分的含量,现设计如下流程:

下列叙述中不正确 的是( )

下列叙述中
| A.n=0.02 | B.m=3.2 |
| C.V=2240 | D.原混合物中FeSO4的质量分数约为89% |
您最近一年使用:0次
2018-03-22更新
|
514次组卷
|
6卷引用:【全国百强校】四川省雅安中学2018-2019学年高一上学期开学考试化学试题
7 . 已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于短周期。A是原子半径最小的元素;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D原子的核外成对电子数是未成对电子数的3倍;E有“生物金属”之称,E4+和氩原子的核外电子排布相同。A、B、D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,A、B两种元素组成的原子个数之比为1 : 1的化合物N是常见的有机溶剂。
请回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)A2D2分子的电子式为____________ ,属于___________ 分子(填“极性”或“非极性”),E的基态原子的外围电子排布式为____________ 。
(2)B、C、D三种元素的第一电离能由小到大的顺序为____________ 。
(3)C元素形成含氧酸酸性强弱:HNO3____________ HNO2(填“>”或“<”)NO3—的空间构型是___________ ,NO2—中心原子的杂化方式为___________
(4)下列叙述正确的是____________ (填序号)。
A. M是极性分子,N是非极性分子
B. M和BD2分子中的中心原子均采用sp2杂化
C. N分子中含有6个σ键和1个大π键
D. BD2晶体的熔点、沸点都比二氧化硅晶体的低
(5)已知:①E的一种氧化物Q,其晶胞结构如图所示:
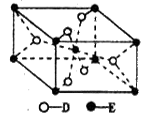
①Q(s)+2Cl2(g)=ECl4(l)+D2(g) △H=+140kJ/mol
②2B(s)+D2(g)=2BD(g) △H=-221kJ/mol
写出物质Q和焦炭、氯气反应生成液态ECl4和BD气体的热化学方程式:____________________
请回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)A2D2分子的电子式为
(2)B、C、D三种元素的第一电离能由小到大的顺序为
(3)C元素形成含氧酸酸性强弱:HNO3
(4)下列叙述正确的是
A. M是极性分子,N是非极性分子
B. M和BD2分子中的中心原子均采用sp2杂化
C. N分子中含有6个σ键和1个大π键
D. BD2晶体的熔点、沸点都比二氧化硅晶体的低
(5)已知:①E的一种氧化物Q,其晶胞结构如图所示:

①Q(s)+2Cl2(g)=ECl4(l)+D2(g) △H=+140kJ/mol
②2B(s)+D2(g)=2BD(g) △H=-221kJ/mol
写出物质Q和焦炭、氯气反应生成液态ECl4和BD气体的热化学方程式:
您最近一年使用:0次
8 . 根据题意回答下列问题
(I)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为________________________________ 。
(2)又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是_____________ kJ。
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是______________ 。
(II)某实验小组测定中和热做了三次实验,所用NaOH溶液的浓度为0.55mol· L-1,盐酸的浓度为0.5mol· L-1,每次取NaOH溶液和盐酸溶液各50 mL,并记录如下原始数据。
(1)已知盐酸、NaOH溶液密度近似为1.00g·cm-3,中和后混合液的比热容c=4.18×10-3 kJ·g-1·℃-1,则该反应的中和热为ΔH=__________ 。
(2)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会________ (填“偏大”、“偏小”或“不变”),其原因是____________________________________________ 。
(3)在中和热测定实验中存在用水洗涤温度计上的盐酸溶液的步骤,若无此操作步骤,则测得的中和热________ (填“偏大”、“偏小”或“不变”)。
(I)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出256.7kJ的热量(相当于25℃、101 kPa下测得的热量)。
(1)反应的热化学方程式为
(2)又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
(II)某实验小组测定中和热做了三次实验,所用NaOH溶液的浓度为0.55mol· L-1,盐酸的浓度为0.5mol· L-1,每次取NaOH溶液和盐酸溶液各50 mL,并记录如下原始数据。
| 实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差(t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
| 2 | 25.1 | 25.1 | 25.1 | 28.4 | 3.3 |
| 3 | 25.1 | 25.1 | 25.1 | 28.5 | 3.4 |
(2)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会
(3)在中和热测定实验中存在用水洗涤温度计上的盐酸溶液的步骤,若无此操作步骤,则测得的中和热
您最近一年使用:0次
9 . 辉铜矿(主要成分为Cu2S)经火法冶炼,可制得Cu和H2SO4,流程如下图所示:
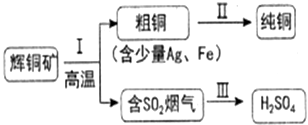
(1)Cu2S中Cu元素的化合价是__________ 价。
(2)Ⅱ中,电解法精炼粗铜(含少量Ag、Fe),CuSO4溶液做电解质溶液:
①粗铜应与直流电源的_________ 极(填“正”或“负”)相连。
②铜在阴极析出,而铁以离子形式留在电解质溶液里的原因是__________________________ 。
(3)Ⅲ中,烟气(主要含SO2、CO2)在较高温度经下图所示方法脱除SO2,并制得H2SO4。
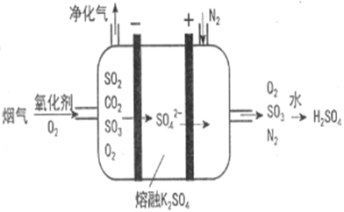
①在阴极放电的物质________________ 。
②在阳极生成SO3的电极反应式是_______________________________ 。
(4)检测烟气中SO2脱除率的步骤如下:
(i).将一定量的净化气(不含SO3)通入足量NaOH溶液后,再加入足量溴水。
(ii)加入浓盐酸,加热溶液至无色无气泡,再加入足量BaCl2溶液。
(iii)过滤、洗涤、干燥,称量沉淀质量。
①用离子方程式表示(i)中溴水的主要作用________________________________ 。
②若沉淀的质量越大,说明SO2的脱除率越________ (填“高”或“低”)。

(1)Cu2S中Cu元素的化合价是
(2)Ⅱ中,电解法精炼粗铜(含少量Ag、Fe),CuSO4溶液做电解质溶液:
①粗铜应与直流电源的
②铜在阴极析出,而铁以离子形式留在电解质溶液里的原因是
(3)Ⅲ中,烟气(主要含SO2、CO2)在较高温度经下图所示方法脱除SO2,并制得H2SO4。

①在阴极放电的物质
②在阳极生成SO3的电极反应式是
(4)检测烟气中SO2脱除率的步骤如下:
(i).将一定量的净化气(不含SO3)通入足量NaOH溶液后,再加入足量溴水。
(ii)加入浓盐酸,加热溶液至无色无气泡,再加入足量BaCl2溶液。
(iii)过滤、洗涤、干燥,称量沉淀质量。
①用离子方程式表示(i)中溴水的主要作用
②若沉淀的质量越大,说明SO2的脱除率越
您最近一年使用:0次
2016-12-09更新
|
802次组卷
|
2卷引用:【全国市级联考】四川省雅安市2017-2018学年高二下学期期末考试化学试题
10 . 将一定质量的镁铝合金投入100 mL一定物质的量浓度的盐酸中,合金全部溶解,向所得溶液中滴加5 mol/L NaOH溶液至过量,生成沉淀的质量与加入氢氧化钠溶液的体积的关系如图所示。
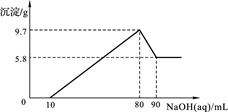
(1)当沉淀达到最大值时,Al(OH)3的质量;
(2)原合金中Mg的质量;
(3)盐酸的物质的量浓度。

(1)当沉淀达到最大值时,Al(OH)3的质量;
(2)原合金中Mg的质量;
(3)盐酸的物质的量浓度。
您最近一年使用:0次
2016-12-09更新
|
1362次组卷
|
5卷引用:2015-2016学年四川省雅安中学高一上期末模拟化学试卷



