1 . 天然水体中的 与空气中的
与空气中的 保持平衡。某地溶洞水体中
保持平衡。某地溶洞水体中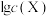 (X为
(X为 、
、 、
、 或
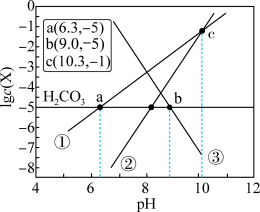
或 )与pH的线性关系如图所示。下列说法不正确的是
)与pH的线性关系如图所示。下列说法不正确的是
 与空气中的
与空气中的 保持平衡。某地溶洞水体中
保持平衡。某地溶洞水体中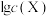 (X为
(X为 、
、 、
、 或
或 )与pH的线性关系如图所示。下列说法不正确的是
)与pH的线性关系如图所示。下列说法不正确的是
A.直线①代表 ,直线③代表 ,直线③代表 |
B.图中 |
C.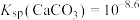 |
D.若空气中的 浓度增加,则水体中的 浓度增加,则水体中的 浓度减小 浓度减小 |
您最近一年使用:0次
2023-04-27更新
|
1017次组卷
|
3卷引用:四川省绵阳市高中2022-2023学年高二下学期理科突击班6月月考化学试题
四川省绵阳市高中2022-2023学年高二下学期理科突击班6月月考化学试题浙江省稽阳联谊学校2022-2023学年高三下学期4月联考化学试题(已下线)题型03 电解质溶液图像分析-2024年高考化学答题技巧与模板构建
2 . 难溶盐 可溶于盐酸,常温下,用
可溶于盐酸,常温下,用 调节
调节 浊液的
浊液的 ,测得体系中
,测得体系中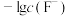 或
或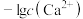 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是

 可溶于盐酸,常温下,用
可溶于盐酸,常温下,用 调节
调节 浊液的
浊液的 ,测得体系中
,测得体系中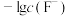 或
或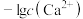 与
与 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.M代表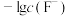 与 与 的变化曲线 的变化曲线 |
B.难溶盐 的溶度积常数 的溶度积常数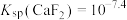 |
C.Y点的溶液中存在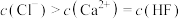 |
D.Z点的溶液中存在 |
您最近一年使用:0次
2023-02-18更新
|
1948次组卷
|
9卷引用:四川省绵阳市南山中学实验学校2022-2023学年高三下学期3月月考理科综合化学试题
四川省绵阳市南山中学实验学校2022-2023学年高三下学期3月月考理科综合化学试题湖南省百校2023届高三开年摸底联考化学试题浙江省杭州学军中学2022-2023学年高三下学期阶段性测试化学试题(已下线)素养卷05 电解质溶液中微粒变化图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)先机卷 04 -【热题狂飙】2023年高考化学样卷(全国卷专用)广东省广州市等5地广州百师信息科技有限公司等2校2022-2023学年高三下学期开学考试化学试题山东省蒙阴第一中学等5校2023届高三开学摸底联考化学试题河南省南阳市第一中学校2023-2024学年高二上学期12月月考化学试题(已下线)选择题11-15
名校
解题方法
3 . 科学家发现固体电解质Li3SBF4快离子导体具有良好的导电能力,为锂离子电池的发展做出了重要贡献。回答下列问题:
(1)基态F原子的价电子排布图为_______ 。B和F均为第2周期元素,在第2周期元素中,第一电离能介于B与F之间的元素有_______ 种。
(2)一种硼酸盐的阴离子为B3O4n-,其结构中只有一个六元环,B的空间化学环境相同,O有两种空间化学环境,画出B3O 的结构图
的结构图_______ (注明所带电荷数)。[B5O6(OH)4]-的结构为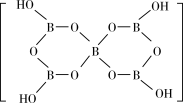 ,则B原子的配位数是
,则B原子的配位数是_______ 。
(3)L3SBF4可由Li2S与LiBF4按一定比例反应合成。Li2S和LiBF4的熔点如表所示:
Li2S与LiBF4均属于_______ 晶体;熔点:Li2S>LiBF4,原因是_______ 。
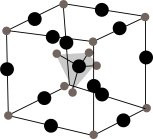
(4)Li3SBF4的晶胞结构如图所示,其中BF 位于体心,则Li+位于
位于体心,则Li+位于_______ (填“顶点”或“棱边”)。设NA为阿伏加德罗常数的值,若该晶胞中Li+与BF 间的最近距离为apm,则晶体密度为
间的最近距离为apm,则晶体密度为_______ g·cm-3,在Li3SBF4晶胞的另一种结构中,BF 位于顶点,则S2-位于
位于顶点,则S2-位于_______ (填“体心”“面心”或“棱边”)。
(1)基态F原子的价电子排布图为
(2)一种硼酸盐的阴离子为B3O4n-,其结构中只有一个六元环,B的空间化学环境相同,O有两种空间化学环境,画出B3O
 的结构图
的结构图 ,则B原子的配位数是
,则B原子的配位数是(3)L3SBF4可由Li2S与LiBF4按一定比例反应合成。Li2S和LiBF4的熔点如表所示:
| 物质 | Li2S | LiBF4 |
| 熔点/℃ | 938 | 300 |
(4)Li3SBF4的晶胞结构如图所示,其中BF
 位于体心,则Li+位于
位于体心,则Li+位于 间的最近距离为apm,则晶体密度为
间的最近距离为apm,则晶体密度为 位于顶点,则S2-位于
位于顶点,则S2-位于
您最近一年使用:0次
名校
4 . 钪是地壳中含量极少的稀土元素,但在照明、合金和陶瓷材料、催化化学等领域具有重要应用价值。钛铁矿主要成分为TiO2、FeO、Fe2O3,还含有Mg、Si、Sc等元素,从钛铁矿中提取Sc2O3的流程如下:

回答下列问题:
(1)“酸浸”时,为提高浸取效率,可以采取的措施有___________ (答两个)。滤渣1的主要成分是___________ 。
(2)“酸浸”后Ti元素转化为TiOSO4,其水解反应的化学方程式是___________ 。
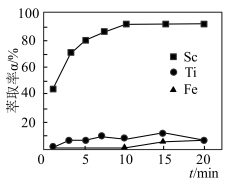
(3)“萃取”时,使用10%P2O4+5%TBP+煤油作为萃取剂,一定条件下萃取率α受振荡时间的影响如图,萃取时适宜的振荡时间为___________ min。“洗钛”所得[TiO(H2O2)]2+为橘黄色的稳定离子,其中氧的化合价有-2、-1两种,则Ti的化合价为___________ 。
(4)“酸溶”后滤液中存在的金属阳离子Sc3+、TiO2+、Fe3+浓度均小于0.01 mol/L,再用氨水调节溶液pH使TiO2+、Fe3+沉淀完全而Sc3+不沉淀,则调pH应控制的pH范围是___________ 。
已知:当离子浓度减小至10-5 mol/L时可认为沉淀完全。lg2=0.3;室温下TiO2+完全沉淀的pH为1.05,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Sc(OH)3]=1.25×10-33。
(5)加草酸“沉钪”的离子方程式为___________ 。
(6)“沉钪”后获得Sc2O3的方法是___________ ,该反应产生的气体必须回收利用,其意义是___________ 。

回答下列问题:
(1)“酸浸”时,为提高浸取效率,可以采取的措施有
(2)“酸浸”后Ti元素转化为TiOSO4,其水解反应的化学方程式是
(3)“萃取”时,使用10%P2O4+5%TBP+煤油作为萃取剂,一定条件下萃取率α受振荡时间的影响如图,萃取时适宜的振荡时间为

(4)“酸溶”后滤液中存在的金属阳离子Sc3+、TiO2+、Fe3+浓度均小于0.01 mol/L,再用氨水调节溶液pH使TiO2+、Fe3+沉淀完全而Sc3+不沉淀,则调pH应控制的pH范围是
已知:当离子浓度减小至10-5 mol/L时可认为沉淀完全。lg2=0.3;室温下TiO2+完全沉淀的pH为1.05,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Sc(OH)3]=1.25×10-33。
(5)加草酸“沉钪”的离子方程式为
(6)“沉钪”后获得Sc2O3的方法是
您最近一年使用:0次
2021-01-07更新
|
1947次组卷
|
7卷引用:四川省绵阳南山中学2021-2022学年高三上学期入学考试理综化学试题
四川省绵阳南山中学2021-2022学年高三上学期入学考试理综化学试题四川省绵阳市梓潼中学校2023-2024学年高三上学期入学考试理科综合化学试题四川省自贡市田家炳中学2021届高三12月月考化学试题(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密06 金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练四川省泸州市泸县第四中学2022届高三三诊模拟考试理科综合化学试题(已下线)工业流程题
名校
解题方法
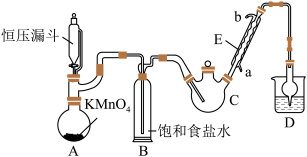
5 . 三氯乙醛(CCl3CHO)是生产农药、医药的重要中间体,实验室制备三氯乙醛的反应装置示意图(加热装置未画出)和有关数据如下:
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
②相关物质的相对分子质量及部分物理性质:
(1)恒压漏斗中盛放的试剂的名称是_____ ,盛放KMnO4仪器的名称是_____ 。
(2)反应过程中C2H5OH和HCl可能会生成副产物C2H5Cl,同时CCl3CHO(三氯乙醛)也能被次氯酸继续氧化生成CCl3COOH(三氯乙酸),写出三氯乙醛被次氯酸氧化生成三氯乙酸的化学方程式______ 。
(3)该设计流程中存在一处缺陷是______ ,导致引起的后果是______ ,装置B的作用是____ 。
(4)反应结束后,有人提出先将C中的混合物冷却到室温,再用分液的方法分离出三氯乙酸。你认为此方案是否可行____ (填是或否),原因是______ 。
(5)测定产品纯度:称取产品0.36g配成待测溶液,加入0.1000mol•L −1碘标准溶液 20.00mL,再加适量Na2CO3溶液,反应完全后加盐酸调溶液pH,立即用0.02000mol•L −1Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液20.00mL。则产品的纯度为_____ (计算结果保留四位有效数字)。滴定原理:CCl3CHO+OH-=CHCl3+HCOO-、HCOO-+I2=H++2I-+CO2、I2+2S2O32-=2I-+S4O62-

①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
②相关物质的相对分子质量及部分物理性质:
相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | |
C2H5OH | 46 | -114. 1 | 78.3 | 与水互溶 |
CC13CHO | 147. 5 | -57. 5 | 97.8 | 可溶于水、乙醇 |
CC13COOH | 163. 5 | 58 | 198 | 可溶于水、乙醇、三氯乙醛 |
C2H5C1 | 64. 5 | -138.7 | 12.3 | 微溶于水,可溶于乙醇 |
(2)反应过程中C2H5OH和HCl可能会生成副产物C2H5Cl,同时CCl3CHO(三氯乙醛)也能被次氯酸继续氧化生成CCl3COOH(三氯乙酸),写出三氯乙醛被次氯酸氧化生成三氯乙酸的化学方程式
(3)该设计流程中存在一处缺陷是
(4)反应结束后,有人提出先将C中的混合物冷却到室温,再用分液的方法分离出三氯乙酸。你认为此方案是否可行
(5)测定产品纯度:称取产品0.36g配成待测溶液,加入0.1000mol•L −1碘标准溶液 20.00mL,再加适量Na2CO3溶液,反应完全后加盐酸调溶液pH,立即用0.02000mol•L −1Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液20.00mL。则产品的纯度为
您最近一年使用:0次
2020-04-02更新
|
1157次组卷
|
7卷引用:四川省绵阳南山中学2020届高三上学期一诊热身考试理科综合化学试题
名校
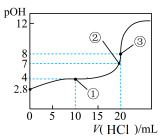
6 . 在25℃时,向50.00mL未知浓度的氨水中逐滴加入0.5mol·L-1的HCl溶液。滴定过程中,溶液的pOH[pOH=-lgc(OH-)]与滴入HCl溶液体积的关系如图所示,则下列说法中正确的是
| A.图中②点所示溶液的导电能力弱于①点 |
| B.③点处水电离出的c(H+)=1×10-8mol·L-1 |
| C.图中点①所示溶液中,c(C1-)>c(NH4+)>c(OH-)>c(H+) |
| D.25℃时氨水的Kb约为5×10-5.6mol·L-1 |
您最近一年使用:0次
2019-05-24更新
|
3118次组卷
|
13卷引用:四川省绵阳中学2023-2024学年高二下学期开学化学试题
四川省绵阳中学2023-2024学年高二下学期开学化学试题【市级联考】山东省烟台市、菏泽市2019届高三下学期5月高考适应性练习(一)理科综合化学试题四川省泸县第五中学2020届高三上学期开学考试理综化学试题备考突破2020高三化学专题强化集训——盐类水解中三大守恒的应用安徽省定远县重点中学2020届高三下学期3月线上模拟考试理科综合化学试题湖南省长沙市湖南师范大学附属中学2022-2023学年高二上学期期末考试化学试题 湖南师范大学附属中学2022-2023学年高二上学期期末考试化学试题山西省实验中学2023-2024学年高二上学期期中考试化学试题黑龙江省齐齐哈尔市2023-2024学年高二上学期1月期末化学试题江西省宜春市上高中学2023-2024学年高二上学期第二次月考化学试卷 黑龙江省双鸭山市第一中学2023-2024学年高二下学期开学化学试题2024年江西省宜春市第一中学高三下学期第三次模拟考试化学试卷四川省达州外国语学校2023-2024学年高二下学期3月月考化学试题
名校
7 . 氮及其化合物在生活及工业生产中有着重要应用。请回答以下问题:
(1)如图是N2(g)、H2(g)与NH3(g)之间转化的能量关系图,则:
①N2(g)与H2(g)反应生成NH3(g)的热化学方程式为___________________ .
②过程(Ⅰ)和过程(Ⅱ)的反应热________ (填“相同”或“不同”).
③某温度下,在1 L恒温恒容容器中充入1molN2和3 mol H2进行上述反应,10 min达到平衡,此时容器内压强变为原来的7/8.
a.该过程的平衡常数的表达式为____________ .
b.N2的平衡转化率为________ .
c.此时若保持容器温度和体积不变,向其中再加入2.25 molN2和0.5 mol NH3,则平衡________ (填“正向”“逆向”或“不”)移动.
(2)用NH3可以消除氮氧化物的污染,已知:
反应Ⅰ:4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH1=a kJ·mol-1 平衡常数为K1
2N2(g)+6H2O(g) ΔH1=a kJ·mol-1 平衡常数为K1
反应Ⅱ:N2(g)+O2(g) 2NO(g) ΔH2=b kJ·mol-1 平衡常数为K2
2NO(g) ΔH2=b kJ·mol-1 平衡常数为K2
反应Ⅲ:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) ΔH3=c kJ·mol-1 平衡常数为K3
5N2(g)+6H2O(g) ΔH3=c kJ·mol-1 平衡常数为K3
则反应Ⅱ中的b=_____ (用含a、c的代数式表示),K3=_____ (用K1和K2表示).反应Ⅲ中的ΔS______ (填“>”“<”或“=”)0.
(3)在恒容的密闭器中,充入一定量的NH3和NO进行上述反应Ⅲ,测得不同温度下反应体系中NH3的转化率(α)与压强p的关系如图所示:
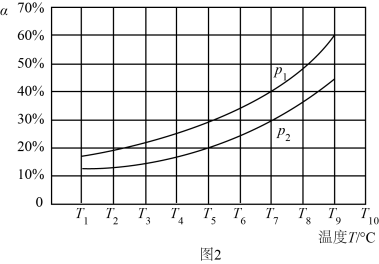
①分析得p1________ p2.(填“>”“<”或“=”)
②下列叙述中,不能作为判断反应Ⅲ已经达到平衡状态的标志的是________ (填序号).
a.N2的浓度不再改变 b.断裂6 mol N—H键的同时,有6 mol H—O键形成
c.容器中压强不再变化 d.混合气体的密度保持不变
(1)如图是N2(g)、H2(g)与NH3(g)之间转化的能量关系图,则:
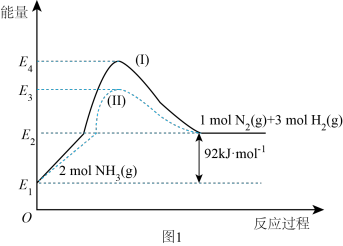
①N2(g)与H2(g)反应生成NH3(g)的热化学方程式为
②过程(Ⅰ)和过程(Ⅱ)的反应热
③某温度下,在1 L恒温恒容容器中充入1molN2和3 mol H2进行上述反应,10 min达到平衡,此时容器内压强变为原来的7/8.
a.该过程的平衡常数的表达式为
b.N2的平衡转化率为
c.此时若保持容器温度和体积不变,向其中再加入2.25 molN2和0.5 mol NH3,则平衡
(2)用NH3可以消除氮氧化物的污染,已知:
反应Ⅰ:4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) ΔH1=a kJ·mol-1 平衡常数为K1
2N2(g)+6H2O(g) ΔH1=a kJ·mol-1 平衡常数为K1反应Ⅱ:N2(g)+O2(g)
 2NO(g) ΔH2=b kJ·mol-1 平衡常数为K2
2NO(g) ΔH2=b kJ·mol-1 平衡常数为K2反应Ⅲ:4NH3(g)+6NO(g)
 5N2(g)+6H2O(g) ΔH3=c kJ·mol-1 平衡常数为K3
5N2(g)+6H2O(g) ΔH3=c kJ·mol-1 平衡常数为K3则反应Ⅱ中的b=
(3)在恒容的密闭器中,充入一定量的NH3和NO进行上述反应Ⅲ,测得不同温度下反应体系中NH3的转化率(α)与压强p的关系如图所示:

①分析得p1
②下列叙述中,不能作为判断反应Ⅲ已经达到平衡状态的标志的是
a.N2的浓度不再改变 b.断裂6 mol N—H键的同时,有6 mol H—O键形成
c.容器中压强不再变化 d.混合气体的密度保持不变
您最近一年使用:0次
2019-04-28更新
|
1186次组卷
|
7卷引用:四川省三台中学实验学校2019-2020学年高二上学期12月月考化学试题
8 . 某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反 应,因此实验小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去)。
已知:常温下,CO能使一些化合物中的金属离子还原。例如:PdCl2 + CO + H2O === Pd↓+ CO2 +2HCl ,反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。
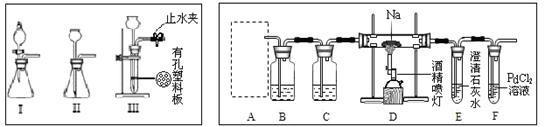
请回答下列问题:
(1)为了制取CO2气体的装置能“随开随用,随关随停”,上图A处应选用的装置是________ (填写 “I”、 “II”或“III”)。若要制取干燥、纯净的CO2气体,装置B中应盛放的试剂是__________ 溶液,装置C中应盛放的试剂是___________ 。
(2)观察实验装置图可知Na与CO2反应的条件是_____________ ,检查装置的气密性完好并装入药品后,在点燃酒精喷灯前,必须进行的操作是________________ 。待装置_______ (填写字母)中出现_________ 现象时,再点燃酒精喷灯,这步操作的目的是______________ 。
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:
① 若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是____________________________ 。
② 若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是________________ 。
(4)请判断②中D装置生成固体的成分是钠的正盐还是酸式盐?请用文字简要说明理由________________ 。
已知:常温下,CO能使一些化合物中的金属离子还原。例如:PdCl2 + CO + H2O === Pd↓+ CO2 +2HCl ,反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。

请回答下列问题:
(1)为了制取CO2气体的装置能“随开随用,随关随停”,上图A处应选用的装置是
(2)观察实验装置图可知Na与CO2反应的条件是
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:
① 若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是
② 若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是
(4)请判断②中D装置生成固体的成分是钠的正盐还是酸式盐?请用文字简要说明理由
您最近一年使用:0次
名校
9 . 铬是人体必需元素,如含量不足会影响糖类和脂类的代谢,过高则会引起急性中毒。工业上往往采取下列循环工艺防止铬的污染:
完成下列填空:
(1)溶液配制:称取一定量纯净的K2Cr2O7晶体配制100ml标准溶液,用蒸馏水完全溶解后,全部转移至_____ 中,加蒸馏水离刻度线1---2厘米处,改用__________ 加水至刻度线。
(2)含Cr2O72-离子的废水在酸性条件下用Fe3O4处理,反应的离子方程式如下,配平该离子反应方程式:
___ Cr2O72-+___ Fe3O4 +__ H+ →__ Cr3+ +__ Fe3+ +__ H2O
(3)工业上处理含Cr2O72-的废水时,一般将剧毒的Cr2O72-转化为Cr3+,以碳为阴极,铁作阳极,电解处理含NaCl、Cr2O72-的酸性废水。写出电极反应:阳极___________ ,阴极_______________________ ;用铁做阳极的目的是:_____________________ 。
(4)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式:____________ 。
(5)向上述反应后的溶液中加入碱溶液,让废水的pH升至8~10,控制适当的温度,使产物中的金属阳离子全部转变为沉淀。回收所得的Cr(OH)3,经处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:① Cr2O72- +6I- + 14H+ →3I2 + 2Cr3+ + 7H2O ② 2S2O32- + I2→S4O62- + 2I- ,准确称取纯净的K2Cr2O7 0.294g ,配成溶液,加足量KI,用Na2S2O3溶液滴定,消耗Na2S2O3溶液25.00mL。则Na2S2O3溶液的物质的量浓度为_____________________ (保留四位有效数字)。
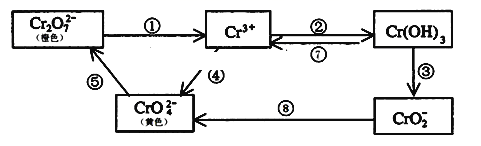
完成下列填空:
(1)溶液配制:称取一定量纯净的K2Cr2O7晶体配制100ml标准溶液,用蒸馏水完全溶解后,全部转移至
(2)含Cr2O72-离子的废水在酸性条件下用Fe3O4处理,反应的离子方程式如下,配平该离子反应方程式:
(3)工业上处理含Cr2O72-的废水时,一般将剧毒的Cr2O72-转化为Cr3+,以碳为阴极,铁作阳极,电解处理含NaCl、Cr2O72-的酸性废水。写出电极反应:阳极
(4)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式:
(5)向上述反应后的溶液中加入碱溶液,让废水的pH升至8~10,控制适当的温度,使产物中的金属阳离子全部转变为沉淀。回收所得的Cr(OH)3,经处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:① Cr2O72- +6I- + 14H+ →3I2 + 2Cr3+ + 7H2O ② 2S2O32- + I2→S4O62- + 2I- ,准确称取纯净的K2Cr2O7 0.294g ,配成溶液,加足量KI,用Na2S2O3溶液滴定,消耗Na2S2O3溶液25.00mL。则Na2S2O3溶液的物质的量浓度为
您最近一年使用:0次
2017-11-02更新
|
640次组卷
|
3卷引用:四川省绵阳市2018届高三一诊模拟(四)化学试题
解题方法
10 . PHB树脂可被微生物降解,对环境友好,有机物F是医药合成中间体。它们的合成路线如下:
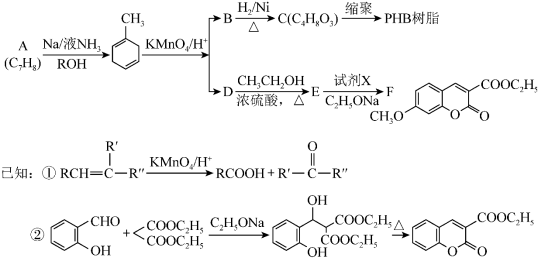
请回答下列问题:
(1)A分子中碳原子的杂化轨道类型是___________ ,化合物B的官能团名称是___________ 。
(2)D→E的化学方程式为______________________________ 。
(3)B→C的反应类型是____________ ,试剂X的结构简式是_____________ 。
(4)由化合物C合成PHB树脂的化学方程式是___________________________ 。
(5)写出满足下列条件的E的所有同分异构体的结构简式:________________ 。
a.核磁共振氢谱有2组峰;
b.不与Na2CO3溶液反应,能发生水解反应生成二元羧酸。

请回答下列问题:
(1)A分子中碳原子的杂化轨道类型是
(2)D→E的化学方程式为
(3)B→C的反应类型是
(4)由化合物C合成PHB树脂的化学方程式是
(5)写出满足下列条件的E的所有同分异构体的结构简式:
a.核磁共振氢谱有2组峰;
b.不与Na2CO3溶液反应,能发生水解反应生成二元羧酸。
您最近一年使用:0次



