名校
1 . 使用铜基催化剂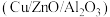 ,以
,以 和
和 合成
合成 是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:
是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:
(1) 的
的 模型名称是
模型名称是___________ , 分子中O的杂化轨道类型是
分子中O的杂化轨道类型是___________ 。
(2)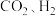 和
和 中,属于极性分子的是
中,属于极性分子的是___________ ,由非极性键结合成的非极性分子是___________ 。
(3) 的沸点
的沸点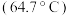 介于
介于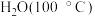 和
和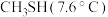 之间,其原因是
之间,其原因是___________ 。
(4) 属于
属于___________ 晶体, 属于
属于___________ 晶体。
(5) 的一种立方晶胞结构如图所示,每个
的一种立方晶胞结构如图所示,每个 周围与它最近且相等距离的
周围与它最近且相等距离的 有
有___________ 个。若该立方晶胞参数为 ,则正负离子的核间距最小为
,则正负离子的核间距最小为___________  ,晶体密度
,晶体密度
___________  (列出算式,阿伏加德罗常数的值为
(列出算式,阿伏加德罗常数的值为 )。
)。
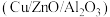 ,以
,以 和
和 合成
合成 是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:
是大规模实现低碳减排和清洁能源再生产的有效路径。回答下列问题:(1)
 的
的 模型名称是
模型名称是 分子中O的杂化轨道类型是
分子中O的杂化轨道类型是(2)
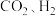 和
和 中,属于极性分子的是
中,属于极性分子的是(3)
 的沸点
的沸点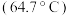 介于
介于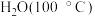 和
和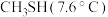 之间,其原因是
之间,其原因是(4)
 属于
属于 属于
属于(5)
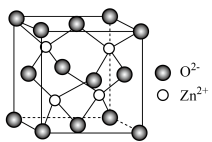
 的一种立方晶胞结构如图所示,每个
的一种立方晶胞结构如图所示,每个 周围与它最近且相等距离的
周围与它最近且相等距离的 有
有 ,则正负离子的核间距最小为
,则正负离子的核间距最小为 ,晶体密度
,晶体密度
 (列出算式,阿伏加德罗常数的值为
(列出算式,阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次
2 . 已知 可形成配离子
可形成配离子 、
、 、
、 。在试管中进行下列实验:
。在试管中进行下列实验:
 可形成配离子
可形成配离子 、
、 、
、 。在试管中进行下列实验:
。在试管中进行下列实验:
A.上述三种配离子中 的配位数不完全相同 的配位数不完全相同 |
B. 和 和 中配位原子均为N 中配位原子均为N |
C.溶度积常数: |
D.稳定性: |
您最近一年使用:0次
名校
3 . 家庭药箱常备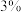 的过氧化氢消毒液。过氧化氢的分子结构如下图所示,两个氢原子犹如分布在半展开的书的两面上。下列关于
的过氧化氢消毒液。过氧化氢的分子结构如下图所示,两个氢原子犹如分布在半展开的书的两面上。下列关于 的说法中正确的是
的说法中正确的是
 的过氧化氢消毒液。过氧化氢的分子结构如下图所示,两个氢原子犹如分布在半展开的书的两面上。下列关于
的过氧化氢消毒液。过氧化氢的分子结构如下图所示,两个氢原子犹如分布在半展开的书的两面上。下列关于 的说法中正确的是
的说法中正确的是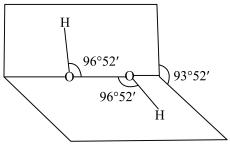
| A.分子中既有极性键又有非极性键 | B.属于非极性分子,易溶于 |
C.两个氧原子均采用 杂化 杂化 | D.分子中既有 键又有 键又有 键 键 |
您最近一年使用:0次
名校
4 . 某有机物的红外光谱如下图,该有机物可能是

A. | B. | C. | D.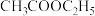 |
您最近一年使用:0次
名校
5 . 无水硫酸铜呈白色,溶于水得蓝色溶液,溶于氨水得深蓝色溶液,这是因为分别形成了 和
和 。某化学实验小组为了探究两种配离子的性质差异,进行如下实验:
。某化学实验小组为了探究两种配离子的性质差异,进行如下实验:
I.向盛有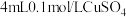 溶液的试管里滴加5滴
溶液的试管里滴加5滴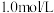 氨水,形成难溶物,继续添加氨水
氨水,形成难溶物,继续添加氨水 ,沉淀溶解并形成深蓝色溶液。
,沉淀溶解并形成深蓝色溶液。
II.向所得深蓝色溶液中加入无水乙醇,有深蓝色晶体析出,将深蓝色晶体过滤、洗涤,取深蓝色晶体溶于水配成溶液a。
III.取一药匙氢氧化铜固体于试管中,加入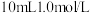 氨水,溶液略变为深蓝色,但沉淀并未见明显溶解。再加入2滴饱和
氨水,溶液略变为深蓝色,但沉淀并未见明显溶解。再加入2滴饱和 溶液,沉淀完全溶解。
溶液,沉淀完全溶解。
IV.取硫酸铜溶液、溶液a分别置于两试管中,向其中各加一枚铁钉,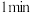 后观察现象,前者铁钉表面有红色固体析出,后者铁钉无现象。
后观察现象,前者铁钉表面有红色固体析出,后者铁钉无现象。
回答下列问题:
(1)实验I生成难溶物时,反应的离子方程式是___________ ,所得溶液呈深蓝色的原因是溶液中存在___________ 。
(2)实验II深蓝色溶液中析出晶体的原因是___________ 。该深蓝色晶体的化学式为 ,受热时首先失去的组分是
,受热时首先失去的组分是 ,则
,则 与
与 之间以
之间以___________ 结合,晶体中配体与 以
以___________ 结合。
(3)实验沉淀溶解反应的化学方程式是___________ 。加入2滴饱和 溶液为什么能促进沉淀溶解?
溶液为什么能促进沉淀溶解?___________ 。
(4)从实验IV可以得出的结论是___________ 。
 和
和 。某化学实验小组为了探究两种配离子的性质差异,进行如下实验:
。某化学实验小组为了探究两种配离子的性质差异,进行如下实验:I.向盛有
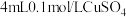 溶液的试管里滴加5滴
溶液的试管里滴加5滴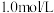 氨水,形成难溶物,继续添加氨水
氨水,形成难溶物,继续添加氨水 ,沉淀溶解并形成深蓝色溶液。
,沉淀溶解并形成深蓝色溶液。II.向所得深蓝色溶液中加入无水乙醇,有深蓝色晶体析出,将深蓝色晶体过滤、洗涤,取深蓝色晶体溶于水配成溶液a。
III.取一药匙氢氧化铜固体于试管中,加入
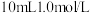 氨水,溶液略变为深蓝色,但沉淀并未见明显溶解。再加入2滴饱和
氨水,溶液略变为深蓝色,但沉淀并未见明显溶解。再加入2滴饱和 溶液,沉淀完全溶解。
溶液,沉淀完全溶解。IV.取硫酸铜溶液、溶液a分别置于两试管中,向其中各加一枚铁钉,
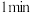 后观察现象,前者铁钉表面有红色固体析出,后者铁钉无现象。
后观察现象,前者铁钉表面有红色固体析出,后者铁钉无现象。回答下列问题:
(1)实验I生成难溶物时,反应的离子方程式是
(2)实验II深蓝色溶液中析出晶体的原因是
 ,受热时首先失去的组分是
,受热时首先失去的组分是 ,则
,则 与
与 之间以
之间以 以
以(3)实验沉淀溶解反应的化学方程式是
 溶液为什么能促进沉淀溶解?
溶液为什么能促进沉淀溶解?(4)从实验IV可以得出的结论是
您最近一年使用:0次
名校
解题方法
6 . W、X、Y、Z为元素周期表中的前四周期元素,原子的最外层电子数之和为12。W与X同周期相邻,X的基态原子价层电子排布为 ;Y与Z同周期,
;Y与Z同周期,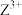 的
的 轨道半充满;四种元素可形成化合物
轨道半充满;四种元素可形成化合物 。回答下列问题:
。回答下列问题:
(1)W的三种单质分别是共价晶体、分子晶体、混合型晶体,则三种单质分别是___________ 、___________ 、___________ 。
(2)单质 化学性质很稳定,其原因是
化学性质很稳定,其原因是___________ 。 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为___________ 。
(3)阴离子 的结构如图所示,五个X原子位于同一平面,则X原子均采用
的结构如图所示,五个X原子位于同一平面,则X原子均采用___________ 杂化,每个X原子未参与杂化的___________ 轨道垂直于五元环平面,相互平行重叠形成大 键,
键, 中的
中的 键总数为
键总数为___________ 个,形成大 键的电子共有
键的电子共有___________ 个。 的化学式为
的化学式为___________ ,它在水中可以电离出配离子 。该配离子的中心离子是
。该配离子的中心离子是___________ ,配位数是___________ 。
(5) 有剧毒,但
有剧毒,但 却允许用作食盐的抗结剂,其最大使用量为
却允许用作食盐的抗结剂,其最大使用量为 (以配离子计),原因是
(以配离子计),原因是___________ 。
 ;Y与Z同周期,
;Y与Z同周期,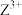 的
的 轨道半充满;四种元素可形成化合物
轨道半充满;四种元素可形成化合物 。回答下列问题:
。回答下列问题:(1)W的三种单质分别是共价晶体、分子晶体、混合型晶体,则三种单质分别是
(2)单质
 化学性质很稳定,其原因是
化学性质很稳定,其原因是 分子中
分子中 键与
键与 键的数目之比为
键的数目之比为(3)阴离子
 的结构如图所示,五个X原子位于同一平面,则X原子均采用
的结构如图所示,五个X原子位于同一平面,则X原子均采用 键,
键, 中的
中的 键总数为
键总数为 键的电子共有
键的电子共有
 的化学式为
的化学式为 。该配离子的中心离子是
。该配离子的中心离子是(5)
 有剧毒,但
有剧毒,但 却允许用作食盐的抗结剂,其最大使用量为
却允许用作食盐的抗结剂,其最大使用量为 (以配离子计),原因是
(以配离子计),原因是
您最近一年使用:0次
名校
解题方法
7 . 下列有关物质结构和性质的说法错误的是
| A.有机物分子中手性碳所连4个原子一定不同 |
| B.互为手性异构体的两种药物,其药效差异可能很大 |
| C.邻羟基苯甲酸的沸点低于对羟基苯甲酸是因为二者形成的氢键不同 |
D.“杯酚”与 通过分子间作用力形成超分子可实现“分子识别” 通过分子间作用力形成超分子可实现“分子识别” |
您最近一年使用:0次
名校
解题方法
8 . 根据下列证据,所得推理错误的是
| 选项 | 证据 | 推理 |
| A | 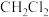 不存在同分异构体 不存在同分异构体 | 碳的4个价键指向四面体的顶点 |
| B | 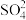 的键长、键角均相等 的键长、键角均相等 |  的空间结构为正四面体,S采用 的空间结构为正四面体,S采用 杂化 杂化 |
| C |  在水中的溶解度比 在水中的溶解度比 大得多 大得多 |  是极性分子, 是极性分子, 是非极性分子 是非极性分子 |
| D |  的键角为 的键角为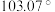 |  为极性分子,O采用 为极性分子,O采用 杂化 杂化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 关于化学键与晶体的下列说法正确的是
| A.金属原子与非金属原子之间一定形成离子键 |
| B.两个非金属原子之间形成的化学键一定是共价键 |
| C.晶体中有阳离子就一定有阴离子 |
| D.碳的同素异形体都是共价晶体 |
您最近一年使用:0次
名校
解题方法
10 . 下列四种羧酸:① 、②
、② 、③
、③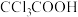 、④
、④ ,酸性由强到弱的顺序是
,酸性由强到弱的顺序是
 、②
、② 、③
、③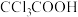 、④
、④ ,酸性由强到弱的顺序是
,酸性由强到弱的顺序是| A.①②③④ | B.②①③④ | C.④③①② | D.④③②① |
您最近一年使用:0次



