名校
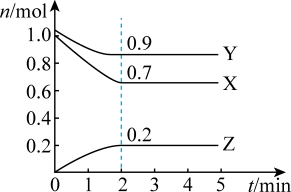
1 . 某温度时,在一个2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。
(1)该反应的化学方程式为___________ 。
(2)反应开始至2min,以气体Z表示的平均反应速率为___________ 。1min时,正反应速率___________ (填“>”“<”或“=”)逆反应速率。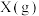 的平衡转化率为
的平衡转化率为___________ 。
(3)恒温恒容条件下,能说明该反应达到化学平衡状态的标志是___________。
①混合气体的压强不再变化
②混合气体的密度不再变化
③X的百分含量不再变化
④混合气体的平均相对分子质量不再变化
⑤v(X):v(Y)=3:1
(4)反应开始至2min末,以气体X表示的平均反应速率为___________ ;反应开始时与反应达平衡状态时的压强之比为___________ 。
(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
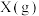 的平衡转化率为
的平衡转化率为(3)恒温恒容条件下,能说明该反应达到化学平衡状态的标志是___________。
①混合气体的压强不再变化
②混合气体的密度不再变化
③X的百分含量不再变化
④混合气体的平均相对分子质量不再变化
⑤v(X):v(Y)=3:1
| A.①②⑤ | B.①③④ | C.②③④ | D.③④⑤ |
(4)反应开始至2min末,以气体X表示的平均反应速率为
您最近一年使用:0次
名校
2 . 利用图所示装置进行铜与硝酸反应的实验。 ___________ 。
(2)使用稀硝酸进行实验:反应开始后,铜丝逐渐变细,有气泡产生,溶液变蓝。
① 铜与稀硝酸反应的离子方程式为___________ 。
② 实验中观察到试管中的气体略有红棕色,其原因是___________ (用化学方程式表示)。
(3)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。 铜与浓硝酸反应的化学方程式为___________ 。

(2)使用稀硝酸进行实验:反应开始后,铜丝逐渐变细,有气泡产生,溶液变蓝。
① 铜与稀硝酸反应的离子方程式为
② 实验中观察到试管中的气体略有红棕色,其原因是
(3)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。 铜与浓硝酸反应的化学方程式为
您最近一年使用:0次
名校
3 . 乙醇和乙酸都是烃的衍生物,其分子中的官能团分别是___________ 与___________ 。乙醇可以发生___________ 反应生成乙醛,乙醛的官能团是___________ 。乙醇和乙酸生成乙酸乙酯的反应方程式为___________ ,乙酸乙酯的官能团是___________ 。
您最近一年使用:0次
4 . 在氮的单质和常见的含氮化合物中:
(1)常用作保护气(如填充灯泡、焊接保护等)的物质是___________ (填名称),原因是___________ 。
(2)常用作制冷剂的物质是___________ (填名称),原因是 ___________ 。
(3)能与酸反应生成盐,在常温下为气态的物质是___________ (填名称);它与盐酸反应的离子方程式是___________ 。
(1)常用作保护气(如填充灯泡、焊接保护等)的物质是
(2)常用作制冷剂的物质是
(3)能与酸反应生成盐,在常温下为气态的物质是
您最近一年使用:0次
名校
5 . 下列气体的主要成分不是甲烷的是
| A.沼气 | B.天然气 | C.煤气 | D.煤层气 |
您最近一年使用:0次
名校
解题方法
6 . 一定条件下,石墨转化为金刚石要吸收能量。在该条件下,下列结论正确的是
| A.金刚石比石墨稳定 |
| B.等质量的金刚石和石墨完全燃烧释放的热量相同 |
| C.金刚石转化为石墨是吸热反应 |
| D.1molC(金刚石)比1molC(石墨)的总能量高 |
您最近一年使用:0次
2024-05-02更新
|
433次组卷
|
2卷引用:四川省甘孜藏族自治州某重点中学2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
7 . 只用一种试剂,将NH4Cl、 、Na2SO4、NaCl 4种物质的溶液区分开,这种试剂是
、Na2SO4、NaCl 4种物质的溶液区分开,这种试剂是
 、Na2SO4、NaCl 4种物质的溶液区分开,这种试剂是
、Na2SO4、NaCl 4种物质的溶液区分开,这种试剂是| A.NaOH溶液 | B.AgNO3溶液 | C.BaCl2溶液 | D. 溶液 溶液 |
您最近一年使用:0次
2024-04-05更新
|
200次组卷
|
5卷引用:四川省甘孜藏族自治州某重点中学2023-2024学年高一下学期4月期中考试化学试题
解题方法
8 . 已知A、B、C、D、E、F为短周期元素,其中C的原子序数最小,它们的最高正价与原子半径关系如图所示。
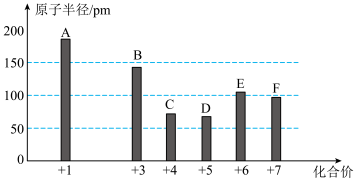
请回答下列问题:
(1)B元素在周期表中的位置为__________ ;D元素能与氢元素组成18电子分子,该分子含有的共价键类型为__________ (填“极性键”或“非极性键”)。
(2)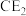 属于严禁携带的易燃易爆液体,其电子式为
属于严禁携带的易燃易爆液体,其电子式为__________ ;A、E、F三种元素形成的简单离子,半径由大到小的顺序是__________ (用离子符号表示)。
(3)写出元素A、B的最高价氧化物的水化物相互反应的离子方程式__________ 。
(4)用C元素的最简单氢化物和 在碱性条件下可以组成燃料电池,电极材料为多孔惰性金属电极;则通入C元素最简单氢化物的一极是该电池的
在碱性条件下可以组成燃料电池,电极材料为多孔惰性金属电极;则通入C元素最简单氢化物的一极是该电池的__________ 极,若线路中转移2mol电子,则消耗的 在标准状况下的体积为
在标准状况下的体积为__________ 。
(5)化合物 在农业上可用作杀虫剂,以及在工业上可用于处理废水中的重金属离子。向
在农业上可用作杀虫剂,以及在工业上可用于处理废水中的重金属离子。向 溶液中滴加酸性
溶液中滴加酸性 溶液,观察到溶液紫色褪去,并有无色无味气体产生,写出该反应的离子方程式
溶液,观察到溶液紫色褪去,并有无色无味气体产生,写出该反应的离子方程式__________ 。

请回答下列问题:
(1)B元素在周期表中的位置为
(2)
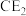 属于严禁携带的易燃易爆液体,其电子式为
属于严禁携带的易燃易爆液体,其电子式为(3)写出元素A、B的最高价氧化物的水化物相互反应的离子方程式
(4)用C元素的最简单氢化物和
 在碱性条件下可以组成燃料电池,电极材料为多孔惰性金属电极;则通入C元素最简单氢化物的一极是该电池的
在碱性条件下可以组成燃料电池,电极材料为多孔惰性金属电极;则通入C元素最简单氢化物的一极是该电池的 在标准状况下的体积为
在标准状况下的体积为(5)化合物
 在农业上可用作杀虫剂,以及在工业上可用于处理废水中的重金属离子。向
在农业上可用作杀虫剂,以及在工业上可用于处理废水中的重金属离子。向 溶液中滴加酸性
溶液中滴加酸性 溶液,观察到溶液紫色褪去,并有无色无味气体产生,写出该反应的离子方程式
溶液,观察到溶液紫色褪去,并有无色无味气体产生,写出该反应的离子方程式
您最近一年使用:0次
9 . 七叶亭是一种适用于抗细菌性痢疾的药物,其结构如图,下列说法正确的是
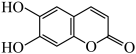

A.分子式为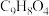 | B.分子中存在2种官能团 |
| C.该物质苯环上的一氯代物有2种 | D.1mol该物质与 发生加成反应,最多可消耗 发生加成反应,最多可消耗 |
您最近一年使用:0次
解题方法
10 . Ⅰ.铁是目前产量最大,使用最广泛的金属。我国目前发现最早的人工冶铁制品是河南三门峡出土的西周晚期的玉柄铁剑。
(1)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,请用化学方程式解释__________ 。
(2)电子工业中常用 溶液作为“腐蚀液”腐蚀电路铜板。为了检验反应后所得混合溶液中还有
溶液作为“腐蚀液”腐蚀电路铜板。为了检验反应后所得混合溶液中还有 ,可选择下列试剂中的
,可选择下列试剂中的__________ (填编号)进行检验,现象是__________ 。
A.KSCN溶液 B.酸性 溶液 C.新制氯水
溶液 C.新制氯水
Ⅱ.一种用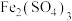 溶液浸取黄铁矿(主要含
溶液浸取黄铁矿(主要含 和少量难溶杂质)的流程如图所示。
和少量难溶杂质)的流程如图所示。

(3) 晶体中阴阳离子个数比为
晶体中阴阳离子个数比为__________ 。
(4)“浸取”的过程中,加快浸取的速率的方法有__________ (写出两项),发生的离子方程式为__________ 。
(5)“操作”如果在实验室里进行,用到的玻璃仪器为__________ 。
(6)从“溶液X”中提取绿矾晶体的操作为:加入Fe粉后,应先浓缩滤液至__________ ,趁热过滤,取滤液,__________ ,过滤、洗涤、干燥。
(1)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前,模具必须进行充分的干燥处理,请用化学方程式解释
(2)电子工业中常用
 溶液作为“腐蚀液”腐蚀电路铜板。为了检验反应后所得混合溶液中还有
溶液作为“腐蚀液”腐蚀电路铜板。为了检验反应后所得混合溶液中还有 ,可选择下列试剂中的
,可选择下列试剂中的A.KSCN溶液 B.酸性
 溶液 C.新制氯水
溶液 C.新制氯水Ⅱ.一种用
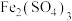 溶液浸取黄铁矿(主要含
溶液浸取黄铁矿(主要含 和少量难溶杂质)的流程如图所示。
和少量难溶杂质)的流程如图所示。
(3)
 晶体中阴阳离子个数比为
晶体中阴阳离子个数比为(4)“浸取”的过程中,加快浸取的速率的方法有
(5)“操作”如果在实验室里进行,用到的玻璃仪器为
(6)从“溶液X”中提取绿矾晶体的操作为:加入Fe粉后,应先浓缩滤液至
您最近一年使用:0次



