解题方法
1 . 副族元素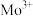 、
、 等元素较
等元素较 更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液
更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液_______ ;锰在周期表中的_______ 区。
(2)“超分子”中各元素(除H外)电负性由大到小的顺序为_______ 。
(3)副族元素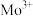 、
、 等元素比
等元素比 更易形成配合物,其原因是
更易形成配合物,其原因是_______ ; 与配体
与配体 形成共价键,提供孤电子对的原子是
形成共价键,提供孤电子对的原子是_______ (填元素符号),其中配体中C原子的杂化方式为_______ , 结合1个O和1个
结合1个O和1个 得到一种常见微粒,其空间构型为
得到一种常见微粒,其空间构型为_______ 。
(4)冠醚能够提升高锰酸钾氧化己烯的速率的原因是_______ 。
(5)氮化钼晶胞结构如图所示,N原子填充Mo围成的八面体空隙中,填充率为100%。_______ ;
② 的熔点
的熔点_______ (填“>”、“<”或“=”) ;
;
③若该八面体边长为 ,则晶胞的密度为
,则晶胞的密度为
_______  (
( 表示啊伏伽德罗常数)。
表示啊伏伽德罗常数)。
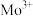 、
、 等元素较
等元素较 更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液
更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液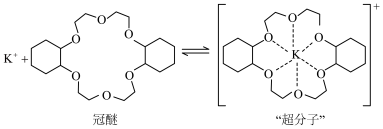
(2)“超分子”中各元素(除H外)电负性由大到小的顺序为
(3)副族元素
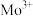 、
、 等元素比
等元素比 更易形成配合物,其原因是
更易形成配合物,其原因是 与配体
与配体 形成共价键,提供孤电子对的原子是
形成共价键,提供孤电子对的原子是 结合1个O和1个
结合1个O和1个 得到一种常见微粒,其空间构型为
得到一种常见微粒,其空间构型为(4)冠醚能够提升高锰酸钾氧化己烯的速率的原因是
(5)氮化钼晶胞结构如图所示,N原子填充Mo围成的八面体空隙中,填充率为100%。

②
 的熔点
的熔点 ;
;③若该八面体边长为
 ,则晶胞的密度为
,则晶胞的密度为
 (
( 表示啊伏伽德罗常数)。
表示啊伏伽德罗常数)。
您最近一年使用:0次
名校
2 . 25℃时,用NaOH溶液分别滴定HA(弱酸)、 、
、 三种溶液,pM[
三种溶液,pM[ ,M表示
,M表示 、
、 或
或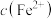 ]随pH变化关系如图所示。下列有关分析不正确的是
]随pH变化关系如图所示。下列有关分析不正确的是
已知:①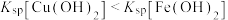 ;②溶液中离子浓度小于
;②溶液中离子浓度小于 可以认为已经除尽。
可以认为已经除尽。
 、
、 三种溶液,pM[
三种溶液,pM[ ,M表示
,M表示 、
、 或
或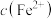 ]随pH变化关系如图所示。下列有关分析不正确的是
]随pH变化关系如图所示。下列有关分析不正确的是已知:①
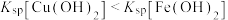 ;②溶液中离子浓度小于
;②溶液中离子浓度小于 可以认为已经除尽。
可以认为已经除尽。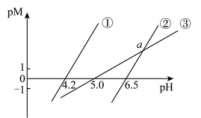
A.图中②代表滴定 溶液的变化关系 溶液的变化关系 |
B.25℃时,要除尽工业废水中的 ,需调整溶液的pH至少为6.7 ,需调整溶液的pH至少为6.7 |
| C.图中a点pH=7 |
D.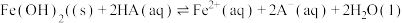 的平衡常数为 的平衡常数为 |
您最近一年使用:0次
名校
解题方法
3 . 化学是以实验为基础的学科。下列根据实验操作及现象能得到相应实验结论的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 常温下,将Fe片分别插入稀硝酸和浓硝酸中,一段时间后,前者有气体产生,后者无明显现象 | 稀硝酸的氧化性比浓硝酸的强 |
| B | 向某溶液中加入浓氢氧化钠溶液并加热,产生能使湿润的红色石蕊试纸变蓝的气体 | 该溶液含有 |
| C | 相同温度下,测定 溶液和 溶液和 溶液的pH,前者pH值更大 溶液的pH,前者pH值更大 | 酸性:   |
| D | 同温下,向体积为2mL 的 的 溶液中先滴加4滴 溶液中先滴加4滴 的KCl溶液,再滴加4滴 的KCl溶液,再滴加4滴 的KI溶液,先产生白色沉淀,再产生黄色沉淀 的KI溶液,先产生白色沉淀,再产生黄色沉淀 | 同温下    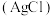 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
4 . X、Y、Z、M为原子序数依次增大的周期表前20号主族元素。X原子的最外层电子数是内层电子数的两倍,Z的原子序数等于X、Y原子序数之和,M为金属元素且与Y同主族。下列说法正确的是
| A.原子半径:Y<Z |
| B.最高价含氧酸酸性:X<Z |
| C.Y和M分别与氧元素形成化合物均只有两种 |
| D.M、X和氧三种元素形成的盐只有一种 |
您最近一年使用:0次
名校
解题方法
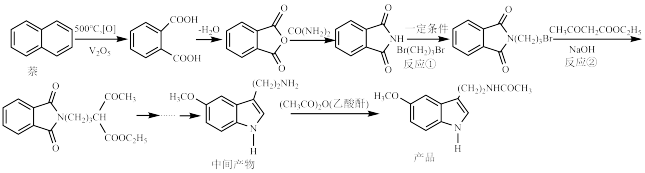
5 . 褪黑激素是一种神经系统激素,具有广泛的生理活性,有镇静镇痛的作用,一种以廉价易得的原料制备褪黑激素的合成路线如图所示:
(1)萘的一氯代物有___________ 种。
(2)1mol邻苯二甲酸与碳酸钠反应最多可产生___________ mol二氧化碳。
(3)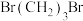 的官能团名称为
的官能团名称为___________ ,写出反应①的化学反应方程式___________ 。
(4)反应②属于___________ 反应(填有机反应类型),写出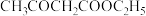 在NaOH水溶液中水解的化学反应方程式
在NaOH水溶液中水解的化学反应方程式___________ 。
(5)1mol中间产物H最多能与___________  发生加成反应,1个加成产物分子中有
发生加成反应,1个加成产物分子中有___________ 个手性碳原子。
(6)最后一步乙酰化反应可能会生成多种不同的乙酰化副产物,写出其中两种副产物的结构简式___________ 。
(1)萘的一氯代物有
(2)1mol邻苯二甲酸与碳酸钠反应最多可产生
(3)
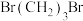 的官能团名称为
的官能团名称为(4)反应②属于
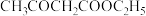 在NaOH水溶液中水解的化学反应方程式
在NaOH水溶液中水解的化学反应方程式(5)1mol中间产物H最多能与
 发生加成反应,1个加成产物分子中有
发生加成反应,1个加成产物分子中有(6)最后一步乙酰化反应可能会生成多种不同的乙酰化副产物,写出其中两种副产物的结构简式
您最近一年使用:0次
2024-05-17更新
|
194次组卷
|
2卷引用:2024届四川省仁寿第一中学校南校区二模理综化学试题
名校
解题方法
6 . 图1是一种居家天然气报警器成品装置,其工作原理如图2所示,其中 可以在固体电解质ZnO2—Na2O中移动。当空间内甲烷达到一定浓度时,传感器随之产生电信号并联动报警。当报警器触发工作时,下列说法不正确的是
可以在固体电解质ZnO2—Na2O中移动。当空间内甲烷达到一定浓度时,传感器随之产生电信号并联动报警。当报警器触发工作时,下列说法不正确的是
 可以在固体电解质ZnO2—Na2O中移动。当空间内甲烷达到一定浓度时,传感器随之产生电信号并联动报警。当报警器触发工作时,下列说法不正确的是
可以在固体电解质ZnO2—Na2O中移动。当空间内甲烷达到一定浓度时,传感器随之产生电信号并联动报警。当报警器触发工作时,下列说法不正确的是
| A.电极a的电势比电极b高 |
B. 在电解质中向电极a移动 在电解质中向电极a移动 |
C.电极a上发生的电极反应为: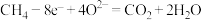 |
D.当电极a消耗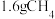 时,电路中有0.8mol电子转移 时,电路中有0.8mol电子转移 |
您最近一年使用:0次
名校
解题方法
7 . 硼元素有“金属材料的维生素”之称,其单质及其化合物的研究在无机化学的发展中占有独特的地位。请回答下列问题:
(1)基态硼原子的电子排布式为:___________ 。
(2)硼的化合物 中氢元素化合价为-1,故而被称为“万能还原剂”,广泛用于有机合成。
中氢元素化合价为-1,故而被称为“万能还原剂”,广泛用于有机合成。 中所含元素电负性由大到小的顺序为:
中所含元素电负性由大到小的顺序为:___________ 。
(3) 与
与 可以通过配位键形成
可以通过配位键形成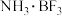 。
。
① 的空间构型为:
的空间构型为:___________ ,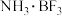 中硼原子的杂化方式为
中硼原子的杂化方式为___________ 。
② 的键角
的键角___________  的键角(填“大于”、“小于”或“等于”)。
的键角(填“大于”、“小于”或“等于”)。
(4)硼酸 晶体中单元结构如图1所示。各单元中的氧原子通过氢键连结成层状结构如图2所示,层与层之间以微弱的分子间力相结合构成整个硼酸晶体。
晶体中单元结构如图1所示。各单元中的氧原子通过氢键连结成层状结构如图2所示,层与层之间以微弱的分子间力相结合构成整个硼酸晶体。___________ 。
②1mol硼酸中含有氢键的数目为___________ 。
③ 在加热过程中会形成链状多硼酸根,其结构如图3所示。已知链状多硼酸根所有氧原子都达到8电子稳定结构,则含n个硼原子的多硼酸根可表示为
在加热过程中会形成链状多硼酸根,其结构如图3所示。已知链状多硼酸根所有氧原子都达到8电子稳定结构,则含n个硼原子的多硼酸根可表示为___________ 。
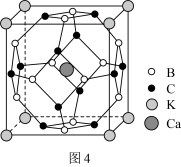
(5)科学家合成了一种含硼高温超导材料,其立方晶胞结构如图4所示。___________ 个面。
②已知晶胞边长为apm,阿伏加德罗常数为 ,则该晶体密度为
,则该晶体密度为___________  (用含
(用含 、a的式子表示,写出表达式即可)。
、a的式子表示,写出表达式即可)。
(1)基态硼原子的电子排布式为:
(2)硼的化合物
 中氢元素化合价为-1,故而被称为“万能还原剂”,广泛用于有机合成。
中氢元素化合价为-1,故而被称为“万能还原剂”,广泛用于有机合成。 中所含元素电负性由大到小的顺序为:
中所含元素电负性由大到小的顺序为:(3)
 与
与 可以通过配位键形成
可以通过配位键形成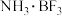 。
。①
 的空间构型为:
的空间构型为: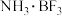 中硼原子的杂化方式为
中硼原子的杂化方式为②
 的键角
的键角 的键角(填“大于”、“小于”或“等于”)。
的键角(填“大于”、“小于”或“等于”)。(4)硼酸
 晶体中单元结构如图1所示。各单元中的氧原子通过氢键连结成层状结构如图2所示,层与层之间以微弱的分子间力相结合构成整个硼酸晶体。
晶体中单元结构如图1所示。各单元中的氧原子通过氢键连结成层状结构如图2所示,层与层之间以微弱的分子间力相结合构成整个硼酸晶体。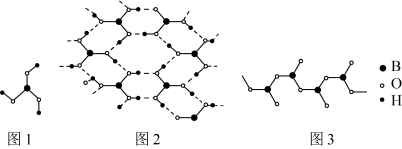
②1mol硼酸中含有氢键的数目为
③
 在加热过程中会形成链状多硼酸根,其结构如图3所示。已知链状多硼酸根所有氧原子都达到8电子稳定结构,则含n个硼原子的多硼酸根可表示为
在加热过程中会形成链状多硼酸根,其结构如图3所示。已知链状多硼酸根所有氧原子都达到8电子稳定结构,则含n个硼原子的多硼酸根可表示为(5)科学家合成了一种含硼高温超导材料,其立方晶胞结构如图4所示。
②已知晶胞边长为apm,阿伏加德罗常数为
 ,则该晶体密度为
,则该晶体密度为 (用含
(用含 、a的式子表示,写出表达式即可)。
、a的式子表示,写出表达式即可)。
您最近一年使用:0次
8 . 氮氧化物 进入同温层可对臭氧层造成破坏,对人类生活造成不利影响,目前工业上可采用多种方法对废气中的氮氧化物进行脱除,回答下列问题:
进入同温层可对臭氧层造成破坏,对人类生活造成不利影响,目前工业上可采用多种方法对废气中的氮氧化物进行脱除,回答下列问题:
(1)SCR法主要是针对柴油发动机产生的 的处理工艺,原理是
的处理工艺,原理是 和
和 在选择性催化剂表面转化为
在选择性催化剂表面转化为 和
和 ,反应历程中的能量变化如下图所示:
,反应历程中的能量变化如下图所示:___________ ,SCR法会产生高分散度的烟尘,会使催化剂的活性下降,原因是___________ 。
(2)甲烷脱硝:

①已知甲烷的燃烧热为890.3kJ/mol,
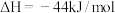 ,
,
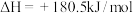 ,则甲烷脱硝反应的
,则甲烷脱硝反应的
___________ kJ/mol。
②800K时,为提高NO的平衡转化率,理论上可以采取的措施有:___________ 。
A.恒容时增加 B.恒压时通入一定量的Ar
B.恒压时通入一定量的Ar
C.移去部分 D.选择合适的催化剂
D.选择合适的催化剂
③一定温度下,将按一定比例混合的反应气匀速通过恒容催化反应器,测得NO去除率同 转化率随反应温度的变化关系如下图所示:
转化率随反应温度的变化关系如下图所示:___________ ;若反应气中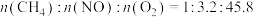 ,起始总压为66kPa,甲烷的平衡转化率为80%(若不考虑过程中存在的其他副反应),计算该温度下反应的分压平衡常数
,起始总压为66kPa,甲烷的平衡转化率为80%(若不考虑过程中存在的其他副反应),计算该温度下反应的分压平衡常数
___________ (以分压表示,分压=总压×物质的量分数,保留两位有效数字)。
(3)中国科学院研究人员报道了一种以铜锡合金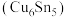 为催化剂,
为催化剂, 在电催化条件下还原NO高效合成氨的方法,并通过DFT计算研究了反应可能得机理如下(*表示催化剂表面吸附位,如
在电催化条件下还原NO高效合成氨的方法,并通过DFT计算研究了反应可能得机理如下(*表示催化剂表面吸附位,如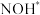 表示吸附于催化剂表面的NOH):
表示吸附于催化剂表面的NOH):
Ⅰ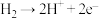 Ⅱ
Ⅱ 
Ⅲ Ⅳ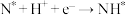
Ⅴ Ⅵ
Ⅵ 
上述反应机理中,第Ⅲ步的转化机理为___________ ;若电路中有4mol电子通过,其中生成 的选择性为95%,则阴极生成
的选择性为95%,则阴极生成 的物质的量为
的物质的量为___________ mol。
 进入同温层可对臭氧层造成破坏,对人类生活造成不利影响,目前工业上可采用多种方法对废气中的氮氧化物进行脱除,回答下列问题:
进入同温层可对臭氧层造成破坏,对人类生活造成不利影响,目前工业上可采用多种方法对废气中的氮氧化物进行脱除,回答下列问题:(1)SCR法主要是针对柴油发动机产生的
 的处理工艺,原理是
的处理工艺,原理是 和
和 在选择性催化剂表面转化为
在选择性催化剂表面转化为 和
和 ,反应历程中的能量变化如下图所示:
,反应历程中的能量变化如下图所示: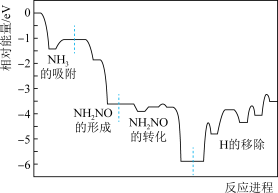
(2)甲烷脱硝:


①已知甲烷的燃烧热为890.3kJ/mol,

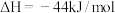 ,
,
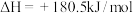 ,则甲烷脱硝反应的
,则甲烷脱硝反应的
②800K时,为提高NO的平衡转化率,理论上可以采取的措施有:
A.恒容时增加
 B.恒压时通入一定量的Ar
B.恒压时通入一定量的ArC.移去部分
 D.选择合适的催化剂
D.选择合适的催化剂③一定温度下,将按一定比例混合的反应气匀速通过恒容催化反应器,测得NO去除率同
 转化率随反应温度的变化关系如下图所示:
转化率随反应温度的变化关系如下图所示: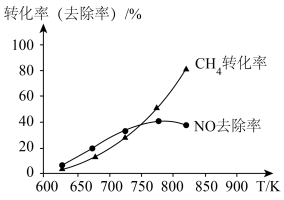
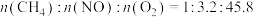 ,起始总压为66kPa,甲烷的平衡转化率为80%(若不考虑过程中存在的其他副反应),计算该温度下反应的分压平衡常数
,起始总压为66kPa,甲烷的平衡转化率为80%(若不考虑过程中存在的其他副反应),计算该温度下反应的分压平衡常数
(3)中国科学院研究人员报道了一种以铜锡合金
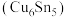 为催化剂,
为催化剂, 在电催化条件下还原NO高效合成氨的方法,并通过DFT计算研究了反应可能得机理如下(*表示催化剂表面吸附位,如
在电催化条件下还原NO高效合成氨的方法,并通过DFT计算研究了反应可能得机理如下(*表示催化剂表面吸附位,如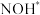 表示吸附于催化剂表面的NOH):
表示吸附于催化剂表面的NOH):Ⅰ
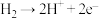 Ⅱ
Ⅱ 
Ⅲ Ⅳ
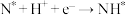
Ⅴ
 Ⅵ
Ⅵ 
上述反应机理中,第Ⅲ步的转化机理为
 的选择性为95%,则阴极生成
的选择性为95%,则阴极生成 的物质的量为
的物质的量为
您最近一年使用:0次
名校
解题方法
9 . 锂离子电池作为重要储能设备在手机、汽车等行业得到了大规模应用。一种基于微波辅助低共熔溶剂的回收方法可实现对废旧锂离子电池中 的回收利用,其主要工艺流程如下:
的回收利用,其主要工艺流程如下: 在溶液中常以
在溶液中常以 (蓝色)和
(蓝色)和 (粉红色)形式存在;
(粉红色)形式存在;
②25℃时,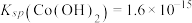 。
。
回答下列问题:
(1) 中Co的化合价为
中Co的化合价为___________ 。
(2)微波具有选择性加热和穿透性强的特点,采用微波共熔技术的优点除了可以减少杂质溶解还有___________ 。
(3)低共熔溶剂中含有一定量的草酸,其作用为___________ ;已知在水浸过程中溶液由蓝色变为粉红色,写出该变化的离子反应方程式___________ 。
(4)25℃时,沉钴反应完成后,溶液的pH=10,此时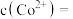
___________ mg/L。
(5)滤饼1在空气中煅烧得 ,写出该反应的化学反应方程式
,写出该反应的化学反应方程式___________ 。
(6)高温烧结过程中需通入空气,该反应中氧化剂与还原剂物质的量之比为___________ ,若通入空气过多过快,造成的不利影响是___________ 。
 的回收利用,其主要工艺流程如下:
的回收利用,其主要工艺流程如下: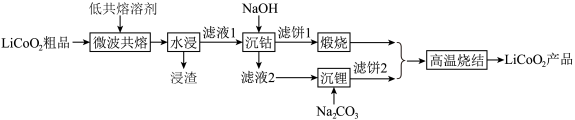
 在溶液中常以
在溶液中常以 (蓝色)和
(蓝色)和 (粉红色)形式存在;
(粉红色)形式存在;②25℃时,
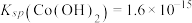 。
。回答下列问题:
(1)
 中Co的化合价为
中Co的化合价为(2)微波具有选择性加热和穿透性强的特点,采用微波共熔技术的优点除了可以减少杂质溶解还有
(3)低共熔溶剂中含有一定量的草酸,其作用为
(4)25℃时,沉钴反应完成后,溶液的pH=10,此时
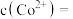
(5)滤饼1在空气中煅烧得
 ,写出该反应的化学反应方程式
,写出该反应的化学反应方程式(6)高温烧结过程中需通入空气,该反应中氧化剂与还原剂物质的量之比为
您最近一年使用:0次
10 . 葡萄糖酸锌(Zn(C6H11O7)2)是目前最常用的补锌剂,某实验小组的同学查阅资料后,用以下两种方法合成了葡萄糖酸锌。回答下列问题:
Ⅰ.直接合成法
将一定量的ZnSO4·7H2O完全溶于水,在90℃水浴条件下逐渐加入一定量的葡萄糖酸钙,20分钟后趁热抽滤,滤液转移至仪器A中浓缩至粘稠状,冷却后加入95%的乙醇并不断搅拌,待沉淀转变为晶体状后抽滤得产品。
(1)仪器A的名称为___________ 。
(2)写出直接合成法生成葡萄糖酸锌的化学反应方程式___________ 。
(3)趁热抽滤所得滤渣为___________ (写化学式),趁热抽滤的目的是___________ 。
(4)此法所得产品中易有较多的 ,原因是
,原因是___________ 。
Ⅱ.间接合成法
①制备葡萄糖酸:向蒸馏水中加入少量浓硫酸,搅拌下分批加入一定量的葡萄糖酸钙,抽滤除去沉淀,滤液经离子交换树脂纯化后得无色高纯度的葡萄糖酸溶液。
②制备葡萄糖酸锌:取上述高纯溶液,加入一定的ZnO,60℃水浴充分反应后除去不溶物,向滤液中加入无水乙醇后用冰水浴冷却,有白色晶体析出,重结晶得纯度较高的葡萄糖酸锌。
(5)制备葡萄糖酸时常得到淡黄色滤液,可加入一定量___________ 进行物理脱色。
(6)重结晶步骤的具体操作为:将粗产品以温水溶解后,加入___________ ,过滤、洗涤、___________ ,称重。
(7)产品中锌含量测定:准确称取0.400g葡萄糖酸锌溶于20mL温水中,加入10mL缓冲溶液,4滴指示剂,用c mol/LEDTA标准溶液滴定至终点,平行测定三次,消耗标准溶液的平均值为V mL,计算产品中锌的质量分数为___________ %(已知锌离子与EDTA按物质的量之比1∶1反应)。
Ⅰ.直接合成法
将一定量的ZnSO4·7H2O完全溶于水,在90℃水浴条件下逐渐加入一定量的葡萄糖酸钙,20分钟后趁热抽滤,滤液转移至仪器A中浓缩至粘稠状,冷却后加入95%的乙醇并不断搅拌,待沉淀转变为晶体状后抽滤得产品。
(1)仪器A的名称为
(2)写出直接合成法生成葡萄糖酸锌的化学反应方程式
(3)趁热抽滤所得滤渣为
(4)此法所得产品中易有较多的
 ,原因是
,原因是Ⅱ.间接合成法
①制备葡萄糖酸:向蒸馏水中加入少量浓硫酸,搅拌下分批加入一定量的葡萄糖酸钙,抽滤除去沉淀,滤液经离子交换树脂纯化后得无色高纯度的葡萄糖酸溶液。
②制备葡萄糖酸锌:取上述高纯溶液,加入一定的ZnO,60℃水浴充分反应后除去不溶物,向滤液中加入无水乙醇后用冰水浴冷却,有白色晶体析出,重结晶得纯度较高的葡萄糖酸锌。
(5)制备葡萄糖酸时常得到淡黄色滤液,可加入一定量
(6)重结晶步骤的具体操作为:将粗产品以温水溶解后,加入
(7)产品中锌含量测定:准确称取0.400g葡萄糖酸锌溶于20mL温水中,加入10mL缓冲溶液,4滴指示剂,用c mol/LEDTA标准溶液滴定至终点,平行测定三次,消耗标准溶液的平均值为V mL,计算产品中锌的质量分数为
您最近一年使用:0次



