解题方法
1 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X与Y位于不同周期,Y与W位于同一主族,Y、Z原子的最外层电子数之和等于它们的内层电子总数之和,W在同周期主族元素的基态原子中第一电离能最大。下列说法中不正确的是
| A.与X同主族的元素的基态原子最外层电子所占轨道呈球形 |
| B.Y、Z、W均位于元素周期表的p区 |
| C.仅由Z、W两种元素组成的化合物不止一种 |
| D.Z的最高价氧化物对应的水化物一定为强酸 |
您最近一年使用:0次
解题方法
2 . 某化学兴趣小组同学对电化学原理进行了一系列探究活动。
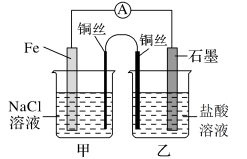
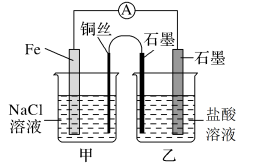
(1)如图,为某化学兴趣小组依据氧化还原反应:___________ (用离子方程式表示)设计的原电池装置,当导线中通过0.5mol电子的电量时,理论上石墨电极上产生气体体积为___________ L(标准状况下)。

(2)该实验小组的同学发现,用吸管吸出铁片附近溶液少许置于试管中,滴加几滴酚酞试剂,溶液变红,针对这一现象,某同学的假设是:铁电极材料不纯(材料中含有碳杂质),所以发生了___________ 腐蚀(填“吸氧”或“析氢”),试写出使酚酞溶液变红的电极反应式为___________ 。
(3)如图其他条件不变,若将盐桥换成n型铜丝,一段时间后,乙装置中石墨为___________ 极(填“正”、“负”、“阴”或“阳”),乙装置中总反应的离子方程式为___________ ,该反应为___________ (填“自发”或“非自发”)的氧化还原反应。___________ ,产物常用___________ 检验,一段时间后,乙装置中溶液pH___________ (填“变大”、“变小”或“不变”)。
(1)如图,为某化学兴趣小组依据氧化还原反应:

(2)该实验小组的同学发现,用吸管吸出铁片附近溶液少许置于试管中,滴加几滴酚酞试剂,溶液变红,针对这一现象,某同学的假设是:铁电极材料不纯(材料中含有碳杂质),所以发生了
(3)如图其他条件不变,若将盐桥换成n型铜丝,一段时间后,乙装置中石墨为
您最近一年使用:0次
3 . 研究含氮化合物对消除环境污染,能源结构的改变,食品添加剂的研究等有重要意义。
(1)甘氨酸锌常用于食品的添加剂,也可代替甘油作烟丝的加香、防冻。一水合甘氨酸锌结构简式如图所示。___________ 。
②基态锌原子的核外电子排布式为___________ ,核外有___________ 种能量不同的电子,最高能层的符号为___________ 。
(2)“中国制造2025”是中国政府实施制造强国战略第一个十年行动领。氮化铬在现代工业中发挥了重要作用。
①基态N原子的价层电子的轨道表示式为___________ 。
②基态Cr原子的价层电子排布式为___________ 。
(3)NO在空气中存在如下反应:2NO(g)+O2(g) 2NO2(g),该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为:
2NO2(g),该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为:___________ 。 ②氨水③
②氨水③ ④
④ 。
。 由大到小顺序是
由大到小顺序是___________ (用序号表示)。
(5)若T℃时,pH=2的醋酸溶液中由水电离出的c(H+)=1×10-11,则该温度下水的离子积常数Kw=___________ 。
室温下VaLpH=1的HCl溶液与VbLpH=12的NaOH溶液混合后pH=3,则Va:Vb=___________ 。
(1)甘氨酸锌常用于食品的添加剂,也可代替甘油作烟丝的加香、防冻。一水合甘氨酸锌结构简式如图所示。

②基态锌原子的核外电子排布式为
(2)“中国制造2025”是中国政府实施制造强国战略第一个十年行动领。氮化铬在现代工业中发挥了重要作用。
①基态N原子的价层电子的轨道表示式为
②基态Cr原子的价层电子排布式为
(3)NO在空气中存在如下反应:2NO(g)+O2(g)
 2NO2(g),该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为:
2NO2(g),该反应分两步完成,其反应历程如图所示:则决定总反应的速率这一步的热化学方程式为: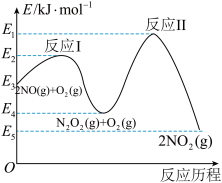
 ②氨水③
②氨水③ ④
④ 。
。 由大到小顺序是
由大到小顺序是(5)若T℃时,pH=2的醋酸溶液中由水电离出的c(H+)=1×10-11,则该温度下水的离子积常数Kw=
室温下VaLpH=1的HCl溶液与VbLpH=12的NaOH溶液混合后pH=3,则Va:Vb=
您最近一年使用:0次
4 . 下列各元素性质的叙述中,正确的是
| A.N、O、F的电负性依次减小 |
B. 、 、 、 、 的第一电离能依次增大 的第一电离能依次增大 |
| C.若X2+和Y2-具有相同的电子层结构,则离子半径:X2+<Y2- |
D.基态 原子的电子排布式为: 原子的电子排布式为: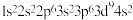 |
您最近一年使用:0次
解题方法
5 . 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)物质的量浓度均为0.1mol/L的下列四种溶液:pH由小到大排列的顺序是___________ 。
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是________ (填序号)。
A. B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:_____________ 。
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=_________ (用含a、b的代数式表示)。
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+___________ 。
(6)将碳酸钠溶液与次氯酸溶液混合,________ (填“是”或“否”)发生反应,若反应请写出反应的离子方程式:_______________ 。(不反应此问不答)
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.
 B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+
(6)将碳酸钠溶液与次氯酸溶液混合,
您最近一年使用:0次
解题方法
6 . 下面是第二周期部分元素基态原子的轨道表示式,据此判断下列说法错误的是
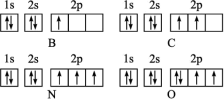
| A.每个原子轨道里最多只能容纳2个电子 |
| B.电子排在同一能级时,总是优先单独占据一个轨道 |
| C.每个能层所具有的能级数等于能层的序数(n) |
| D.若一个能级中有2个电子,则其自旋一定相反 |
您最近一年使用:0次
名校
7 . 喷泉实验装置如图所示。应用下列各组气体一溶液,能出现喷泉现象的是

| 气体 | 溶液 | |
| A |  | 稀盐酸 |
| B |  | 稀 溶液 溶液 |
| C |  | 稀硫酸 |
| D |  | 饱和 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-24更新
|
84次组卷
|
2卷引用:四川省眉山市彭山区第一中学2023-2024学年高一下学期4月第一次月考化学试题
解题方法
8 . 高锰酸钾生产过程中产生的废锰渣(主要成分为 、KOH、MgO和
、KOH、MgO和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下:
回答以下问题:
(1)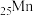 的电子排布式:
的电子排布式:___________ 。
(2)提高“反应Ⅰ”速率可采取的措施是___________ (除“加热”外,任写一种),滤渣A的主要成分为___________ (填化学式)。
(3)“反应Ⅱ”中硫铁矿(FeS₂)的作用为___________ 。
(4)“反应Ⅲ”的离子方程式为___________ 。
(5)“调pH”步骤中,应调节pH的范围是___________ 。
 、KOH、MgO和
、KOH、MgO和 )可用于制备
)可用于制备 晶体,工艺流程如下:
晶体,工艺流程如下: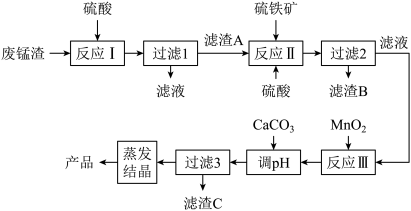
| 金属离子 |  |  |  |  |
| 开始沉淀pH | 2.10 | 7.45 | 9.27 | 9.60 |
| 完全沉淀pH | 3.20 | 8.95 | 10.87 | 11.13 |
(1)
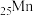 的电子排布式:
的电子排布式:(2)提高“反应Ⅰ”速率可采取的措施是
(3)“反应Ⅱ”中硫铁矿(FeS₂)的作用为
(4)“反应Ⅲ”的离子方程式为
(5)“调pH”步骤中,应调节pH的范围是
您最近一年使用:0次
9 . 短周期元素A、B、C、D的原子序数依次增大,A元素原子的核外电子只有一种运动状态:基态B原子s能级的电子总数比p能级的多1;基态C原子中成对电子数是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题
(1)B原子的轨道表示式___________ 。
(2)A和C原子个数比为1∶1的化合物的电子式___________ 。
(3)元素A、B、C中,第一电离能最大的是___________ (填元素名称)。
(4)在B、C、D三种元素的简单离子中,其离子的半径最小的是___________ 。(填离子符号)
(5)C的简单氢化物的键角小于B的简单氢化物,其原因是___________ 。
(6)BC₃的空间结构为___________ 。
(7)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB晶体的密度为a g⋅cm ,则晶体中两个最近D原子之间的距离为
,则晶体中两个最近D原子之间的距离为___________ pm(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
(1)B原子的轨道表示式
(2)A和C原子个数比为1∶1的化合物的电子式
(3)元素A、B、C中,第一电离能最大的是
(4)在B、C、D三种元素的简单离子中,其离子的半径最小的是
(5)C的简单氢化物的键角小于B的简单氢化物,其原因是
(6)BC₃的空间结构为
(7)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB晶体的密度为a g⋅cm
 ,则晶体中两个最近D原子之间的距离为
,则晶体中两个最近D原子之间的距离为 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。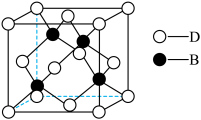
您最近一年使用:0次
解题方法
10 . 某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法正确的是

| A.氢化物沸点:X>Y | B.电负性:W<X<Y<Z |
| C.第一电离能:W<X<Y<Z | D.原子半径:M<X<Y<Z |
您最近一年使用:0次



