1 . 锂离子电池具有质量小、体积小、储存和输出能量大等特点。一种锂离子电池的结构如图所示,电池反应式为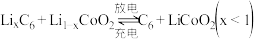 ,下列说法正确的是
,下列说法正确的是
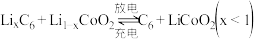 ,下列说法正确的是
,下列说法正确的是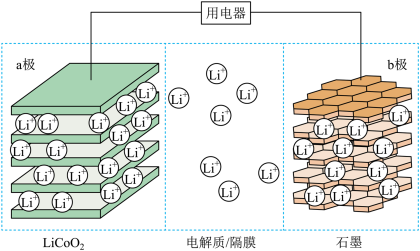
A.放电时 在电解质中由 在电解质中由 极向 极向 极迁移 极迁移 |
B.充电时 极接外电源的正极 极接外电源的正极 |
C.放电时, 极电极反应式: 极电极反应式: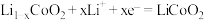 |
D.充电时若转移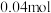 电子,石墨电极将减重 电子,石墨电极将减重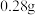 |
您最近一年使用:0次
2 . 化合物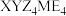 可作肥料,所含的5种元素位于主族,在每个短周期均有分布。E在地壳中含量最多,Y的基态原子p轨道半充满,Y和M同族且原子半径M更大。X与M同周期,X的基态原子最外层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布。E在地壳中含量最多,Y的基态原子p轨道半充满,Y和M同族且原子半径M更大。X与M同周期,X的基态原子最外层电子排布式为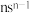 ,下列说法正确的是
,下列说法正确的是
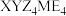 可作肥料,所含的5种元素位于主族,在每个短周期均有分布。E在地壳中含量最多,Y的基态原子p轨道半充满,Y和M同族且原子半径M更大。X与M同周期,X的基态原子最外层电子排布式为
可作肥料,所含的5种元素位于主族,在每个短周期均有分布。E在地壳中含量最多,Y的基态原子p轨道半充满,Y和M同族且原子半径M更大。X与M同周期,X的基态原子最外层电子排布式为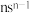 ,下列说法正确的是
,下列说法正确的是A.元素电负性: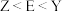 | B.简单氢化物稳定性: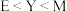 |
C.第一电离能: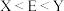 | D.元素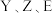 之间只能形成共价化合物 之间只能形成共价化合物 |
您最近一年使用:0次
3 . 室温下,下列探究方案能达到实验目的的是
| 选项 | 探究方案 | 实验目的 |
| A | 用不同浓度、等体积的 溶液分别与相同浓度相同体积的 溶液分别与相同浓度相同体积的 溶液反应,观察现象 溶液反应,观察现象 | 探究浓度对反应速率的影响 |
| B | 用 试纸测定同浓度 试纸测定同浓度 和 和 溶液的 溶液的 ,比较溶液 ,比较溶液 大小 大小 | 比较 与 与 的酸性强弱 的酸性强弱 |
| C | 向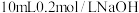 溶液中滴加2滴 溶液中滴加2滴 溶液,产生白色沉淀。再滴加2滴 溶液,产生白色沉淀。再滴加2滴 溶液,又生成红褐色沉淀 溶液,又生成红褐色沉淀 | 证明在相同温度下 : :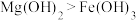 |
| D | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体,溶液红色变浅 固体,溶液红色变浅 | 证明 溶液中存在水解平衡 溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 2021年,中国科学院天津工业生物技术研究所马延和研究员带领团队,采用一种类似“搭积木”的方式,从头设计、构建了11步反应的非自然固碳与淀粉合成途径,在实验室中首次实现从二氧化碳到淀粉分子的全合成。其原理首先是利用化学催化剂将高浓度二氧化碳在高密度氢能作用下合成 。
。
(1)已知: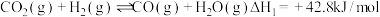

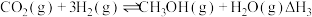
①
_______  。
。
②下列有利于提高 平衡产率的条件是
平衡产率的条件是_______ (填编号)。
A.高温、高压 B.高温、低压 C.低温、高压 D.低温、低压
(2)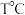 时,
时, 条件下,向
条件下,向 刚性容器中充入
刚性容器中充入 和
和 ,发生反应:
,发生反应: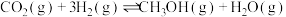 ,测得不同时刻容器内压强变化如下表:
,测得不同时刻容器内压强变化如下表:
反应前2小时内的平均反应速率 为
为_______  ,该温度下平衡常数
,该温度下平衡常数 为
为_______  (可以只列出计算式)。
(可以只列出计算式)。
(3)在催化条件下,密闭容器内通入一定量的 和
和 发生下列反应:
发生下列反应:
反应I: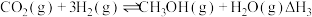
反应Ⅱ: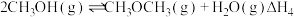
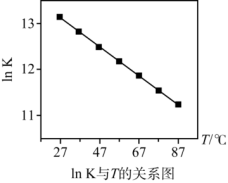
①实验测得反应Ⅱ的平衡常数(记作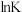 )与温度(
)与温度( )的关系如下图所示,则
)的关系如下图所示,则
_______ 0(填“>”或“<”)。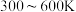 范围内,甲醇的含量逐渐增大而甲醚的百分含量逐渐减小的可能原因是
范围内,甲醇的含量逐渐增大而甲醚的百分含量逐渐减小的可能原因是_______ 。 制取甲醇的反应装置如图所示:
制取甲醇的反应装置如图所示:_______ (填“正”或“负”),生成甲醇的电极反应式为_______ 。
 。
。(1)已知:
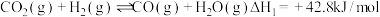

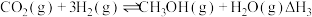
①

 。
。②下列有利于提高
 平衡产率的条件是
平衡产率的条件是A.高温、高压 B.高温、低压 C.低温、高压 D.低温、低压
(2)
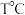 时,
时, 条件下,向
条件下,向 刚性容器中充入
刚性容器中充入 和
和 ,发生反应:
,发生反应: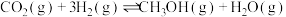 ,测得不同时刻容器内压强变化如下表:
,测得不同时刻容器内压强变化如下表:时间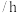 | 1 | 2 | 3 | 4 | 5 | 6 |
压强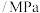 | 80 | 75 | 72 | 71 | 70 | 70 |
 为
为 ,该温度下平衡常数
,该温度下平衡常数 为
为 (可以只列出计算式)。
(可以只列出计算式)。(3)在催化条件下,密闭容器内通入一定量的
 和
和 发生下列反应:
发生下列反应:反应I:
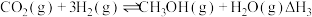
反应Ⅱ:
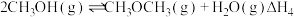
①实验测得反应Ⅱ的平衡常数(记作
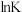 )与温度(
)与温度( )的关系如下图所示,则
)的关系如下图所示,则
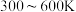 范围内,甲醇的含量逐渐增大而甲醚的百分含量逐渐减小的可能原因是
范围内,甲醇的含量逐渐增大而甲醚的百分含量逐渐减小的可能原因是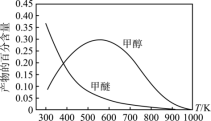
 制取甲醇的反应装置如图所示:
制取甲醇的反应装置如图所示: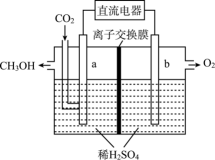
您最近一年使用:0次
5 . 在恒容密闭容器中发生如下反应: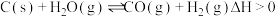 ,下列有关说法正确的是
,下列有关说法正确的是
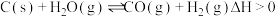 ,下列有关说法正确的是
,下列有关说法正确的是A.使用催化剂能提高 的平衡产率 的平衡产率 |
| B.该反应在高温下能自发进行 |
| C.增加反应物浓度能加快反应速率是因为反应物分子中活化分子百分数增加 |
D.增大压强,平衡逆向移动,则化学平衡常数 减小 减小 |
您最近一年使用:0次
6 . 废旧银锌纽扣电池(含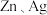 、石墨及少量
、石墨及少量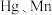 等)的正极片中回收银的工艺流程如图:
等)的正极片中回收银的工艺流程如图:错误 的是
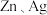 、石墨及少量
、石墨及少量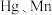 等)的正极片中回收银的工艺流程如图:
等)的正极片中回收银的工艺流程如图: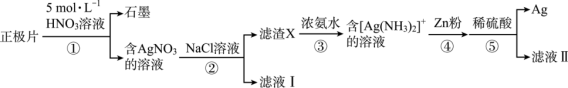
A.①中产生的气体为 |
B.②中使用饱和 溶液有利于提高 溶液有利于提高 的回收率 的回收率 |
C.⑤中加稀硫酸的目的是分离 和 和 |
D.滤渣X主要成分是 |
您最近一年使用:0次
7 . 设 表示阿伏加德罗常数数值,下列说法正确的是
表示阿伏加德罗常数数值,下列说法正确的是
 表示阿伏加德罗常数数值,下列说法正确的是
表示阿伏加德罗常数数值,下列说法正确的是A. 和 和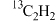 组成的混合物所含的电子数为 组成的混合物所含的电子数为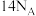 |
B. 溶液中 溶液中 的数目小于 的数目小于 |
C.一定条件下, 与 与 混合后充分反应,转移电子的数目为 混合后充分反应,转移电子的数目为 |
D.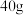 处于基态的氩气中含有的 处于基态的氩气中含有的 轨道电子总数为 轨道电子总数为 |
您最近一年使用:0次
8 . 在日常生产和生活中涉及到许多化学反应,对下列操作事实的解释离子方程式书写错误 的是
A.常温下,测得 醋酸 醋酸 约为2.9: 约为2.9: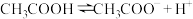 |
B.铅蓄电池放电时正极反应式: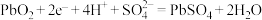 |
C.工人处理锅炉水垢时先用饱和 溶液对水垢进行浸泡: 溶液对水垢进行浸泡: |
D.实验室通常采用排饱和食盐水的方法收集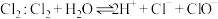 |
您最近一年使用:0次
9 . 下列有关热化学方程式书写与对应表述均正确的是
A.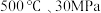 下,将 下,将 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放出热量 ,放出热量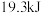 ,其热化学方程式为: ,其热化学方程式为: |
B.稀醋酸与稀 溶液反应: 溶液反应: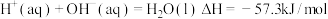 |
C.已知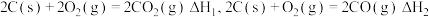 ,则 ,则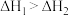 |
D. 的燃烧热为 的燃烧热为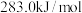 ,则 ,则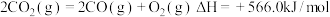 |
您最近一年使用:0次
解题方法
10 . 自然界是各类物质相互依存、各种变化相互制约的复杂平衡体系,而水溶液中的离子平衡是其中一个重要方面。请根据所学知识,回答下列问题:
(1)查阅资料获得 时部分弱酸
时部分弱酸 的数据:
的数据: 。
。
①常温下,氢氟酸溶液加水稀释过程中,下列表达式的数据变大的是_______ (填编号)。
A. B.
B.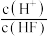 C.
C.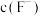
② 时,将浓度相等的
时,将浓度相等的 与
与 溶液等体积混合,溶液呈
溶液等体积混合,溶液呈_______ 性,结合有关数据和文字解释原因_______ 。
③已知 溶液呈弱碱性,试用离子反应方程式解释原因
溶液呈弱碱性,试用离子反应方程式解释原因_______ 。
④同浓度的 溶液和
溶液和 溶液相比,后者溶液中
溶液相比,后者溶液中
_______ 前者溶液中 (填“小于”、“等于”或“大于”)。
(填“小于”、“等于”或“大于”)。
(2)已知 溶液为中性,又知
溶液为中性,又知 溶液加到
溶液加到 溶液中有无色无味气体放出,现有
溶液中有无色无味气体放出,现有 时的4种溶液:
时的4种溶液:
A. B.
B. C.
C. D.
D.
①试推断 溶液的
溶液的
_______ 7(填“小于”、“等于”或“大于”)。
②将物质的量浓度相同的以上4种溶液按 浓度由大到小的顺序排列是
浓度由大到小的顺序排列是_______ (填编号)。
(1)查阅资料获得
 时部分弱酸
时部分弱酸 的数据:
的数据: 。
。①常温下,氢氟酸溶液加水稀释过程中,下列表达式的数据变大的是
A.
 B.
B.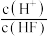 C.
C.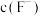
②
 时,将浓度相等的
时,将浓度相等的 与
与 溶液等体积混合,溶液呈
溶液等体积混合,溶液呈③已知
 溶液呈弱碱性,试用离子反应方程式解释原因
溶液呈弱碱性,试用离子反应方程式解释原因④同浓度的
 溶液和
溶液和 溶液相比,后者溶液中
溶液相比,后者溶液中
 (填“小于”、“等于”或“大于”)。
(填“小于”、“等于”或“大于”)。(2)已知
 溶液为中性,又知
溶液为中性,又知 溶液加到
溶液加到 溶液中有无色无味气体放出,现有
溶液中有无色无味气体放出,现有 时的4种溶液:
时的4种溶液:A.
 B.
B. C.
C. D.
D.
①试推断
 溶液的
溶液的
②将物质的量浓度相同的以上4种溶液按
 浓度由大到小的顺序排列是
浓度由大到小的顺序排列是
您最近一年使用:0次



