名校
1 . X、Y、Z、M为原子序数依次增大的周期表前20号主族元素。X原子的最外层电子数是内层电子数的两倍,Z的原子序数等于X、Y原子序数之和,M为金属元素且与Y同主族。下列说法正确的是
| A.原子半径:Y<Z |
| B.最高价含氧酸酸性:X<Z |
| C.Y和M分别与氧元素形成化合物均只有两种 |
| D.M、X和氧三种元素形成的盐只有一种 |
您最近一年使用:0次
名校
解题方法
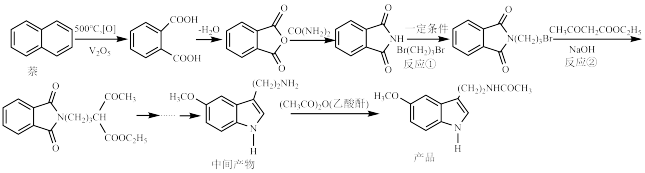
2 . 褪黑激素是一种神经系统激素,具有广泛的生理活性,有镇静镇痛的作用,一种以廉价易得的原料制备褪黑激素的合成路线如图所示:
(1)萘的一氯代物有___________ 种。
(2)1mol邻苯二甲酸与碳酸钠反应最多可产生___________ mol二氧化碳。
(3)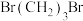 的官能团名称为
的官能团名称为___________ ,写出反应①的化学反应方程式___________ 。
(4)反应②属于___________ 反应(填有机反应类型),写出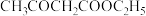 在NaOH水溶液中水解的化学反应方程式
在NaOH水溶液中水解的化学反应方程式___________ 。
(5)1mol中间产物H最多能与___________  发生加成反应,1个加成产物分子中有
发生加成反应,1个加成产物分子中有___________ 个手性碳原子。
(6)最后一步乙酰化反应可能会生成多种不同的乙酰化副产物,写出其中两种副产物的结构简式___________ 。
(1)萘的一氯代物有
(2)1mol邻苯二甲酸与碳酸钠反应最多可产生
(3)
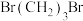 的官能团名称为
的官能团名称为(4)反应②属于
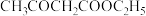 在NaOH水溶液中水解的化学反应方程式
在NaOH水溶液中水解的化学反应方程式(5)1mol中间产物H最多能与
 发生加成反应,1个加成产物分子中有
发生加成反应,1个加成产物分子中有(6)最后一步乙酰化反应可能会生成多种不同的乙酰化副产物,写出其中两种副产物的结构简式
您最近一年使用:0次
2024-05-17更新
|
314次组卷
|
2卷引用:2024届四川省仁寿第一中学校南校区二模理综化学试题
名校
解题方法
3 . 图1是一种居家天然气报警器成品装置,其工作原理如图2所示,其中 可以在固体电解质ZnO2—Na2O中移动。当空间内甲烷达到一定浓度时,传感器随之产生电信号并联动报警。当报警器触发工作时,下列说法不正确的是
可以在固体电解质ZnO2—Na2O中移动。当空间内甲烷达到一定浓度时,传感器随之产生电信号并联动报警。当报警器触发工作时,下列说法不正确的是
 可以在固体电解质ZnO2—Na2O中移动。当空间内甲烷达到一定浓度时,传感器随之产生电信号并联动报警。当报警器触发工作时,下列说法不正确的是
可以在固体电解质ZnO2—Na2O中移动。当空间内甲烷达到一定浓度时,传感器随之产生电信号并联动报警。当报警器触发工作时,下列说法不正确的是
| A.电极a的电势比电极b高 |
B. 在电解质中向电极a移动 在电解质中向电极a移动 |
C.电极a上发生的电极反应为: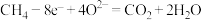 |
D.当电极a消耗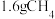 时,电路中有0.8mol电子转移 时,电路中有0.8mol电子转移 |
您最近一年使用:0次
名校
解题方法
4 . 硼元素有“金属材料的维生素”之称,其单质及其化合物的研究在无机化学的发展中占有独特的地位。请回答下列问题:
(1)基态硼原子的电子排布式为:___________ 。
(2)硼的化合物 中氢元素化合价为-1,故而被称为“万能还原剂”,广泛用于有机合成。
中氢元素化合价为-1,故而被称为“万能还原剂”,广泛用于有机合成。 中所含元素电负性由大到小的顺序为:
中所含元素电负性由大到小的顺序为:___________ 。
(3) 与
与 可以通过配位键形成
可以通过配位键形成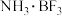 。
。
① 的空间构型为:
的空间构型为:___________ ,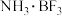 中硼原子的杂化方式为
中硼原子的杂化方式为___________ 。
② 的键角
的键角___________  的键角(填“大于”、“小于”或“等于”)。
的键角(填“大于”、“小于”或“等于”)。
(4)硼酸 晶体中单元结构如图1所示。各单元中的氧原子通过氢键连结成层状结构如图2所示,层与层之间以微弱的分子间力相结合构成整个硼酸晶体。
晶体中单元结构如图1所示。各单元中的氧原子通过氢键连结成层状结构如图2所示,层与层之间以微弱的分子间力相结合构成整个硼酸晶体。___________ 。
②1mol硼酸中含有氢键的数目为___________ 。
③ 在加热过程中会形成链状多硼酸根,其结构如图3所示。已知链状多硼酸根所有氧原子都达到8电子稳定结构,则含n个硼原子的多硼酸根可表示为
在加热过程中会形成链状多硼酸根,其结构如图3所示。已知链状多硼酸根所有氧原子都达到8电子稳定结构,则含n个硼原子的多硼酸根可表示为___________ 。
(5)科学家合成了一种含硼高温超导材料,其立方晶胞结构如图4所示。___________ 个面。
②已知晶胞边长为apm,阿伏加德罗常数为 ,则该晶体密度为
,则该晶体密度为___________  (用含
(用含 、a的式子表示,写出表达式即可)。
、a的式子表示,写出表达式即可)。
(1)基态硼原子的电子排布式为:
(2)硼的化合物
 中氢元素化合价为-1,故而被称为“万能还原剂”,广泛用于有机合成。
中氢元素化合价为-1,故而被称为“万能还原剂”,广泛用于有机合成。 中所含元素电负性由大到小的顺序为:
中所含元素电负性由大到小的顺序为:(3)
 与
与 可以通过配位键形成
可以通过配位键形成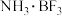 。
。①
 的空间构型为:
的空间构型为: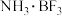 中硼原子的杂化方式为
中硼原子的杂化方式为②
 的键角
的键角 的键角(填“大于”、“小于”或“等于”)。
的键角(填“大于”、“小于”或“等于”)。(4)硼酸
 晶体中单元结构如图1所示。各单元中的氧原子通过氢键连结成层状结构如图2所示,层与层之间以微弱的分子间力相结合构成整个硼酸晶体。
晶体中单元结构如图1所示。各单元中的氧原子通过氢键连结成层状结构如图2所示,层与层之间以微弱的分子间力相结合构成整个硼酸晶体。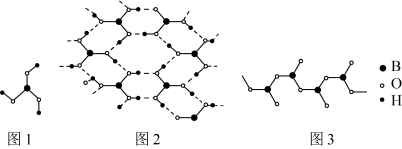
②1mol硼酸中含有氢键的数目为
③
 在加热过程中会形成链状多硼酸根,其结构如图3所示。已知链状多硼酸根所有氧原子都达到8电子稳定结构,则含n个硼原子的多硼酸根可表示为
在加热过程中会形成链状多硼酸根,其结构如图3所示。已知链状多硼酸根所有氧原子都达到8电子稳定结构,则含n个硼原子的多硼酸根可表示为(5)科学家合成了一种含硼高温超导材料,其立方晶胞结构如图4所示。
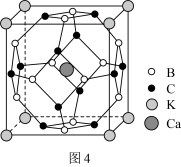
②已知晶胞边长为apm,阿伏加德罗常数为
 ,则该晶体密度为
,则该晶体密度为 (用含
(用含 、a的式子表示,写出表达式即可)。
、a的式子表示,写出表达式即可)。
您最近一年使用:0次
5 . 氮氧化物 进入同温层可对臭氧层造成破坏,对人类生活造成不利影响,目前工业上可采用多种方法对废气中的氮氧化物进行脱除,回答下列问题:
进入同温层可对臭氧层造成破坏,对人类生活造成不利影响,目前工业上可采用多种方法对废气中的氮氧化物进行脱除,回答下列问题:
(1)SCR法主要是针对柴油发动机产生的 的处理工艺,原理是
的处理工艺,原理是 和
和 在选择性催化剂表面转化为
在选择性催化剂表面转化为 和
和 ,反应历程中的能量变化如下图所示:
,反应历程中的能量变化如下图所示:___________ ,SCR法会产生高分散度的烟尘,会使催化剂的活性下降,原因是___________ 。
(2)甲烷脱硝:

①已知甲烷的燃烧热为890.3kJ/mol,
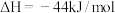 ,
,
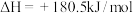 ,则甲烷脱硝反应的
,则甲烷脱硝反应的
___________ kJ/mol。
②800K时,为提高NO的平衡转化率,理论上可以采取的措施有:___________ 。
A.恒容时增加 B.恒压时通入一定量的Ar
B.恒压时通入一定量的Ar
C.移去部分 D.选择合适的催化剂
D.选择合适的催化剂
③一定温度下,将按一定比例混合的反应气匀速通过恒容催化反应器,测得NO去除率同 转化率随反应温度的变化关系如下图所示:
转化率随反应温度的变化关系如下图所示:___________ ;若反应气中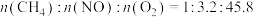 ,起始总压为66kPa,甲烷的平衡转化率为80%(若不考虑过程中存在的其他副反应),计算该温度下反应的分压平衡常数
,起始总压为66kPa,甲烷的平衡转化率为80%(若不考虑过程中存在的其他副反应),计算该温度下反应的分压平衡常数
___________ (以分压表示,分压=总压×物质的量分数,保留两位有效数字)。
(3)中国科学院研究人员报道了一种以铜锡合金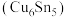 为催化剂,
为催化剂, 在电催化条件下还原NO高效合成氨的方法,并通过DFT计算研究了反应可能得机理如下(*表示催化剂表面吸附位,如
在电催化条件下还原NO高效合成氨的方法,并通过DFT计算研究了反应可能得机理如下(*表示催化剂表面吸附位,如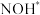 表示吸附于催化剂表面的NOH):
表示吸附于催化剂表面的NOH):
Ⅰ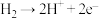 Ⅱ
Ⅱ 
Ⅲ Ⅳ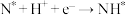
Ⅴ Ⅵ
Ⅵ 
上述反应机理中,第Ⅲ步的转化机理为___________ ;若电路中有4mol电子通过,其中生成 的选择性为95%,则阴极生成
的选择性为95%,则阴极生成 的物质的量为
的物质的量为___________ mol。
 进入同温层可对臭氧层造成破坏,对人类生活造成不利影响,目前工业上可采用多种方法对废气中的氮氧化物进行脱除,回答下列问题:
进入同温层可对臭氧层造成破坏,对人类生活造成不利影响,目前工业上可采用多种方法对废气中的氮氧化物进行脱除,回答下列问题:(1)SCR法主要是针对柴油发动机产生的
 的处理工艺,原理是
的处理工艺,原理是 和
和 在选择性催化剂表面转化为
在选择性催化剂表面转化为 和
和 ,反应历程中的能量变化如下图所示:
,反应历程中的能量变化如下图所示: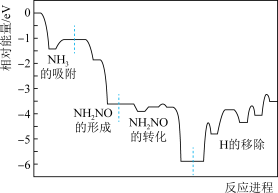
(2)甲烷脱硝:


①已知甲烷的燃烧热为890.3kJ/mol,

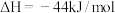 ,
,
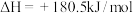 ,则甲烷脱硝反应的
,则甲烷脱硝反应的
②800K时,为提高NO的平衡转化率,理论上可以采取的措施有:
A.恒容时增加
 B.恒压时通入一定量的Ar
B.恒压时通入一定量的ArC.移去部分
 D.选择合适的催化剂
D.选择合适的催化剂③一定温度下,将按一定比例混合的反应气匀速通过恒容催化反应器,测得NO去除率同
 转化率随反应温度的变化关系如下图所示:
转化率随反应温度的变化关系如下图所示: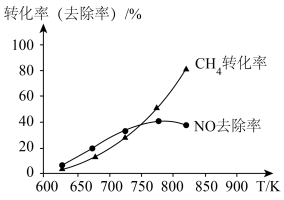
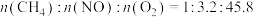 ,起始总压为66kPa,甲烷的平衡转化率为80%(若不考虑过程中存在的其他副反应),计算该温度下反应的分压平衡常数
,起始总压为66kPa,甲烷的平衡转化率为80%(若不考虑过程中存在的其他副反应),计算该温度下反应的分压平衡常数
(3)中国科学院研究人员报道了一种以铜锡合金
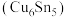 为催化剂,
为催化剂, 在电催化条件下还原NO高效合成氨的方法,并通过DFT计算研究了反应可能得机理如下(*表示催化剂表面吸附位,如
在电催化条件下还原NO高效合成氨的方法,并通过DFT计算研究了反应可能得机理如下(*表示催化剂表面吸附位,如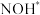 表示吸附于催化剂表面的NOH):
表示吸附于催化剂表面的NOH):Ⅰ
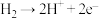 Ⅱ
Ⅱ 
Ⅲ Ⅳ
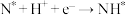
Ⅴ
 Ⅵ
Ⅵ 
上述反应机理中,第Ⅲ步的转化机理为
 的选择性为95%,则阴极生成
的选择性为95%,则阴极生成 的物质的量为
的物质的量为
您最近一年使用:0次
名校
解题方法
6 . 锂离子电池作为重要储能设备在手机、汽车等行业得到了大规模应用。一种基于微波辅助低共熔溶剂的回收方法可实现对废旧锂离子电池中 的回收利用,其主要工艺流程如下:
的回收利用,其主要工艺流程如下: 在溶液中常以
在溶液中常以 (蓝色)和
(蓝色)和 (粉红色)形式存在;
(粉红色)形式存在;
②25℃时,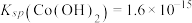 。
。
回答下列问题:
(1) 中Co的化合价为
中Co的化合价为___________ 。
(2)微波具有选择性加热和穿透性强的特点,采用微波共熔技术的优点除了可以减少杂质溶解还有___________ 。
(3)低共熔溶剂中含有一定量的草酸,其作用为___________ ;已知在水浸过程中溶液由蓝色变为粉红色,写出该变化的离子反应方程式___________ 。
(4)25℃时,沉钴反应完成后,溶液的pH=10,此时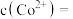
___________ mg/L。
(5)滤饼1在空气中煅烧得 ,写出该反应的化学反应方程式
,写出该反应的化学反应方程式___________ 。
(6)高温烧结过程中需通入空气,该反应中氧化剂与还原剂物质的量之比为___________ ,若通入空气过多过快,造成的不利影响是___________ 。
 的回收利用,其主要工艺流程如下:
的回收利用,其主要工艺流程如下: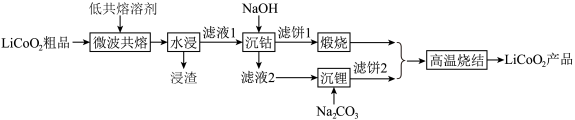
 在溶液中常以
在溶液中常以 (蓝色)和
(蓝色)和 (粉红色)形式存在;
(粉红色)形式存在;②25℃时,
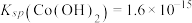 。
。回答下列问题:
(1)
 中Co的化合价为
中Co的化合价为(2)微波具有选择性加热和穿透性强的特点,采用微波共熔技术的优点除了可以减少杂质溶解还有
(3)低共熔溶剂中含有一定量的草酸,其作用为
(4)25℃时,沉钴反应完成后,溶液的pH=10,此时
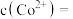
(5)滤饼1在空气中煅烧得
 ,写出该反应的化学反应方程式
,写出该反应的化学反应方程式(6)高温烧结过程中需通入空气,该反应中氧化剂与还原剂物质的量之比为
您最近一年使用:0次
名校
7 . 设 为阿伏伽德罗常数的值,下列叙述正确的是
为阿伏伽德罗常数的值,下列叙述正确的是
 为阿伏伽德罗常数的值,下列叙述正确的是
为阿伏伽德罗常数的值,下列叙述正确的是A.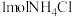 中所含共价键的数目为 中所含共价键的数目为 |
B.pH=2的稀硫酸中 数目为 数目为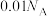 |
C. 和 和 的固体混合物中含有阳离子数目为 的固体混合物中含有阳离子数目为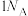 |
D.用惰性电极电解 溶液,当阳极产生标况下的气体体积为224mL时,电路中转移电子数为 溶液,当阳极产生标况下的气体体积为224mL时,电路中转移电子数为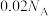 |
您最近一年使用:0次
名校
解题方法
8 . 有机化合物M是一种重要的香料,广泛用于牙膏、口香糖和各种饮料中。在三氟甲磺酸(CF3SO3H)催化作用下M可生成N,反应过程如图所示。下列说法不正确的是
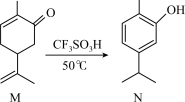
| A.M和N互为同分异构体 |
| B.M的一氯代物有7种 |
| C.M和N均能使酸性高锰酸钾溶液褪色 |
| D.N中所有碳原子处于同一平面 |
您最近一年使用:0次
9 . 中国科学院研究团队在人工合成淀粉方面取得重大突破性进展,首次在实验室实现了二氧化碳到淀粉的合成,为解决粮食危机和实现碳循环利用提供了有效途径。回答下列问题:
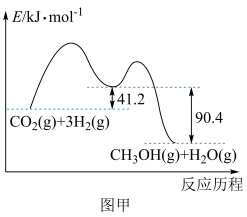
(1)人工合成淀粉的第一步是利用化学催化剂将高浓度二氧化碳在高密度氢能作用下还原成一碳化合物,其反应过程如图甲所示,则该反应的热化学方程式为_______ 。
(2)在一定条件下,若上述反应的平衡常数为K1,已知存在副反应 ,平衡常数为K2,则反应
,平衡常数为K2,则反应 的平衡常数
的平衡常数
_______ (用K1、K2表示)。
(3)选择合适的催化剂,可用CO2和H2合成重要的化工原料C2H4,假设在压强为100 kPa的恒压容器中只存在反应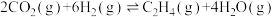 ,不同投料比时,CO2的平衡转化率随温度的变化如图乙所示(已知投料比
,不同投料比时,CO2的平衡转化率随温度的变化如图乙所示(已知投料比 )。
)。
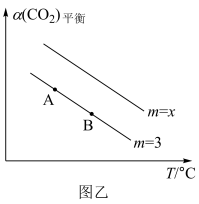
① 图乙中,x_______ 3(填“>”“<”或“=”,下同),该反应的ΔH_______ 0,有利于该反应自发进行的条件是_______ (填“高温”“低温”或“任意温度”);
② 图乙A、B两点中,ʋ正(A)_______ ʋ正(B)(填“>”“<”或“=”),理由是_______ ;
③ 恒温恒压下,以投料比m = 3进行该反应,下列能判断该反应已达平衡的标志有_______ (填标号);
A. 保持不变
保持不变
B.CO2的转化率与H2的转化率相等
C.断裂6 mol H—H键的同时,生成8 mol H—O键
D.容器中混合气体的密度保持不变
④ 已知B点纵坐标为40%,则该反应B点的压强平衡常数Kp =_______ (列出计算表达式)。
(1)人工合成淀粉的第一步是利用化学催化剂将高浓度二氧化碳在高密度氢能作用下还原成一碳化合物,其反应过程如图甲所示,则该反应的热化学方程式为

(2)在一定条件下,若上述反应的平衡常数为K1,已知存在副反应
 ,平衡常数为K2,则反应
,平衡常数为K2,则反应 的平衡常数
的平衡常数
(3)选择合适的催化剂,可用CO2和H2合成重要的化工原料C2H4,假设在压强为100 kPa的恒压容器中只存在反应
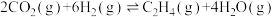 ,不同投料比时,CO2的平衡转化率随温度的变化如图乙所示(已知投料比
,不同投料比时,CO2的平衡转化率随温度的变化如图乙所示(已知投料比 )。
)。
① 图乙中,x
② 图乙A、B两点中,ʋ正(A)
③ 恒温恒压下,以投料比m = 3进行该反应,下列能判断该反应已达平衡的标志有
A.
 保持不变
保持不变B.CO2的转化率与H2的转化率相等
C.断裂6 mol H—H键的同时,生成8 mol H—O键
D.容器中混合气体的密度保持不变
④ 已知B点纵坐标为40%,则该反应B点的压强平衡常数Kp =
您最近一年使用:0次
2024-05-15更新
|
109次组卷
|
3卷引用:2024届四川省仁寿第一中学校南校区高三下学期模拟考试(四)理综试题-高中化学
名校
解题方法
10 . 铝酸铋[Bi(AlO2)3]是一种能够有效调理胃肠功能、促进疾病恢复的常见药物,常用辉铋矿(主要成分为Bi2S3,还含少量Cu2S和Ag2O)和铝土矿(主要成分为Al2O3,还含少量Fe2O3和SiO2)利用如下流程制取:
② BiCl3易溶于水,易水解,Bi(OH)3不溶于水和碱。
回答下列问题:
(1)辉铋矿“酸浸”过程中,需要控制温度不超过50℃的原因是_______ 。
(2)辉铋矿“酸浸”时S元素转化为单质硫,浸渣1的成分为_______ 。“酸浸”时Bi2S3转化的离子方程式为_______ 。
(3)“沉铋”时氨水稍过量的目的是_______ ;“沉铁”时稍过量的NaOH能否用氨水代替:_______ (填“能”或“否”)。
(4)Bi(NO3)3溶液和NaAlO2溶液混合前,Bi(NO3)3溶液中往往含少量硝酸,NaAlO2溶液中往往含少量NaOH,其目的是_______ 。
(5)Bi(NO3)3溶液和NaAlO2溶液混合充分反应,写出制取Bi(AlO2)3的化学方程式_______ ,利用1 kg含77.1% Bi2S3的辉铋矿与足量铝土矿作用制得868.5 g Bi(AlO2)3,则铝酸铋的产率为_______ 。
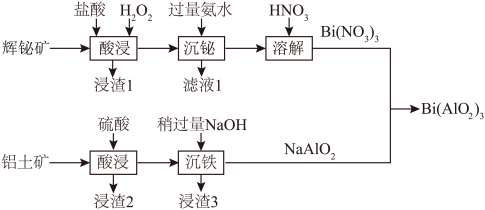
② BiCl3易溶于水,易水解,Bi(OH)3不溶于水和碱。
回答下列问题:
(1)辉铋矿“酸浸”过程中,需要控制温度不超过50℃的原因是
(2)辉铋矿“酸浸”时S元素转化为单质硫,浸渣1的成分为
(3)“沉铋”时氨水稍过量的目的是
(4)Bi(NO3)3溶液和NaAlO2溶液混合前,Bi(NO3)3溶液中往往含少量硝酸,NaAlO2溶液中往往含少量NaOH,其目的是
(5)Bi(NO3)3溶液和NaAlO2溶液混合充分反应,写出制取Bi(AlO2)3的化学方程式
您最近一年使用:0次
2024-05-15更新
|
128次组卷
|
3卷引用:2024届四川省仁寿第一中学校南校区高三下学期模拟考试(四)理综试题-高中化学



