1 . 某研究性学习小组学生根据氧化还原反应规律,探究 、
、 与
与 反应的情况,提出假设并进行相关实验。
反应的情况,提出假设并进行相关实验。
Ⅰ.从理论上分析 和
和 都既有氧化性又有还原性,于是提出如下假设:
都既有氧化性又有还原性,于是提出如下假设:
假设1: 氧化
氧化 ;
;
假设2: 氧化
氧化 。
。
(1)甲同学设计如图装置进行实验:___________ 。
②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B,向其中加入适量 粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是___________ 。乙同学用改进后的装置,重复了甲同学的实验操作,观察到红棕色气体迅速消失;带火星的木条未复燃,得出结论:假设Ⅰ正确。则 和
和 反应的化学方程式是
反应的化学方程式是___________ 。
Ⅱ.该研究性学习小组同学还认为易与 发生反应,应该更易被氧化。查阅资料:
发生反应,应该更易被氧化。查阅资料: ;
;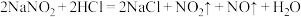 ;酸性条件下,能与
;酸性条件下,能与 反应生成
反应生成 和
和 。
。
(3)丙同学用下图所示装置(部分夹持装置略)探究 与
与 的反应。
的反应。 ,目的是
,目的是___________ 。
②B中观察到的主要现象的是___________ (填字母编号)。
a.铜片逐渐溶解,溶液变为蓝色
b.有红棕色气泡产生
c.有无色气泡产生
③C、E中所盛装的试剂不能是___________ (填字母编号)。
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④充分反应后,检验D装置中产物的方法是:取D装置中产物少许,___________ ,则产物是 。
。
 、
、 与
与 反应的情况,提出假设并进行相关实验。
反应的情况,提出假设并进行相关实验。Ⅰ.从理论上分析
 和
和 都既有氧化性又有还原性,于是提出如下假设:
都既有氧化性又有还原性,于是提出如下假设:假设1:
 氧化
氧化 ;
;假设2:
 氧化
氧化 。
。(1)甲同学设计如图装置进行实验:

②待试管B中充满红棕色气体,关闭旋塞a和b;取下试管B,向其中加入适量
 粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。
粉末,塞上塞子,轻轻振荡试管内粉末,观察到红棕色气体迅速消失;再将带火星的木条迅速伸进试管内,木条复燃。结论:甲同学认为假设2正确。
(2)乙同学认为甲同学设计的实验存在缺陷,为达到实验目的,在A、B之间应增加一个装置,该装置的作用是
 和
和 反应的化学方程式是
反应的化学方程式是Ⅱ.该研究性学习小组同学还认为易与
 发生反应,应该更易被氧化。查阅资料:
发生反应,应该更易被氧化。查阅资料: ;
;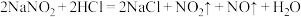 ;酸性条件下,能与
;酸性条件下,能与 反应生成
反应生成 和
和 。
。(3)丙同学用下图所示装置(部分夹持装置略)探究
 与
与 的反应。
的反应。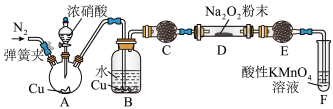
 ,目的是
,目的是②B中观察到的主要现象的是
a.铜片逐渐溶解,溶液变为蓝色
b.有红棕色气泡产生
c.有无色气泡产生
③C、E中所盛装的试剂不能是
a.无水硫酸铜 b.无水氯化钙 c.碱石灰 d.生石灰
④充分反应后,检验D装置中产物的方法是:取D装置中产物少许,
 。
。
您最近一年使用:0次
2024-04-08更新
|
629次组卷
|
5卷引用:四川省自贡市蜀光中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
2 . 管道工人曾经用浓氨水检验氯气管道是否泄漏。当浓氨水靠近氯气泄漏处时会产生大量白烟,这一现象体现了氨的哪些性质?
①易挥发 ②易溶于水 ③还原性 ④氧化性 ⑤碱性 ⑥酸性
①易挥发 ②易溶于水 ③还原性 ④氧化性 ⑤碱性 ⑥酸性
| A.①②③ | B.①③⑤ | C.②④⑥ | D.③④⑤ |
您最近一年使用:0次
2020-09-05更新
|
74次组卷
|
3卷引用:四川省自贡市田家炳中学2021届高三上学期开学考试化学试题
名校
3 .  的防治与利用对环境保护意义重大。
的防治与利用对环境保护意义重大。
(1)实验室用浓硫酸和亚硫酸钠制取
 的化学方程式为
的化学方程式为(2)实验室制取干燥的
 时,收集
时,收集 所需装置的接口连接顺序为
所需装置的接口连接顺序为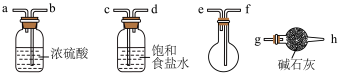
(3)用下图装置探究
 的还原性或氧化性。
的还原性或氧化性。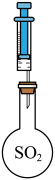
限选试剂:NaOH溶液、稀硫酸、酸性高锰酸钾溶液、淀粉-KI溶液、新制 溶液。
溶液。
步骤 | 现象 | 结论 |
用注射器将① | 产生乳白色浑浊 |
|
用注射器将② | ③ |
|
(4)某小组利用下列装置测定空气中
 的含量。
的含量。
已知该反应的化学方程式为:
若空气流速为 ,当观察到
,当观察到 。假定样品中的
。假定样品中的 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是 。
。
您最近一年使用:0次
名校
解题方法
4 . 下列有关实验的操作、现象和结论有错误的是
| 操作 | 现象 | 实验结论 | |
| A | 将SO2通入酸性KMnO4溶液 | 溶液褪色 | SO2具有还原性 |
| B | 将SO2通入H2S溶液 | 产生淡黄色沉淀 | SO2具有氧化性 |
| C | 向蔗糖中加入浓硫酸,将产生的气体通入溴水 | 蔗糖膨胀变黑,溴水褪色 | 浓硫酸具有脱水性和氧化性 |
| D | 将淀粉与稀硫酸混合加热后,加入少量新制Cu(OH)2,再加热 | 无砖红色沉淀生成 | 淀粉没有水解,或水解后没有葡萄糖生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-31更新
|
1012次组卷
|
6卷引用:四川省自贡市2022-2023学年高一下学期期末考试化学试题
名校
5 . 目前,能较稳定存在的氯的氧化物有Cl2O、ClO2、Cl2O7等。有关数据见表:
请回答下列问题:
(1)常温、常压下,三种氧化物中属于气体的是__________ 。
(2)Cl2O7属于酸性氧化物,它与水反应的离子方程式为__________ 。
(3)ClO2是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒。在消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,说明ClO2具有__________ 性。
(4)工业上可以用下列反应制备ClO2:2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4,请用单线桥法表示出该反应电子转移的方向和数目______________ 。
(5)工业上制备ClO2的反应原理为:2NaClO3+4HCl(浓)=2ClO2↑+Cl2↑+2H2O+2NaCl。
①浓盐酸在反应中显示出来的性质是__________ (填序号)。
A.还原性 B.氧化性 C.酸性
②若上述反应中产生0.1molClO2,则转移的电子数为__________ 。
| 化学式 | Cl2O | ClO2 | Cl2O7 |
| 沸点/℃ | 3.8 | 11.0 | 82.0 |
请回答下列问题:
(1)常温、常压下,三种氧化物中属于气体的是
(2)Cl2O7属于酸性氧化物,它与水反应的离子方程式为
(3)ClO2是一种常用的消毒剂,我国从2000年起逐步用ClO2代替氯气对饮用水进行消毒。在消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,说明ClO2具有
(4)工业上可以用下列反应制备ClO2:2NaClO3+H2SO4+SO2=2ClO2+2NaHSO4,请用单线桥法表示出该反应电子转移的方向和数目
(5)工业上制备ClO2的反应原理为:2NaClO3+4HCl(浓)=2ClO2↑+Cl2↑+2H2O+2NaCl。
①浓盐酸在反应中显示出来的性质是
A.还原性 B.氧化性 C.酸性
②若上述反应中产生0.1molClO2,则转移的电子数为
您最近一年使用:0次
2018-12-21更新
|
270次组卷
|
4卷引用:四川省自贡市田家炳中学2019-2020学年高一下学期开学考试化学试题
6 . 下图横坐标、纵坐标分别表示一定条件下氧化剂的氧化性、还原剂的还原性由弱到强的变化,1、2、3点表示了横纵坐标对应微粒在水溶液中反应的产物。下列说法正确的是
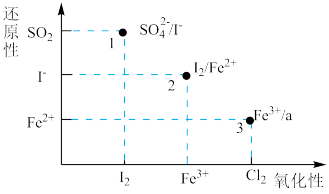
A.反应1中 的S失电子表现氧化性 的S失电子表现氧化性 | B.反应2的离子方程式为: |
C.反应3的产物a是 | D.从图可推得 能氧化 能氧化 、 、 |
您最近一年使用:0次
2022-12-09更新
|
357次组卷
|
8卷引用:四川省自贡市蜀光中学2023-2024学年高一上学期10月月考化学试题
7 . 根据下列实验操作和现象,所得到的实验结论正确的是
选项 | 实验操作和现象 | 实验结论 |
| A | 将浓硫酸滴到蔗糖表面,固体变黑膨胀 | 浓硫酸具有吸水性和强氧化性 |
| B | 向NaI溶液中滴加少量氯水和CCl4,振荡、静置,下层溶液显紫色 | 还原性:I->Cl- |
| C | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结 | NH4Cl固体可以升华 |
| D | 向某溶液中滴加几滴新制氯水,振荡,再加入少量KSCN溶液,溶液变为红色 | 该溶液中一定含有Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-22更新
|
1874次组卷
|
5卷引用:四川省自贡市富顺县城关中学2021-2022学年高一下学期期中考试化学试题
四川省自贡市富顺县城关中学2021-2022学年高一下学期期中考试化学试题广东省广州市2022届高三下学期二模综合测试化学试题(已下线)微专题13 亚铁离子、三价铁离子的性质及检验-备战2023年高考化学一轮复习考点微专题(已下线)微专题08 氧化性和还原性强弱的实验探究及应用-备战2023年高考化学一轮复习考点微专题(已下线)T11-化学实验方案与设计
8 . 已知反应:①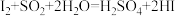 ;②
;② ;③
;③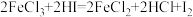 。下列说法不正确的是
。下列说法不正确的是
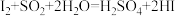 ;②
;② ;③
;③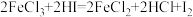 。下列说法不正确的是
。下列说法不正确的是A.氧化性: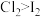 |
B.还原性: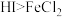 |
C.反应①中氧化剂与还原剂的质量之比为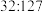 |
D.反应③中被氧化的元素与被还原的元素的质量之比为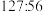 |
您最近一年使用:0次
2021-08-04更新
|
992次组卷
|
8卷引用:四川省自贡市2021-2022学年高一上学期期末考试化学试题
四川省自贡市2021-2022学年高一上学期期末考试化学试题陕西省榆林市2020-2021学年高一上学期期末检测化学试题河南省林州市2021-2022学年高一上学期期末考试化学试题(已下线)1.3.2 氧化剂与还原剂 氧化还原反应规律-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)湖南省永州市第一中学2022-2023学年高一上学期期末考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第一单元03巩固练云南省普洱市第一中学2022-2023学年高一下学期期末考试化学试题(已下线)专题03 氧化还原反应【考题猜想】(10大题型)-2023-2024学年高一化学上学期期中考点大串讲(人教版2019必修第一册)
解题方法
9 . 化学与生活密切相关,下列有关说法错误的是
| A.碘酒在处理伤口时,应用了I2的氧化性 |
| B.明矾净水,利用了Al(OH)3胶粒的吸附性质 |
| C.铁粉可以用于食品保鲜,涉及到Fe的还原性 |
| D.苏打水是Na2CO3饱和溶液,可以缓解胃酸过多 |
您最近一年使用:0次
解题方法
10 . 工业上,以钛铁矿为原料制备二氧化钛的工艺流程如下图所示。钛铁矿主要成分为钛酸亚铁( FeTiO3),其中一部分Fe2+在风化过程中会转化为+3价。
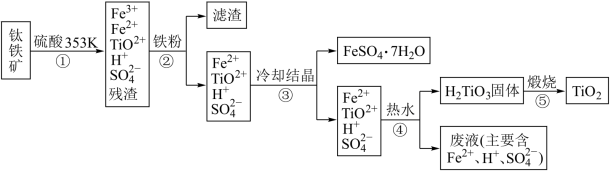
已知:TiO(OH)2(即H2TiO3)为两性氢氧化物
(1)步骤②中,发生主要反应的离子方程式为__________ 。
(2)步骤③中,实现混合物的分离是利用物质的__________ 填字母序号)。
A.熔沸点差异 B.溶解性差异 C.氧化性、还原性差异
(3)步骤②、③、④中,均需用到的操作是__________ (填操作名称)。
(4)请结合化学用语,用化学平衡理论解释步骤④中将TiO2+转化为H2TiO3的原理:__________ 。
(5)上述工艺流程中可以循环利用的物质是__________
(6)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。

①写出阳极所发生反应的电极反应式__________ 。
②在制备金属Ti前后,CaO的质量将__________ (填“增大”、“不变”或“减小”)。

已知:TiO(OH)2(即H2TiO3)为两性氢氧化物
(1)步骤②中,发生主要反应的离子方程式为
(2)步骤③中,实现混合物的分离是利用物质的
A.熔沸点差异 B.溶解性差异 C.氧化性、还原性差异
(3)步骤②、③、④中,均需用到的操作是
(4)请结合化学用语,用化学平衡理论解释步骤④中将TiO2+转化为H2TiO3的原理:
(5)上述工艺流程中可以循环利用的物质是
(6)研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置获得金属钙,并以钙为还原剂,还原二氧化钛制备金属钛。

①写出阳极所发生反应的电极反应式
②在制备金属Ti前后,CaO的质量将
您最近一年使用:0次



