名校
1 . 伯舒替尼(J)是一种激酶抑制剂,可用于治疗成人慢性粒细胞性白血病。其一种合成路线如图。请回答下列问题:___________ ,设计A→B、G→H的目的为___________ 。
(2)物质B中所含官能团的名称为___________ ,C的结构简式为___________ 。
(3) 的化学名称为
的化学名称为___________ 。
(4)D→E的反应方程式为___________ 。
(5)K比化合物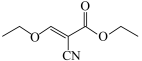 少两个H原子,K的芳香族同分异构体中,符合下列条件的结构有
少两个H原子,K的芳香族同分异构体中,符合下列条件的结构有___________ 种,核磁共振氢谱图上只有3组峰的结构简式为___________ (写一种即可)。
a.苯环上有4个取代基 b. 与苯环直接相连 c.能与氯化铁溶液发生显色反应
与苯环直接相连 c.能与氯化铁溶液发生显色反应
(6)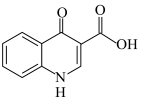 是一种新型的
是一种新型的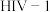 整合酶链转移抑制剂,设计以
整合酶链转移抑制剂,设计以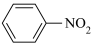 、
、 为含碳原料制备
为含碳原料制备 的合成路线(其他无机试剂或溶剂等任选)。
的合成路线(其他无机试剂或溶剂等任选)。___________

(2)物质B中所含官能团的名称为
(3)
 的化学名称为
的化学名称为(4)D→E的反应方程式为
(5)K比化合物
 少两个H原子,K的芳香族同分异构体中,符合下列条件的结构有
少两个H原子,K的芳香族同分异构体中,符合下列条件的结构有a.苯环上有4个取代基 b.
 与苯环直接相连 c.能与氯化铁溶液发生显色反应
与苯环直接相连 c.能与氯化铁溶液发生显色反应(6)
 是一种新型的
是一种新型的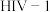 整合酶链转移抑制剂,设计以
整合酶链转移抑制剂,设计以 、
、 为含碳原料制备
为含碳原料制备 的合成路线(其他无机试剂或溶剂等任选)。
的合成路线(其他无机试剂或溶剂等任选)。
您最近一年使用:0次
2024-03-30更新
|
403次组卷
|
4卷引用:贵州省安顺市部分学校2024届高三下学期二模考试化学试题
2 . 丁酸龙葵酯是一种新型香料,一种合成路线如下:
(1)A的名称为___________ 。
(2)E中含氧官能团的名称是____________ 。
(3)反应⑥的反应类型是____________ ,试剂X是______________ 。
(4)反应②由B生成C的化学方程式为______________ 。
(5)芳香化合物W是E的同分异构体,W苯环上有2个取代基,能使Br2/CCl4溶液褪色,与FeCl3溶液作用显紫色。满足上述条件的W的结构有______ 种(不考虑立体异构),写出核磁共振氢谱为五组峰,峰面积比为3︰2︰2︰2︰1的W的结构简式_______ 。
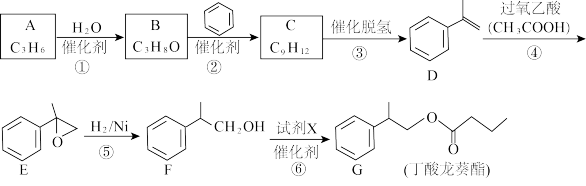
已知:
(1)A的名称为
(2)E中含氧官能团的名称是
(3)反应⑥的反应类型是
(4)反应②由B生成C的化学方程式为
(5)芳香化合物W是E的同分异构体,W苯环上有2个取代基,能使Br2/CCl4溶液褪色,与FeCl3溶液作用显紫色。满足上述条件的W的结构有
(6)乙酸环己酯(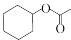 )是一种食用香料,设计由环己烯、乙酸和过氧乙酸为原料制备乙酸环己酯的合成路线
)是一种食用香料,设计由环己烯、乙酸和过氧乙酸为原料制备乙酸环己酯的合成路线
您最近一年使用:0次
2019-05-08更新
|
495次组卷
|
2卷引用:2020届贵州省安顺市高三第一次模拟理综试题-高中化学
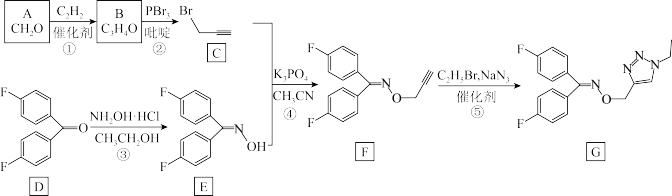
3 . 化合物G具有良好的抗肿瘤生物活性,其合成路线如下:
(1)反应①的反应类型是___________ ;B的结构简式是___________ 。
(2)C的化学名称为___________ 。
(3)D中官能团的名称是___________ 。
(4)反应④的反应方程式为___________ ;研究发现该反应存在反应限度,加入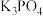 能提高F的产率,其原因是
能提高F的产率,其原因是___________ 。
(5)X是D的同分异构体,写出满足如下条件的X的结构简式___________ 。(不考虑立体异构,只需写出3个)
①与D具有完全相同的官能团;
②含有两个苯环且两个氟原子连接在同一个苯环上。
(6)利用以上合成路线中的相关反应,设计由苯乙烯和溴乙烷制备 的合成路线:
的合成路线:___________ (无机试剂任选)。
(1)反应①的反应类型是
(2)C的化学名称为
(3)D中官能团的名称是
(4)反应④的反应方程式为
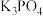 能提高F的产率,其原因是
能提高F的产率,其原因是(5)X是D的同分异构体,写出满足如下条件的X的结构简式
①与D具有完全相同的官能团;
②含有两个苯环且两个氟原子连接在同一个苯环上。
(6)利用以上合成路线中的相关反应,设计由苯乙烯和溴乙烷制备
 的合成路线:
的合成路线:
您最近一年使用:0次
4 . 2018年8月3日我国确诊首例非洲猪瘟疫情。10月25日,农业农村部新闻办公室发布,贵州省毕节市发生非洲猪瘟疫情。目前最有效的药物要主要成分的一种合成路线如图所示:
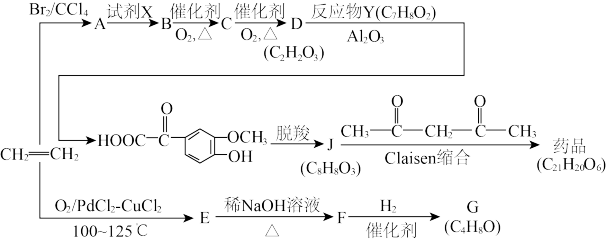
已知:
①E、G能发生银镜反应
②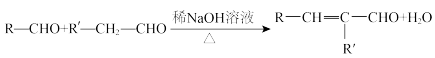 (R、R表示烃基或氢)。
(R、R表示烃基或氢)。
请回答下列问题:
(1)G的名称是____________________ ;D中所含官能团的名称是____________________ 。
(2)Y的结构简式为__________________ ;A生成B的反应类型是__________________ 。
(3)据最新报道,乙烯与双氧水在催化剂作用下反应生成B,产率较高。写出该反应的化学方程式____________________________________________ 。
(4)简述逐一检测出F中官能团的实验操作与现象结论______________________ 。
(5)在J的同分异构体中,同时满足下列条件的同分异构体有___________ 种。
i.既能发生水解反应,又能发生银镜反应;
ii.遇氯化铁溶液发生显色反应。
(6)参照上述流程,以苯乙烯为原料,设计路线制备某药物中间体
 :
: _________________________________ 。

已知:
①E、G能发生银镜反应
②
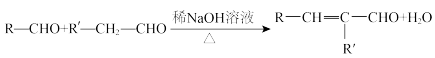 (R、R表示烃基或氢)。
(R、R表示烃基或氢)。请回答下列问题:
(1)G的名称是
(2)Y的结构简式为
(3)据最新报道,乙烯与双氧水在催化剂作用下反应生成B,产率较高。写出该反应的化学方程式
(4)简述逐一检测出F中官能团的实验操作与现象结论
(5)在J的同分异构体中,同时满足下列条件的同分异构体有
i.既能发生水解反应,又能发生银镜反应;
ii.遇氯化铁溶液发生显色反应。
(6)参照上述流程,以苯乙烯为原料,设计路线制备某药物中间体
 :
:
您最近一年使用:0次
2019-03-03更新
|
302次组卷
|
2卷引用:【市级联考】贵州省安顺市普通高中2019届高三上学期期末考试理科综合化学试题
5 . 芳香族化合物A 和E 可以合成芳香酯I,合成路线如图所示:
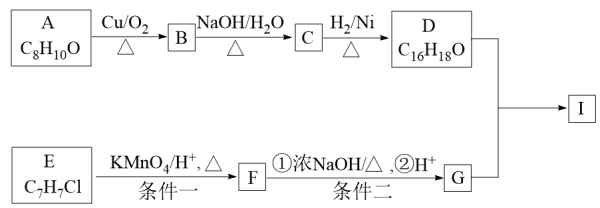
已知:
①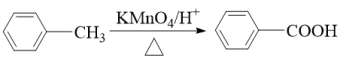
②2RCH2CHO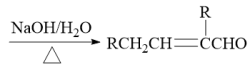
③B的苯环上只有一个取代基,且能发生银镜反应;
④E的核磁共振氢谱有3组峰
请回答下列问题:
(1)A 的结构简式为________ ,B 的化学名称是________ 。
(2)C→D的反应类型为________ ,F 中所含官能团的名称是________ 。
(3)条件一与条件二能否互换____ (填“能”或“否”),原因是_________ 。
(4)写出D 与G 反应的化学方程式_______________ 。
(5)A 的同分异构体很多,其中能使FeCl3溶液显紫色有___ 种,写出其中一种核磁共振氢谱有4 组峰的分子的结构简式________ 。
(6)结合题中信息,写出以溴乙烷为原料制备1-丁醇的合成路线图______ (无机试剂任选),合成路线流程图示例如下: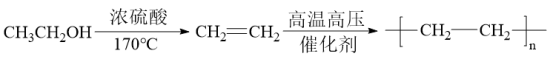 。
。

已知:
①
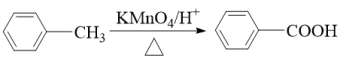
②2RCH2CHO
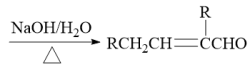
③B的苯环上只有一个取代基,且能发生银镜反应;
④E的核磁共振氢谱有3组峰
请回答下列问题:
(1)A 的结构简式为
(2)C→D的反应类型为
(3)条件一与条件二能否互换
(4)写出D 与G 反应的化学方程式
(5)A 的同分异构体很多,其中能使FeCl3溶液显紫色有
(6)结合题中信息,写出以溴乙烷为原料制备1-丁醇的合成路线图
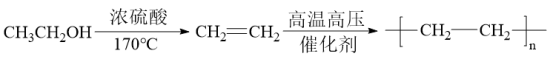 。
。
您最近一年使用:0次
解题方法
6 . K是一种抗病毒药物的重要中间体,K的一种合成路线如下(部分试剂和条件略去)。
(1)A中官能团的名称为___________ 。
(2)B中碳原子的轨道杂化类型为___________ 。
(3)由C生成E的化学方程式为___________ 。
(4)E→F的反应类型为___________ 。
(5)H的结构简式为___________ 。
(6)K分子中具有孤电子对的原子数目有___________ 个。
(7)在H的同分异构体中,同时满足下列条件的共有___________ 种(不考虑立体异构)。
①含有苯环且苯环上只有一个取代基;
②能与金属钠反应产生 。
。
其中,不含手性碳原子的同分异构体的结构简式为___________ (任写一种)。
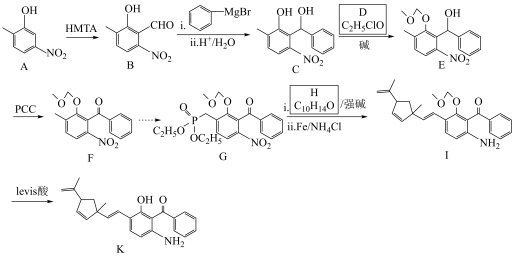
已知:.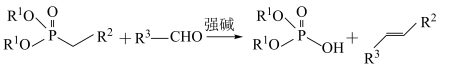
(1)A中官能团的名称为
(2)B中碳原子的轨道杂化类型为
(3)由C生成E的化学方程式为
(4)E→F的反应类型为
(5)H的结构简式为
(6)K分子中具有孤电子对的原子数目有
(7)在H的同分异构体中,同时满足下列条件的共有
①含有苯环且苯环上只有一个取代基;
②能与金属钠反应产生
 。
。其中,不含手性碳原子的同分异构体的结构简式为
您最近一年使用:0次
解题方法
7 . 有机高分子化合物G的合成路线如下:
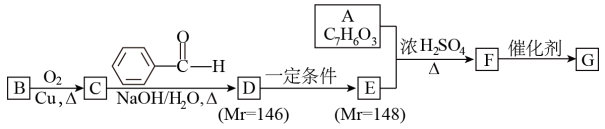
已知:①A(C7H6O3)既能与NaHCO3溶液反应,又能与FeCl3溶液发生显色反应,其1H核磁共振谱有4个峰;②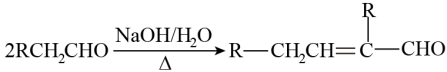 。
。
请回答:
(1)要测定有机物D和E相对分子质量(Mr),通常使用的仪器是____ ;B的名称为___ ,D中含有的官能团名称为_____ 。
(2)D→E的反应类型为_____ ,高分子化合物G的结构简式为________________ 。
(3)A+E→F的化学方程式为:_________________________________ 。
(4)D发生银镜反应的化学方程式为:______________________________ 。
(5)符合下列条件的E的同分异构体有_______ 种(不考虑立体异构)。写出其中任意一种异构体的结构简式____ 。①含有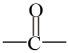 ,②苯环上有两个取代基
,②苯环上有两个取代基

已知:①A(C7H6O3)既能与NaHCO3溶液反应,又能与FeCl3溶液发生显色反应,其1H核磁共振谱有4个峰;②
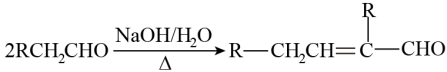 。
。请回答:
(1)要测定有机物D和E相对分子质量(Mr),通常使用的仪器是
(2)D→E的反应类型为
(3)A+E→F的化学方程式为:
(4)D发生银镜反应的化学方程式为:
(5)符合下列条件的E的同分异构体有
 ,②苯环上有两个取代基
,②苯环上有两个取代基
您最近一年使用:0次
8 . 二甲醚制备两种方法原理如下
第一种方法:丹麦Topspe工艺的合成气一步法,是专门针对天然气原料开发的一项新技术。
①2CH4(g)+O2(g) CH3OCH3(g)+H2O(g) △H1
CH3OCH3(g)+H2O(g) △H1
第二种方法:二甲醚生产二步法,即先合成甲醇,甲醇在催化剂下制二甲醚。
②CO(g)+2H2(g) CH3OH(g) △H2
CH3OH(g) △H2
③2CH3OH(g) CH3OCH3 (g)+H2O(g) △H3
CH3OCH3 (g)+H2O(g) △H3
(1)若由合成气(CO、H2)直接制备 1molCH3OCH3(g),且生成H2O(1),整个过程中放出的热量为244kJ,则△H2=___________ kJ·mol-1。(已知:H2O(1)=H2O(g) △H=+44.0 kJ/mol)
(2)下列有关反应①叙述不正确的是___________
a.达到平衡后,升高温度,ν正减少、ν逆增大,平衡逆向移动
b.当四种物质的浓度相等,反应达到化学平衡状态
c.若改变条件,反应物的转化率一定增大,正反应速率一定大于逆反应速率
d.当达到平衡时2v正(O2)=v逆(CH4)
e.向该恒容平衡体系中充入氩气,ν正、ν逆均增大,平衡向右移动
(3)有人模拟制备原理Ⅱ,绘制如图甲图象:
i说明CO的转化率随温度升高先增大后减小的原因:______________________ 。
ii.反应②自发进行的条件是______________________ 。
iii.若在350℃时的2L的密闭容器中充入2 mol CO和6molH2,8min达到平衡,c(CH3OCH3)=0.3mol·L-1,用H2表示反应②的速率是___________ ;可逆反应③的平衡常数K3=___________ 。
iv.若350℃时测得容器中n(CH3OH)=n(CH3OCH3),此时反应③v(正)___________ ν(逆),说明原因_________ 。


甲 乙
(4)光能储存一般是指将光能转换为电能或化学能进行储存,利用太阳光、CO2、H2O生成二甲醚的光能储存装置如图乙所示则b极的电极反应式为___________________________ 。
第一种方法:丹麦Topspe工艺的合成气一步法,是专门针对天然气原料开发的一项新技术。
①2CH4(g)+O2(g)
 CH3OCH3(g)+H2O(g) △H1
CH3OCH3(g)+H2O(g) △H1第二种方法:二甲醚生产二步法,即先合成甲醇,甲醇在催化剂下制二甲醚。
②CO(g)+2H2(g)
 CH3OH(g) △H2
CH3OH(g) △H2③2CH3OH(g)
 CH3OCH3 (g)+H2O(g) △H3
CH3OCH3 (g)+H2O(g) △H3(1)若由合成气(CO、H2)直接制备 1molCH3OCH3(g),且生成H2O(1),整个过程中放出的热量为244kJ,则△H2=
(2)下列有关反应①叙述不正确的是
a.达到平衡后,升高温度,ν正减少、ν逆增大,平衡逆向移动
b.当四种物质的浓度相等,反应达到化学平衡状态
c.若改变条件,反应物的转化率一定增大,正反应速率一定大于逆反应速率
d.当达到平衡时2v正(O2)=v逆(CH4)
e.向该恒容平衡体系中充入氩气,ν正、ν逆均增大,平衡向右移动
(3)有人模拟制备原理Ⅱ,绘制如图甲图象:
i说明CO的转化率随温度升高先增大后减小的原因:
ii.反应②自发进行的条件是
iii.若在350℃时的2L的密闭容器中充入2 mol CO和6molH2,8min达到平衡,c(CH3OCH3)=0.3mol·L-1,用H2表示反应②的速率是
iv.若350℃时测得容器中n(CH3OH)=n(CH3OCH3),此时反应③v(正)


甲 乙
(4)光能储存一般是指将光能转换为电能或化学能进行储存,利用太阳光、CO2、H2O生成二甲醚的光能储存装置如图乙所示则b极的电极反应式为
您最近一年使用:0次
解题方法
9 . CO2是一种常用的化工原料。
Ⅰ.以CO2与NH3为原料可以合成尿素[CO(NH2)2]。合成尿素的反应为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g)。
CO(NH2)2(s)+H2O(g)。
(1)在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率的变化情况如图所示。该反应的ΔH________ (填“>”、“<”或“=”,下同)0,若y表示压强,则y1________ y2,若y表示反应开始时的n(NH3)/n(CO2),则y1________ y2。
(2)T℃时,若向容积为2L的恒容密闭容器中加入3mol NH3和1mol CO2,达到平衡时,容器内压强为开始时的3/4。若保持条件不变,再向该容器中加入0.5mol CO2和1mol H2O,NH3的转化率将________ (填“增大”、“减小”或“不变”)。
Ⅱ.CO2与H2反应可用于生产甲醇。
(3)已知氢气与甲醇的燃烧热分别为285.8kJ·mol-1、726.5kJ·mol-1,则CO2与H2反应产生液态甲醇与液态水的热化学方程式为_____ 。
(4)如图是某甲醇燃料电池工作的示意图。
质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol·L-1 H2SO4溶液。电极a上发生的电极反应为____ ,当电池中有1mol e-发生转移时左右两侧溶液的质量之差为_____ g(假设反应物耗尽,忽略气体的溶解)。
(5)写出Na2CO3溶液中各离子浓度的大小关系__________________ 。
Ⅰ.以CO2与NH3为原料可以合成尿素[CO(NH2)2]。合成尿素的反应为2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g)。
CO(NH2)2(s)+H2O(g)。(1)在不同温度及不同y值下合成尿素,达到平衡时,氨气转化率的变化情况如图所示。该反应的ΔH

(2)T℃时,若向容积为2L的恒容密闭容器中加入3mol NH3和1mol CO2,达到平衡时,容器内压强为开始时的3/4。若保持条件不变,再向该容器中加入0.5mol CO2和1mol H2O,NH3的转化率将
Ⅱ.CO2与H2反应可用于生产甲醇。
(3)已知氢气与甲醇的燃烧热分别为285.8kJ·mol-1、726.5kJ·mol-1,则CO2与H2反应产生液态甲醇与液态水的热化学方程式为
(4)如图是某甲醇燃料电池工作的示意图。
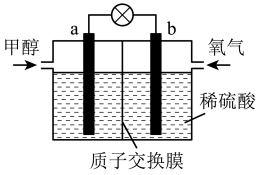
质子交换膜(只有质子能够通过)左右两侧的溶液均为1L 2mol·L-1 H2SO4溶液。电极a上发生的电极反应为
(5)写出Na2CO3溶液中各离子浓度的大小关系
您最近一年使用:0次
名校
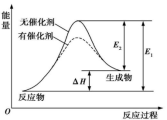
10 . 合成气(CO和H2)是目前化工常用的原料,下面是用甲烷制备合成气的两种方法:①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
 CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
CO(g)+3H2(g) ΔH1=+216 kJ·mol-1;②2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH2=-72 kJ·mol-1。其中一个反应的反应过程与能量变化关系如图所示。则下列说法正确的是
| A.E1表示2CH4(g)+O2(g)=2CO(g)+4H2(g)的活化能 |
B.E2表示CH4(g)+H2O(g) CO(g)+3H2(g)的活化能 CO(g)+3H2(g)的活化能 |
| C.该图示为反应②的反应过程与能量变化示意图 |
| D.一般情况下,加入催化剂,既能降低E1,也能降低E2,但不能改变E1与E2的差值 |
您最近一年使用:0次
2018-01-20更新
|
459次组卷
|
6卷引用:贵州省安顺市平坝第一高级中学2019-2020学年高二上学期期中考试化学试题



