名校
1 . 下列有关热化学方程式的说法正确的是
A.甲烷的燃烧热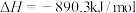 ,则甲烷燃烧的热化学方程式可表示为 ,则甲烷燃烧的热化学方程式可表示为 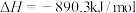 |
B.500℃、30MPa下,将 和 和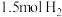 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学反应方程式为: ,放热19.3kJ,其热化学反应方程式为:  |
C.HCl和NaOH反应的中和热 ,则: ,则: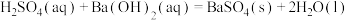 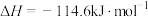 |
D.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 相同 相同 |
您最近一年使用:0次
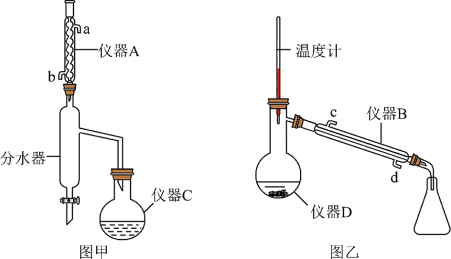
2 . 苯甲酸乙酯( )可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:
)可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:
步骤①:在烧瓶中加入苯甲酸12.2g、乙醇60.0mL、浓硫酸5.0mL、适量环己烷。按如图所示安装好装置,加热烧瓶,控制一定温度加热回流2h。
步骤②:将烧瓶中的反应液倒入盛有100.0mL水的烧杯中,加入Na2CO3至溶液呈中性。
步骤③:用分液漏斗分离出有机层,再用乙醚萃取水层中的残留产品,二者合并,加到图乙的蒸馏装置中,加入沸石与无水硫酸镁,加热蒸馏制得产品5.0mL。
回答下列问题:
(1)仪器A的名称为___________ ,冷凝水的出水口为___________ (填“a”或“b”),本实验中浓硫酸的作用是___________ 。
(2)环己烷、乙醇和水可形成共沸物,沸点为62.1℃,仪器C的最佳加热方式为___________ 。
(3)写出制备苯甲酸乙酯反应的化学方程式:___________ 。
(4)图甲中分水器的“分水”原理是冷凝液在分水器中分层,上层有机层从支管处流回烧瓶,下层水层从分水器下口放出,反应结束的标志是___________ 。
(5)步骤②中加入Na2CO3的作用是___________ 。
(6)该实验中苯甲酸乙酯的产率为___________ %(保留三位有效数字)。
 )可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:
)可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:步骤①:在烧瓶中加入苯甲酸12.2g、乙醇60.0mL、浓硫酸5.0mL、适量环己烷。按如图所示安装好装置,加热烧瓶,控制一定温度加热回流2h。
步骤②:将烧瓶中的反应液倒入盛有100.0mL水的烧杯中,加入Na2CO3至溶液呈中性。
步骤③:用分液漏斗分离出有机层,再用乙醚萃取水层中的残留产品,二者合并,加到图乙的蒸馏装置中,加入沸石与无水硫酸镁,加热蒸馏制得产品5.0mL。
| 物质名称 | 苯甲酸 | 乙醇 | 环己烷 | 苯甲酸乙酯 |
| 相对分子质量 | 122 | 46 | 84 | 150 |
| 密度/g·cm-3 | 1.2659 | 0.7893 | 0.7318 | 1.0500 |
| 沸点/℃ | 249.2 | 78.3 | 80.8 | 212.61 |
(1)仪器A的名称为
(2)环己烷、乙醇和水可形成共沸物,沸点为62.1℃,仪器C的最佳加热方式为
(3)写出制备苯甲酸乙酯反应的化学方程式:
(4)图甲中分水器的“分水”原理是冷凝液在分水器中分层,上层有机层从支管处流回烧瓶,下层水层从分水器下口放出,反应结束的标志是
(5)步骤②中加入Na2CO3的作用是
(6)该实验中苯甲酸乙酯的产率为
您最近一年使用:0次
3 . 完成下列问题。___________ (填序号,下同);属于加成反应的是___________ ;属于氧化反应的是___________ 。
①乙烯使酸性高锰酸钾溶液褪色;②由乙烯制一氯乙烷;③乙醇在铜催化作用下制乙醛; ④乙酸和乙醇反应生成乙酸乙酯。
(1)现有各组物质:①O2和O3 ②CH2=CH-CH3和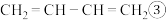
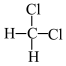 和
和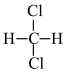
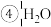 和
和 和
和 和质量数为238中子数为146的原子⑦
和质量数为238中子数为146的原子⑦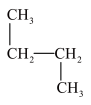 和
和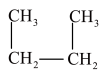 ⑧
⑧ 和CH3(CH2)3CH3。属于同种物质的是
和CH3(CH2)3CH3。属于同种物质的是
①乙烯使酸性高锰酸钾溶液褪色;②由乙烯制一氯乙烷;③乙醇在铜催化作用下制乙醛; ④乙酸和乙醇反应生成乙酸乙酯。
您最近一年使用:0次
名校
解题方法
4 . 下列说法错误的是
| A.相对分子质量为86,含有3个甲基的链状烷烃有2种 |
| B.分子式为C4H9Cl的有机物有4种 |
| C.分子式为C8H18,主链含有5个碳原子的链状烷烃有5种 |
| D.C5H12的一溴代物有8种 |
您最近一年使用:0次
名校
5 . 下列化学用语正确的是
A.丙烷分子的球棍模型: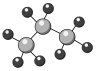 |
| B.乙醇分子式:C2 H5 OH |
C.一氯甲烷的电子式: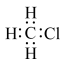 |
D.CCl4空间填充模型: |
您最近一年使用:0次
名校
6 . 回答下列问题。
(1)理论上不能设计为原电池的化学反应是___________ 。
a.4Li+FeS2=Fe+2Li2S b.CH4+2O2=CO2+2H2O
c.Ag2O+Zn+H2O=2Ag+Zn(OH)2. d.CuSO4+H2S=CuS↓+H2SO4
(2)某小组为探究Fe与Fe3+能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和KNO3溶液的琼脂)。___________ ,盐桥中 向
向___________ 烧杯移动(填“甲”或“乙”)。
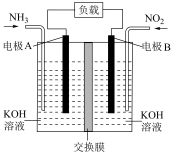
(3)某学习小组设计如图所示装置,有效降低含氮化合物的排放,同时充分利用化学能,相同温度和压强下,A,B两电极产生气体的体积比为___________ ,B电极的电极反应方程式为___________ 。
(1)理论上不能设计为原电池的化学反应是
a.4Li+FeS2=Fe+2Li2S b.CH4+2O2=CO2+2H2O
c.Ag2O+Zn+H2O=2Ag+Zn(OH)2. d.CuSO4+H2S=CuS↓+H2SO4
(2)某小组为探究Fe与Fe3+能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和KNO3溶液的琼脂)。
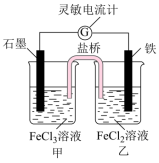
 向
向(3)某学习小组设计如图所示装置,有效降低含氮化合物的排放,同时充分利用化学能,相同温度和压强下,A,B两电极产生气体的体积比为
您最近一年使用:0次
名校
7 . 海洋是一座巨大的化学资源宝库,如图是从海水中提取若干种化学物质的流程图,则下列说法正确的是
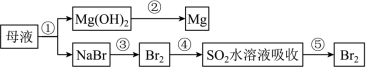
| A.从经济效益角度考虑,工业上①中沉淀Mg2+使用的试剂是氢氧化钠 |
| B.②中包含制取MgCl2溶液、MgCl2·6H2O、无水MgCl2及电解法冶炼Mg几个阶段 |
| C.③④⑤中溴元素均被氧化 |
| D.③④⑤步骤主要目的是减少环境污染 |
您最近一年使用:0次
名校
8 . 下列说法正确的是
| A.乙醇能使酸性高锰酸钾溶液或酸性重铬酸钾溶液褪色 |
| B.聚丙烯的链节为-CH2-CH2-CH2- |
| C.含有碳和氢两种元素的有机化合物一定是烃 |
| D.等质量的苯和乙烯充分燃烧消耗O2的量:苯<乙烯 |
您最近一年使用:0次
9 . 下列说法正确的是
| A.石油的裂解气、煤干馏得到的焦炉气都能使酸性高锰酸钾溶液褪色 |
| B.煤的干馏、气化,石油的分馏都是物理变化 |
| C.石油没有固定熔沸点,但分馏产物有固定的熔沸点 |
| D.石油裂解的目的是提高汽油的产量和质量 |
您最近一年使用:0次
名校
解题方法
10 . 提纯下列物质(括号内为少量杂质),不能达到目的的是
| 选项 | 混合物 | 除杂试剂 | 分离方法 |
| A | 乙酸乙酯(乙酸) | 饱和Na2CO3溶液 | 分液 |
| B | 乙醇(水) | 生石灰 | 蒸馏 |
| C | 乙醇(乙酸) | NaOH溶液 | 蒸馏 |
| D | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



