1 . 下列溶液中的微粒浓度关系正确的是
A.Na2CO3溶液中离子浓度大小关系为 |
B.0.1mol/L NaHCO3溶液中  |
C.80℃时,0.1mol/L NaHSO4溶液中由水电离出的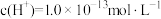 |
| D.常温下,pH=4的CH3COOH溶液与pH=10的NaOH溶液等体积混合后,溶液的pH=7 |
您最近一年使用:0次
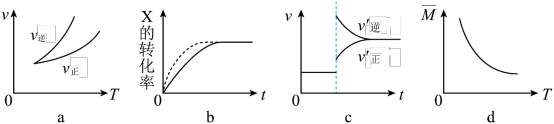
2 . 在密闭容器中进行反应: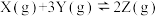 ,有关下列图像的说法错误的是
,有关下列图像的说法错误的是
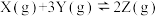 ,有关下列图像的说法错误的是
,有关下列图像的说法错误的是
| A.依据图a可判断正反应为放热反应 |
| B.在图b中,虚线可表示使用了催化剂 |
| C.若正反应的△H>0,图c可表示升高温度使平衡向逆反应方向移动 |
| D.由图d中混合气体的平均相对分子质量随温度的变化情况,可推知正反应的△H>0 |
您最近一年使用:0次
3 . 下图表示 (g)和
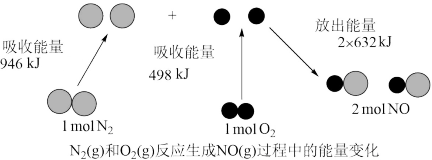
(g)和 (g)反应生成NO(g)过程中的能量变化,下列说法不正确的是
(g)反应生成NO(g)过程中的能量变化,下列说法不正确的是
 (g)和
(g)和 (g)反应生成NO(g)过程中的能量变化,下列说法不正确的是
(g)反应生成NO(g)过程中的能量变化,下列说法不正确的是
A. 化学性质稳定,是因为断开 化学性质稳定,是因为断开 分子中的化学键需要吸收较多能量 分子中的化学键需要吸收较多能量 |
B.1mol  (g)和1mol (g)和1mol  (g)所具有的能量之和比2mol NO(g)的能量高 (g)所具有的能量之和比2mol NO(g)的能量高 |
C.1mol  (g)和1mol (g)和1mol  (g)后应生成2mol NO(g),需吸收能量180kJ (g)后应生成2mol NO(g),需吸收能量180kJ |
D.NO(g)分解为 (g)和 (g)和 (g)是放热反应 (g)是放热反应 |
您最近一年使用:0次
4 . 研究电解质在水溶液中的平衡能了解它的存在形式。已知部分弱酸的电离常数如下表:
(1)①常温下,pH相同的三种溶液HF、H2CO3、H2S,物质的量浓度最小的是_______ 。
②将少量H2S通入Na2CO3溶液,反应的离子方程式是_______ 。
③0.1mol·L-1的HF溶液,其电离百分数为8%,则该溶液的pH=_______ (已知lg2=0.3)
(2)25℃时,向足量的NaCN溶液中通入少量CO2,所发生反应的离子方程式为_______ 。
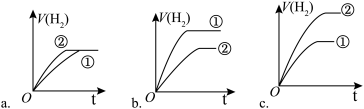
(3)pH相同、体积相同的盐酸和氢氟酸两种溶液盐酸分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示氢氟酸)
(4)烟气中的SO2可引起酸雨,可利用氢氧化钠溶液吸收。吸收SO2的过程中,溶液中H2SO3、 、
、 三者所占物质的量分数(a)随pH变化的关系如图所示。由图可知H2SO3第一级电离平衡常数Ka1=
三者所占物质的量分数(a)随pH变化的关系如图所示。由图可知H2SO3第一级电离平衡常数Ka1=_______ 。

(5)25℃,101KPa时,1g氢气完全燃烧生成液态水,放出142.9kJ热量,请写出氢气燃烧热的热化学方程式_______ (结果取整数)。
| 化学式 | HF | H2CO3 | H2S | HCN |
| 电离平衡常数K(25℃) | 7.2×10-4 | Ka1=4.4×10-7 Ka2=9.1×10-11 | Ka1=9.1×10-8 Ka2=1.1×10-11 | K=4.9×10-10 |
(1)①常温下,pH相同的三种溶液HF、H2CO3、H2S,物质的量浓度最小的是
②将少量H2S通入Na2CO3溶液,反应的离子方程式是
③0.1mol·L-1的HF溶液,其电离百分数为8%,则该溶液的pH=
(2)25℃时,向足量的NaCN溶液中通入少量CO2,所发生反应的离子方程式为
(3)pH相同、体积相同的盐酸和氢氟酸两种溶液盐酸分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是

(4)烟气中的SO2可引起酸雨,可利用氢氧化钠溶液吸收。吸收SO2的过程中,溶液中H2SO3、
 、
、 三者所占物质的量分数(a)随pH变化的关系如图所示。由图可知H2SO3第一级电离平衡常数Ka1=
三者所占物质的量分数(a)随pH变化的关系如图所示。由图可知H2SO3第一级电离平衡常数Ka1=
(5)25℃,101KPa时,1g氢气完全燃烧生成液态水,放出142.9kJ热量,请写出氢气燃烧热的热化学方程式
您最近一年使用:0次
5 . 以NOx为主要成分的雾霾的综合治理是当前重要的研究课题。汽车尾气中的NO(g)和CO(g)在一定条件下可发生反应生成无毒的N2和CO2:2NO(g)+2CO(g)⇌N2(g)+2CO2(g) ΔH3=-746.5kJ/mol。
(1)某研究小组在三个容积为5L的恒容密闭容器中,分别充入0.4molNO和0.4molCO。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示:(填"<"、">""或"=",)

①温度:T1_______ T2.
②CO的平衡转化率:I_______ Ⅱ_______ Ⅲ
③反应速率:a点的v逆_______ b点的v正
④T2时的平衡常数K=_______ 。
(2)将NO和CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测量的脱氮率(脱氮率即NO的转化率)如图所示。M点_______ (填“是”或“不是”)对应温度下的平衡脱氮率,说明理由_______ 。

(1)某研究小组在三个容积为5L的恒容密闭容器中,分别充入0.4molNO和0.4molCO。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图所示:(填"<"、">""或"=",)

①温度:T1
②CO的平衡转化率:I
③反应速率:a点的v逆
④T2时的平衡常数K=
(2)将NO和CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测量的脱氮率(脱氮率即NO的转化率)如图所示。M点

您最近一年使用:0次
6 . 一个真空密闭恒容容器中盛有amolPCl5,加热到200℃发生如下反应:PCl5(g)⇌PCl3(g)+Cl2(g),反应达到平衡时,混合气体中PCl3所占体积分数为M%。若同一温度的同一容器中,最初投入2amolPCl5,反应达平衡时,混合气体中PCl3所占体积分数为N%。则M和N的关系是
| A.M>N | B.M=N | C.M<N | D.无法确定 |
您最近一年使用:0次
7 . 下列有关合成氨工业的叙述,不可用勒夏特列原理来解释的是
| A.将NO2和N2O4的混合气体加压后,颜色先变深后变浅 |
| B.高压比常压条件更有利于合成氨的反应 |
| C.低温更有利于合成氨的反应 |
| D.使用铁触媒,使N2和H2混合气体有利于合成氨 |
您最近一年使用:0次
8 . 下列事实中一定不能证明CH3COOH是弱电解质的是
①等物质的量浓度、等体积的盐酸、CH3COOH溶液和足量锌反应,根据产生氢气的多少
②用CH3COOH溶液做导电实验,灯泡很暗
③等pH、等体积的盐酸、CH3COOH溶液和足量锌反应,CH3COOH放出的氢气较多
④0.1mol·L-1CH3COOH溶液的c(H+)=1.0×10-2mol·L-1
①等物质的量浓度、等体积的盐酸、CH3COOH溶液和足量锌反应,根据产生氢气的多少
②用CH3COOH溶液做导电实验,灯泡很暗
③等pH、等体积的盐酸、CH3COOH溶液和足量锌反应,CH3COOH放出的氢气较多
④0.1mol·L-1CH3COOH溶液的c(H+)=1.0×10-2mol·L-1
| A.①② | B.②③ | C.①③ | D.③④ |
您最近一年使用:0次
9 . 下列反应符合如图信息的是


| A.接触室中二氧化硫催化氧化成三氧化硫 |
| B.碳酸氢钠固体与盐酸溶液 |
| C.氢氧化钠溶液中滴加稀盐酸 |
| D.生石灰加水制熟石灰 |
您最近一年使用:0次
10 . 一定温度下,向一恒容器密闭容器中充入2mol  和1mol
和1mol  ,发生反应:
,发生反应: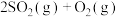

 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是
 和1mol
和1mol  ,发生反应:
,发生反应: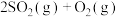

 ,下列有关该反应的说法正确的是
,下列有关该反应的说法正确的是| A.其他条件不变,降低温度,v(正)增大、v(逆)减小,平衡正移 |
B.其他条件不变,移走一定量的 ,v(正)不变、v(逆)减小,平衡正移 ,v(正)不变、v(逆)减小,平衡正移 |
| C.温度不变,向该容器中充入气体Ar,容器压强增大,反应速率增大 |
| D.加入催化剂可以加快化学反应速率和提高产率 |
您最近一年使用:0次



